Søker: University of Massachusetts og E. R. Squibb & Sons L.L.C.
|
|
|
- Stefan Hermansen
- 7 år siden
- Visninger:
Transkript
1 O.nr / EH/KN/KN Patentsøknad nr Søker: University of Massachusetts og E. R. Squibb & Sons L.L.C. Tittel: Isolert monoklonalt antistoff eller antigen bindende del derav, samt anvendelse derav og farmasøytisk preparat, isolert nukleinsyre, ekspresjonsvektor, vertscelle, sett og preparat. TRYKNINGSKLARE DOKUMENTER
2 1 Foreliggende oppfinnelse omfatter isolert monoklonalt antistoff eller antigen bindende del derav, samt anvendelse derav og farmasøytisk preparat, isolert nukleinsyre, ekspresjonsvektor, vertscelle, sett og preparat. Bakgrunn for oppfinnelsen Clostridium difficile (C. difficile) er en gram-positiv bakterie som forårsaker gastrointestinal sykdom hos mennesker. C. difficile er den mest vanlige årsak til infeksiøs 5 diaré hos sykehuspasienter og er én av de mest vanlige sykehusinfeksjoner totalt (Kelly et al., New Eng. J. Med., 330:257-62, 1994). Sykdom forbundet med dette patogenet kan faktisk ramme så mange som tre million pasienter innlagt på sykehus pr. år i USA (McFarland et al., New Eng. J. Med., 320:204-10, 1989; Johnson et al., Lancet, 336:97-100, 1990). 10 Behandling med antibiotika slik som ampicillin, amoxicillin, cefalosporiner og klindamycin som forstyrrer normal tarmflora kan tillate kolonisering i tarmen med C. difficile og fører til C. difficile-sykdom (Kelly og Lamont, Annu. Rev. Med., 49:375-90, 1998). Oppstart av C. difficile-sykdom inntreffer typisk fire til ni dager etter start av antibiotikabehandling, men kan også forekomme etter avbrytelse av antibiotikabehandling. 15 C. difficile kan frembringe symptomer i spekteret fra mild til alvorlig diaré og kolitt, omfattende pseudomembranøs kolitt (PMC), en alvorlig form av kolitt karakterisert ved abdominal smerte, vannholdig diaré og systemisk sykdom (f.eks., feber, kvalme). Tilbakefall av sykdom kan forekomme hos opptil 20% av pasientene behandlet for en første sykdomsepisode og de som har et tilbakefall har større risiko for ytterligere 20 tilbakefall (Kelly og Lamont, Annu. Rev. Med., 49:375-90, 1998). C. difficile-sykdom er antatt å være forårsaket av virkningene av to eksotoksiner, toksin A og toksin B, på tarmepitel. Begge toksinene er høymolekylvekt proteiner ( kda) som katalyserer kovalent modifikasjon av Rho-proteiner, små GTPbindingsproteiner involvert i aktinpolymerisering, i vertsceller. Modifikasjon av Rho- 25 proteiner ved toksinene inaktiverer dem, hvilket fører til depolymerisering av aktinfilamenter og celledød. Begge toksinene er letale for mus når injisert parenteralt (Kelly og Lamont, Annu. Rev. Med., 49:375-90, 1998). C. difficile-sykdom kan diagnostiseres ved analyser som detekterer tilstedeværelse eller aktivitet av toksin A eller toksin B i avføringsprøver, f.eks., enzymimmunanalyser. 30 Cytotoksin-analyser kan anvendes for å detektere toksinaktivitet. For å utføre en cytotoksin-analyse, blir avføring filtrert for å fjerne bakterier og de cytopatiske effektene
3 2 av toksiner på dyrkede celler blir bestemt (Merz et al., J. Clin. Microbiol., 32: , 1994). C. difficile-behandling er komplisert ved det faktum at antibiotika utløser C. difficile-assosiert sykdom. Allikevel er antibiotika for øyeblikket det primære valget for 5 behandling. Antibiotika som er minst egnet til å forårsake C. difficile-assosiert sykdom slik som vankomycin og metronidazol anvendes ofte. Vankomycinresistens som utvikles i andre mikroorganismer er en grunn til bekymring ved anvendelse av dette antibiotika for behandling, ettersom det er den eneste effektive behandlingen for infeksjon med andre mikroorganismer (Gerding, Curr. Top. Microbiol. Immunol., 250:127-39, 2000). 10 Probiotiske metoder, hvor et subjekt blir administrert ikke-patogene mikroorganismer som antagelig konkurrerer om plass med de patogene bakteriene, anvendes også. For eksempel er behandling med en kombinasjon av vankomycin og Saccharomyces boulardii rapportert (McFarland et al., JAMA., 271(24):1913-8, Erratum i: JAMA, 272(7):518, 1994). Det har blitt utviklet vaksiner som beskytter dyr fra letal provokasjon i infeksiøse 15 modeller av sykdom (Torres et al., Infect. Immun. 63(12): ,1995). I tillegg har polyklonale antistoffer blitt vist å beskytte hamstere fra sykdom når administrert ved injeksjon eller fôring (Giannasca et al., Infect. Immun. 67(2):527-38, 1999; Kink og Williams, Infect. Immun., 66(5): , 1998). Det har blitt isolert murine monoklonale antistoffer som binder til C. difficile-toksiner og nøytraliserer deres aktiviteter in vivo og in 20 vitro (Corthier et al., Infect. Immun., 59(3):1192-5, 1991). Det er noen angivelser om at humane polyklonale antistoffer inneholdende toksin-nøytraliserende antistoffer kan forhindre tilbakefall av C. difficile (Salcedo et al., Gut., 41(3):366-70, 1997). Antistoffrespons mot toksin A har blitt korrelert med sykdomsutfall, hvilket indikerer effektiviteten av humorale responser med hensyn til å kontrollere infeksjon. Individer med 25 kraftige toksin A ELISA-responser hadde mindre alvorlig sykdom sammenlignet med individer med lave nivåer av toksin A antistoff (Kyne et al., Lancet, 357(9251):189-93, 2001). De individuelle rollene av toksin A og toksin B ved sykdomspatogenese og rollen til anti-toksin antistoffer ved beskyttelse mot C. difficile-sykdom er kontroversielle 30 og kan avhenge av verten. Hos mennesker har anti-toksin A antistoffresponsen blitt korrelert med sykdomsutfall, hvilket indikerer et krav om anti-toksin A-respons for beskyttelse. Denne observasjonen står i kontrast til angivelser av sykdomsforårsakende C. difficile-organismer som kun uttrykker toksin B, hvilket antyder at toksin B kan bidra til
4 3 sykdom hos mennesker. Disse toksin A-negative stammene kan også forårsake sykdom hos hamstere (Sambol et al., J. Infect. Dis., 183(12):1760-6, 2001). KINK JOHN A. ET AL., "Antibodies to recombinant Clostridium difficule toxins A and B are effective treatment and prevent relapse of C. difficile-associated disease 5 in a hamster model of infection", Infection and Immunity, American Society for Microbiology, vol. 66, no. 5, 1998, side beskriver virkningen av C. difficile toksin A og B på patogenese og muligheten til å behandle sykdom forårsaket av C. difficile med et antistoff rettet mot rekombinante epitoper på toksin A og B. 10 DENG XIAO K. ET AL., "Recombinant single-chain variable fragment antibodies directed against Clostridium difficile toxin B produced by use of an optimized phage display system", Clinical and Diagnostic Laboratory Immunology, vol. 10, no. 4, 2003, side Her er det fremstilt enkelt-kjede antistoffer (scfv) mot Clostridium difficile toksin B fra en muse B celle hybridoma cellelinje 5A8 som produserer 15 monoklonale antistoffer mot toksinet. WO A2 beskriver anvendelse av interleukin-4 antagonister og sammensetninger derav. Oppsummering av oppfinnelsen Foreliggende oppfinnelse omfatter isolert monoklonalt antistoff eller antigen bindende del derav, samt anvendelse derav og farmasøytisk preparat, isolert nukleinsyre, ekspresjonsvektor, vertscelle, sett og preparat. 20 Foreliggende oppfinnelse er følgelig basert, delvis, på det funnet at administrering av antistoffer mot C. difficile toksin A til et subjekt kan beskytte subjektet mot tilbakefall av C. difficile-mediert sykdom in vivo. Administrering av antistoffer mot ett eller begge av toksin A og toksin B kan forhindre primær C. difficile-mediert sykdom. Antistoffer med høy affinitet mot C. difficile-toksiner kan produseres, f.eks., i mus, slik som transgene mus 25 som uttrykker gensegmenter for humant immunoglobulin. Disse antistoffene kan nøytralisere cytotoksisitet av toksinet in vitro og nøytralisere toksin-enterotoksisitet in vivo. Antistoffer som gjenkjenner toksin A og/eller toksin B kan hemme og beskytte mot sykdom in vivo. I ett aspekt angår oppfinnelsen et isolert monoklonalt antistoff eller antigen 30 bindende del derav, som spesifikt binder til et eksotoksin av Clostridium difficile (C.
5 4 difficile) omfattende tung og lettkjede variabel region CDR1, CDR2 og CDR3 sekvenser valgt fra gruppen bestående av: (i) en tungkjede variabel region CDR1 angitt i SEKV ID NR:7; en tungkjede variabel region CDR2 angitt i SEKV ID NR:8; 5 en tungkjede variabel region CDR3 angitt i SEKV ID NR:9; en lettkjede variabel region CDR1 angitt i SEKV ID NR:16; en lettkjede variabel region CDR2 angitt i SEKV ID NR:17; en lettkjede variabel region CDR3 angitt i SEKV ID NR:18; 10 (ii) en tungkjede variabel region CDR1 angitt i SEKV ID NR:10; en tungkjede variabel region CDR2 angitt i SEKV ID NR:11; en tungkjede variabel region CDR3 angitt i SEKV ID NR:12; en lettkjede variabel region CDR1 angitt i SEKV ID NR:19; en lettkjede variabel region CDR2 angitt i SEKV ID NR:20; 15 en lettkjede variabel region CDR3 angitt i SEKV ID NR:21; (iii) en tungkjede variabel region CDR1 angitt i SEKV ID NR:13; en tungkjede variabel region CDR2 angitt i SEKV ID NR:14; en tungkjede variabel region CDR3 angitt i SEKV ID NR:15; 20 en lettkjede variabel region CDR1 angitt i SEKV ID NR:22; en lettkjede variabel region CDR2 angitt i SEKV ID NR:23; en lettkjede variabel region CDR3 angitt i SEKV ID NR:24; og (iv) en tungkjede variabel region CDR1 angitt i SEKV ID NR:62; 25 en tungkjede variabel region CDR2 angitt i SEKV ID NR:64; en tungkjede variabel region CDR3 angitt i SEKV ID NR:66; en lettkjede variabel region CDR1 angitt i SEKV ID NR:68; en lettkjede variabel region CDR2 angitt i SEKV ID NR:70; en lettkjede variabel region CDR3 angitt i SEKV ID NR: I visse utførelsesformer binder antistoffene eller antigenbindende deler derav spesifikt til C. difficile-toksin A (toksin A). I andre utførelsesformer binder antistoffet eller antigenbindende deler derav spesifikt til C. difficile-toksin B (toksin B). I andre
6 5 utførelsesformer binder antistoffene eller antigenbindende deler derav spesifikt til både toksin A og toksin B. I visse utførelsesformer nøytraliserer antistoffene eller antigenbindende deler derav toksin A in vitro, hemmer binding av toksin A til mammalske celler og/eller hemmer C. 5 difficile-mediert sykdom in vivo. I forskjellige utførelsesformer har antistoffene eller antigenbindende deler derav én eller flere av de følgende egenskapene: når administrert til en mus, beskytter de musen mot administrering av et C. difficile-toksin i en mengde som ville være dødelig for en kontrollmus ikke administrert antistoffet; beskytter mot eller hemmer C. difficile-mediert 10 kolitt, antibiotikaassosiert kolitt eller pseudomembranøs kolitt (PMC) hos et subjekt; beskytter mot eller hemmer diaré hos et subjekt; og/eller hemmer tilbakefall av C. difficilemediert sykdom. Antistoffene eller antigenbindende deler derav kan spesifikt binde til en epitop innenfor den N-terminale halvdelen av toksin A, f.eks., en epitop mellom aminosyrene av toksin A. I andre utførelsesformer, binder antistoffene eller antigenbindende deler derav spesifikt til en epitop innenfor det C-terminale reseptorbindende domenet av toksin A, f.eks., en epitop mellom aminosyrene av toksin A, eller en epitop mellom aminosyrene , f.eks., en epitop innenfor aminosyrerestene , eller av toksin A. I andre utførelsesformer, binder antistoffene eller 20 antigenbindende deler derav spesifikt en epitop innenfor aminosyrene 1-600, , eller av toksin A. Andre spesielle antistoffer eller antigenbindende deler derav, kan spesifikt binde til en epitop innenfor aminosyrerestene 1-100, , , , , , , , , , , , , , , , , eller , , , , av toksin A eller hvilket som helst intervall, del eller område derav. I visse utførelsesformer binder antistoffene eller antigenbindende deler derav spesifikt til toksin A med en K D på mindre enn ca. 20 x 10-6 M. I en bestemt utførelsesform, binder antistoffet eller antigenbindende del derav, spesifikt til toksin A 30 med en K D på mindre enn ca. 10 x 10-7 M, mindre enn ca. 10 x 10-8 M, mindre enn ca. 10 x 10-9 M eller mindre enn ca. 10 x M. I andre bestemte utførelsesformer, binder antistoffet eller antigenbindende del derav, spesifikt til toksin A med en K D på mindre enn ca. 50 x M, mindre enn ca. 20 x M, mindre enn ca. 15 x M, mindre enn ca. 8 x M eller mindre enn ca. 5 x M.
7 6 I forskjellige andre utførelsesformer, omfatter antistoffene eller antigenbindende deler derav en variabel tung kjede region omfattende en aminosyresekvens minst 80%, 85%, 90%, 95%, 98%, 99% eller mer identisk med en variabel tung kjede region aminosyresekvens av antistoffet produsert av klon 3D8 (SEKV ID NR:1), 1B11 (SEKV ID 5 NR:2) eller 3H2 (SEKV ID NR:3). I visse utførelsesformer, omfatter antistoffene eller antigenbindende deler derav en variabel lett kjede region omfattende en aminosyresekvens minst 80%, 85%, 90%, 95%, 98%, 99% eller mer identisk med en variabel lett kjede region aminosyresekvens av antistoffet produsert av klon 3D8 (SEKV ID NR:4), 1B11 (SEKV ID NR:5) eller 3H2 10 (SEKV ID NR:6). I visse utførelsesformer, omfatter antistoffene eller antigenbindende deler derav hver både en variabel tung kjede region omfattende en aminosyresekvens minst 80%, 85%, 90%, 95%, 98%, 99% eller mer identisk med en variabel tung kjede region aminosyresekvens av antistoffet produsert av klon 3D8 (SEKV ID NR:1), 1B11 (SEKV ID 15 NR:2) eller 3H2 (SEKV ID NR:3) og en variabel lett kjede region omfattende en aminosyresekvens minst 80%, 85%, 90%, 95%, 98%, 99% eller mer identisk med en variabel lett kjede aminosyresekvens av klon 3D8 (SEKV ID NR:4), 1B11 (SEKV ID NR:5) eller 3H2 (SEKV ID NR:6). I forskjellige utførelsesformer binder antistoffene eller antigenbindende deler derav 20 spesifikt til en epitop som overlapper med en epitop bundet av et antistoff produsert av klon 3D8, 1B11 eller 3H2 og/eller konkurrerer om binding til toksin A med et antistoff produsert av klon 3D8, 1B11 eller 3H2. En variabel tung kjede region av antistoffene eller antigenbindende deler derav kan omfatte én eller flere komplementaritetsbestemmende regioner (CDR er) som er minst 80%, 85%, 25 90%, 95% eller 99% eller mer identisk med en CDR av antistoffet produsert av klon 3D8 (SEKV ID NR:7-9), 1B11(SEKV ID NR:10-12) eller 3H2 (SEKV ID NR:13-15) (også vist i Tabell 1). En variabel lett kjede region av antistoffene eller antigenbindende deler derav kan omfatte én eller flere CDR er som er minst 80%, 85%, 90%, 95% eller 99% eller mer 30 identisk med en CDR av en variabel lett kjede region av antistoffet produsert av klon 3D8 (SEKV ID NR:16-18), 1B11 (SEKV ID NR:19-21) eller 3H2 (SEKV ID NR:22-24) (også vist i Tabell 2). En variabel tung kjede region av antistoffene eller antigenbindende deler derav kan omfatte én eller flere komplementaritetsbestemmende regioner (CDR er) som er minst
8 7 80%, 85%, 90%, 95% eller 99% eller mer identisk med en CDR av antistoffet produsert av klon 3D8 (SEKV ID NR:7-9), 1B11(SEKV ID NR:10-12) eller 3H2 (SEKV ID NR:13-15) og en variabel lett kjede region av antistoffene eller antigenbindende deler derav kan omfatte én eller flere CDR er som er minst 80%, 85%, 90%, 95%, 99% eller mer identisk 5 med en CDR av en variabel lett kjede region av antistoffet produsert av klon 3D8 (SEKV ID NR:16-18), 1B11 (SEKV ID NR:19-21) eller 3H2 (SEKV ID NR:22-24). En variabel tung kjede region av antistoffene eller antigenbindende deler derav kan omfatte tre CDR er som er minst 80%, 85%, 90%, 95% eller 99% eller mer identisk med en CDR av en variabel tung kjede region av antistoffet produsert av klon 3D8 (SEKV ID 10 NR:7-9), 1B11(SEKV ID NR:10-12) eller 3H2 (SEKV ID NR:13-15). I noen utførelsesformer omfatter en variabel lett kjede region av antistoffene eller antigenbindende deler derav tre CDR er som er minst 80%, 85%, 90%, 95%, 99% eller mer identisk med en CDR av en variabel lett kjede region av antistoffet produsert av klon 3D8 (SEKV ID NR:16-18), 1B11 (SEKV ID NR:19-21) eller 3H2 (SEKV ID NR:22-24). 15 I noen utførelsesformer omfatter en variabel lett kjede region av antistoffene eller antigenbindende deler derav én eller flere CDR er som er minst 80%, 85%, 90%, 95% eller 99% eller mer identisk med en CDR av en variabel lett kjede region av antistoffet produsert av klon 3D8 (SEKV ID NR:16-18), 1B11 (SEKV ID NR:19-21) eller 3H2 (SEKV ID NR:22-24), og en variabel tung kjede region av antistoffene eller 20 antigenbindende deler derav omfatter tre CDR er som er minst 80%, 85%, 90%, 95% eller 99% eller mer identisk med en CDR av en variabel tung kjede region av antistoffet produsert av klon 3D8 (SEKV ID NR:7-9), 1B11(SEKV ID NR:10-12) eller 3H2 (SEKV ID NR:13-15). Den variable lett kjede regionen kan omfatte tre CDR er som er minst 80%, 85%, 90%, 95% eller 99% eller mer identisk med en CDR av en variabel lett kjede region 25 av antistoffet produsert av klon 3D8 (SEKV ID NR:16-18), 1B11 (SEKV ID NR:19-21) eller 3H2 (SEKV ID NR:22-24). I visse utførelsesformer omfatter en variabel tung kjede region av antistoffene eller antigenbindende deler derav tre CDR er som er identiske med en CDR av en variabel tung kjede region av antistoffet produsert av klon 3D8 (SEKV ID NR:7-9), 1B11 (SEKV ID 30 NR:10-12) eller 3H2 (SEKV ID NR:13-15), og en variabel lett kjede region av antistoffene eller antigenbindende deler derav omfatter tre CDR er som er identiske med en CDR av en variabel lett kjede region av antistoffet produsert av klon 3D8 (SEKV ID NR:16-18), 1B11 (SEKV ID NR:19-21) eller 3H2 (SEKV ID NR:22-24), f.eks., en variabel lett kjede region og variabel tung kjede region av antistoffet eller antigenbindende del derav er identisk med
9 8 en variabel lett kjede region og variabel tung kjede region av antistoffet produsert av klon 3D8 (SEKV ID NR:1, SEKV ID NR:4), 1B11 (SEKV ID NR:2, SEKV ID NR:5) eller 3H2 (SEKV ID NR:3, SEKV ID NR:6). I noen utførelsesformer nøytraliserer antistoffene eller antigenbindende deler derav 5 toksin B in vitro, hemmer binding av toksin B til mammalske celler og/eller nøytraliserer toksin B in vivo. I noen utførelsesformer binder antistoffene eller antigenbindende deler derav spesifikt til en epitop i en C-terminal del av toksin B (f.eks., mellom aminosyrene av toksin B). Andre spesielle antistoffer eller antigenbindende deler derav, kan binde 10 spesifikt til en epitop innenfor aminosyrerestene 1-100, , , , , , , , , , , , , , , , , eller av toksin B eller hvilket som helst intervall, del eller område derav. I visse utførelsesformer binder antistoffene eller antigenbindende deler derav 15 spesifikt til toksin B med en K D lavere enn ca. 20 x 10-6 M. I en bestemt utførelsesform, binder antistoffet eller antigenbindende del derav, spesifikt til toksin B med en K D på lavere enn ca. 10 x 10-7 M, lavere enn ca. 10 x 10-8 M, lavere enn ca. 10 x 10-9 M eller lavere enn ca. 10 x M. I andre spesielle utførelsesformer, binder antistoffet eller antigenbindende del derav, spesifikt til toksin B med en K D lavere enn ca. 50 x M, 20 lavere enn ca. 20 x M, lavere enn ca. 15 x M, lavere enn ca. 8 x M eller lavere enn ca. 5 x M. I forskjellige andre utførelsesformer omfatter antistoffene eller antigenbindende deler derav en variabel tung kjede region omfattende en aminosyresekvens som er minst 80%, 85%, 90%, 95%, 98%, 99% eller mer identisk med en variabel tung kjede region 25 aminosyresekvens av antistoffet produsert av klon (dvs., aminosyresekvensen vist i SEKV ID NR:54), 2A11, eller 1G10. I visse utførelsesformer omfatter antistoffene eller antigenbindende deler derav en variabel lett kjede region omfattende en aminosyresekvens som er minst 80%, 85%, 90%, 95%, 98%, 99% eller mer identisk med en variabel tung kjede region aminosyresekvens av 30 antistoffet produsert av klon (dvs., aminosyresekvensen vist i SEKV ID NR:58), 2A11, eller 1G10. I visse utførelsesformer omfatter antistoffene eller antigenbindende deler derav hver både en variabel tung kjede region omfattende en aminosyresekvens minst 80%, 85%, 90%, 95%, 98%, 99% eller mer identisk med en variabel tung kjede region
10 9 aminosyresekvens av antistoffet produsert av klon (dvs., aminosyresekvensen vist i SEKV ID NR:54), 2A11 eller 1G10 og en variabel lett kjede region omfattende en aminosyresekvens som er minst 80%, 85%, 90%, 95%, 98%, 99% eller mer identisk med en variabel lett kjede aminosyresekvens av antistoffet produsert av klon (dvs., 5 aminosyresekvensen vist i SEKV ID NR:58), 2A11, eller 1G10. I forskjellige utførelsesformer binder antistoffene eller antigenbindende deler derav spesifikt til en epitop som overlapper med en epitop bundet av et antistoff produsert av klon , 2A11 eller 1G10 og/eller konkurrerer om binding til toksin B med et antistoff produsert av klon , 2A11 eller 1G En variabel tung kjede region av antistoffene eller antigenbindende deler derav kan omfatte én eller flere komplementaritetsbestemmende regioner (CDR er) som er minst 80%, 85%, 90%, 95% eller 99% eller mer identisk med en CDR av antistoffet produsert av klon (SEKV ID NR: 62, 64 eller 66), 2A11 eller 1G10 (Tabell 3). En variabel lett kjede region av antistoffene eller antigenbindende deler derav kan 15 omfatte én eller flere komplementaritetsbestemmende regioner (CDR er) som er minst 80%, 85%, 90%, 95% eller 99% eller mer identisk med en CDR av antistoffet produsert av klon (SEKV ID NR: 68, 70 eller 72), 2A11 eller 1G10 (Tabell 4). En variabel tung kjede region av antistoffene eller antigenbindende deler derav kan omfatte én eller flere komplementaritetsbestemmende regioner (CDR er) som er minst 20 80%, 85%, 90%, 95% eller 99% eller mer identiske med en CDR av antistoffet produsert av klon (SEKV ID NR: 62, 64 eller 66), 2A11 eller 1G10, og en variabel lett kjede region av antistoffene eller antigenbindende deler derav kan omfatte én eller flere CDR er som er minst 80%, 85%, 90%, 95%, 99% eller mer identisk med en CDR av en variabel lett kjede region av antistoffet produsert av klon (SEKV ID NR: 68, eller 72), 2A11 eller 1G10. En variabel tung kjede region av antistoffene eller antigenbindende deler derav kan omfatte tre CDR er som er minst 80%, 85%, 90%, 95% eller 99% eller mer identisk med en CDR av en variabel tung kjede region av antistoffet produsert av klon (SEKV ID NR: 62, 64 eller 66), 2A11 eller 1G I visse utførelsesformer omfatter den variable lett kjede regionen av antistoffene eller antigenbindende deler derav tre CDR er som er minst 80%, 85%, 90%, 95%, 99% eller mer identisk med en CDR av en variabel lett kjede region av antistoffet produsert av klon (SEKV ID NR: 68, 70 eller 72), 2A11 eller 1G10.
11 10 I andre utførelsesformer omfatter den variable lett kjede regionen av antistoffene eller antigenbindende deler derav én eller flere CDR er som er minst 80%, 85%, 90%, 95% eller 99% eller mer identisk med en CDR av en variabel lett kjede region av antistoffet produsert av klon (SEKV ID NR: 68, 70 eller 72), 2A11 eller 1G10, og en 5 variabel tung kjede region av antistoffene eller antigenbindende deler derav omfatter tre CDR er som er minst 80%, 85%, 90%, 95% eller 99% eller mer identiske med en CDR av en variabel tung kjede region av antistoffet produsert av klon (SEKV ID NR: 62, 64 eller 66), 2A11 eller 1G10. Den variable lett kjede regionen kan omfatte tre CDR er som er minst 80%, 85%, 90%, 95% eller 99% eller mer identisk med en CDR av en 10 variabel lett kjede region av antistoffet produsert av klon (SEKV ID NR: 68, 70 eller 72), 2A11 eller 1G10. I enda andre utførelsesformer omfatter den variable tung kjede regionen av antistoffene eller antigenbindende deler derav tre CDR er som er identiske med en CDR av en variabel tung kjede region av antistoffet produsert av klon (SEKV ID NR: 62, eller 66), 2A11 eller 1G10, og en variabel lett kjede region av antistoffene eller antigenbindende deler derav omfatter tre CDR er som er identiske med en CDR av en variabel lett kjede region av antistoffet produsert av klon (SEKV ID NR: 68, 70 eller 72), 2A11 eller 1G10, f.eks., en variabel lett kjede region og variabel tung kjede region av antistoffet eller antigenbindende del derav er identisk med en variabel lett kjede 20 region og variabel tung kjede region av antistoffet produsert av klon (SEKV ID NR: 62, 64 eller 66), 2A11 eller 1G10. Antistoffene eller antigenbindende deler derav kan være fullengde antistoffer, kan omfatte et effektordomene, f.eks., et Fc-domene, kan være immunglobulin gamma isotypeantistoffer, enkeltkjede antistoffer eller Fab-fragmenter. Antistoffene eller antigenbindende 25 deler derav kan videre omfatte en farmasøytisk akseptabel bærer og/eller et merke. I forskjellige utførelsesformer er blandinger omfattende antistoffene eller antigenbindende deler derav fri for andre humane polypeptider (f.eks., de inneholder mindre enn 5% humane polypeptider forskjellig fra antistoffene eller antigenbindende deler derav). 30 I forskjellige utførelsesformer er blandinger omfattende: (a) et isolert humant monoklonalt antistoff eller antigenbindende del derav som spesifikt binder til et eksotoksin fra C. difficile; og (b) et polyklonalt antistoff eller antigenbindende del derav som spesifikt binder til et eksotoksin av C. difficile.
12 11 I én utførelsesform binder det humane monoklonale antistoffet eller antigenbindende del derav spesifikt til C. difficile toksin A og det polyklonale antistoffet eller antigenbindende del derav binder spesifikt til C. difficile toksin B. I én utførelsesform binder det humane monoklonale antistoffet eller antigenbindende del derav spesifikt til C. 5 difficile toksin B og det polyklonale antistoffet eller antigenbindende del derav binder spesifikt til C. difficile toksin A. Antistoffene kan omfatte andre trekk beskrevet her. Foreliggende oppfinnelse omfatter følgelig et farmasøytisk preparat omfattende antistoffet eller antigen bindende del derav, iføgle hvilken som helst av de foregående kravene i en farmasøytisk akseptabel bærer. 10 Foreliggende oppfinnelse omfatter videre en isolert nukleinsyre omfattende en sekvens som koder for et polypeptid som angitt i SEKV ID NR:1, SEKV ID NR:2, SEKV ID NR:3, SEKV ID NR:4, SEKV ID NR:5, SEKV ID NR:6, SEKV ID NR:54, SEKV ID NR:56, SEKV ID NR:58 eller SEKV ID NR:60. Foreliggende oppfinnelse omfatter videre en ekspresjonsvektor omfattende 15 nukleinsyren ifølge krav 22. Foreliggende oppfinnelse omfatter videre en vertscelle omfattende nukleinsyren ifølge krav 22. Foreliggende oppfinnelse omfatter videre et sett omfattende et isolert monoklonalt antistoff eller antigen bindende del derav, ifølge et hvilket som helst av de foregående 20 kravene og instruksjoner for anvendelse for behandling av C. difficile-mediert sykdom. Foreliggende oppfinnelse omfatter videre et preparat omfattende et første monoklonalt antistoff et andre monoklonalt antistoff, hvor: (a) det første antistoffet eller antigen bindende delen derav, som omfatter tung og lettkjede variable regioner som angitt i henholdsvis SEKV ID NRs:1 og 4, SEKV ID 25 NRs:2 og 5 eller SEKV ID NRs:3 og 6, og (b) den andre antistoff eller antigen bindende delen derav, som omfatter tung og lettkjede variable regioner som angitt i henholdsvis SEKV ID NRs:54 og 58. Foreliggende oppfinnelse omfatter videre anvendelse av et antistoff eller antigen bindende del derav, ifølge hvilke som helst av de foregående kravene for å produsere et 30 farmasøytisk preparat for behandling av C. difficile sykdom ved å hemme symptomene på sykdommen eller forhindre tilbakekomst av C. difficile-mediert sykdom. I et annet aspekt angår oppfinnelsen isolerte humane monoklonale antistoffer eller antigenbindende deler derav som spesifikt binder til et eksotoksin av Clostridium difficile (C. difficile), hvor antistoffene: (a) omfatter en tung kjede variabel region som er produktet
13 12 av eller avledet fra et humant VH 5-51-gen; og/eller (b) omfatter en lett kjede variabel region som er produktet av eller avledet fra et humant V A27-gen. Antistoffene eller antigenbindende deler derav også kan omfatte andre trekk beskrevet her. Det er heri beskrevet isolerte polypeptider som omfatter en antigenbindende del av 5 et antistoff produsert av hybridom klon 3D8, 1B11 eller 3H2 (også referert til her som 3D8, 1B11 og 3H2 ). Det er heri beskrevet isolerte polypeptider som omfatter en antigenbindende del av et antistoff produsert av hybridom klon , 2A11 eller 1G10 (også referert til her som , 2A11 og 1G10 ). 10 I et annet aspekt er det beskrevet isolerte monoklonale antistoffer eller antigenbindende deler derav som spesifikt binder til et eksotoksin fra C. difficile, nøytraliserer toksinet, hemmer og/eller beskytter mot C. difficile-mediert sykdom. I én utførelsesform er antistoffene eller antigenbindende deler derav mammalske (f.eks., human) antistoffer eller antigenbindende deler derav. Antistoffene eller antigenbindende 15 deler derav kan omfatte andre trekk beskrevet her. I et annet aspekt er det beskrevet blandinger omfattende: (a) et isolert humant monoklonalt antistoff eller antigenbindende del derav som spesifikt binder til C. difficile toksin A; og (b) et isolert humant monoklonalt antistoff eller antigenbindende del derav som spesifikt binder til C. difficile toksin B. 20 I et annet aspekt er det beskrevet isolerte nukleinsyrer omfattende en sekvens som koder for polypeptider minst 75%, 80%, 85%, 90%, 95%, 99% eller mer identisk med SEKV ID NR:1, 2, 3, 4, 5 eller 6; f.eks., hvor nukleinsyresekvensen er minst 75%, 80%, 85%, 90%, 95%, 99% eller mer identisk med SEKV ID NRs:38, 39, 40, 35, 36 eller 37. Det er videre beskrevets ekspresjonsvektorer omfattende en nukleinsyre som koder for et 25 polypeptid minst 75%, 80%, 85%, 90%, 95%, 99% eller mer identisk med SEKV ID NR:1, 2, 3, 4, 5 eller 6; f.eks., hvor nukleinsyresekvensen er minst 75%, 80%, 85%, 90%, 95%, 99% eller mer identisk med SEKV ID NR:38, 39, 40, 35, 36 eller 37, så vel som vertsceller, f.eks., bakterieceller, f.eks., E. coli-celler, omfattende en nukleinsyre som koder for et polypeptid minst 75%, 80%, 85%, 90%, 95%, 99% eller mer identisk med 30 SEKV ID NR:1, 2, 3, 4, 5 eller 6; f.eks., hvor nukleinsyresekvensen er minst 75%, 80%, 85%, 90%, 95%, 99% eller mer identisk med SEKV ID NR:38, 39, 40, 35, 36 eller 37. I et annet aspekt er det beskrevet isolerte nukleinsyrer omfattende en sekvens som koder for et polypeptid som er minst 75%, 80%, 85%, 90%, 95%, 99% eller mer identisk med SEKV ID NR: 54, 56, 58 eller 60, for eksempel hvor nukleinsyresekvensen er minst
14 13 75%, 80%, 85%, 90%, 95%, 99% eller mer identisk med SEKV ID NR: 55, 57, 59 eller 61. Det er også beskrevet ekspresjonsvektorer omfattende en nukleinsyre som koder for et polypeptid minst 75%, 80%, 85%, 90%, 95%, 99% eller mer identisk med SEKV ID NR: 54, 56, 58 eller 60, for eksempel hvor nukleinsyresekvensen er minst 75%, 80%, 85%, 5 90%, 95%, 99% eller mer identisk med SEKV ID NR: 55, 57, 59 eller 61. Det er videre beskrevet vertsceller, f.eks., bakterieceller, f.eks., E. coli-celler, som omfatter en nukleinsyre som koder for et polypeptid som er minst 75%, 80%, 85%, 90%, 95%, 99% eller mer identisk med SEKV ID NR: 54, 56, 58 eller 60, for eksempel hvor nukleinsyresekvensen er minst 75%, 80%, 85%, 90%, 95%, 99% eller mer identisk med 10 SEKV ID NR: 55, 57, 59 eller 61. Vertscellene kan også være eukaryote celler, f.eks., gjærceller, mammalske celler, f.eks., ovarieceller fra kinesisk hamster (CHO-celler), NS0-celler eller myelomceller. I et annet aspekt angår oppfinnelsen sett som angitt ovenfor. Settet kan omfatte instruksjoner for anvendelse for forebygging eller behandling av C. difficile-mediert 15 sykdom. Settet kan videre omfatte et polyklonalt antistoff eller antigenbindende del derav som spesifikt binder et eksotoksin fra C. difficile. I én utførelsesform binder det humane monoklonale antistoffet eller antigenbindende del derav spesifikt til C. difficiletoksin A. I én utførelsesform binder det polyklonale antistoffet eller antigenbindende delen 20 derav spesifikt til C. difficile-toksin B. Det er mulig å behandle C. difficile-sykdom hos et subjekt ved å administrere til subjektet et isolert humant monoklonalt antistoff eller antigenbindende del derav som spesifikt binder til et eksotoksin fra Clostridium difficile (C. difficile) i en mengde effektiv til å hemme C. difficile-sykdom, f.eks., C. difficile-mediert kolitt, antibiotikaassosiert 25 kolitt, C. difficile-mediert pseudomembranøs kolitt (PMC) eller diaré eller tilbakefall av C. difficile-mediert sykdom. Antistoffet eller antigenbindende del derav kan administreres, f.eks., intravenøst, intramuskulært eller subkutant, til subjektet. Antistoffet eller antigenbindende del derav kan administreres alene eller i kombinasjon med et annet terapeutisk middel, f.eks., et andre humant monoklonalt 30 antistoff eller antigenbindende del derav. I ett eksempel binder antistoffet eller antigenbindende del derav spesifikt til C. difficile toksin A og det andre humane monoklonale antistoffet eller antigenbindende del derav binder spesifikt til C. difficile toksin B. I et annet eksempel er det andre midlet et antibiotika, f.eks., vankomycin eller
15 14 metronidazol. Det andre midlet kan være polyklonalt gamma-globulin (f.eks., humant gamma-globulin). I en bestemt utførelsesform administreres et antistoff eller antigenbindende del derav som omfatter en variabel lett kjede region og en variabel tung kjede region identisk 5 med den variable lett kjede regionen og den variable tunge kjede regionen av antistoffet produsert av klon 3D8 (dvs., omfattende en variabel lett kjede region-sekvens identisk med SEKV ID NR:4 og en variabel tung kjede region-sekvens identisk med SEKV ID NR:1). I en annen utførelsesform blir dette antistoffet eller antigenbindende del derav administrert i kombinasjon med et antistoff eller antigenbindende del derav som omfatter 10 en variabel lett kjede region og en variabel tung kjede region identisk med den variable lett kjede regionen og den variable tunge kjede regionen av antistoffet produsert av klon (dvs., omfattende en variabel lett kjede region-sekvens identisk med SEKV ID NR:58 og en variabel tung kjede region-sekvens identisk med SEKV ID NR:54). I enda en annen utførelsesform blir et antistoff eller antigenbindende del produsert 15 av klon 3D8 (dvs., omfattende en variabel lett kjede region-sekvens identisk med SEKV ID NR:4 og en variabel tung kjede region-sekvens identisk med SEKV ID NR:1), administrert i kombinasjon med et antistoff eller antigenbindende del derav produsert av klon (dvs., omfattende en variabel lett kjede region-sekvens identisk med SEKV ID NR:58 og en variabel tung kjede region-sekvens identisk med SEKV ID 20 NR:54). Det er mulig å fremstille et antistoff eller antigenbindende del derav som spesifikt binder til et eksotoksin fra C. difficile, ved å immunisere et transgent ikke-humant dyr som har et genom omfattende et humant tung kjede transgen og et humant lett kjede transgen med en sammensetning som omfatter et inaktivert eksotoksin og isolering av et antistoff 25 fra dyret. Eksotoksinet kan inaktiveres, for eksempel ved behandling med UDP-dialdehyd eller ved mutasjon (f.eks., ved anvendelse av rekombinante metoder). Metoden kan videre omfatte evaluering av binding av antistoffet til eksotoksinet. Det er videre mulig å fremstille et humant monoklonalt antistoff eller antigenbindende del derav ved å tilveiebringe en nukleinsyre som koder for et humant 30 monoklonalt antistoff eller antigenbindende del derav som spesifikt binder til et eksotoksin fra C. difficile og som uttrykker nukleinsyren i en vertscelle. Det er videre beskrevet et hybridom eller transfectom omfattende en nukleinsyre som koder for antigenbindende deler (f.eks., CDR er eller variable regioner) av antistoffet produsert av klon 3D8, 1B11 eller 3H2. Hybridomet eller transfectomet kan omfatte en
16 15 nukleinsyre som koder for antigenbindende deler (f.eks., CDR er eller variable regioner) av antistoffet produsert av klon , 2A11 eller 1G10. Det er mulig å fremstille et hybridom som uttrykker et antistoff som spesifikt binder til et eksotoksin fra C. difficile ved å immunisere et transgent ikke-humant dyr som 5 har et genom som omfatter et humant tung kjede transgen og et humant lett kjede transgen, med en sammensetning som omfatter eksotoksinet, hvor toksinet er inaktivert; isolering av splenocytter fra dyret; fremstilling av hybridomer fra splenocyttene; og selektere et hybridom som gir et antistoff som spesifikt binder til eksotoksinet. Behandling av mennesker med humane monoklonale antistoffer gir mange fordeler. 10 For eksempel er antistoffene egnet til å være mindre immunogene for mennesker enn ikkehumane antistoffer. Behandlingen er rask; inaktivering av toksin kan inntreffe så snart antistoffet når infeksjonsstedene og direkte nøytraliserer de(t) sykdomsforårsakende toksinet(toksinene). Humane antistoffer lokaliseres til passende steder hos mennesker mer effektivt enn ikke-humane antistoffer. Videre er behandlingen spesifikk for C. difficile og 15 det er lite sannsynlig at den forstyrrer normal tarmflora, i motsetning til tradisjonell antibiotikabehandling. Andre trekk og fordeler ifølge oppfinnelsen vil fremgå av den følgende detaljerte beskrivelsen og fra kravene. 20 Kort beskrivelse av figurene Figur 1 er en tabell som lister opp aminosyresekvensene av VH og VL-kjedene kodet for av mrna-sekvenser fra hver klon. Små bokstaver representerer aminosyrer i lederpeptidet. CDR er er understreket. Klon 3D8, som uttrykker 6 unike lett kjede V-regioner, uttrykte bare gruppe I aminosyresekvensen. 25 Figur 2A er en representasjon av aminosyre og nukleinsyresekvensene av VL-kjeden uttrykt ved klon 3D8. Genene for V-segment og J-segment er listet opp over aminosyre og nukleinsyresekvensene. CDR ene er overstreket. Figur 2B er a representasjon av aminosyre og nukleinsyresekvensene av VH-kjeden uttrykt ved klon 3D8. Genene for V-segment, D-segment og J-segment er listet opp over 30 aminosyre og nukleinsyresekvensene. CDR ene er overstreket. Figur 3A er en representasjon av aminosyre og nukleinsyresekvensene av VL-kjeden uttrykt ved klon 1B11. Genene for V-segment og J-segment er listet opp over aminosyre og nukleinsyresekvensene. CDR ene er overstreket.
17 16 Figur 3B er en representasjon av aminosyre og nukleinsyresekvensene av VH-kjeden uttrykt ved klon 1B11. Genene for V-segment, D-segment og J-segment er listet opp over aminosyre og nukleinsyresekvensene. CDR ene er overstreket. Figur 4A er en representasjon av aminosyre og nukleinsyresekvensene av VL-kjeden 5 uttrykt ved klon 33,3H2 (referert til her som 3H2; 33,3H2 og 3H2 blir anvendt om hverandre her). Genene for V-segment og J-segment er listet opp over aminosyre og nukleinsyresekvensene. CDR ene er overstreket. Figur 4B er en representasjon av aminosyre og nukleinsyresekvensene av VH-kjeden uttrykt ved klon 33,3H2. Genene for V-segment og J-segment er listet opp over aminosyre 10 og nukleinsyresekvensene. CDR ene er overstreket. Figur 5 er en kurve som viser resultatene av ELISA-analyse, som målte binding av anti-toksin A monoklonale antistoffer til toksin A. Figurene 6A-B er et sett av kurver som viser resultater av in vitro nøytraliseringsforsøk i nærvær og fravær av anti-toksin A monoklonale antistoffer. FIG. 15 6A viser resultater for analyser utført med IMR-90-celler. FIG. 6B viser resultater for analyse utført med T-84-celler. Figur 7 er en skjematisk fremstilling av toksin A-polypeptidet, som angir fragmenter som ble analysert for epitopkartlegging-studier. Figur 8A-B er skjematiske fremstillinger av toksin A-fragmenter analysert for 20 epitopkartlegging-studier. Figur 9 er en tabell som lister opp resultatene av in vivo-analyser for å bestemme beskyttelse av mus mot letal provokasjon med toksin A ved anti-toksin A monoklonale antistoffer. Figur 10 er en kurve som viser resultatene av analyser av mus ileum løkke væske- 25 akkumulering for å måle effektivitet av nøytralisering av anti-toksin antistoff in vivo. Figur 11A er et skjematisk diagram av tidslinjen for administrering av forskjellige midler til hamstere i en hamster tilbakefall-modell. Figur 11B er en kurve som viser resultatene av analysene som prosentandelen av hamstere som overlever klindamycinbehandling fulgt av provokasjon med C. difficile. 30 Figur 12 er en kurve som viser resultater av hamster tilbakefallsanalyse som prosentandelen av hamstere som overlever klindamycinbehandling fulgt av provokasjon med C. difficile. Figur 13 er en kurve som viser resultater av analyser hvor in vitro-nøytralisering av toksin A og toksin B ble målt i nærvær og fravær av polyklonale antisera fra geiter
18 17 immunisert med toksoid B. G330 angir prøver hvor sera fra geit nr. 330 ble testet. G331 angir prøver hvor sera fra geit nr. 331 ble testet. Figur 14 er et skjematisk diagram av tidslinjen for administrering av forskjellige midler til hamstere i en hamster tilbakefall-modell. 5 Figur 15 er en kurve som viser resultatene av hamster tilbakefall-analysen som prosentandelen av hamstere som overlever klindamycinbehandling fulgt av C. difficileprovokasjon. Hamstere ble behandlet med vankomycin, vankomycin og 3D8, vankomycin og antisera fra geit nr. 331 eller vankomycin, 3D8 og antisera fra geit nr Figur 16 er en kurve som viser resultatene av hamster tilbakefalls-analyse som 10 prosentandelen av friske dyr etter klindamycinbehandling fulgt av C. difficile-provokasjon. Geit 331 angir antisera fra geit nr Figur 17 er en kurve som viser resultatene av hamster tilbakefall-analyser som prosentandelen av hamstere som overlever klindamycinbehandling fulgt av C. difficileprovokasjon. Hamstere ble immunisert med et fragment av toksin B før 15 klindamycinbehandling. Hamstere ble behandlet med vankomycin, vankomycin og 3D8 eller mottok ingen behandling. Figur 18 er en kurve som viser resultatene av hamster tilbakefallsanalyse som prosentandelen av friske dyr etter klindamycinbehandling fulgt av C. difficile provokasjon. Hamstere ble immunisert med et fragment av toksin B før klindamycinbehandling. 20 Figur 19 er et skjematisk diagram av tidslinjen for administrering av forskjellige midler til hamstere i en C. difficile direkte provokasjon-modell. 331 angir antisera fra geit nr Clinda angir behandling med klindamycin. Figur 20 er en kurve som viser resultatene av direkte provokasjonsanalyse som prosentandelen av hamstere som overlever direkte C. difficile-provokasjon. 25 Figur 21 er en kurve som viser resultatene av direkte provokasjonsanalyse som prosentandelen av friske dyr etter direkte provokasjon med C. difficile. Figur 22 er en fremstilling av aminosyresekvensen av C. difficile toksin A. Figur 23 er en fremstilling av aminosyresekvensen av C. difficile toksin B. Figur 24 er en kurve som viser resultatene av analyse av primær provokasjon som 30 prosentandelen av hamstere som overlever direkte C. difficile-provokasjon. Figur 25 er en kurve som viser resultatene av primær provokasjonsanalyse som prosentandelen av hamstere som overlever direkte C. difficile-provokasjon. Figur 26 er en kurve som viser resultatene av primær provokasjonsanalyse som prosentdelen av hamstere som overlever direkte C. difficile-provokasjon.
19 18 Figur 27 er en kurve som viser resultater av forsøk hvor in vitro nøytralisering av toksin A og toksin B ble målt i nærvær av monoklonale antistoffer mot toksin B eller geit polyklonale sera mot toksin B. Figur 28 er en fremstilling av aminosyre og nukleinsyresekvensene av VH-kjeden 5 uttrykt ved klon Genene for V-segmentet, D-segmentet og J-segmentet er listet opp over aminosyre og nukleinsyresekvensene. CDR ene er overstreket. Figur 29 er en fremstilling av aminosyre og nukleinsyresekvensene av VL-kjeden uttrykt ved klon Genene for V-segmentet og J-segmentet er listet opp over aminosyre og nukleinsyresekvensene. CDR ene er overstreket. 10 Figur 30 er en fremstilling av aminosyre og relatert kjønnscellesekvens av VH-kjeden uttrykt ved klon Genene for V-segmentet, D-segmentet og J-segmentet er listet opp over aminosyresekvensene. CDR ene er overstreket. Figur 31 er en fremstilling av aminosyre og relaterte kjønnscellesekvenser av VLkjeden uttrykt ved klon Genene for V-segmentet og J-segmentet er listet opp over 15 aminosyresekvensene. CDR ene er overstreket. Figur 32 er en skjematisk fremstilling av toksin B-polypeptidet, som angir fragmenter som ble analysert for epitopkartlegging-studier. 20 Like referansesymboler i de forskjellige figurene angir like elementer. Detaljert beskrivelse av oppfinnelsen For å gi en klar forståelse av beskrivelsen og kravene er de følgende definisjonene hensiktsmessig gitt nedenfor. 25 Definisjoner Betegnelsen toksin A refererer til toksin A-proteinet kodet for av C. difficile. Aminosyresekvensen av C. difficile toksin A (SEKV ID NR:41) er gitt i GenBank under aksesjonsnummer A37052, versjon GI (se også Figur 22). Toksin B angir toksin B-proteinet kodet for av C. difficile. Aminosyresekvensen av C. difficile toksin B (SEKV 30 ID NR: 42) er gitt i GenBank under aksesjonsnummer S70172, versjon GI (se også Figur 23). Protein anvendes om hverandre med polypeptid. Et "anti-c. difficile-antistoff" er et antistoff som interagerer med (f.eks., binder til) et protein eller annen komponent produsert av C. difficile-bakterier. Et anti-toksinantistoff er et antistoff som interagerer med et toksin produsert av C. difficile (f.eks.,
20 19 toksin A eller toksin B). Et anti-toksin protein-antistoff kan binde til en epitop, f.eks., en konformasjonell eller en lineær epitop eller til et fragment av fullengde toksin-proteinet. Et "humant antistoff," er et antistoff som har variable og konstante regioner avledet fra human kjønnscelle immunglobulinsekvenser. De humane antistoffene beskrevet her kan 5 omfatte aminosyrerester ikke kodet for av human kjønnscelle immunglobulinsekvenser (f.eks., mutasjoner innført ved tilfeldig eller setespesifikke mutagenese in vitro eller ved somatisk mutasjon in vivo). Et anti-toksin antistoff eller antigenbindende del derav, kan administreres alene eller i kombinasjon med et andre middel. Subjektet kan være en pasient infisert med C. 10 difficile eller som har et symptom på C. difficile-assosiert sykdom ( CDAD ; f.eks., diaré, kolitt, abdominal smerte) eller en predisponering for C. difficile-assosiert sykdom (f.eks., som gjennomgår behandling med antibiotika eller som har erfart C. difficile-assosiert sykdom og med risiko for tilbakefall av sykdommen). Behandlingen kan være å kurere, helbrede, lindre, lette, endre, avhjelpe, forbedre, døyve, forbedre eller påvirke infeksjonen 15 og sykdommen forbundet med infeksjonen, symptomene på sykdommen eller predisponeringen for sykdommen. En mengde av et anti-toksin antistoff effektiv for å behandle en CDAD eller en "terapeutisk effektiv mengde," er en mengde av antistoffet som er effektiv, ved administrering av enkel eller multippel dose til et subjekt, for å hemme CDAD i et subjekt. 20 En terapeutisk effektiv mengde av antistoffet eller antistoffragment kan variere i henhold til faktorer slik som sykdomstilstanden, alder, kjønn og vekt av individet og evnen av antistoffet eller antistoff-andelen til å fremkalle en ønsket respons i individet. En terapeutisk effektiv mengde er også én hvor hvilke som helst toksiske eller skadelige effekter av antistoffet eller antistoff-andelen oppveies av de terapeutisk fordelaktige 25 effektene. Evnen av et antistoff til å hemme en målbar parameter kan evalueres i et dyremodellsystem prediktiv for effektivitet hos mennesker. For eksempel evnen av et antitoksin antistoff til å beskytte mus fra letal provokasjon med C. difficile kan predikere effektivitet hos mennesker. Andre dyremodeller prediktive for effektivitet er beskrevet her, slik som tarm ligeringsmodell beskrevet i eksemplene. Alternativt kan denne egenskapen 30 av et antistoff eller antistoffblanding evalueres ved undersøkelse av forbindelsens evne til å modulere, hvor slik modulering er in vitro ved analyser kjent for fagfolk. In vitro-analyser omfatter bindingsforsøk, slik som ELISA og nøytraliseringsforsøk. En mengde av et anti-toksin antistoff effektiv for å forebygge en lidelse eller "en profylaktisk effektiv mengde," av antistoffet er en mengde som er effektiv, ved
21 20 administrering av enkelt eller multippel dose til subjektet, for å forebygge eller forsinke opptreden av oppstart eller tilbakefall av CDAD eller hemme et symptom derav. Imidlertid, dersom lengre tidsintervaller for beskyttelse er ønsket, kan økte doser administreres. 5 Betegnelsene pine, "indusere," "hemme," "forsterker," "heve," "øke," "redusere," eller lignende, f.eks., som betyr kvantitative forskjeller mellom to tilstander, refererer til en forskjell, f.eks., en statistisk eller klinisk signifikant forskjell, mellom de to tilstandene. Som anvendt her refererer "spesifikk binding'' eller spesifikt binder til evnen av et antistoff til å: (1) binde til et toksin fra C. difficile med en affinitet på minst 1 x 10 7 M og (2) binde til et toksin fra C. difficile med en affinitet som er minst to ganger høyere enn dets affinitet for et uspesifikt antigen. Et "antistoff" er et protein omfattende minst én eller to, tung (H) kjede variable regioner (forkortet her som VHC) og minst én eller to lett (L) kjede variable regioner (forkortet her som VLC). VHC og VLC-regionene kan deles ytterligere opp i regioner av 15 hypervariabilitet, betegnet "komplementaritetsbestemmende regioner" ("CDR"), innfelt med regioner som er mer konserverte, betegnet "struktur ( rammeverk ) regioner" (FR). Størrelsen av struktur ( rammeverk )-regionen og CDR ene har blitt nøyaktig definert (se Kabat, E.A., et al. Sequences of Proteins of Immunological Interest, Femte Utgave, U.S. Department of Health and Human Services, NIH Publikasjon nr , 1991 og Chotia, 20 C. et al., J. Mol. Biol. 196: , 1987). Fortrinnsvis er hver VHC og VLC sammensatt av tre CDR er og fire FR er, arrangert fra den aminoterminale til den karboksyterminale enden i den følgende rekkefølgen: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. VHC eller VLC-kjeden av antistoffet kan videre omfatte hele eller del av en tung eller lett kjede konstant region. I én utførelsesform, er antistoffet en tetramer av to tunge 25 immunglobulinkjeder og to lette immunglobulinkjeder, hvor de tunge og lette immunglobulinkjedene er innbyrdes forbundet ved, f.eks., disulfidbindinger. Den tunge kjede konstante regionen omfatter tre domener, CH1, CH2 og CH3. Den lette kjede konstante regionen er omfattet av ett domene, CL. Den variable regionen av de tunge og lette kjedene inneholder et bindende domene som interagerer med et antigen. De konstante 30 regionene av antistoffene medierer typisk bindingen av antistoffet til vertsvev eller faktorer, inkludert forskjellige celler av immunsystemet (f.eks., effektorceller) og den første komponenten (Clq) av det klassiske komplementsystemet. Betegnelsen "antistoff" omfatter intakte immunglobuliner av typene IgA, IgG, IgE, IgD, IgM (så vel som subtyper derav), hvor de lette kjedene av immunglobulinet kan være av typene kappa eller lambda.
PATENTKRAV. og en første lett kjede og en andre lett kjede, hvor første og andre lette kjeder er forskjellige.
 1 PATENTKRAV 1. Isolert monoklonalt antistoff som bærer en forskjellig spesifisitet i hvert kombinasjonssete og som består av to kopier av et enkelt tung kjede polypeptid og en første lett kjede og en
1 PATENTKRAV 1. Isolert monoklonalt antistoff som bærer en forskjellig spesifisitet i hvert kombinasjonssete og som består av to kopier av et enkelt tung kjede polypeptid og en første lett kjede og en
2. Polypeptid ifølge krav 1, hvor polypeptidet utløser en beskyttende immunrespons hos en pattedyrvert mot stammer av C.difficile.
 1 Patentkrav 1 1. Polypeptid som omfatter et første fragment og et andre fragment, hvor (i) det første fragmentet er et toksin A repeterende domenefragment; (ii) det andre fragmentet er et toksin B repeterende
1 Patentkrav 1 1. Polypeptid som omfatter et første fragment og et andre fragment, hvor (i) det første fragmentet er et toksin A repeterende domenefragment; (ii) det andre fragmentet er et toksin B repeterende
EP Patentkrav. 1. En sammensetning som omfatter:
 1 Patentkrav EP2129 1 2 3 1. En sammensetning som omfatter: et fusjonsprotein som omfatter første og andre peptid-deler, karakterisert ved at nevnte første peptid-del består av en aminosyresekvens valgt
1 Patentkrav EP2129 1 2 3 1. En sammensetning som omfatter: et fusjonsprotein som omfatter første og andre peptid-deler, karakterisert ved at nevnte første peptid-del består av en aminosyresekvens valgt
NORGE. Patentstyret (12) SØKNAD (19) NO (21) (13) A1
 (12) SØKNAD (19) NO (21) 20093386 (13) A1 NORGE (51) Int Cl. C07K 16/18 (2006.01) C07K 16/12 (2006.01) C07K 16/08 (2006.01) A61K 39/395 (2006.01) C12P 21/08 (2006.01) C12N 15/13 (2006.01) A61P 35/00 (2006.01)
(12) SØKNAD (19) NO (21) 20093386 (13) A1 NORGE (51) Int Cl. C07K 16/18 (2006.01) C07K 16/12 (2006.01) C07K 16/08 (2006.01) A61K 39/395 (2006.01) C12P 21/08 (2006.01) C12N 15/13 (2006.01) A61P 35/00 (2006.01)
EP Patentkrav
 1 EP26727 Patentkrav 1. Monoklonalt antistoff, eller et funksjonelt fragment derav som spesifikt gjenkjenner ett eller flere Siglec- polypeptider bestående av en aminosyresekvens som beskrevet i hvilket
1 EP26727 Patentkrav 1. Monoklonalt antistoff, eller et funksjonelt fragment derav som spesifikt gjenkjenner ett eller flere Siglec- polypeptider bestående av en aminosyresekvens som beskrevet i hvilket
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2131860 B1 (19) NO NORGE (51) Int Cl. A61K 39/395 (2006.01) Patentstyret (21) Oversettelse publisert 2014.03.24 (80) Dato for Den Europeiske Patentmyndighets
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2131860 B1 (19) NO NORGE (51) Int Cl. A61K 39/395 (2006.01) Patentstyret (21) Oversettelse publisert 2014.03.24 (80) Dato for Den Europeiske Patentmyndighets
Undervisning på Dialysen 27/2
 Undervisning på Dialysen 27/2 Anaerob sporedannende bakterie Tilhører tykktarmens normalflora hos 5 10 % av oss (50% hos spedbarn, 2 3% hos voksne) Bakterien dør fort utenfor tarmen, men sporene utskilles
Undervisning på Dialysen 27/2 Anaerob sporedannende bakterie Tilhører tykktarmens normalflora hos 5 10 % av oss (50% hos spedbarn, 2 3% hos voksne) Bakterien dør fort utenfor tarmen, men sporene utskilles
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2129396 B1 (19) NO NORGE (1) Int Cl. A61K 39/39 (06.01) A61P 3/00 (06.01) Patentstyret (21) Oversettelse publisert 14.01.13 (80) Dato for Den Europeiske
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2129396 B1 (19) NO NORGE (1) Int Cl. A61K 39/39 (06.01) A61P 3/00 (06.01) Patentstyret (21) Oversettelse publisert 14.01.13 (80) Dato for Den Europeiske
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2328616 B1 (19) NO NORWAY (1) Int Cl. A61K 39/39 (2006.01) C07K 16/18 (2006.01) Norwegian Industrial Property Office (21) Translation Published
(12) Translation of european patent specification (11) NO/EP 2328616 B1 (19) NO NORWAY (1) Int Cl. A61K 39/39 (2006.01) C07K 16/18 (2006.01) Norwegian Industrial Property Office (21) Translation Published
Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten
 1 Patentkrav 1. Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten omfatter: innsetting inn i et gnagercellegenom;
1 Patentkrav 1. Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten omfatter: innsetting inn i et gnagercellegenom;
Forløp av ikke-adaptiv og adaptiv immunrespons. Mononukleære celler, metylfiolett farging
 Forløp av ikke-adaptiv og adaptiv immunrespons Mononukleære celler, metylfiolett farging 1 Nøytrofile granulocytter Gjenkjennelsesprinsipper medfødt vs. adaptiv immunitet Toll Like Receptors Mikroorganismer
Forløp av ikke-adaptiv og adaptiv immunrespons Mononukleære celler, metylfiolett farging 1 Nøytrofile granulocytter Gjenkjennelsesprinsipper medfødt vs. adaptiv immunitet Toll Like Receptors Mikroorganismer
ANTI-HEPCIDINANTISTOFFER OG ANVENDELSER DERAV. Beskrivelse
 1 ANTI-HEPCIDINANTISTOFFER OG ANVENDELSER DERAV Beskrivelse 5 10 Den foreliggende oppfinnelse er innen det medisinske felt, særlig innen feltet for antistoffer mot humant modent hepcidin. Oppfinnelsen
1 ANTI-HEPCIDINANTISTOFFER OG ANVENDELSER DERAV Beskrivelse 5 10 Den foreliggende oppfinnelse er innen det medisinske felt, særlig innen feltet for antistoffer mot humant modent hepcidin. Oppfinnelsen
2. Fremgangsmåten ifølge krav 1, hvori dsrna-duplekset har en lengde fra 8 basepar (bp) ti 30 bp.
 1 Patentkrav 1. Fremgangsmåte for å endre et mål-dna, der fremgangsmåten omfatter å bringe mål-dna-et i kontakt med et kompleks omfattende: (a) et Cas9-polypeptid og (b) et enkeltmolekyl-rna som er målrettet
1 Patentkrav 1. Fremgangsmåte for å endre et mål-dna, der fremgangsmåten omfatter å bringe mål-dna-et i kontakt med et kompleks omfattende: (a) et Cas9-polypeptid og (b) et enkeltmolekyl-rna som er målrettet
Vankomycinresistente enterokokker VRE Epidemiologi/utbruddet på Haukeland Universitetssjukehus
 Vankomycinresistente enterokokker VRE Epidemiologi/utbruddet på Haukeland Universitetssjukehus Kristin Stenhaug Kilhus LIS, Mikrobiologisk avdeling Haukeland Universitetssykehus 2 Enterokokker Gram positive
Vankomycinresistente enterokokker VRE Epidemiologi/utbruddet på Haukeland Universitetssjukehus Kristin Stenhaug Kilhus LIS, Mikrobiologisk avdeling Haukeland Universitetssykehus 2 Enterokokker Gram positive
«Immunterapi» Kreftutvikling. Myelomatose. Immunterapi. Anders'Sundan Senter'for'myelomforskning Institutt'for'klinisk'og'molekylær'medisin,'NTNU
 «Immunterapi» Kreftutvikling Myelomatose Immunterapi Anders'Sundan Senter'for'myelomforskning Institutt'for'klinisk'og'molekylær'medisin,'NTNU 1 Kreft er genetiske sykdommer i den forstand at det alltid
«Immunterapi» Kreftutvikling Myelomatose Immunterapi Anders'Sundan Senter'for'myelomforskning Institutt'for'klinisk'og'molekylær'medisin,'NTNU 1 Kreft er genetiske sykdommer i den forstand at det alltid
idet, en eller flere innskuddshendelser anvender den setespesifikke rekombinasjonen,
 1 Patentkrav 1. Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten omfatter: innsetting inn i et gnagercellegenom;
1 Patentkrav 1. Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten omfatter: innsetting inn i et gnagercellegenom;
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2391650 B1 (19) NO NORGE (51) Int Cl. C07K 16/24 (2006.01) A61K 39/00 (2006.01) A61K 39/395 (2006.01) Patentstyret (21) Oversettelse publisert 2015.03.09
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2391650 B1 (19) NO NORGE (51) Int Cl. C07K 16/24 (2006.01) A61K 39/00 (2006.01) A61K 39/395 (2006.01) Patentstyret (21) Oversettelse publisert 2015.03.09
NORGE. Patentstyret (12) SØKNAD (19) NO (21) (13) A1. (51) Int Cl.
 (12) SØKNAD (19) NO (21) 171288 (13) A1 NORGE (1) Int Cl. C07K 16/18 (06.01) C07K 16/28 (06.01) A61K 39/39 (06.01) Patentstyret (21) Søknadsnr 171288 (86) Int.inng.dag og søknadsnr 0.09.02 PCT/US0/031401
(12) SØKNAD (19) NO (21) 171288 (13) A1 NORGE (1) Int Cl. C07K 16/18 (06.01) C07K 16/28 (06.01) A61K 39/39 (06.01) Patentstyret (21) Søknadsnr 171288 (86) Int.inng.dag og søknadsnr 0.09.02 PCT/US0/031401
1. En ikke-naturlig forekommende eller konstruert sammensetning omfattende:
 1 Patentkrav EP2931898 1. En ikke-naturlig forekommende eller konstruert sammensetning omfattende: et leveringssystem som er operativt konfigurert for å levere CRISPR-Caskomplekskomponenter eller polynukleotidsekvenser
1 Patentkrav EP2931898 1. En ikke-naturlig forekommende eller konstruert sammensetning omfattende: et leveringssystem som er operativt konfigurert for å levere CRISPR-Caskomplekskomponenter eller polynukleotidsekvenser
(12) Translation of european patent specification
 NO/EP20 (12) Translation of european patent specification (11) NO/EP 20 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (2006.01) A61P 3/00 (2006.01) A61P 37/00 (2006.01) Norwegian Industrial Property Office
NO/EP20 (12) Translation of european patent specification (11) NO/EP 20 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (2006.01) A61P 3/00 (2006.01) A61P 37/00 (2006.01) Norwegian Industrial Property Office
individ som lider av dette eller til å forhindre forekomst hos et risikoindivid.
 1 OPPFINNELSESOMRÅDE Foreliggende beskrivelse vedrører fremgangsmåter for behandling og/eller forebyggelse av reumatoid artritt. Slike fremgangsmåter kan benyttes til å behandle et individ som lider av
1 OPPFINNELSESOMRÅDE Foreliggende beskrivelse vedrører fremgangsmåter for behandling og/eller forebyggelse av reumatoid artritt. Slike fremgangsmåter kan benyttes til å behandle et individ som lider av
Clostridium difficile
 Clostridium difficile -antibiotikaens svøbe Jørgen Vildershøj Bjørnholt Avdeling for mikrobiologi, OUS og Institutt for klinisk medisin, UiO Disclosures: None. The author is solely responsible for the
Clostridium difficile -antibiotikaens svøbe Jørgen Vildershøj Bjørnholt Avdeling for mikrobiologi, OUS og Institutt for klinisk medisin, UiO Disclosures: None. The author is solely responsible for the
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 263813 B1 (19) NO NORWAY (1) Int Cl. C07K 16/18 (2006.01) A61K 39/39 (2006.01) A61P 37/06 (2006.01) Norwegian Industrial Property Office (21)
(12) Translation of european patent specification (11) NO/EP 263813 B1 (19) NO NORWAY (1) Int Cl. C07K 16/18 (2006.01) A61K 39/39 (2006.01) A61P 37/06 (2006.01) Norwegian Industrial Property Office (21)
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2242771 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61P 3/00 (06.01) Patentstyret (21) Oversettelse publisert 13.09. (80) Dato for Den Europeiske
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2242771 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61P 3/00 (06.01) Patentstyret (21) Oversettelse publisert 13.09. (80) Dato for Den Europeiske
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 99826 B1 (19) NO NORGE (1) Int Cl. C07K 16/18 (06.01) A61K 39/39 (06.01) A61P 2/28 (06.01) Patentstyret (21) Oversettelse publisert 14.02.17 (80)
(12) Oversettelse av europeisk patentskrift (11) NO/EP 99826 B1 (19) NO NORGE (1) Int Cl. C07K 16/18 (06.01) A61K 39/39 (06.01) A61P 2/28 (06.01) Patentstyret (21) Oversettelse publisert 14.02.17 (80)
Hva er en vaksine? Hanne Nøkleby, Nasjonalt folkehelseinstitutt
 Hva er en vaksine? Hanne Nøkleby, Nasjonalt folkehelseinstitutt Utgangspunktet Mange infeksjonssykdommer gir langvarig / livslang immunitet Vaksinering har som mål å få kroppen til å utvikle samme immunitet
Hva er en vaksine? Hanne Nøkleby, Nasjonalt folkehelseinstitutt Utgangspunktet Mange infeksjonssykdommer gir langvarig / livslang immunitet Vaksinering har som mål å få kroppen til å utvikle samme immunitet
1. Isolert protein omfattende et stabilisert aktivin IIB reseptor polypeptid, hvori polypeptidet er valgt fra gruppen bestående av:
 1 Patentkrav. 1. Isolert protein omfattende et stabilisert aktivin IIB reseptor polypeptid, hvori polypeptidet er valgt fra gruppen bestående av: (a) et polypeptid bestående av sekvensen representert ved
1 Patentkrav. 1. Isolert protein omfattende et stabilisert aktivin IIB reseptor polypeptid, hvori polypeptidet er valgt fra gruppen bestående av: (a) et polypeptid bestående av sekvensen representert ved
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2152880 B1 (19) NO NORGE (51) Int Cl. C12N 15/13 (2006.01) A01K 67/027 (2006.01) Patentstyret (21) Oversettelse publisert 2011.12.19 (80) Dato for
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2152880 B1 (19) NO NORGE (51) Int Cl. C12N 15/13 (2006.01) A01K 67/027 (2006.01) Patentstyret (21) Oversettelse publisert 2011.12.19 (80) Dato for
Polynukleotid som omfatter en nukleinsyre valgt fra gruppen som består av: a) en nukleinsyre med en nukleinsyresekvens som vist i SEKV. ID nr.
 168 PATENTKRAV 1. Polynukleotid som omfatter en nukleinsyre valgt fra gruppen som består av: a) en nukleinsyre med en nukleinsyresekvens som vist i SEKV. ID nr. 1; 5 b) en nukleinsyre som koder for et
168 PATENTKRAV 1. Polynukleotid som omfatter en nukleinsyre valgt fra gruppen som består av: a) en nukleinsyre med en nukleinsyresekvens som vist i SEKV. ID nr. 1; 5 b) en nukleinsyre som koder for et
1. Medfødt og ervervet immunitet. Karl Schenck, V2015
 1. Medfødt og ervervet immunitet Karl Schenck, V2015 Medfødt og ervervet immunforsvar Antimicrobial peptides «Alltid beredt!» Relativt uspesifikt Må aktiveres Spesifikt Komponenter av medfødt immunitet
1. Medfødt og ervervet immunitet Karl Schenck, V2015 Medfødt og ervervet immunforsvar Antimicrobial peptides «Alltid beredt!» Relativt uspesifikt Må aktiveres Spesifikt Komponenter av medfødt immunitet
Bioteknologi i dag muligheter for fremtiden
 Bioteknologi i dag muligheter for fremtiden Arvestoff Genetisk materiale, DNA. Baser En del av et nukleotid som betegnes med bokstavene A, C, G og T. Med disse fire bokstavene skriver DNAtrådene sine beskjeder
Bioteknologi i dag muligheter for fremtiden Arvestoff Genetisk materiale, DNA. Baser En del av et nukleotid som betegnes med bokstavene A, C, G og T. Med disse fire bokstavene skriver DNAtrådene sine beskjeder
Clostridium difficile - diagnostikk og epidemiologi i Norge
 Clostridium difficile - diagnostikk og epidemiologi i Norge André Ingebretsen Avd. for smittevern og Avd. for mikrobiologi Nasjonalt referanselaboratorium for Clostridium difficile Oslo universitetssykehus
Clostridium difficile - diagnostikk og epidemiologi i Norge André Ingebretsen Avd. for smittevern og Avd. for mikrobiologi Nasjonalt referanselaboratorium for Clostridium difficile Oslo universitetssykehus
EP Patentkrav. 1. En forbindelse med formel I: eller et farmasøytisk akseptabelt salt derav, hvori: R 1 er CD 3 ; og R 2 er CH 3 ;
 1 Patentkrav EP237183 1. En forbindelse med formel I: eller et farmasøytisk akseptabelt salt derav, hvori: 1 2 R 1 er CD 3 ; og R 2 er CH 3 ; for anvendelse i behandling av et individ som lider av eller
1 Patentkrav EP237183 1. En forbindelse med formel I: eller et farmasøytisk akseptabelt salt derav, hvori: 1 2 R 1 er CD 3 ; og R 2 er CH 3 ; for anvendelse i behandling av et individ som lider av eller
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2451844 B1 (19) NO NORWAY (51) Int Cl. C07K 16/28 (2006.01) Norwegian Industrial Property Office (21) Translation Published 2015.09.21 (80)
(12) Translation of european patent specification (11) NO/EP 2451844 B1 (19) NO NORWAY (51) Int Cl. C07K 16/28 (2006.01) Norwegian Industrial Property Office (21) Translation Published 2015.09.21 (80)
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2606064 B1 (19) NO NORWAY (1) Int Cl. C07K 16/00 (06.01) C07K 16/24 (06.01) C07K 16/28 (06.01) C07K 16/46 (06.01) C12N 1/ (06.01) Norwegian
(12) Translation of european patent specification (11) NO/EP 2606064 B1 (19) NO NORWAY (1) Int Cl. C07K 16/00 (06.01) C07K 16/24 (06.01) C07K 16/28 (06.01) C07K 16/46 (06.01) C12N 1/ (06.01) Norwegian
CLOSTRIDIUM DIFFICILE OG SMITTEVERN
 CLOSTRIDIUM DIFFICILE OG SMITTEVERN 19. 20. og 27. april 2016 Torunn Nygård Smittevernlege OUS Ullevål CLOSTRIDIUM DIFFICILE Gram positiv, anaerob stav Sporedanner Isolert første gang i 1935, Hall & O`Toole
CLOSTRIDIUM DIFFICILE OG SMITTEVERN 19. 20. og 27. april 2016 Torunn Nygård Smittevernlege OUS Ullevål CLOSTRIDIUM DIFFICILE Gram positiv, anaerob stav Sporedanner Isolert første gang i 1935, Hall & O`Toole
Det vedlegges et nytt kravsett som ønskes lagt til grunn for søknadens videre behandling.
 Patentstyret Postboks 8160 Dept 0033 Oslo Patentavdelingen Dato 26. mars 2014 Deres ref. 200031183 Vår ref. E29031 TFU/MJU Norsk patentsøknad nr. 20031183 Vaksine - SmithKline Beecham Biologicals SA Det
Patentstyret Postboks 8160 Dept 0033 Oslo Patentavdelingen Dato 26. mars 2014 Deres ref. 200031183 Vår ref. E29031 TFU/MJU Norsk patentsøknad nr. 20031183 Vaksine - SmithKline Beecham Biologicals SA Det
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2188312 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (06.01) A61P 3/00 (06.01) Norwegian Industrial Property Office (21) Translation Published.11.02
(12) Translation of european patent specification (11) NO/EP 2188312 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (06.01) A61P 3/00 (06.01) Norwegian Industrial Property Office (21) Translation Published.11.02
Antibiotikabruk og mikrobielle økologiske effekter
 Antibiotikabruk og mikrobielle økologiske effekter Ragnhild Raastad Oslo universitetssykehus Disposisjon I. Introduksjon II. a. Hva er økologi? b. Normalflora Antibiotikabruk og resistens a. Internasjonalt
Antibiotikabruk og mikrobielle økologiske effekter Ragnhild Raastad Oslo universitetssykehus Disposisjon I. Introduksjon II. a. Hva er økologi? b. Normalflora Antibiotikabruk og resistens a. Internasjonalt
NITO Bioingeniørfaglig Institutt kurs i Immunologi The Edge, Tromsø, 11. februar 2015. Generell Immunologi
 NITO Bioingeniørfaglig Institutt kurs i Immunologi The Edge, Tromsø, 11. februar 2015 Generell Immunologi Tor B Stuge Immunologisk forskningsgruppe, IMB Universitetet i Tromsø Innhold: 1. Immunsystemets
NITO Bioingeniørfaglig Institutt kurs i Immunologi The Edge, Tromsø, 11. februar 2015 Generell Immunologi Tor B Stuge Immunologisk forskningsgruppe, IMB Universitetet i Tromsø Innhold: 1. Immunsystemets
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2150617 B1 (19) NO NORGE (51) Int Cl. C12N 15/85 (2006.01) C12N 15/86 (2006.01) Patentstyret (21) Oversettelse publisert 2015.03.02 (80) Dato for
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2150617 B1 (19) NO NORGE (51) Int Cl. C12N 15/85 (2006.01) C12N 15/86 (2006.01) Patentstyret (21) Oversettelse publisert 2015.03.02 (80) Dato for
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2059534 B1 (19) NO NORGE (51) Int Cl. A61K 39/395 (2006.01) A61P 37/06 (2006.01) C07K 14/52 (2006.01) C07K 14/54 (2006.01) C07K 16/24 (2006.01) Patentstyret
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2059534 B1 (19) NO NORGE (51) Int Cl. A61K 39/395 (2006.01) A61P 37/06 (2006.01) C07K 14/52 (2006.01) C07K 14/54 (2006.01) C07K 16/24 (2006.01) Patentstyret
C. DIFF QUIK CHEK COMPLETE. Få hele det diagnostiske bildet med bare én test. TRYKK HER FOR Å SE NESTE SIDE
 C. DIFF QUIK CHEK COMPLETE Få hele det diagnostiske bildet med bare én test. TRYKK HER FOR Å SE SIDE KLINIKER Vil anvendelige C. difficiletestresultater på under 30 minutter bedre pasientbehandlingen?
C. DIFF QUIK CHEK COMPLETE Få hele det diagnostiske bildet med bare én test. TRYKK HER FOR Å SE SIDE KLINIKER Vil anvendelige C. difficiletestresultater på under 30 minutter bedre pasientbehandlingen?
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2336329 B1 (19) NO NORGE (51) Int Cl. C12N 15/13 (2006.01) A01K 67/027 (2006.01) Patentstyret (21) Oversettelse publisert 2013.02.04 (80) Dato for
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2336329 B1 (19) NO NORGE (51) Int Cl. C12N 15/13 (2006.01) A01K 67/027 (2006.01) Patentstyret (21) Oversettelse publisert 2013.02.04 (80) Dato for
Medikamentell Behandling
 www.printo.it/pediatric-rheumatology/no/intro Medikamentell Behandling Versjon av 2016 13. Biologiske legemidler Gjennom bruk av biologiske legemidler har nye behandlingsprinsipper mot revmatisk sykdom
www.printo.it/pediatric-rheumatology/no/intro Medikamentell Behandling Versjon av 2016 13. Biologiske legemidler Gjennom bruk av biologiske legemidler har nye behandlingsprinsipper mot revmatisk sykdom
Oppgave: MED1100-3_OPPGAVE2_H16_KONT
 Side 10 av 35 Oppgave: MED1100-3_OPPGAVE2_H16_KONT Del 1: Ola har en arvelig betinget kombinert immundefekt med mangel på både T-celler og B-celler. Ola får derfor gjentatte Hvorfor er Ola beskyttet mot
Side 10 av 35 Oppgave: MED1100-3_OPPGAVE2_H16_KONT Del 1: Ola har en arvelig betinget kombinert immundefekt med mangel på både T-celler og B-celler. Ola får derfor gjentatte Hvorfor er Ola beskyttet mot
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 26098 B1 (19) NO NORWAY (1) Int Cl. C07K 14/08 (06.01) C12Q 1/70 (06.01) Norwegian Industrial Property Office (21) Translation Published 16..24
(12) Translation of european patent specification (11) NO/EP 26098 B1 (19) NO NORWAY (1) Int Cl. C07K 14/08 (06.01) C12Q 1/70 (06.01) Norwegian Industrial Property Office (21) Translation Published 16..24
europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 217099 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61K 39/39 (06.01) A61P 3/00 (06.01) Patentstyret (21) Oversettelse publisert 14.02.17 (80)
(12) Oversettelse av europeisk patentskrift (11) NO/EP 217099 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61K 39/39 (06.01) A61P 3/00 (06.01) Patentstyret (21) Oversettelse publisert 14.02.17 (80)
PASIENTHEFTE ULCERØS KOLITT
 PASIENTHEFTE ULCERØS KOLITT INNHOLDSFORTEGNELSE Hva er ulcerøs kolitt?... 5 Symptomer... 7 Diagnose... 9 Årsaker til ulcerøs kolitt... 11 Prognose... 13 Behandling... 13 Hva kan man gjøre selv... 15 Hva
PASIENTHEFTE ULCERØS KOLITT INNHOLDSFORTEGNELSE Hva er ulcerøs kolitt?... 5 Symptomer... 7 Diagnose... 9 Årsaker til ulcerøs kolitt... 11 Prognose... 13 Behandling... 13 Hva kan man gjøre selv... 15 Hva
PASIENTHEFTE CROHNS SYKDOM
 PASIENTHEFTE CROHNS SYKDOM INNHOLDSFORTEGNELSE Hva er Crohns sykdom?... 5 Symptomer... 7 Diagnose... 9 Årsaker til Crohns sykdom... 11 Prognose... 13 Behandling... 15 3 Hva er Crohns sykdom? Crohns sykdom
PASIENTHEFTE CROHNS SYKDOM INNHOLDSFORTEGNELSE Hva er Crohns sykdom?... 5 Symptomer... 7 Diagnose... 9 Årsaker til Crohns sykdom... 11 Prognose... 13 Behandling... 15 3 Hva er Crohns sykdom? Crohns sykdom
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 26727 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (06.01) A61K 31/122 (06.01) A61K 31/32 (06.01) A61K 31/93 (06.01) A61K 31/663 (06.01) A61K 39/39
(12) Translation of european patent specification (11) NO/EP 26727 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (06.01) A61K 31/122 (06.01) A61K 31/32 (06.01) A61K 31/93 (06.01) A61K 31/663 (06.01) A61K 39/39
Flervalgsoppgaver: Immunsystemet
 Flervalgsoppgaver - immunsystemet Hver oppgave har ett riktig svaralternativ. Immunsystemet 1 Vaksinasjon der det tilføres drepte, sykdomsfremkallende virus gir A) passiv, kunstig immunitet B) aktiv kunstig,
Flervalgsoppgaver - immunsystemet Hver oppgave har ett riktig svaralternativ. Immunsystemet 1 Vaksinasjon der det tilføres drepte, sykdomsfremkallende virus gir A) passiv, kunstig immunitet B) aktiv kunstig,
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 240726 B1 (19) NO NORGE (1) Int Cl. H0K 3/36 (2006.01) H0K 3/42 (2006.01) H0K 3/46 (2006.01) Patentstyret (21) Oversettelse publisert 2014.03.17 (80)
(12) Oversettelse av europeisk patentskrift (11) NO/EP 240726 B1 (19) NO NORGE (1) Int Cl. H0K 3/36 (2006.01) H0K 3/42 (2006.01) H0K 3/46 (2006.01) Patentstyret (21) Oversettelse publisert 2014.03.17 (80)
Forelesninger i BI Cellebiologi. Denaturering og renaturering. Figure 3-13
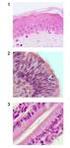 Figure 3.9 Denaturering og renaturering Figure 3-13 Denaturering og renaturering Figure 3-14 Viser tre trinn i refolding av et protein som har vært denaturert. Molten globule -formen er en intermediær
Figure 3.9 Denaturering og renaturering Figure 3-13 Denaturering og renaturering Figure 3-14 Viser tre trinn i refolding av et protein som har vært denaturert. Molten globule -formen er en intermediær
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2173379 B1 (19) NO NORWAY (1) Int Cl. A61K 39/39 (2006.01) Norwegian Industrial Property Office (21) Translation Published 2016.01.2 (80) Date
(12) Translation of european patent specification (11) NO/EP 2173379 B1 (19) NO NORWAY (1) Int Cl. A61K 39/39 (2006.01) Norwegian Industrial Property Office (21) Translation Published 2016.01.2 (80) Date
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 11 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61K 39/39 (06.01) Patentstyret (21) Oversettelse publisert 1.02.02 (80) Dato for Den Europeiske
(12) Oversettelse av europeisk patentskrift (11) NO/EP 11 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61K 39/39 (06.01) Patentstyret (21) Oversettelse publisert 1.02.02 (80) Dato for Den Europeiske
Nytte av prokalsitonin og nøytrofil CD64 som markør for postoperativ infeksjon
 Nytte av prokalsitonin og nøytrofil CD64 som markør for postoperativ infeksjon Kurs i hematologi 18. 19. mai 2015 KS møtesenter, Oslo Kristin Husby, Spesialbioingeniør Prosjektet er utført ved Tverrfaglig
Nytte av prokalsitonin og nøytrofil CD64 som markør for postoperativ infeksjon Kurs i hematologi 18. 19. mai 2015 KS møtesenter, Oslo Kristin Husby, Spesialbioingeniør Prosjektet er utført ved Tverrfaglig
Preparatomtale (SPC) 2 KVALITATIV OG KVANTITATIV SAMMENSETNING En dose à 0,5 ml inneholder: Vi polysakkarid fra Salmonella typhi
 1 LEGEMIDLETS NAVN Preparatomtale (SPC) Typherix 25 mikrogram/0,5 ml, injeksjonsvæske, oppløsning. Vaksine mot tyfoidfeber (Vi polysakkarid) 2 KVALITATIV OG KVANTITATIV SAMMENSETNING En dose à 0,5 ml inneholder:
1 LEGEMIDLETS NAVN Preparatomtale (SPC) Typherix 25 mikrogram/0,5 ml, injeksjonsvæske, oppløsning. Vaksine mot tyfoidfeber (Vi polysakkarid) 2 KVALITATIV OG KVANTITATIV SAMMENSETNING En dose à 0,5 ml inneholder:
Viktig sikkerhetsinformasjon for helsepersonell
 Viktig sikkerhetsinformasjon for helsepersonell Hemlibra (emicizumab) Subkutan injeksjon Dette materiellet beskriver viktige risikominimeringstiltak. Se preparatomtalen (SPC) for Hemlibra for ytterligere
Viktig sikkerhetsinformasjon for helsepersonell Hemlibra (emicizumab) Subkutan injeksjon Dette materiellet beskriver viktige risikominimeringstiltak. Se preparatomtalen (SPC) for Hemlibra for ytterligere
1 FYS3710 Immunologi
 1 2 Immunsystemet Dette kan best sammenlignes med et allestedsnærværende geriljaforsvar mot fremmede molekyler 3 Definisjoner av begreper. Infeksjon: Invasjon i kroppen av infeksiøse agens. Disse omfatter
1 2 Immunsystemet Dette kan best sammenlignes med et allestedsnærværende geriljaforsvar mot fremmede molekyler 3 Definisjoner av begreper. Infeksjon: Invasjon i kroppen av infeksiøse agens. Disse omfatter
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2068887 B1 (19) NO NORGE (51) Int Cl. A61K 31/70 (2006.01) A61K 38/16 (2006.01) A61K 39/395 (2006.01) A61P 25/00 (2006.01) C07H 21/00 (2006.01) C07K
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2068887 B1 (19) NO NORGE (51) Int Cl. A61K 31/70 (2006.01) A61K 38/16 (2006.01) A61K 39/395 (2006.01) A61P 25/00 (2006.01) C07H 21/00 (2006.01) C07K
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 213917 B1 (19) NO NORGE (1) Int Cl. A61K 4/06 (06.01) A61K 31/36 (06.01) A61K 38/19 (06.01) A61P 37/06 (06.01) Patentstyret (21) Oversettelse publisert
(12) Oversettelse av europeisk patentskrift (11) NO/EP 213917 B1 (19) NO NORGE (1) Int Cl. A61K 4/06 (06.01) A61K 31/36 (06.01) A61K 38/19 (06.01) A61P 37/06 (06.01) Patentstyret (21) Oversettelse publisert
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 076 B1 (19) NO NORGE (1) Int Cl. C07K 16/46 (06.01) C07K 16/ (06.01) C07K 16/24 (06.01) Patentstyret (21) Oversettelse publisert 12.11.0 (80) Dato
(12) Oversettelse av europeisk patentskrift (11) NO/EP 076 B1 (19) NO NORGE (1) Int Cl. C07K 16/46 (06.01) C07K 16/ (06.01) C07K 16/24 (06.01) Patentstyret (21) Oversettelse publisert 12.11.0 (80) Dato
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2222697 B1 (19) NO NORGE (1) Int Cl. C07K 14/70 (06.01) Patentstyret (21) Oversettelse publisert 13.04.29 (80) Dato for Den Europeiske Patentmyndighets
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2222697 B1 (19) NO NORGE (1) Int Cl. C07K 14/70 (06.01) Patentstyret (21) Oversettelse publisert 13.04.29 (80) Dato for Den Europeiske Patentmyndighets
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2178916 B1 (19) NO NORGE (51) Int Cl. C07K 16/28 (2006.01) A61K 39/395 (2006.01) A61P 35/00 (2006.01) Patentstyret (21) Oversettelse publisert 2015.05.11
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2178916 B1 (19) NO NORGE (51) Int Cl. C07K 16/28 (2006.01) A61K 39/395 (2006.01) A61P 35/00 (2006.01) Patentstyret (21) Oversettelse publisert 2015.05.11
Mikrobiologiske prøver ved borreliose i allmennpraksis. Nils Grude Avd. ovl. Mikrobiologisk avd. SiV, Tønsberg
 Mikrobiologiske prøver ved borreliose i allmennpraksis Nils Grude Avd. ovl. Mikrobiologisk avd. SiV, Tønsberg Diagnostikk i lab.: Dyrkning Nukleinsyre amplifikasjon Serologi ELISA/CLIA Immunoblot Indikasjon,
Mikrobiologiske prøver ved borreliose i allmennpraksis Nils Grude Avd. ovl. Mikrobiologisk avd. SiV, Tønsberg Diagnostikk i lab.: Dyrkning Nukleinsyre amplifikasjon Serologi ELISA/CLIA Immunoblot Indikasjon,
PEPTIDER FOR VAKSINER MOT BJØRKEALLERGI
 PEPTIDER FOR VAKSINER MOT BJØRKEALLERGI 1 P a t e n t k r a v 1. Sammensetning egnet for anvendelse ved forebygging eller behandling av allergi mot bjørkepollen omfattende: i) polypeptidet ifølge SEQ ID
PEPTIDER FOR VAKSINER MOT BJØRKEALLERGI 1 P a t e n t k r a v 1. Sammensetning egnet for anvendelse ved forebygging eller behandling av allergi mot bjørkepollen omfattende: i) polypeptidet ifølge SEQ ID
Klinisk molekylærmedisin (5): Eksempler på funksjonelle analyser
 Pediatrisk Endokrinologi 2003;17: 64-69 Klinisk molekylærmedisin (5): Eksempler på funksjonelle analyser Pål Rasmus Njølstad 1,2,3, Lise Bjørkhaug 1 1 Seksjon for pediatri, Institutt for klinisk medisin
Pediatrisk Endokrinologi 2003;17: 64-69 Klinisk molekylærmedisin (5): Eksempler på funksjonelle analyser Pål Rasmus Njølstad 1,2,3, Lise Bjørkhaug 1 1 Seksjon for pediatri, Institutt for klinisk medisin
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2193803 B1 (19) NO NORGE (51) Int Cl. A61K 39/00 (2006.01) C12N 15/13 (2006.01) Patentstyret (21) Oversettelse publisert 2012.02.13 (80) Dato for
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2193803 B1 (19) NO NORGE (51) Int Cl. A61K 39/00 (2006.01) C12N 15/13 (2006.01) Patentstyret (21) Oversettelse publisert 2012.02.13 (80) Dato for
MENVEO vaksine mot meningokokkinfeksjon gruppe A, C, W135 og Y (konjugert)
 MENVEO vaksine mot meningokokkinfeksjon gruppe A, C, W135 og Y (konjugert) Christian Syvertsen, Seksjon for biologiske legemidler og vaksiner September 2010. Menveo godkjent i sentral prosedyre (EU) European
MENVEO vaksine mot meningokokkinfeksjon gruppe A, C, W135 og Y (konjugert) Christian Syvertsen, Seksjon for biologiske legemidler og vaksiner September 2010. Menveo godkjent i sentral prosedyre (EU) European
'1$YDNVLQHUÃHQÃQ\ÃYDNVLQDVMRQVVWUDWHJLÃ
 '1$YDNVLQHUÃHQÃQ\ÃYDNVLQDVMRQVVWUDWHJLÃ $XGXQÃ1HUODQGÃ 'HWÃHUÃLQJHQÃWYLOÃRPÃDWÃYDNVLQHULQJÃHUÃHQÃDYÃKRYHGJUXQQHQHÃWLOÃDWÃILVNHRSSGUHWWÃ KDUÃYRNVWÃWLOÃHQÃDYÃ1RUJHVÃVW UVWHÃQ ULQJHUÃLÃO SHWÃDYÃGHÃVLVWHÃÃnUHQHÃ7UDVVÃLÃ
'1$YDNVLQHUÃHQÃQ\ÃYDNVLQDVMRQVVWUDWHJLÃ $XGXQÃ1HUODQGÃ 'HWÃHUÃLQJHQÃWYLOÃRPÃDWÃYDNVLQHULQJÃHUÃHQÃDYÃKRYHGJUXQQHQHÃWLOÃDWÃILVNHRSSGUHWWÃ KDUÃYRNVWÃWLOÃHQÃDYÃ1RUJHVÃVW UVWHÃQ ULQJHUÃLÃO SHWÃDYÃGHÃVLVWHÃÃnUHQHÃ7UDVVÃLÃ
Oppgave: MED1100-3_OPPGAVE2_V18_ORD
 Side 15 av 46 Oppgave: MED1100-3_OPPGAVE2_V18_ORD Del 1: Hvilke av de følgende celler uttrykker normalt (i hvilende tilstand) HLA klasse II molekyler hos mennesket? Angi de tre riktigste svarene. Fibroblaster
Side 15 av 46 Oppgave: MED1100-3_OPPGAVE2_V18_ORD Del 1: Hvilke av de følgende celler uttrykker normalt (i hvilende tilstand) HLA klasse II molekyler hos mennesket? Angi de tre riktigste svarene. Fibroblaster
Inaktiverte hele bakterieceller av Haemophilus parasuis serotype 5, stamme 4800: 0,05 mg total nitrogen, induserer 9,1 ELISA enheter *.
 1. VETERINÆRPREPARATETS NAVN Porcilis Glässer Vet. injeksjonsvæske, suspensjon til gris 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 dose (2 ml) inneholder: Virkestoff(er): Inaktiverte hele bakterieceller
1. VETERINÆRPREPARATETS NAVN Porcilis Glässer Vet. injeksjonsvæske, suspensjon til gris 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 dose (2 ml) inneholder: Virkestoff(er): Inaktiverte hele bakterieceller
Informasjon om CDI. (Clostridium difficile-infeksjon) til pasienter og pårørende
 Informasjon om CDI (Clostridium difficile-infeksjon) til pasienter og pårørende N oen bakterier er livsviktige for vår eksistens. Alle mennesker har sin egen sammensetning av bakterier som lever i symbiose
Informasjon om CDI (Clostridium difficile-infeksjon) til pasienter og pårørende N oen bakterier er livsviktige for vår eksistens. Alle mennesker har sin egen sammensetning av bakterier som lever i symbiose
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2197903 B1 (19) NO NORGE (1) Int Cl. C07K 14/21 (06.01) A61K 38/16 (06.01) C07K 19/00 (06.01) C12N 1/11 (06.01) C12N 1/62 (06.01) Patentstyret (21)
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2197903 B1 (19) NO NORGE (1) Int Cl. C07K 14/21 (06.01) A61K 38/16 (06.01) C07K 19/00 (06.01) C12N 1/11 (06.01) C12N 1/62 (06.01) Patentstyret (21)
FORBEDRET HUMANISERT ANTI-HUMANT
 FORBEDRET HUMANISERT ANTI-HUMANT alfa9-integrin-antistoff 1 10 Den foreliggende oppfinnelsen vedrører et forbedret humanisert anti-humant a9- integrin-antistoff som definert ved de medfølgende kravene.
FORBEDRET HUMANISERT ANTI-HUMANT alfa9-integrin-antistoff 1 10 Den foreliggende oppfinnelsen vedrører et forbedret humanisert anti-humant a9- integrin-antistoff som definert ved de medfølgende kravene.
6. Antistoffklasser og deres funksjon Komplementsystemet. Immunisering. Hypersensitivitet. Toleranse.
 Immunologi 3. semester, V2015 6. Antistoffklasser og deres funksjon Komplementsystemet. Immunisering. Hypersensitivitet. Toleranse. Karl Schenck Institutt for oral biologi Antistoffklasser og deres funksjon
Immunologi 3. semester, V2015 6. Antistoffklasser og deres funksjon Komplementsystemet. Immunisering. Hypersensitivitet. Toleranse. Karl Schenck Institutt for oral biologi Antistoffklasser og deres funksjon
Sammenligningen mellom Arabidopsis thaliana genomet og de kjente genomene fra cyanobakterier, gjær, bananflue og nematode, viser bl. a.
 Sammenligningen mellom Arabidopsis thaliana genomet og de kjente genomene fra cyanobakterier, gjær, bananflue og nematode, viser bl. a. Antall gener som er involvert i cellulær kommunikasjon og signaloverføring
Sammenligningen mellom Arabidopsis thaliana genomet og de kjente genomene fra cyanobakterier, gjær, bananflue og nematode, viser bl. a. Antall gener som er involvert i cellulær kommunikasjon og signaloverføring
Barn påp. reise. 8. sept. 2006 Harald Hauge overlege
 Barn påp reise 8. sept. 2006 Harald Hauge overlege Risiko for alvorlig infeksjoner hos de minste barnna NORMENN PÅ REISE ÅR 2006 Ca. 1,2 mill. nordmenn dro ut av Norge juli med fly!! 1 av 3 blir syke på
Barn påp reise 8. sept. 2006 Harald Hauge overlege Risiko for alvorlig infeksjoner hos de minste barnna NORMENN PÅ REISE ÅR 2006 Ca. 1,2 mill. nordmenn dro ut av Norge juli med fly!! 1 av 3 blir syke på
ARBEIDSGRUPPE HELSEDIREKTORATET. Testing: ELISA OG WESTERN BLOT (Immunoblot) Min konklusjon
 ARBEIDSGRUPPE HELSEDIREKTORATET Testing: ELISA OG WESTERN BLOT (Immunoblot) En moderne Western blot som baserer seg på rekombinante in vivo antigener er å foretrekke da en her bruker spesifikke antigener
ARBEIDSGRUPPE HELSEDIREKTORATET Testing: ELISA OG WESTERN BLOT (Immunoblot) En moderne Western blot som baserer seg på rekombinante in vivo antigener er å foretrekke da en her bruker spesifikke antigener
europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 224064 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) Patentstyret (21) Oversettelse publisert 14.12.1 (80) Dato for Den Europeiske Patentmyndighets
(12) Oversettelse av europeisk patentskrift (11) NO/EP 224064 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) Patentstyret (21) Oversettelse publisert 14.12.1 (80) Dato for Den Europeiske Patentmyndighets
Influensavaksiner - fra produksjon til injeksjon
 Influensavaksiner - fra produksjon til injeksjon Kine Willbergh og Hilde Bakke Avdeling for vaksine Vaksinedagene 7.-8. september 2006 1 Disposisjon Influensavaksiner, ulike typer» Levende, svekket vaksine
Influensavaksiner - fra produksjon til injeksjon Kine Willbergh og Hilde Bakke Avdeling for vaksine Vaksinedagene 7.-8. september 2006 1 Disposisjon Influensavaksiner, ulike typer» Levende, svekket vaksine
VIKTIG SIKKERHETSINFORMASJON TIL FORSKRIVER
 VIKTIG SIKKERHETSINFORMASJON TIL FORSKRIVER CIMZIA Denne veiledningen har til hensikt å informere legene om hvordan bruken av CIMZIA kan optimaliseres, og den gir spesifikke anbefalinger for bruk og kontraindikasjoner
VIKTIG SIKKERHETSINFORMASJON TIL FORSKRIVER CIMZIA Denne veiledningen har til hensikt å informere legene om hvordan bruken av CIMZIA kan optimaliseres, og den gir spesifikke anbefalinger for bruk og kontraindikasjoner
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2379600 B1 (19) NO NORGE (1) Int Cl. C07K 16/38 (06.01) A61K 39/39 (06.01) A61P 7/04 (06.01) Patentstyret (21) Oversettelse publisert 14.06.23 (80)
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2379600 B1 (19) NO NORGE (1) Int Cl. C07K 16/38 (06.01) A61K 39/39 (06.01) A61P 7/04 (06.01) Patentstyret (21) Oversettelse publisert 14.06.23 (80)
(19) NO (11) 327303 (13) B1
 (12) PATENT (19) NO (11) 327303 (13) B1 NORGE (1) Int Cl. A61K 31/07 (06.01) A61K 31/122 (06.01) A61P 1/04 (06.01) Patentstyret (21) Søknadsnr 199949 (86) Int.inng.dag og søknadsnr 1998.02.0 PCT/EP98/00628
(12) PATENT (19) NO (11) 327303 (13) B1 NORGE (1) Int Cl. A61K 31/07 (06.01) A61K 31/122 (06.01) A61P 1/04 (06.01) Patentstyret (21) Søknadsnr 199949 (86) Int.inng.dag og søknadsnr 1998.02.0 PCT/EP98/00628
Biola Dokumentert effekt på magen. Ved Marianne Hope Abel Ernæringsrådgiver i TINE BA
 Biola Dokumentert effekt på magen Ved Marianne Hope Abel Ernæringsrådgiver i TINE BA Probiotika på markedet Ulike typer bakterier Ulik mengde bakterier Varierende dokumentasjon Probiotiske produkter fra
Biola Dokumentert effekt på magen Ved Marianne Hope Abel Ernæringsrådgiver i TINE BA Probiotika på markedet Ulike typer bakterier Ulik mengde bakterier Varierende dokumentasjon Probiotiske produkter fra
Hvor farlig er det å puste inn bioaerosoler?
 Hvor farlig er det å puste inn bioaerosoler? Symptomer og sykdom ved eksponering for bioaerosoler Helse effekter Infeksjon Patogener Toksiske effekter Mykotoksiner Inflammasjon Uspesifikt medfødt immunforsvar
Hvor farlig er det å puste inn bioaerosoler? Symptomer og sykdom ved eksponering for bioaerosoler Helse effekter Infeksjon Patogener Toksiske effekter Mykotoksiner Inflammasjon Uspesifikt medfødt immunforsvar
Generell immunologi og immunforsvaret på 45 minutt
 Generell immunologi og immunforsvaret på 45 minutt NITO BIOINGENIØRFAGLIG INSTITUTT, Immunologi og immunologiske metoder, etterutdanningskurs 27. 28.november 2018 Kirsti Hokland bioingeniør og universitetslektor
Generell immunologi og immunforsvaret på 45 minutt NITO BIOINGENIØRFAGLIG INSTITUTT, Immunologi og immunologiske metoder, etterutdanningskurs 27. 28.november 2018 Kirsti Hokland bioingeniør og universitetslektor
 www.printo.it/pediatric-rheumatology/no/intro PAPA SYNDROM Versjon av 2016 1. HVA ER PAPA 1.1 Hva er det? Forkortelsen PAPA står for pyogen artritt (leddbetennelse), pyoderma gangrenosum og akne. Det er
www.printo.it/pediatric-rheumatology/no/intro PAPA SYNDROM Versjon av 2016 1. HVA ER PAPA 1.1 Hva er det? Forkortelsen PAPA står for pyogen artritt (leddbetennelse), pyoderma gangrenosum og akne. Det er
Anti-CD79b-antistoffer og -immunkonjugater og fremgangsmåter for anvendelse
 1 Anti-CD79b-antistoffer og -immunkonjugater og fremgangsmåter for anvendelse Beskrivelse OPPFINNELSENS OMRÅDE Den foreliggende oppfinnelse angår stoffsammensetninger som er nyttige for behandling av hematopoietisk
1 Anti-CD79b-antistoffer og -immunkonjugater og fremgangsmåter for anvendelse Beskrivelse OPPFINNELSENS OMRÅDE Den foreliggende oppfinnelse angår stoffsammensetninger som er nyttige for behandling av hematopoietisk
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2176 B1 (19) NO NORWAY (1) Int Cl. A01K 67/027 (06.01) C07K 16/00 (06.01) C07K 16/46 (06.01) C12N 1/8 (06.01) Norwegian Industrial Property
(12) Translation of european patent specification (11) NO/EP 2176 B1 (19) NO NORWAY (1) Int Cl. A01K 67/027 (06.01) C07K 16/00 (06.01) C07K 16/46 (06.01) C12N 1/8 (06.01) Norwegian Industrial Property
ANTISTOFFER MOT NERVEVEKSTFAKTOR (NGF) MED FORBEDRET STABILITET IN VIVO
 1 ANTISTOFFER MOT NERVEVEKSTFAKTOR (NGF) MED FORBEDRET STABILITET IN VIVO Bakgrunn for oppfinnelsen 1 Nervevekstfaktor (nerve growth factor, NGF) er et utskilt protein som ble oppdaget for over 0 år siden
1 ANTISTOFFER MOT NERVEVEKSTFAKTOR (NGF) MED FORBEDRET STABILITET IN VIVO Bakgrunn for oppfinnelsen 1 Nervevekstfaktor (nerve growth factor, NGF) er et utskilt protein som ble oppdaget for over 0 år siden
7.Rostafuroksinet for anvendelse ifølge hvilket som helst av kravene 1 til 6,
 Patentkrav 1.Rostafuroksin for anvendelse ved behandling eller forebygging av en kardiovaskulær tilstand hos et individ hvori individet er blitt valgt til å være en bærer av: minst én polymorfisme valgt
Patentkrav 1.Rostafuroksin for anvendelse ved behandling eller forebygging av en kardiovaskulær tilstand hos et individ hvori individet er blitt valgt til å være en bærer av: minst én polymorfisme valgt
DOBBELTSKRÅNENDE BAUGTANK FOR NLG-FARTØY
 DOBBELTSKRÅNENDE BAUGTANK FOR NLG-FARTØY 1 Oppfinnelsens tekniske område Den foreliggende oppfinnelsen vedrører fremstilling av tette og varmeisolerte tanker integrert i en bæresktruktur, særlig skroget
DOBBELTSKRÅNENDE BAUGTANK FOR NLG-FARTØY 1 Oppfinnelsens tekniske område Den foreliggende oppfinnelsen vedrører fremstilling av tette og varmeisolerte tanker integrert i en bæresktruktur, særlig skroget
Viktig sikkerhetsinformasjon
 Viktig sikkerhetsinformasjon Din veiledning om YERVOY for YERVOY TM Informasjonsbrosjyre pasientertil pasient Dette opplæringsmateriellet er et obligatorisk vilkår for markedsføringstillatelsen for å minske
Viktig sikkerhetsinformasjon Din veiledning om YERVOY for YERVOY TM Informasjonsbrosjyre pasientertil pasient Dette opplæringsmateriellet er et obligatorisk vilkår for markedsføringstillatelsen for å minske
Viktig informasjon for pasienter
 Ditt navn: Din adresse: Ditt telefonnummer: Din leges navn: _ Din leges adresse: _ Behandling av psoriasis med Stelara Viktig informasjon for pasienter Din leges telefonnummer: _ Her kan du notere legens
Ditt navn: Din adresse: Ditt telefonnummer: Din leges navn: _ Din leges adresse: _ Behandling av psoriasis med Stelara Viktig informasjon for pasienter Din leges telefonnummer: _ Her kan du notere legens
Epigenetikk; arvesynden i ny innpakning? Dag O. Hessen University of Oslo, Dept. Biology Center of Ecological and Evolutionary Synthesis (CEES)
 Epigenetikk; arvesynden i ny innpakning? Dag O. Hessen University of Oslo, Dept. Biology Center of Ecological and Evolutionary Synthesis (CEES) Den genetiske kode Oppnøstingen av den genetiske kode foregikk
Epigenetikk; arvesynden i ny innpakning? Dag O. Hessen University of Oslo, Dept. Biology Center of Ecological and Evolutionary Synthesis (CEES) Den genetiske kode Oppnøstingen av den genetiske kode foregikk
Hva er myelomatose? Hva er immunterapi?
 Hva er myelomatose? Hva er immunterapi? Anders Sundan Senter for myelomforskning KREFTFORENINGEN 1 Kreft er genetiske sykdommer i den forstand at det alltid er genetiske forandringer (mutasjoner) i kreftcellene
Hva er myelomatose? Hva er immunterapi? Anders Sundan Senter for myelomforskning KREFTFORENINGEN 1 Kreft er genetiske sykdommer i den forstand at det alltid er genetiske forandringer (mutasjoner) i kreftcellene
Trenger vi mer eller mindre forsøksfisk?
 Trenger vi mer eller mindre forsøksfisk? Trenger vi mer eller mindre forsøksfisk? Nasjonal plattform for alternativer Renate Johansen renate.johansen@veths.no Ja, vi trenger mer forsøksfisk for å løse
Trenger vi mer eller mindre forsøksfisk? Trenger vi mer eller mindre forsøksfisk? Nasjonal plattform for alternativer Renate Johansen renate.johansen@veths.no Ja, vi trenger mer forsøksfisk for å løse
Immunstimulanter for potensiering av torskens naturlige immunsystem
 Store programmer HAVBRUK - En næring i vekst Faktaark www.forskningsradet.no/havbruk Immunstimulanter for potensiering av torskens naturlige immunsystem Prosjekt: Immunostimulation of Atlantic cod (Gadus
Store programmer HAVBRUK - En næring i vekst Faktaark www.forskningsradet.no/havbruk Immunstimulanter for potensiering av torskens naturlige immunsystem Prosjekt: Immunostimulation of Atlantic cod (Gadus
