EP Patentkrav. 1. En sammensetning som omfatter:
|
|
|
- Unni Ervik
- 7 år siden
- Visninger:
Transkript
1 1 Patentkrav EP En sammensetning som omfatter: et fusjonsprotein som omfatter første og andre peptid-deler, karakterisert ved at nevnte første peptid-del består av en aminosyresekvens valgt fra: villtype-b7- DC, en aminosyresekvens som har minst 98 % identitet til aminosyrene -221 eller -121 av SEQ ID NO: 1, og som konkurrerer in vitro med villtype-b7-dc for binding til PD-1, et fragment av B7-DC som konkurrerer in vitro med villtype-b7-dc for binding til PD-1, og et ekstracellulært domene av B7-DC og nevnte andre peptid-del som omfatter en del av et immunoglobulin (Ig); hvor mennesket er én til hvem en sammensetning som omfatter et potenserende middel valgt fra gruppen bestående av: cyklofosfamid, en analog av cyklofosfamid, sunitinib, anti-tgffi, imatinib, antracykliner, oksaliplatin og doksorubicin, og hvor dosen av potenserende middel er ikke effektiv til å ha direkte anti-tumoraktivitet, er tidligere blitt administrert; og hvor T-celleresponsen oppnådd etter administrering av fusjonsproteinet er større enn T-celleresponsen oppnådd ved å administrere enten fusjonsprotein alene eller det potenserende middel alene. 2. Sammensetning omfattende et potenserende middel valgt fra gruppen bestående av: cyklofosfamid, en analog av cyklofosfamid, sunitinib, anti-tgffi, imatinib, antracykliner, oksaliplatin og doksorubicin, karakterisert ved at doseringen av det potenserende middel ikke er effektivt til å ha direkte anti-tumoraktivitet; hvor mennesket er én til hvem en sammensetning som omfatter et fusjonsprotein som omfatter første og andre peptid-deler, hvor nevnte første peptid-del består av en aminosyresekvens valgt fra: villtype-b7-dc, en aminosyresekvens som har minst 98 % identitet til aminosyrene -221 eller -121 av SEQ ID NO: 1, og som konkurrerer in vitro med villtype-b7-dc for binding til PD-1, et fragment av B7-DC som konkurrerer in vitro med villtype-b7- DC for binding til PD-1, og et ekstracellulært domene av B7-DC og nevnte andre peptid-del som omfatter en del av en immunoglobulin (Ig), deretter skal administreres; og hvor T-celleresponsen oppnådd etter administrering av fusjonsproteinet er større
2 2 enn T-celleresponsen oppnådd ved å administrere enten fusjonsproteinet alene eller det potenserende middel alene. 3. Sammensetning for anvendelse i henhold til krav 1 eller 2, hvor nevnte første peptid-del består av et villtype-b7-dc-polypeptid. 4. Sammensetning for anvendelse i henhold til krav 3, hvor nevnte B7-DC er et humant B7-DC Sammensetning for anvendelse i henhold til krav 1 eller 2, hvor nevnte første peptid-del består av et fragment av B7-DC som ikke utgjør noen del av den transmembrane del av nevnte B7-DC-polypeptid. 6. Sammensetning for anvendelse i henhold til krav, hvor nevnte første peptid-del består av den oppløselige del av nevnte B7-DC-polypeptid og nevnte andre peptid-del omfatter Fc-regionen til et antistoff, men omfatter ikke noe av den variable region av nevnte antistoff. 7. Sammensetning for anvendelse i henhold til krav eller 6, hvor nevnte første peptid-del består av aminosyresekvensen i SEQ ID NO: 3, og at nevnte andre polypeptid-del omfatter Fc-regionen til et antistoff, men omfatter ikke noe av den variable region av nevnte antistoff. 8. Sammensetning for anvendelse i henhold til krav 1 eller 2, hvor nevnte første peptid-del består av en aminosyresekvens som har minst 98 % identitet til aminosyrene til 221 eller til 121 av SEQ ID NO: Sammensetning for anvendelse i henhold til krav 8, hvor nevnte første peptid-del består av aminosyre-sekvensen av aminosyrene til 221 eller til 121 av SEQ ID NO: Sammensetning for anvendelse i henhold til krav 1 eller 2, hvor fusjonsproteinet omfatter en aminosyresekvens som har minst 9 % identitet med sekvensen av SEQ ID NO: 9,, 12 eller Sammensetning for anvendelse i henhold til krav, hvor fusjonsproteinet omfatter en aminosyresekvens av SEQ ID NO: 9,, 12 eller 13.
3 3 12. Sammensetning for anvendelse i henhold til hvilket som helst av de foregående krav, hvor nevnte fusjonsprotein er en monomer. 13. Sammensetning for anvendelse i henhold til hvilket som helst av kravene 1 til 11, hvor nevnte fusjonsprotein danner en dimer. 14. Sammensetning for anvendelse i henhold til krav 13, hvor nevnte fusjonsprotein danner en homodimer Sammensetning for anvendelse i henhold til krav 13, hvor nevnte fusjonsprotein danner en heterodimer. 16. Sammensetning for anvendelse i henhold til hvilket som helst av de foregående krav, hvor nevnte potensierende middel er cyklofosfamid eller en analog av cyklofosfamid. 17. Sammensetning for anvendelse i henhold til hvilket som helst av de foregående krav for anvendelse i en fremgangsmåte for ethvert av de foregående krav, hvor nevnte potenserende middel administreres minst X timer før administrering av nevnte fusjonsprotein, hvor X er valgt fra 1, 2, 3,,, 1,, 24 og Sammensetning for anvendelse i henhold til hvilket som helst av de foregående krav, hvor nevnte fusjonsprotein omfatter et fragment av villtype-b7-dc som konkurrerer in vitro med villtype-b7-dc for binding til PD Sammensetning for anvendelse i henhold til krav 18, hvor nevnte fragmentet av villtype-b7-dc ikke omfatter noen del av det transmembrane parti av et slikt polypeptid.. Sammensetning for anvendelse i henhold til krav 18, hvor nevnte B7-DCpolypeptid er humant B7-DC-polypeptid. 21. Sammensetning for anvendelse i henhold til krav 1 eller 2, hvor nevnte første peptid-del består av det ekstracellulære domene av B7-DC eller et polypeptid som avviker fra denne ved bare konservative aminosyresubstitusjoner. 22. Sammensetning for anvendelse i henhold til hvilket som helst av de foregående krav, hvor nevnte fusjonsprotein blir anvendt i en mengde som er tilstrekkelig for å
4 4 behandle kreft eller infeksjon av en øket T-celle-mediert immunrespons Sammensetning for anvendelse i henhold til krav 1 eller 2, hvor fremgangsmåten omfatter behandling av kreft. 24. Sammensetning for anvendelse i henhold til krav 1 eller 2, hvor fremgangsmåten omfatter behandling av en infeksjonssykdom. 2. Sammensetning for anvendelse i henhold til krav 23, hvor nevnte kreft er blærekreft, hjernekreft, brystkreft, livmorhalskreft, kolorektal kreft, spiserørskreft, nyrekreft, leverkreft, lungekreft, nasofarynkskreft, bukspyttkjertelkreft, prostatakreft, hudkreft, magekreft, livmorkreft, eggstokkreft, testikkelkreft eller hematologisk kreft. 26. Sammensetning for anvendelse i henhold til krav 23, for anvendelse i nevnte fremgangsmåte, hvor fremgangsmåten videre omfatter administrering av minst ett ytterligere middel valgt fra gruppen bestående av en anti-pd-1-antistoff, et anti- CTLA4-antistoff, en mitose-inhibitor, en aromatase-inhibitor, en A2AR-antagonist, og en angiogenese-inhibitor med nevnte fusjonsprotein. 27. Et del-sett som omfatter: et fusjonsprotein som omfatter en første og andre peptid-del, karakterisert ved at nevnte første peptid-del består av aminosyrene til 221 av SEQ ID NO: 1, og nevnte andre peptid-del omfatter en del av et immunoglobulin (Ig); og cyklofosfamid; for anvendelse i en fremgangsmåte for behandling av kreft; hvor cyklofosfamid blir administrert før nevnte fusjonsprotein og nevnte fusjonsprotein administreres uten cyklofosfamid etter administrering av cyklofosfamid; hvor doseringen av cyklofosfamid ikke er effektiv til å ha direkte anti-tumor aktivitet. 28. Sammensetning for anvendelse i henhold til krav 27, hvor nevnte andre peptid parti omfatter aminosyrene av human IgGI. 29. Sammensetning for anvendelse i henhold til krav 27 for anvendelse i fremgangsmåten som angitt i krav 27, hvor nevnte cyklofosfamid blir administrert til
5 nevnte pasient i minst 24 timer før administrering av fusjonsproteinet.. Sett av deler som omfatter: 1 et fusjonsprotein som omfatter første og andre peptid-deler, karakterisert ved at nevnte første peptid-del består av en aminosyresekvens valgt fra: villtype-b7- DC, en aminosyresekvens som har minst 98 % identitet til aminosyrene -221 eller -121 av SEQ ID NO: 1, og som konkurrerer in vitro med villtype-b7-dc for binding til PD-1, et fragment av B7-DC som konkurrerer in vitro med villtype-b7-dc for binding til PD-1, og et ekstracellulært domene av B7-DC og nevnte andre peptid-del som omfatter en del av et immunoglobulin (Ig); og et potenserende middel valgt fra gruppen bestående av: cyklofosfamid, en analog av cyklofosfamid, sunitinib, anti-tgffi, imatinib, antracykliner, oksaliplatin og doksorubicin; hvor nevnte potenserende middel skal administreres før nevnte fusjonsprotein og nevnte fusjonsprotein skal administreres uten nevnte potenserende middel etter administrasjon av nevnte potenserende middel; hvor doseringen av det potenserende middel ikke er effektivt til å ha direkte antitumoraktivitet; og hvor T-celleresponsen oppnådd etter administrering av fusjonsproteinet er større enn T-celleresponsen oppnådd ved å administrere enten fusjonsproteinet alene eller det potenserende middel alene.
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 230129 B1 (19) NO NORWAY (1) Int Cl. C07K 14/47 (06.01) C07K 14/2 (06.01) C07K 14/70 (06.01) C07K 14/71 (06.01) C12N 1/62 (06.01) Norwegian
(12) Translation of european patent specification (11) NO/EP 230129 B1 (19) NO NORWAY (1) Int Cl. C07K 14/47 (06.01) C07K 14/2 (06.01) C07K 14/70 (06.01) C07K 14/71 (06.01) C12N 1/62 (06.01) Norwegian
1. Forbindelse, eller et terapeutisk akseptabelt salt derav, hvor forbindelsen er valgt fra gruppen omfattende:
 1 Patentkrav 1. Forbindelse, eller et terapeutisk akseptabelt salt derav, hvor forbindelsen er valgt fra gruppen omfattende: - Gruppe 1: 4-[4-(3,3-difenylprop-2-enyl)piperazin-1-yl]-N-[(3-nitrofenyl)sulfonyl]
1 Patentkrav 1. Forbindelse, eller et terapeutisk akseptabelt salt derav, hvor forbindelsen er valgt fra gruppen omfattende: - Gruppe 1: 4-[4-(3,3-difenylprop-2-enyl)piperazin-1-yl]-N-[(3-nitrofenyl)sulfonyl]
EP Patentkrav
 1 EP26727 Patentkrav 1. Monoklonalt antistoff, eller et funksjonelt fragment derav som spesifikt gjenkjenner ett eller flere Siglec- polypeptider bestående av en aminosyresekvens som beskrevet i hvilket
1 EP26727 Patentkrav 1. Monoklonalt antistoff, eller et funksjonelt fragment derav som spesifikt gjenkjenner ett eller flere Siglec- polypeptider bestående av en aminosyresekvens som beskrevet i hvilket
2. Polypeptid ifølge krav 1, hvor polypeptidet utløser en beskyttende immunrespons hos en pattedyrvert mot stammer av C.difficile.
 1 Patentkrav 1 1. Polypeptid som omfatter et første fragment og et andre fragment, hvor (i) det første fragmentet er et toksin A repeterende domenefragment; (ii) det andre fragmentet er et toksin B repeterende
1 Patentkrav 1 1. Polypeptid som omfatter et første fragment og et andre fragment, hvor (i) det første fragmentet er et toksin A repeterende domenefragment; (ii) det andre fragmentet er et toksin B repeterende
PATENTKRAV. 2. Analog av glukagon (SEQ ID nr. 1) som har GIP-agonistaktivitet, med de. følgende modifiseringene:
 1 PATENTKRAV 1 2 1. Analog av glukagon (SEQ ID nr. 1) som har GIP-agonistaktivitet, med de følgende modifiseringene: (a) en aminosyremodifisering på posisjon 1 som overfører GIPagonistaktivitet, eventuelt
1 PATENTKRAV 1 2 1. Analog av glukagon (SEQ ID nr. 1) som har GIP-agonistaktivitet, med de følgende modifiseringene: (a) en aminosyremodifisering på posisjon 1 som overfører GIPagonistaktivitet, eventuelt
Pasient- og pakkeforløp Pasientrettigheter
 Pasient- og pakkeforløp Pasientrettigheter Torstein Rønningen Fagavdelingen Innhold Standardiserte pasientforløp Sykehusinterne standardiserte pasientforløp HF-interne standardiserte pasientforløp Regionale
Pasient- og pakkeforløp Pasientrettigheter Torstein Rønningen Fagavdelingen Innhold Standardiserte pasientforløp Sykehusinterne standardiserte pasientforløp HF-interne standardiserte pasientforløp Regionale
PATENTKRAV. og en første lett kjede og en andre lett kjede, hvor første og andre lette kjeder er forskjellige.
 1 PATENTKRAV 1. Isolert monoklonalt antistoff som bærer en forskjellig spesifisitet i hvert kombinasjonssete og som består av to kopier av et enkelt tung kjede polypeptid og en første lett kjede og en
1 PATENTKRAV 1. Isolert monoklonalt antistoff som bærer en forskjellig spesifisitet i hvert kombinasjonssete og som består av to kopier av et enkelt tung kjede polypeptid og en første lett kjede og en
Pakkeforløp for kreft
 Pakkeforløp for kreft Nye pakkeforløp og noen erfaringer Kjell Magne Tveit, strategidirektør for kreftområdet 22. september 2015 Pakkeforløpene er en logistikkreform Ikke nye retningslinjer for diagnostikk,
Pakkeforløp for kreft Nye pakkeforløp og noen erfaringer Kjell Magne Tveit, strategidirektør for kreftområdet 22. september 2015 Pakkeforløpene er en logistikkreform Ikke nye retningslinjer for diagnostikk,
Pakkeforløp for kreft
 Pakkeforløp for kreft Hva er status etter fire måneder? Anne Hafstad, prosjektdirektør 28 pakkeforløp 26 organspesifikke forløp 1 metastaser uten kjent utgangspunkt 1 diagnostisk pakkeforløp 1. januar
Pakkeforløp for kreft Hva er status etter fire måneder? Anne Hafstad, prosjektdirektør 28 pakkeforløp 26 organspesifikke forløp 1 metastaser uten kjent utgangspunkt 1 diagnostisk pakkeforløp 1. januar
Om statistikken. Indikatorer for organspesifikke pakkeforløp. Beskrivelse av sentrale indikatorer for Pakkeforløp for kreft,
 Om statistikken Pakkeforløp er standard pasientforløp som beskriver organisering av utredning og behandling, dialog med pasient og pårørende, samt ansvarsplassering og konkrete forløpstider. En viktig
Om statistikken Pakkeforløp er standard pasientforløp som beskriver organisering av utredning og behandling, dialog med pasient og pårørende, samt ansvarsplassering og konkrete forløpstider. En viktig
Pakkeforløp for kreft
 Pakkeforløp for kreft Hva er status etter fire måneder? Dagens Medisin Kreftkonferanse 23. april 2015 Kjell Magne Tveit, strategidirektør for kreftområdet Bindinger Oslo universitetssykehus: Fagdirektør
Pakkeforløp for kreft Hva er status etter fire måneder? Dagens Medisin Kreftkonferanse 23. april 2015 Kjell Magne Tveit, strategidirektør for kreftområdet Bindinger Oslo universitetssykehus: Fagdirektør
PEPTIDER FOR VAKSINER MOT BJØRKEALLERGI
 PEPTIDER FOR VAKSINER MOT BJØRKEALLERGI 1 P a t e n t k r a v 1. Sammensetning egnet for anvendelse ved forebygging eller behandling av allergi mot bjørkepollen omfattende: i) polypeptidet ifølge SEQ ID
PEPTIDER FOR VAKSINER MOT BJØRKEALLERGI 1 P a t e n t k r a v 1. Sammensetning egnet for anvendelse ved forebygging eller behandling av allergi mot bjørkepollen omfattende: i) polypeptidet ifølge SEQ ID
Analyser innen ventetid BUP og pakkeforløp kreft. Vedlegg styresak
 Analyser innen ventetid BUP og pakkeforløp kreft Vedlegg styresak 76-2018 Ventetid BUP Ventetid for pasienter med helsehjelpen påstartet Ventetid avviklede BUP HSØ 2016 2017 2018 Akershus universitetssykehus
Analyser innen ventetid BUP og pakkeforløp kreft Vedlegg styresak 76-2018 Ventetid BUP Ventetid for pasienter med helsehjelpen påstartet Ventetid avviklede BUP HSØ 2016 2017 2018 Akershus universitetssykehus
1. Isolert protein omfattende et stabilisert aktivin IIB reseptor polypeptid, hvori polypeptidet er valgt fra gruppen bestående av:
 1 Patentkrav. 1. Isolert protein omfattende et stabilisert aktivin IIB reseptor polypeptid, hvori polypeptidet er valgt fra gruppen bestående av: (a) et polypeptid bestående av sekvensen representert ved
1 Patentkrav. 1. Isolert protein omfattende et stabilisert aktivin IIB reseptor polypeptid, hvori polypeptidet er valgt fra gruppen bestående av: (a) et polypeptid bestående av sekvensen representert ved
Pakkeforløp for kreft seminar 27.mai 2015 Fastlegens rolle og samarbeidet mellom fastlegene og sykehusene
 Pakkeforløp for kreft seminar 27.mai 2015 Fastlegens rolle og samarbeidet mellom fastlegene og sykehusene Trygve Kongshavn Fastlege Avd sjef Praksiskonsulentordningen (PKO) i vestre Viken Målsetning: Trygghet
Pakkeforløp for kreft seminar 27.mai 2015 Fastlegens rolle og samarbeidet mellom fastlegene og sykehusene Trygve Kongshavn Fastlege Avd sjef Praksiskonsulentordningen (PKO) i vestre Viken Målsetning: Trygghet
Velkommen til samling forløpskoordinatorer 22 september 2015. Gro Sævil Haldorsen Regional prosessleder innføring av pakkeforløp Helse Sør-Øst RHF
 Velkommen til samling forløpskoordinatorer 22 september 2015 Gro Sævil Haldorsen Regional prosessleder innføring av pakkeforløp Helse Sør-Øst RHF Forløpskoordinatorrollen er viktig Sommerferie avvikling
Velkommen til samling forløpskoordinatorer 22 september 2015 Gro Sævil Haldorsen Regional prosessleder innføring av pakkeforløp Helse Sør-Øst RHF Forløpskoordinatorrollen er viktig Sommerferie avvikling
1. En ikke-naturlig forekommende eller konstruert sammensetning omfattende:
 1 Patentkrav EP2931898 1. En ikke-naturlig forekommende eller konstruert sammensetning omfattende: et leveringssystem som er operativt konfigurert for å levere CRISPR-Caskomplekskomponenter eller polynukleotidsekvenser
1 Patentkrav EP2931898 1. En ikke-naturlig forekommende eller konstruert sammensetning omfattende: et leveringssystem som er operativt konfigurert for å levere CRISPR-Caskomplekskomponenter eller polynukleotidsekvenser
Monitorering av pakkeforløp kreft
 Colourbox Stein Olav Gystad, Norsk pasientregister Lillestrøm 28. oktober 2015 Tema Tilbakemeldinger fra NPR Måloppnåelse for Helse Sør-Øst RHF per september 2015 Videre arbeid Tilbakemeldinger fra NPR
Colourbox Stein Olav Gystad, Norsk pasientregister Lillestrøm 28. oktober 2015 Tema Tilbakemeldinger fra NPR Måloppnåelse for Helse Sør-Øst RHF per september 2015 Videre arbeid Tilbakemeldinger fra NPR
Pakkeforløp for kreft
 Pakkeforløp for kreft Status nasjonalt og erfaringer på tvers av regionene Kjell Magne Tveit, strategidirektør for kreftområdet 28. oktober 2015 Målsetning: Trygghet og forutsigbarhet Pasienter skal oppleve
Pakkeforløp for kreft Status nasjonalt og erfaringer på tvers av regionene Kjell Magne Tveit, strategidirektør for kreftområdet 28. oktober 2015 Målsetning: Trygghet og forutsigbarhet Pasienter skal oppleve
Pakkeforløp for kreft - hvordan går det? Eva K. Håndlykken, NPR
 Pakkeforløp for kreft - hvordan går det? Eva K. Håndlykken, NPR Tema Hva er pakkeforløp? Måloppnåelse for per september 2015 (foreløpige tall) Videre arbeid Målsetning: Trygghet og forutsigbarhet Pasienter
Pakkeforløp for kreft - hvordan går det? Eva K. Håndlykken, NPR Tema Hva er pakkeforløp? Måloppnåelse for per september 2015 (foreløpige tall) Videre arbeid Målsetning: Trygghet og forutsigbarhet Pasienter
NWE/HBA P NO / NO D1. SNS-595 og metoder for anvendelse av det samme.
 NWE/HBA.04.1 P6060144NO01 11731-006-01/222-006 2900 NO D1 Sunesis Pharmaceuticals, Inc. Avdelt fra patentsøknad nr. 064647 SNS-9 og metoder for anvendelse av det samme. 1 SNS-9 og metoder for anvendelse
NWE/HBA.04.1 P6060144NO01 11731-006-01/222-006 2900 NO D1 Sunesis Pharmaceuticals, Inc. Avdelt fra patentsøknad nr. 064647 SNS-9 og metoder for anvendelse av det samme. 1 SNS-9 og metoder for anvendelse
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2188312 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (06.01) A61P 3/00 (06.01) Norwegian Industrial Property Office (21) Translation Published.11.02
(12) Translation of european patent specification (11) NO/EP 2188312 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (06.01) A61P 3/00 (06.01) Norwegian Industrial Property Office (21) Translation Published.11.02
NWE/HBA P NO / NO D1. SNS-595 for anvendelse i en metode for behandling av leukemi.
 NWE/HBA 21.09.16 P6060144NO01 11731-006-01/222-006 2900 NO D1 Sunesis Pharmaceuticals, Inc. Avdelt fra patentsøknad nr. 064647 SNS-9 for anvendelse i en metode for behandling av leukemi. 1 Foreliggende
NWE/HBA 21.09.16 P6060144NO01 11731-006-01/222-006 2900 NO D1 Sunesis Pharmaceuticals, Inc. Avdelt fra patentsøknad nr. 064647 SNS-9 for anvendelse i en metode for behandling av leukemi. 1 Foreliggende
SNS-595 og metoder for anvendelse av det samme
 1 SNS-9 og metoder for anvendelse av det samme Foreliggende oppfinnelse vedrører farmasøytiske sammensetninger og metoder for anvendelse av SNS-9 for behandling av kreft. SNS-9 OG METODER FOR ANVENDELSE
1 SNS-9 og metoder for anvendelse av det samme Foreliggende oppfinnelse vedrører farmasøytiske sammensetninger og metoder for anvendelse av SNS-9 for behandling av kreft. SNS-9 OG METODER FOR ANVENDELSE
EP Patentkrav. 1. En forbindelse med formel (II): eller et farmasøytisk akseptabelt salt derav, hvor:
 1 Patentkrav EP2781 1. En forbindelse med formel (II): eller et farmasøytisk akseptabelt salt derav, hvor: 1 2 A er 0; P er R c -C(O)-; R c er R D ; R D er 2-pyrazinyl; R a er isobutyl; R a1 er -CH2-R
1 Patentkrav EP2781 1. En forbindelse med formel (II): eller et farmasøytisk akseptabelt salt derav, hvor: 1 2 A er 0; P er R c -C(O)-; R c er R D ; R D er 2-pyrazinyl; R a er isobutyl; R a1 er -CH2-R
Forløpskoordinatorens rolle i Pakkeforløp for kreft. Fagseminar Sundvolden 29.10.15
 Forløpskoordinatorens rolle i Pakkeforløp for kreft Fagseminar Sundvolden 29.10.15 1 2 PAKKEFORLØP FOR KREFT Utarbeidet av Helsedirektoratet Politisk oppdrag fra Helse- og omsorgsdepartementet, som skal
Forløpskoordinatorens rolle i Pakkeforløp for kreft Fagseminar Sundvolden 29.10.15 1 2 PAKKEFORLØP FOR KREFT Utarbeidet av Helsedirektoratet Politisk oppdrag fra Helse- og omsorgsdepartementet, som skal
Pakkeforløp hjerneslag. Cesilie Aasen og Liv Hege Kateraas Helsedirektoratet Rehabiliteringskonferansen Lillestrøm juni 2017
 Pakkeforløp hjerneslag Cesilie Aasen og Liv Hege Kateraas Helsedirektoratet Rehabiliteringskonferansen Lillestrøm juni 2017 Helsemyndighetens fokus og arbeide på feltet Revisjon av Nasjonal retningslinje
Pakkeforløp hjerneslag Cesilie Aasen og Liv Hege Kateraas Helsedirektoratet Rehabiliteringskonferansen Lillestrøm juni 2017 Helsemyndighetens fokus og arbeide på feltet Revisjon av Nasjonal retningslinje
Pakkeforløp for kreft Status Kjell Magne Tveit, PMU 2016
 Pakkeforløp for kreft Status 2016 Kjell Magne Tveit, PMU 2016 28 pakkeforløp 26 organspesifikke forløp 1 metastaser med ukjent utgangspunkt 1 diagnostisk pakkeforløp 1. januar 2015: Implementering av pakkeforløp
Pakkeforløp for kreft Status 2016 Kjell Magne Tveit, PMU 2016 28 pakkeforløp 26 organspesifikke forløp 1 metastaser med ukjent utgangspunkt 1 diagnostisk pakkeforløp 1. januar 2015: Implementering av pakkeforløp
NORGE. Patentstyret (12) SØKNAD (19) NO (21) (13) A1. (51) Int Cl.
 (12) SØKNAD (19) NO (21) 171288 (13) A1 NORGE (1) Int Cl. C07K 16/18 (06.01) C07K 16/28 (06.01) A61K 39/39 (06.01) Patentstyret (21) Søknadsnr 171288 (86) Int.inng.dag og søknadsnr 0.09.02 PCT/US0/031401
(12) SØKNAD (19) NO (21) 171288 (13) A1 NORGE (1) Int Cl. C07K 16/18 (06.01) C07K 16/28 (06.01) A61K 39/39 (06.01) Patentstyret (21) Søknadsnr 171288 (86) Int.inng.dag og søknadsnr 0.09.02 PCT/US0/031401
Kreft nye pakkeforløp Østfold. Andreas Stensvold MD, PhD Avdelingssjef Kreftavdelingen Sykehuset Østfold 13 mars 2015
 Kreft nye pakkeforløp Østfold Andreas Stensvold MD, PhD Avdelingssjef Kreftavdelingen Sykehuset Østfold 13 mars 2015 Disposisjon Bakgrunn Diagnoseveilederene Hjemmesiden til SØF Henvisninger innhold Forløpskoordinator
Kreft nye pakkeforløp Østfold Andreas Stensvold MD, PhD Avdelingssjef Kreftavdelingen Sykehuset Østfold 13 mars 2015 Disposisjon Bakgrunn Diagnoseveilederene Hjemmesiden til SØF Henvisninger innhold Forløpskoordinator
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 26727 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (06.01) A61K 31/122 (06.01) A61K 31/32 (06.01) A61K 31/93 (06.01) A61K 31/663 (06.01) A61K 39/39
(12) Translation of european patent specification (11) NO/EP 26727 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (06.01) A61K 31/122 (06.01) A61K 31/32 (06.01) A61K 31/93 (06.01) A61K 31/663 (06.01) A61K 39/39
Pakkeforløp for kreft
 Pakkeforløp for kreft Utfordringer knyttet til de nye forløpene Kjell Magne Tveit, strategidirektør for kreftområdet Pakkeforløp implementering 1. mai 2015: Implementering av 10 pakkeforløp Diagnostisk
Pakkeforløp for kreft Utfordringer knyttet til de nye forløpene Kjell Magne Tveit, strategidirektør for kreftområdet Pakkeforløp implementering 1. mai 2015: Implementering av 10 pakkeforløp Diagnostisk
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2173379 B1 (19) NO NORWAY (1) Int Cl. A61K 39/39 (2006.01) Norwegian Industrial Property Office (21) Translation Published 2016.01.2 (80) Date
(12) Translation of european patent specification (11) NO/EP 2173379 B1 (19) NO NORWAY (1) Int Cl. A61K 39/39 (2006.01) Norwegian Industrial Property Office (21) Translation Published 2016.01.2 (80) Date
idet, en eller flere innskuddshendelser anvender den setespesifikke rekombinasjonen,
 1 Patentkrav 1. Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten omfatter: innsetting inn i et gnagercellegenom;
1 Patentkrav 1. Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten omfatter: innsetting inn i et gnagercellegenom;
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2185198 B1 (19) NO NORWAY (51) Int Cl. A61K 39/395 (2006.01) A61P 35/00 (2006.01) C07K 16/40 (2006.01) Norwegian Industrial Property Office
(12) Translation of european patent specification (11) NO/EP 2185198 B1 (19) NO NORWAY (51) Int Cl. A61K 39/395 (2006.01) A61P 35/00 (2006.01) C07K 16/40 (2006.01) Norwegian Industrial Property Office
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2131860 B1 (19) NO NORGE (51) Int Cl. A61K 39/395 (2006.01) Patentstyret (21) Oversettelse publisert 2014.03.24 (80) Dato for Den Europeiske Patentmyndighets
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2131860 B1 (19) NO NORGE (51) Int Cl. A61K 39/395 (2006.01) Patentstyret (21) Oversettelse publisert 2014.03.24 (80) Dato for Den Europeiske Patentmyndighets
2. Fremgangsmåten ifølge krav 1, hvori dsrna-duplekset har en lengde fra 8 basepar (bp) ti 30 bp.
 1 Patentkrav 1. Fremgangsmåte for å endre et mål-dna, der fremgangsmåten omfatter å bringe mål-dna-et i kontakt med et kompleks omfattende: (a) et Cas9-polypeptid og (b) et enkeltmolekyl-rna som er målrettet
1 Patentkrav 1. Fremgangsmåte for å endre et mål-dna, der fremgangsmåten omfatter å bringe mål-dna-et i kontakt med et kompleks omfattende: (a) et Cas9-polypeptid og (b) et enkeltmolekyl-rna som er målrettet
EP Patentkrav
 1 Patentkrav EP2097387 1. En forbindelse, eller en tautomer derav, eller et farmasøytisk akseptabelt salt av nevnte forbindelse eller nevnte tautomer, hvor nevnte forbindelse er valgt fra gruppen bestående
1 Patentkrav EP2097387 1. En forbindelse, eller en tautomer derav, eller et farmasøytisk akseptabelt salt av nevnte forbindelse eller nevnte tautomer, hvor nevnte forbindelse er valgt fra gruppen bestående
Pakkeforløp for kreft
 Pakkeforløp for kreft Kurs for fastleger 25. august 2015 Kjell Magne Tveit Fagdirektør, Stab medisin, helsefag og utvikling Ingvild Strømsholm Rådgiver, Stab medisin, helsefag og utvikling Hva er et pakkeforløp?
Pakkeforløp for kreft Kurs for fastleger 25. august 2015 Kjell Magne Tveit Fagdirektør, Stab medisin, helsefag og utvikling Ingvild Strømsholm Rådgiver, Stab medisin, helsefag og utvikling Hva er et pakkeforløp?
Virksomhetsrapport august 2018
 Virksomhetsrapport august 2018 Styresak 054-2018 Fagdirektør Per Engstrand Konstituert økonomidirektør Annlaug Øygarden Brekke 13.09.2018 Innhold 1. Oppsummering 2. Kvalitet og pasientbehandling 3. Aktivitet
Virksomhetsrapport august 2018 Styresak 054-2018 Fagdirektør Per Engstrand Konstituert økonomidirektør Annlaug Øygarden Brekke 13.09.2018 Innhold 1. Oppsummering 2. Kvalitet og pasientbehandling 3. Aktivitet
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2328616 B1 (19) NO NORWAY (1) Int Cl. A61K 39/39 (2006.01) C07K 16/18 (2006.01) Norwegian Industrial Property Office (21) Translation Published
(12) Translation of european patent specification (11) NO/EP 2328616 B1 (19) NO NORWAY (1) Int Cl. A61K 39/39 (2006.01) C07K 16/18 (2006.01) Norwegian Industrial Property Office (21) Translation Published
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2391650 B1 (19) NO NORGE (51) Int Cl. C07K 16/24 (2006.01) A61K 39/00 (2006.01) A61K 39/395 (2006.01) Patentstyret (21) Oversettelse publisert 2015.03.09
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2391650 B1 (19) NO NORGE (51) Int Cl. C07K 16/24 (2006.01) A61K 39/00 (2006.01) A61K 39/395 (2006.01) Patentstyret (21) Oversettelse publisert 2015.03.09
Hva er Immunterapi? Anders Sundan Senter for myelomforskning, NTNU
 Hva er Immunterapi? Anders Sundan Senter for myelomforskning, NTNU 1 3 typer immunterapi; Antistoffer som aktiverer immunforsvaret mot kreftcellene. (Anti-CTLA4, -PD1/PD1L) Antistoffer som binder kreftceller
Hva er Immunterapi? Anders Sundan Senter for myelomforskning, NTNU 1 3 typer immunterapi; Antistoffer som aktiverer immunforsvaret mot kreftcellene. (Anti-CTLA4, -PD1/PD1L) Antistoffer som binder kreftceller
OVERSIKT PAKKEFORLØPENE FOR KREFT VED OSLO UNIVERSITETSSYKEHUS (OUS)
 OVERSIKT PAKKEFORLØPENE FOR KREFT VED OSLO UNIVERSITETSSYKEHUS () Side 1-4: Side 5-23: Oversikt over pakkeforløp ved med angivelse av klinikk,, lokalisering og ansvarsområde i pakkeforløpet. Trykk på den
OVERSIKT PAKKEFORLØPENE FOR KREFT VED OSLO UNIVERSITETSSYKEHUS () Side 1-4: Side 5-23: Oversikt over pakkeforløp ved med angivelse av klinikk,, lokalisering og ansvarsområde i pakkeforløpet. Trykk på den
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2948184 B1 (19) NO NORWAY (51) Int Cl. A61K 47/48 (2006.01) Norwegian Industrial Property Office (21) Translation Published 2016.08.08 (80)
(12) Translation of european patent specification (11) NO/EP 2948184 B1 (19) NO NORWAY (51) Int Cl. A61K 47/48 (2006.01) Norwegian Industrial Property Office (21) Translation Published 2016.08.08 (80)
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 263813 B1 (19) NO NORWAY (1) Int Cl. C07K 16/18 (2006.01) A61K 39/39 (2006.01) A61P 37/06 (2006.01) Norwegian Industrial Property Office (21)
(12) Translation of european patent specification (11) NO/EP 263813 B1 (19) NO NORWAY (1) Int Cl. C07K 16/18 (2006.01) A61K 39/39 (2006.01) A61P 37/06 (2006.01) Norwegian Industrial Property Office (21)
Langversjon. Kodeveileder. Pakkeforløp for organspesifikk kreft
 Kodeveileder Denne veilederen er en beskrivelse av registreringen knyttet til pakkeforløp for organspesifikk kreft. Registreringen beskrives overordnet i kapittel 1, med en mer utdypende og supplerende
Kodeveileder Denne veilederen er en beskrivelse av registreringen knyttet til pakkeforløp for organspesifikk kreft. Registreringen beskrives overordnet i kapittel 1, med en mer utdypende og supplerende
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2477628 B1 (19) NO NORGE (1) Int Cl. C07D 487/04 (2006.01) A61K 31/497 (2006.01) A61K 31/67 (2006.01) A61K 31/70 (2006.01) Patentstyret (21) Oversettelse
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2477628 B1 (19) NO NORGE (1) Int Cl. C07D 487/04 (2006.01) A61K 31/497 (2006.01) A61K 31/67 (2006.01) A61K 31/70 (2006.01) Patentstyret (21) Oversettelse
LANGVERSJON KODEVEILEDER. Pakkeforløp for organspesifikk kreft
 KODEVEILEDER Denne veilederen er en beskrivelse av registreringen knyttet til pakkeforløp for organspesifikk kreft. Registreringen beskrives overordnet i kapittel 1, med en mer utdypende og supplerende
KODEVEILEDER Denne veilederen er en beskrivelse av registreringen knyttet til pakkeforløp for organspesifikk kreft. Registreringen beskrives overordnet i kapittel 1, med en mer utdypende og supplerende
FR tilveiebringer et kimært antistoff med variabelt område som kan gjenkjenne interleukin-2-reseptor.
 1 1 2 3 Den foreliggende søknaden har prioritet i forhold til US foreløpig søknad nr. 60/469,600 innsendt 6. mai 03, US foreløpige søknad nr. 60/487,964 innsendt 17. juli 03 og US foreløpigs søknad nr.
1 1 2 3 Den foreliggende søknaden har prioritet i forhold til US foreløpig søknad nr. 60/469,600 innsendt 6. mai 03, US foreløpige søknad nr. 60/487,964 innsendt 17. juli 03 og US foreløpigs søknad nr.
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 211778 B1 (19) NO NORWAY (1) Int Cl. A61K 38/16 (06.01) C07K 7/08 (06.01) Norwegian Industrial Property Office (21) Translation Published 1.09.07
(12) Translation of european patent specification (11) NO/EP 211778 B1 (19) NO NORWAY (1) Int Cl. A61K 38/16 (06.01) C07K 7/08 (06.01) Norwegian Industrial Property Office (21) Translation Published 1.09.07
europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 217099 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61K 39/39 (06.01) A61P 3/00 (06.01) Patentstyret (21) Oversettelse publisert 14.02.17 (80)
(12) Oversettelse av europeisk patentskrift (11) NO/EP 217099 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61K 39/39 (06.01) A61P 3/00 (06.01) Patentstyret (21) Oversettelse publisert 14.02.17 (80)
Privat kreftbehandling på Aleris - kuriositet eller todelt helsevesen?
 Privat kreftbehandling på Aleris - kuriositet eller todelt helsevesen? Marius Normann, fagansvarlig onkolog, Aleris Kreftsenter DMs Kreftkonferanse 4. april 2019 «Interessekonflikter» Radiumhospitalet
Privat kreftbehandling på Aleris - kuriositet eller todelt helsevesen? Marius Normann, fagansvarlig onkolog, Aleris Kreftsenter DMs Kreftkonferanse 4. april 2019 «Interessekonflikter» Radiumhospitalet
Styresak Rapportering per august 2018
 Styresak 076-2018 Rapportering per august 2018 11.09.2018 Innhold 1. Målekort 2. Kvalitet og pasientbehandling 3. Prioritering av psykisk helsevern og TSB 4. Aktivitet 5. Bemanning 6. Produktivitet 7.
Styresak 076-2018 Rapportering per august 2018 11.09.2018 Innhold 1. Målekort 2. Kvalitet og pasientbehandling 3. Prioritering av psykisk helsevern og TSB 4. Aktivitet 5. Bemanning 6. Produktivitet 7.
Innhold. 1. Oppsummering. 2. Statusbilde. 3. Kvalitet og pasientbehandling. 4. Prioritering av psykisk helsevern og TSB. 5. Aktivitet. 6.
 Helse Sør-Øst RHF Gode og likeverdige helsetjenester til alle som trenger det, når de trenger det, uavhengig av alder, bosted, etnisk bakgrunn, kjønn og økonomi. Styresak Mars 2018 16.04.2018 1 Innhold
Helse Sør-Øst RHF Gode og likeverdige helsetjenester til alle som trenger det, når de trenger det, uavhengig av alder, bosted, etnisk bakgrunn, kjønn og økonomi. Styresak Mars 2018 16.04.2018 1 Innhold
«Immunterapi» Kreftutvikling. Myelomatose. Immunterapi. Anders'Sundan Senter'for'myelomforskning Institutt'for'klinisk'og'molekylær'medisin,'NTNU
 «Immunterapi» Kreftutvikling Myelomatose Immunterapi Anders'Sundan Senter'for'myelomforskning Institutt'for'klinisk'og'molekylær'medisin,'NTNU 1 Kreft er genetiske sykdommer i den forstand at det alltid
«Immunterapi» Kreftutvikling Myelomatose Immunterapi Anders'Sundan Senter'for'myelomforskning Institutt'for'klinisk'og'molekylær'medisin,'NTNU 1 Kreft er genetiske sykdommer i den forstand at det alltid
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2140006 B1 (19) NO NORWAY (51) Int Cl. C12N 15/53 (2006.01) C12N 9/02 (2006.01) C12P 7/64 (2006.01) Norwegian Industrial Property Office (21)
(12) Translation of european patent specification (11) NO/EP 2140006 B1 (19) NO NORWAY (51) Int Cl. C12N 15/53 (2006.01) C12N 9/02 (2006.01) C12P 7/64 (2006.01) Norwegian Industrial Property Office (21)
KODEVEILEDER. Pakkeforløp for organspesifikk kreft
 KODEVEILEDER Pakkeforløp for organspesifikk kreft Denne veilederen er en beskrivelse av registreringen knyttet til pakkeforløp for organspesifikk kreft. Registreringen beskrives overordnet i kapittel 1,
KODEVEILEDER Pakkeforløp for organspesifikk kreft Denne veilederen er en beskrivelse av registreringen knyttet til pakkeforløp for organspesifikk kreft. Registreringen beskrives overordnet i kapittel 1,
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2222697 B1 (19) NO NORGE (1) Int Cl. C07K 14/70 (06.01) Patentstyret (21) Oversettelse publisert 13.04.29 (80) Dato for Den Europeiske Patentmyndighets
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2222697 B1 (19) NO NORGE (1) Int Cl. C07K 14/70 (06.01) Patentstyret (21) Oversettelse publisert 13.04.29 (80) Dato for Den Europeiske Patentmyndighets
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 22799 B1 (19) NO NORGE (1) Int Cl. A61K 31/23 (06.01) A61K 31/047 (06.01) A61K 31/231 (06.01) A61K 31/232 (06.01) A61K 31/3 (06.01) A61K 31/93 (06.01)
(12) Oversettelse av europeisk patentskrift (11) NO/EP 22799 B1 (19) NO NORGE (1) Int Cl. A61K 31/23 (06.01) A61K 31/047 (06.01) A61K 31/231 (06.01) A61K 31/232 (06.01) A61K 31/3 (06.01) A61K 31/93 (06.01)
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 213917 B1 (19) NO NORGE (1) Int Cl. A61K 4/06 (06.01) A61K 31/36 (06.01) A61K 38/19 (06.01) A61P 37/06 (06.01) Patentstyret (21) Oversettelse publisert
(12) Oversettelse av europeisk patentskrift (11) NO/EP 213917 B1 (19) NO NORGE (1) Int Cl. A61K 4/06 (06.01) A61K 31/36 (06.01) A61K 38/19 (06.01) A61P 37/06 (06.01) Patentstyret (21) Oversettelse publisert
Immunsystemet Immunterapien og dens ulike former Kreftsykdommer som behandles Bivirkninger av immunterapi Laboratorieanalyser nå og i fremtiden
 AGENDA Immunsystemet Immunterapien og dens ulike former Kreftsykdommer som behandles Bivirkninger av immunterapi Laboratorieanalyser nå og i fremtiden 1 IMMUNSYSTEMET Immunsystemet vårt er designet for
AGENDA Immunsystemet Immunterapien og dens ulike former Kreftsykdommer som behandles Bivirkninger av immunterapi Laboratorieanalyser nå og i fremtiden 1 IMMUNSYSTEMET Immunsystemet vårt er designet for
Pakkeforløp - status og resultater. Prosjektdirektør Anne Hafstad
 Pakkeforløp - status og resultater Prosjektdirektør Anne Hafstad Målsetning: Trygghet og forutsigbarhet Pasienter skal oppleve forutsigbarhet og oversikt over forløpet God informasjon og pasientmedvirkning
Pakkeforløp - status og resultater Prosjektdirektør Anne Hafstad Målsetning: Trygghet og forutsigbarhet Pasienter skal oppleve forutsigbarhet og oversikt over forløpet God informasjon og pasientmedvirkning
Vedlegg til vignette 58/11-2 Innføring av nye kreftlegemidler
 Stein Kaasa på vegne av arbeidsgruppen for utarbeidelse av nasjonale retningslinjer for behandling av sarkom Sykdom Bløtvevssarkom 1 Antall pasienter Usikre tall, mellom 160 og 300 diagnostiseres årlig
Stein Kaasa på vegne av arbeidsgruppen for utarbeidelse av nasjonale retningslinjer for behandling av sarkom Sykdom Bløtvevssarkom 1 Antall pasienter Usikre tall, mellom 160 og 300 diagnostiseres årlig
Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten
 1 Patentkrav 1. Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten omfatter: innsetting inn i et gnagercellegenom;
1 Patentkrav 1. Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten omfatter: innsetting inn i et gnagercellegenom;
Polynukleotid som omfatter en nukleinsyre valgt fra gruppen som består av: a) en nukleinsyre med en nukleinsyresekvens som vist i SEKV. ID nr.
 168 PATENTKRAV 1. Polynukleotid som omfatter en nukleinsyre valgt fra gruppen som består av: a) en nukleinsyre med en nukleinsyresekvens som vist i SEKV. ID nr. 1; 5 b) en nukleinsyre som koder for et
168 PATENTKRAV 1. Polynukleotid som omfatter en nukleinsyre valgt fra gruppen som består av: a) en nukleinsyre med en nukleinsyresekvens som vist i SEKV. ID nr. 1; 5 b) en nukleinsyre som koder for et
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 211264 B1 (19) NO NORWAY (1) Int Cl. C07D 209/08 (2006.01) A61K 31/63 (2006.01) A61P 3/00 (2006.01) C07D 213/71 (2006.01) C07D 231/6 (2006.01)
(12) Translation of european patent specification (11) NO/EP 211264 B1 (19) NO NORWAY (1) Int Cl. C07D 209/08 (2006.01) A61K 31/63 (2006.01) A61P 3/00 (2006.01) C07D 213/71 (2006.01) C07D 231/6 (2006.01)
DATO: SAKSBEHANDLER: Eldar Søreide SAKEN GJELDER: Tertialrapport 03/16 Nasjonale kvalitetsindikatorer
 STYRESAK GÅR TIL: FORETAK: Styremedlemmer Helse Stavanger HF DATO: 27.08.2017 SAKSBEHANDLER: Eldar Søreide SAKEN GJELDER: Tertialrapport 03/16 Nasjonale kvalitetsindikatorer ARKIVSAK: 2017/02 STYRESAK:
STYRESAK GÅR TIL: FORETAK: Styremedlemmer Helse Stavanger HF DATO: 27.08.2017 SAKSBEHANDLER: Eldar Søreide SAKEN GJELDER: Tertialrapport 03/16 Nasjonale kvalitetsindikatorer ARKIVSAK: 2017/02 STYRESAK:
NORGE. Patentstyret (12) SØKNAD (19) NO (21) (13) A1
 (12) SØKNAD (19) NO (21) 20093386 (13) A1 NORGE (51) Int Cl. C07K 16/18 (2006.01) C07K 16/12 (2006.01) C07K 16/08 (2006.01) A61K 39/395 (2006.01) C12P 21/08 (2006.01) C12N 15/13 (2006.01) A61P 35/00 (2006.01)
(12) SØKNAD (19) NO (21) 20093386 (13) A1 NORGE (51) Int Cl. C07K 16/18 (2006.01) C07K 16/12 (2006.01) C07K 16/08 (2006.01) A61K 39/395 (2006.01) C12P 21/08 (2006.01) C12N 15/13 (2006.01) A61P 35/00 (2006.01)
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2186889 B1 (19) NO NORWAY (51) Int Cl. C07K 14/47 (2006.01) A61K 38/00 (2006.01) C12N 5/0783 (2010.01) C12N 5/0784 (2010.01) A61K 35/12 (2015.01)
(12) Translation of european patent specification (11) NO/EP 2186889 B1 (19) NO NORWAY (51) Int Cl. C07K 14/47 (2006.01) A61K 38/00 (2006.01) C12N 5/0783 (2010.01) C12N 5/0784 (2010.01) A61K 35/12 (2015.01)
Pakkeforløp for kreft og Handlingsplan for kreftbehandling orientering til styret
 Pakkeforløp for kreft og Handlingsplan for kreftbehandling orientering til styret Svein Mjåland Avdelingsleder Senter for kreftbehandling og prosjektleder for handlingsplan for kreft Styremøte 21. 05.15
Pakkeforløp for kreft og Handlingsplan for kreftbehandling orientering til styret Svein Mjåland Avdelingsleder Senter for kreftbehandling og prosjektleder for handlingsplan for kreft Styremøte 21. 05.15
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2451844 B1 (19) NO NORWAY (51) Int Cl. C07K 16/28 (2006.01) Norwegian Industrial Property Office (21) Translation Published 2015.09.21 (80)
(12) Translation of european patent specification (11) NO/EP 2451844 B1 (19) NO NORWAY (51) Int Cl. C07K 16/28 (2006.01) Norwegian Industrial Property Office (21) Translation Published 2015.09.21 (80)
Søker: University of Massachusetts og E. R. Squibb & Sons L.L.C.
 O.nr. 113075/ EH/KN/KN Patentsøknad nr. 20063767 Søker: University of Massachusetts og E. R. Squibb & Sons L.L.C. Tittel: Isolert monoklonalt antistoff eller antigen bindende del derav, samt anvendelse
O.nr. 113075/ EH/KN/KN Patentsøknad nr. 20063767 Søker: University of Massachusetts og E. R. Squibb & Sons L.L.C. Tittel: Isolert monoklonalt antistoff eller antigen bindende del derav, samt anvendelse
EP Patentkrav. 1. En forbindelse med formel I: eller et farmasøytisk akseptabelt salt derav, hvori: R 1 er CD 3 ; og R 2 er CH 3 ;
 1 Patentkrav EP237183 1. En forbindelse med formel I: eller et farmasøytisk akseptabelt salt derav, hvori: 1 2 R 1 er CD 3 ; og R 2 er CH 3 ; for anvendelse i behandling av et individ som lider av eller
1 Patentkrav EP237183 1. En forbindelse med formel I: eller et farmasøytisk akseptabelt salt derav, hvori: 1 2 R 1 er CD 3 ; og R 2 er CH 3 ; for anvendelse i behandling av et individ som lider av eller
Amgen Europe B.V. Nplate_EU_DosingCalculator_RMP_v3.0_NO_MAR2019. Nplate (romiplostim) Dosekalkulator
 Amgen Europe B.V. Nplate_EU_DosingCalculator_RMP_v3.0_NO_MAR2019 Nplate (romiplostim) Dosekalkulator Veiledning for håndtering Nplate kan kun rekonstitueres med sterilt vann til injeksjonsvæsker uten konserveringsmidler.
Amgen Europe B.V. Nplate_EU_DosingCalculator_RMP_v3.0_NO_MAR2019 Nplate (romiplostim) Dosekalkulator Veiledning for håndtering Nplate kan kun rekonstitueres med sterilt vann til injeksjonsvæsker uten konserveringsmidler.
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 220279 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (2006.01) A61K 39/00 (2006.01) Norwegian Industrial Property Office (21) Translation Published
(12) Translation of european patent specification (11) NO/EP 220279 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (2006.01) A61K 39/00 (2006.01) Norwegian Industrial Property Office (21) Translation Published
Estimering av behovet for PET/CT i
 Estimering av behovet for PET/CT i Kunnskapsesenterets nye PPT-mal 2010 Bjørn Anton Graff, Elisabeth Jeppesen, Espen Movik, Inger Natvig Norderhaug Inger Natvig Norderhaug, forskningsleder 10 år med utredning
Estimering av behovet for PET/CT i Kunnskapsesenterets nye PPT-mal 2010 Bjørn Anton Graff, Elisabeth Jeppesen, Espen Movik, Inger Natvig Norderhaug Inger Natvig Norderhaug, forskningsleder 10 år med utredning
EP Patentkrav. 1. Forbindelse med generell formel (I): R 1 representerer. hvor * indikerer festepunktet for gruppen til resten av molekylet;
 1 Patentkrav EP2791136 1. Forbindelse med generell formel (I): hvor: R 1 representerer hvor * indikerer festepunktet for gruppen til resten av molekylet; R 2 representerer 1 hvor * indikerer festepunktet
1 Patentkrav EP2791136 1. Forbindelse med generell formel (I): hvor: R 1 representerer hvor * indikerer festepunktet for gruppen til resten av molekylet; R 2 representerer 1 hvor * indikerer festepunktet
c) Beskriv mekanismen(e) som under B-cellemodningen sikrer at B-celler ikke blir autoreaktive og gjenkjenner kroppens egne strukturer.
 Oppgave 1 (9 poeng) Immunologi Læringsmål: ID 3.1.1, 3.1.3 Jesper er en gutt på 3 år som blir innlagt for andre gang med lungebetennelse. Ved analyse av en blodprøve oppdages det at serumet til Jesper
Oppgave 1 (9 poeng) Immunologi Læringsmål: ID 3.1.1, 3.1.3 Jesper er en gutt på 3 år som blir innlagt for andre gang med lungebetennelse. Ved analyse av en blodprøve oppdages det at serumet til Jesper
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 11 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61K 39/39 (06.01) Patentstyret (21) Oversettelse publisert 1.02.02 (80) Dato for Den Europeiske
(12) Oversettelse av europeisk patentskrift (11) NO/EP 11 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61K 39/39 (06.01) Patentstyret (21) Oversettelse publisert 1.02.02 (80) Dato for Den Europeiske
Hva gjør vi på molekylærpatologisk laboratorium?
 Bioingeniørkongressen 2016 Hva gjør vi på molekylærpatologisk laboratorium? Dag Andre Nymoen Ingeniør/stipendiat Patologen OUS Laboratorium for molekylærpatologi www.molpat.no Operasjon Biopsi Makrobeskjæring
Bioingeniørkongressen 2016 Hva gjør vi på molekylærpatologisk laboratorium? Dag Andre Nymoen Ingeniør/stipendiat Patologen OUS Laboratorium for molekylærpatologi www.molpat.no Operasjon Biopsi Makrobeskjæring
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2193803 B1 (19) NO NORGE (51) Int Cl. A61K 39/00 (2006.01) C12N 15/13 (2006.01) Patentstyret (21) Oversettelse publisert 2012.02.13 (80) Dato for
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2193803 B1 (19) NO NORGE (51) Int Cl. A61K 39/00 (2006.01) C12N 15/13 (2006.01) Patentstyret (21) Oversettelse publisert 2012.02.13 (80) Dato for
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2606064 B1 (19) NO NORWAY (1) Int Cl. C07K 16/00 (06.01) C07K 16/24 (06.01) C07K 16/28 (06.01) C07K 16/46 (06.01) C12N 1/ (06.01) Norwegian
(12) Translation of european patent specification (11) NO/EP 2606064 B1 (19) NO NORWAY (1) Int Cl. C07K 16/00 (06.01) C07K 16/24 (06.01) C07K 16/28 (06.01) C07K 16/46 (06.01) C12N 1/ (06.01) Norwegian
Målrettet behandling
 Målrettet behandling en del av persontilpasset/skreddersydd behandling Informasjon fra Kreftforeningen Målet med dette faktaarket er å gi en kortfattet og generell informasjon til pasienter og pårørende
Målrettet behandling en del av persontilpasset/skreddersydd behandling Informasjon fra Kreftforeningen Målet med dette faktaarket er å gi en kortfattet og generell informasjon til pasienter og pårørende
Notat. Administrerande direktør si orientering pkt. 1 Styresak 033/2015 O Styremøte 29.05.2015
 Notat Går til: Styremedlemmer Føretak: Helse Førde HF Dato: 19.05.2015 Frå: Administrerande direktør Sakhandsamar: Saka gjeld: Hans Johan Breidablik Kreftpakkeforløp og oppfølging Administrerande direktør
Notat Går til: Styremedlemmer Føretak: Helse Førde HF Dato: 19.05.2015 Frå: Administrerande direktør Sakhandsamar: Saka gjeld: Hans Johan Breidablik Kreftpakkeforløp og oppfølging Administrerande direktør
Innføring av nye kreftlegemidler
 Innføring av nye kreftlegemidler Stein Kaasa Strategidirektør, Avdeling sykehustjenester Figur 1. Antall krefttilfeller i Norge, 2000-2009. Med kreftregisterets fremskrivning til 2020. Tidsfrister Vurdering
Innføring av nye kreftlegemidler Stein Kaasa Strategidirektør, Avdeling sykehustjenester Figur 1. Antall krefttilfeller i Norge, 2000-2009. Med kreftregisterets fremskrivning til 2020. Tidsfrister Vurdering
(12) Translation of european patent specification
 NO/EP20 (12) Translation of european patent specification (11) NO/EP 20 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (2006.01) A61P 3/00 (2006.01) A61P 37/00 (2006.01) Norwegian Industrial Property Office
NO/EP20 (12) Translation of european patent specification (11) NO/EP 20 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (2006.01) A61P 3/00 (2006.01) A61P 37/00 (2006.01) Norwegian Industrial Property Office
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2344449 B1 (19) NO NORWAY (1) Int Cl. C07C 311/20 (2006.01) A61K 31/18 (2006.01) A61P 29/00 (2006.01) C07C 311/28 (2006.01) C07D 213/2 (2006.01)
(12) Translation of european patent specification (11) NO/EP 2344449 B1 (19) NO NORWAY (1) Int Cl. C07C 311/20 (2006.01) A61K 31/18 (2006.01) A61P 29/00 (2006.01) C07C 311/28 (2006.01) C07D 213/2 (2006.01)
NITO Bioingeniørfaglig Institutt kurs i Immunologi The Edge, Tromsø, 11. februar 2015. Generell Immunologi
 NITO Bioingeniørfaglig Institutt kurs i Immunologi The Edge, Tromsø, 11. februar 2015 Generell Immunologi Tor B Stuge Immunologisk forskningsgruppe, IMB Universitetet i Tromsø Innhold: 1. Immunsystemets
NITO Bioingeniørfaglig Institutt kurs i Immunologi The Edge, Tromsø, 11. februar 2015 Generell Immunologi Tor B Stuge Immunologisk forskningsgruppe, IMB Universitetet i Tromsø Innhold: 1. Immunsystemets
Helgelandssykehusets rolle i møte med kreftpasienten
 Medisinsk direktør Fred A. Mürer 21.Januar 2010 Medisinsk direktør Helgelandssykehuset HF Side 1 Helgelandssykehusets rolle i møte med kreftpasienten Arbeidsdeling i Helgelandssykehuset Helgelandssykehuset
Medisinsk direktør Fred A. Mürer 21.Januar 2010 Medisinsk direktør Helgelandssykehuset HF Side 1 Helgelandssykehusets rolle i møte med kreftpasienten Arbeidsdeling i Helgelandssykehuset Helgelandssykehuset
AVGJØRELSE 5. januar 2016 Sak PAT 15/001. Klagenemnda for industrielle rettigheter sammensatt av følgende utvalg:
 AVGJØRELSE 5. januar 2016 Sak PAT 15/001 Klager: Genentech Inc. Representert ved: Tandbergs Patentkontor AS Klagenemnda for industrielle rettigheter sammensatt av følgende utvalg: Elisabeth Ohm, Tom Kristensen
AVGJØRELSE 5. januar 2016 Sak PAT 15/001 Klager: Genentech Inc. Representert ved: Tandbergs Patentkontor AS Klagenemnda for industrielle rettigheter sammensatt av følgende utvalg: Elisabeth Ohm, Tom Kristensen
Forelesninger i BI Cellebiologi. Denaturering og renaturering. Figure 3-13
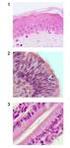 Figure 3.9 Denaturering og renaturering Figure 3-13 Denaturering og renaturering Figure 3-14 Viser tre trinn i refolding av et protein som har vært denaturert. Molten globule -formen er en intermediær
Figure 3.9 Denaturering og renaturering Figure 3-13 Denaturering og renaturering Figure 3-14 Viser tre trinn i refolding av et protein som har vært denaturert. Molten globule -formen er en intermediær
Forslag til nasjonal metodevurdering
 Forslagsskjema, Versjon 2 17. mars 2014 Forslag til nasjonal metodevurdering Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Forslagsskjema, Versjon 2 17. mars 2014 Forslag til nasjonal metodevurdering Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Undersøkelse om pasienters erfaringer fra sykehus
 PasOpp 2007 Undersøkelse om pasienters erfaringer fra sykehus Høst 2007 Hensikten med undersøkelsen Hensikten med denne undersøkelsen er å få vite mer om hvordan pasienter med en kreftdiagnose vurderer
PasOpp 2007 Undersøkelse om pasienters erfaringer fra sykehus Høst 2007 Hensikten med undersøkelsen Hensikten med denne undersøkelsen er å få vite mer om hvordan pasienter med en kreftdiagnose vurderer
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2164866 B1 (19) NO NORGE (51) Int Cl. A61K 38/03 (2006.01) A61K 31/337 (2006.01) A61K 47/48 (2006.01) C07K 14/00 (2006.01) C07K 16/22 (2006.01) C07K
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2164866 B1 (19) NO NORGE (51) Int Cl. A61K 38/03 (2006.01) A61K 31/337 (2006.01) A61K 47/48 (2006.01) C07K 14/00 (2006.01) C07K 16/22 (2006.01) C07K
(12) Translation of European patent specification
 (12) Translation of European patent specification (11) NO/EP 2370463 B1 (19) NO NORWAY (1) Int Cl. C07K 14/49 (06.01) C07K 14/71 (06.01) Norwegian Industrial Property Office (21) Translation Published
(12) Translation of European patent specification (11) NO/EP 2370463 B1 (19) NO NORWAY (1) Int Cl. C07K 14/49 (06.01) C07K 14/71 (06.01) Norwegian Industrial Property Office (21) Translation Published
7.Rostafuroksinet for anvendelse ifølge hvilket som helst av kravene 1 til 6,
 Patentkrav 1.Rostafuroksin for anvendelse ved behandling eller forebygging av en kardiovaskulær tilstand hos et individ hvori individet er blitt valgt til å være en bærer av: minst én polymorfisme valgt
Patentkrav 1.Rostafuroksin for anvendelse ved behandling eller forebygging av en kardiovaskulær tilstand hos et individ hvori individet er blitt valgt til å være en bærer av: minst én polymorfisme valgt
Utvikling av nye kreftbehandlinger -hundens rolle
 Utvikling av nye kreftbehandlinger -hundens rolle Þóra J. Jónasdóttir, DVM, PhD Norges veterinærhøgskole Disposisjon Bakgrunn og komparative kreftformer Muligheter ved forskning på spontan kreft hos hund
Utvikling av nye kreftbehandlinger -hundens rolle Þóra J. Jónasdóttir, DVM, PhD Norges veterinærhøgskole Disposisjon Bakgrunn og komparative kreftformer Muligheter ved forskning på spontan kreft hos hund
Generell immunologi og immunforsvaret på 45 minutt
 Generell immunologi og immunforsvaret på 45 minutt NITO BIOINGENIØRFAGLIG INSTITUTT, Immunologi og immunologiske metoder, etterutdanningskurs 27. 28.november 2018 Kirsti Hokland bioingeniør og universitetslektor
Generell immunologi og immunforsvaret på 45 minutt NITO BIOINGENIØRFAGLIG INSTITUTT, Immunologi og immunologiske metoder, etterutdanningskurs 27. 28.november 2018 Kirsti Hokland bioingeniør og universitetslektor
Oppgave: MED1100-3_OPPGAVE2_V18_ORD
 Side 15 av 46 Oppgave: MED1100-3_OPPGAVE2_V18_ORD Del 1: Hvilke av de følgende celler uttrykker normalt (i hvilende tilstand) HLA klasse II molekyler hos mennesket? Angi de tre riktigste svarene. Fibroblaster
Side 15 av 46 Oppgave: MED1100-3_OPPGAVE2_V18_ORD Del 1: Hvilke av de følgende celler uttrykker normalt (i hvilende tilstand) HLA klasse II molekyler hos mennesket? Angi de tre riktigste svarene. Fibroblaster
