Veileder for oppdragsforskning ved OUS
|
|
|
- Marianne Samuelsen
- 5 år siden
- Visninger:
Transkript
1 Veileder for oppdragsforskning ved OUS Versjon
2 Innholdsfortegnelse Innholdsfortegnelse Endringer siden forrige versjon Hensikt og omfang Ansvar Fremgangsmåte Vurdering av gjennomførbarhet (feasibility) Planlegging, forankring og godkjenning Oppstarts- og formaliseringsfasen Innmelding av studie til Inven Budsjett og kontrakt Kvalitetssikring og formalisering av avtaler Registreringer og søknader Gjennomføringsfasen Elektronisk studiearkiv Oppstartsmøte/initiering Studiemedisin (legemiddelstudier) ,4 Randomisering Monitorering Endringer i studieprotokoll Rapportering av bivirkninger Økonomioppfølging Avslutnings- og arkiveringsfasen Melding om studieslutt Økonomisk sluttoppgjør Arkivering Interne (OUS og HSØ) referansedokumenter Versjon
3 1 Endringer siden forrige versjon Dette er tredje versjon av dokumentet. Teksten i noen kapitler er redigert og oppdatert. Melding om klinisk utprøvning og evaluering av medisinsk utstyr skal nå sendes Statens legemiddelverk. Avsnittet om pasientreiser er oppdatert etter ny pasientreiseforskrift. 2 Hensikt og omfang Hensikten med dette dokumentet er å gi en praktisk veiledning til de som er involvert i oppdragsforskning generelt og klinisk legemiddelutprøving og utprøvning av medisinsk teknisk utstyr spesielt. 3 Ansvar Ansvar i henhold til denne veileder følger OUS retningslinjer slik det er definert i ehåndboksdokumentene: Roller og ansvar i kliniske legemiddelutprøvinger og utprøvning av medisinsk teknisk utstyr, Forskningsinstruksen, Forskningsprosedyren og forvaltningsavtale med Inven2. 4 Fremgangsmåte 4.1 Vurdering av gjennomførbarhet (feasibility) En fesasibilityprosess finner ofte sted før beslutning om studien skal gjennomføres er tatt. I denne prosessen må bl.a. følgende avklares: Er pasientgrunnlaget til stede? Har avdelingen konkurrerende studier? Har avdelingen ressurser til å håndtere studien? Er logistikken i studien gjennomførbar? Har sykehuset det nødvendige utstyret for å utføre studieprosedyrene? Har serviceavdelingene kapasitet og ressurser til å følge opp studien? 4.2 Planlegging, forankring og godkjenning Hovedutprøver (PI) er ansvarlig for å forankre studien ved egen avdeling samt ved berørte serviceavdelinger for å sikre at det finnes tilgjengelige ressurser og kapasitet for å gjennomføre studien. Hovedutprøver er også ansvarlig for å søke om intern godkjenning fra Seksjon for informasjonssikkerhet og personvern. Dette gjøres ved å sende Skjema for behandling av helseforskningsdata sammen med protokoll, kopi av REK-søknad og pasientinformasjon til godkjenning@ous-hf.no. Dette bør skje samtidig med innsendelse av søknaden til REK. Utprøving av medisinsk-teknisk utstyr avklares med leder av Forsknings-og utviklingsavdelingen, Medisinsk teknologisk virksomhetsområde (tlf: ), se ehåndbok. Versjon
4 Der hvor utlevering av helse- og personopplysninger skjer elektronisk til ekstern virksomhet (f.eks. ecrf), må det fremlegges en risikovurdering av løsningen. Informasjon om dette finnes her: Utlevering av helse- og personopplysninger Når REK sender svar på søknaden til prosjektleder, får Seksjon for informasjonssikkerhet og personvern automatisk en kopi av svaret. 4.3 Oppstarts- og formaliseringsfasen Innmelding av studie til Inven2 Inven2 ivaretar avtalemessige og økonomiske forhold i alle studier med industriell sponsor. Inven2 håndterer også økonomisk oppfølging underveis i studien. Når det er besluttet at studien skal gjennomføres ved OUS og protokoll foreligger, skal sponsor eller sponsors representant melde studien til Inven2 ved å sende inn nettbasert skjema «Research Information Form» Hver studie får et unikt prosjektnummer (M-nummer). Dette skal brukes i all videre korrespondanse med Inven2, i kontrakt og ved fakturering Budsjett og kontrakt Inven2 setter opp en budsjettmal tilpasset studieprotokollen. Budsjettmalen sendes til hovedutprøver som er ansvarlig for å fylle ut skjemaet og returnere det til Inven2. Dette innebærer å: Estimere antall timer for studiesykepleier og lege ved hvert studiebesøk, samt tidsbruk i forbindelse med oppstart og andre avtalte oppgaver, f.eks. REK-søknad (for nasjonal koordinerende utprøver) og tiltak i forbindelse med rekruttering av pasienter. Innhente svar på pris- og kapasitetsforespørsler til serviceavdelingene som skal utføre studieprosedyrer. Skjema for prisforespørsel og veiledning finnes på nettsiden for oppdragsforskning. For at serviceavdelinger skal kunne gi riktig pris på sine prosedyrer, er det viktig at alle protokoller og manualer foreligger. Vurdere om sykehusapoteket skal involveres eller om medikamentene skal oppbevares lokalt. Inven2 håndterer egne avtaler for sykehusapotekene. Dersom medikamentene skal oppbevares lokalt på avdelingen, sjekk sponsors krav til oppbevaring som temperatur, lys, fuktighet osv. Når apoteket ikke er involvert er det spesielt viktig å avtale kontaktperson og leveringsadresse for studiemedikamentene med oppdragsgiver Kvalitetssikring og formalisering av avtaler Studieavtalen mellom oppdragsgiver, Inven2 og OUS skal godkjennes og signeres av avdelingsleder (på vegne av OUS), Inven2 og oppdragsgiver. Dersom avdelingsleder også er utprøver i studien skal klinikkleder signere avtalen. Hovedutprøver signerer på at han/hun lest og forstått avtalen. Versjon
5 4.3.4 Registreringer og søknader Sponsor er som regel behjelpelig med å få ferdigstilt søknader og de nødvendige vedlegg som kreves ved innsendelse av søknader om godkjenning av studien. For å unngå forsinkelser er det nødvendig å avklare arbeidsfordelingen mellom sponsor og hovedutprøver på et tidlig tidspunkt. Dette er spesielt viktig når sponsoren bruker en Contract Research Organisation (CRO) til å administrere studien. Statens Legemiddelverk (SLV) ved legemiddelstudier Som regel er det sponsor som søker om godkjenning hos SLV. SLV vurderer kliniske utprøvinger av legemidler og medisinsk-teknisk utstyr, både med og uten markedsføringstillatelse. Dersom sponsor forespør prosjektlederen om å søke myndighetene finnes det en veileder på SLVs nettsider. Regional Etisk Komité for helseforskning (REK) REK skal forhåndsgodkjenne medisinske- og helsefaglige forskningsprosjekter og generelle forskningsbiobanker, samt gi dispensasjon fra taushetsplikt for annen type forskning. Det er nasjonalt koordinerende utprøvers (NC) ansvar å søke om godkjenning av studien, men sponsor er ofte behjelpelig med utforming av søknaden, samtykker og andre dokumenter. NC oppretter en prosjektsøknad i REK-portalen, og kan gi tilgang til én eller flere medbrukere. Medbrukerne får direkte lese- og skrivetilgang, men det er kun NC som kan sende inn prosjektsøknaden. Dersom studien foregår ved flere sentra i Norge må hvert senter oppgis som forskningsansvarlig i prosjektsøknaden. REK har utarbeidet maler for pasientinformasjon og samtykke. Malene bør følges i størst mulig grad. Det er NC som står ansvarlig for pasientinformasjonen og det er derfor viktig at man inntar en aktiv rolle i utarbeidelse av denne. Forskningsbiobank En forskningsbiobank er en samling humant biologisk materiale som anvendes i et forskningsprosjekt eller skal anvendes til forskning (jf. Helseforskningsloven). Som regel er det sponsor som oppretter studiespesifikk forskningsbiobank. Dersom det skal opprettes en biobank lokalt på OUS skal dette skje i tråd med Helseforskningsloven og i samsvar med institusjonens prosedyrer og retningslinjer for forskning. Registrering av studier i ClinicalTrials.gov Normalt er det sponsor eller CRO som tar seg av registreringen av studien i Clinical- Trials.gov. EudraCT Nummer I de fleste tilfeller er det Sponsor eller CRO som sender inn EudraCT-skjema for å registrere studien i European Clinical Trials Database. Registreringen generer et EudraCT-nummer som man trenger for å søke om godkjenning av studiestart hos Statens Legemiddelverk (SLV) ved legemiddelstudier og Regional etisk komité (REK) for både legemiddel- og andre type oppdragsstudier. EudraCT-skjema legges ved søknaden. Versjon
6 Helsenorge.no Kliniske behandlings- og rehabiliteringsstudier som kan påvirke pasientforløpet til forskningsdeltakerne og som er åpne for inklusjon, eller der REK-godkjenning foreligger og startdato er fastsatt, publiseres på sykehusets nettside for kliniske studier. Studier som er publisert her vil speiles på Helsenorges nettside helsenorge.no/kliniske-studier. Nettsiden er etablert på oppdrag fra Helse og omsorgsdepartementet (HOD) og skal fungere som en nasjonal oversikt. På denne måten kan pasienter, pårørende og henvisende leger se og orientere seg om hvilke studier som foregår ved hvilke helseforetak. Det er NC som er ansvarlig for å registrere studien. For fremgangsmåte, se ehåndboksdokumentet Registrering av kliniske studier i ClinicalTrials.gov og publisering på OUS' nettsider oslo-universitetssykehus.no med visning på helsenorge.no 4.4 Gjennomføringsfasen Når alle registreringer og godkjenninger er på plass, studieavtalen signert og sponsor har gitt klarsignal, kan studien starte. Følgende anbefales å gjøre før man starter inklusjon av pasienter: Gjennomgang av det elektroniske arkivet hvor alle utkast av de forskjellige dokumenter blir lagt i enten eldre versjoner - eller utkast -mappen. Kun siste versjon -mappen skal inneholde de dokumenter som er godkjent av godkjenningsinstanser og som skal brukes i studien. Lage et flytskjema med alle studieprosedyrer (f.eks. i Excel) for å planlegge studieforløp for hver enkel pasient. Sjekke om alt nødvendig utstyr er på plass (laboratorieutstyr, EKG-maskin etc.). Sjekke når studiemedisinen blir tilgjengelig, ev. retningslinjer for oppbevaring. Sjekke om alt studiepersonell har gjennomført ev. e-læringsprogrammer for å få de nødvendige tilganger til f. eks e-crf og bildeoverføringsprogrammer. Samle inn oppdaterte CV-er fra alt personell involvert i studien. Fordele arbeidsoppgaver og fylle dette inn i delegeringslogg Bestemme hva som er kildedata og hvor disse finnes (DIPS, lab-ark, dagbøker, etc.) Elektronisk studiearkiv Det oppfordres til å benytte den standardiserte malen for elektronisk lagring av studiedokumentasjon som finnes på OUS nettside for oppdragsforskning. Dette er imidlertid ikke et godkjent dokumentstyringssystem, såessensiell dokumentasjon bør derfor i tillegg lagres i papirform under studiens gjennomføring Oppstartsmøte/initiering Oppstartsmøtet er et samarbeid mellom sponsor og ansvarlig utprøver (PI) for studien. Sponsor er ansvarlig for å belyse vitenskapelig bakgrunn for studien og hva som testes, gi en grundig gjennomgang av studieprosedyrene, samt forventede bivirkninger og behandling av disse. PI er ansvarlig for å innkalle studiepersonale og de personer på serviceavdelinger som er ansvarlige for studieprosedyrer. Versjon
7 I forbindelse med oppstart/initiering er det vanlig at sponsor utleverer studiepermer til Investigator Site File (ISF). Det anbefales at man gjør seg kjent med inndelingen i permene og begynner å legge inn dokumenter helt fra starten av studien. ISF skal være oppdatert til enhver tid i forbindelse med monitorering eller audit (kontrollbesøk) fra sponsoren, men også fordi myndighetene kan komme på inspeksjonsbesøk på kort varsel Studiemedisin (legemiddelstudier) Bestilling og levering Når apoteket ikke er involvert, er det spesielt viktig å avtale med sponsor hvor studiemedisinen skal leveres. Avtal levering til minste detalj; sykehus, bygning, etasje, rom og hvem de skal leveres til. Be sponsor om å informere mottakeren når studiemedisinene sendes slik at det er mulig å følge med om de blir levert riktig. Dersom studiemedisinene blir levert med temperaturregistrering under transport, sjekk at det ikke har vært noen temperaturavvik under transporten og gi tilbakemelding til sponsor. Ved mottak, sjekk pakkseddelen mot innholdet som for eksempel: batchnummer, holdbarhet, virkestoff/styrke/mengde, antall pakninger osv. Oppbevaring Dersom studiemedisinene skal oppbevares på avdelingen, skal de lagres i henhold til oppbevaringsbetingelser beskrevet i enten Investigators Brochure (IB), for legemidler uten markedsføringstillatelse i Norge, eller Summary of Product Characteristics (SmPC), for legemidler med markedsføringstillatelse i Norge. Studiemedisinen skal oppbevares adskilt fra andre legemidler i et låsbart skap eller rom med adgangskontroll. Konferer med sponsor hvor ofte oppbevaringsbetingelser som for eksempel temperatur skal loggføres. Administrering av studiemedisin Det skal alltid føres medikamentregnskap for studiemedisin. Konferer med sponsor hvordan regnskapet skal føres eller bruk skjemaene vedlagt den nasjonale prosedyren: Legemiddelhåndtering ved gjennomføring av kliniske legemiddelstudier. 4.4,4 Randomisering Randomiseringen er beskrevet i protokollen og omfatter en plan for allokering av studiedeltakere til behandlings- og/eller dosegrupper. Det finnes forskjellige systemer for randomisering og det er viktig at sponsor forklarer på oppstartsmøte hvordan randomiseringen foregår i praksis. Ved dobbelblinde studier bør sponsor også forklare rutinene for avblinding Monitorering Taushetserklæring Til tross for at monitor har skrevet under en taushetserklæring hos sin arbeidsgiver, krever OUS at monitoren skriver under OUS taushetserklæring som finnes i e-håndbok på norsk eller engelsk. Dette behøver ikke å være per studie, men én taushetserklæring som vedkommende skriver under for alle studier hun/han arbeider med på OUS. Den signerte Versjon
8 taushetserklæringen sendes til sakarkivet for elektronisk arkivering Monitor bør få en kopi av erklæringen. Tilgang til pasientjournal I henhold til prosedyren Tilgang til DIPS for forsknings- og kvalitetsregistre i ehåndbok kan monitor gis tilgang til den elektroniske pasientjournalen for de pasientene som deltar i studien. Dette krever imidlertid at monitor har en bruker-id hos OUS. For å få dette må monitor meldes inn i Personalportalen som en forenklet ansettelse. Videre må monitor gjøres kjent med OUS sikkerhetsinstruks og få opplæring i DIPS. Tilgangen er strengt personlig og ved bytte av monitor må tilgangen slettes. I mange tilfeller kan prosessen med å gi eksterne monitorer elektronisk tilgang til pasientjournalen være for omfattende. Løsningen er da å skrive ut kun de notater fra pasientjournalen som er aktuelle for studien. Utskriftene fra journalen oppbevares i pasientens studieperm og makuleres umiddelbart etter at pasienten avslutter studien. Det er viktig å presisere overfor sponsor at utskrifter fra journal er et øyeblikksbilde og ikke i seg selv kan regnes som kildedata da kilden alltid vil være OUS elektroniske journalsystem Endringer i studieprotokoll Endringer i studieprotokollen som medfører en endringssøknad til REK og/eller SLV skal også meldes internt til Oslo Sykehusservice og personvernombudet, som ved oppstart. Endringen meldes via e-post til godkjenning@ous-hf.no, hvor man legger ved endringssøknaden med vedlegg sendt inn til REK Rapportering av bivirkninger PI har ansvar for å melde bivirkninger til sponsor og sistnevnte er ansvarlig for å rapportere til Statens legemiddelverk (SLV). Følgende dokumenter skal sendes av sponsor: Rapporter om bivirkninger og SUSARs (suspected, unexpected, serious, adverse reactions) Årsrapport Oppdatering av Investigational Medicinal Product Dossier (IMPD) Oppdatering av Investigators Brochure (IB) og Dear Investigator Letter (DIL) 90-dagersmelding etter avsluttet klinisk utprøving Sluttrapport Økonomioppfølging Fakturagrunnlag Med utgangspunkt i budsjettmalen (se avsnitt Budsjett og kontrakt) setter Inven2 opp et fakturagrunnlag for studien. Dette fakturagrunnlaget sendes ut halvårlig og skal fylles ut med datoer for studieprosedyrer som er gjennomført og monitorert siden forrige rapportering. På Inven2s nettsider kan du finne en veileder for utfylling av fakturagrunnlaget. Ved spørsmål eller endringer vedrørende økonomioppfølging kan det tas kontakt med Inven2s økonomiavdeling eller avdeling for kliniske studier. Versjon
9 Pasientreiser Pasienter som deltar i kliniske studier har rett til dekning av reiseutgifter på samme måte som pasienter som kommer til ordinær behandling når studien er godkjent i helseforetaket se helsenorge.no for informasjon om hvordan reisen refunderes. Reiser under 10 km dekkes ikke og eventuell refusjon av dette må avtales med sponsor. 4.5 Avslutnings- og arkiveringsfasen Melding om studieslutt Studien regnes som avsluttet når siste pasient er ute av studien ved alle sentrene, alle data er samlet inn og sponsor har gitt beskjed om at de ikke har flere spørsmål. Hovedutprøver har ansvar for at alle essensielle dokumenter arkiveres i Investigator Site File (ISF) og at studien formelt avsluttes. Husk å gi beskjed til serviceavdelinger om at studien er avsluttet. Sponsor har ansvar for at sluttmelding sendes til SLV innen 90 dager etter at studien er avsluttet i Norge og (ved internasjonale studier) innen 90 dager etter at studien er avsluttet i alle land. Sluttrapport sendes SLV innen 12 måneder etter definert slutt i EudraCT-skjemaet, dvs. når utprøvingen i alle land er avsluttet. Se SLVs nettside «Rapportering for kliniske studier». Til REK sendes sluttmelding ved prosjektslutt, som definert i søknaden. Sluttrapportering er også beskrevet i SOP Sluttrapportering til SLV og REK. Merk at dette dokumentet er skrevet med tanke på studier med ikke-kommersiell sponsor. Det skal også sendes en beskjed til personvernombud ved OUS om at studien er avsluttet Økonomisk sluttoppgjør Prosjektleder er ansvarlig for å informere Inven2 om at studien er avsluttet slik at sluttfakturering kan utføres og studiekonto gjøres opp. I den forbindelse er det også viktig å informere serviceavdelinger om at studien er avsluttet Arkivering For kliniske legemiddelutprøvinger er kravet til oppbevaring av essensielle dokumenter minimum 15 år etter at studien er avsluttet ved alle senter. Se NorCRIN SOP Avslutning og arkivering av kliniske legemiddelutprøvninger. OUS har en avtale med firmaet Iron Mountain for lagring av papirdokumenter. Kostnader forbundet med dette dekkes av industripart og inkluderes i avtalen. Det er utarbeidet en retningslinje for hvordan dette håndteres: Praktiske løsninger for lagring av papirdokumentasjon i kliniske legemiddelutprøvninger Versjon
10 5 Interne (OUS og HSØ) referansedokumenter 1. OUS Instruks: Ansvars- og myndighetsforhold i forskning (Forskningsinstruksen) 2. Samarbeidsavtale mellom Helse Sør Øst RHF (helseregionen) og Legemiddelindustrien (LMI) 3. OUS Retningslinje: Samhandling med industri og næringsliv - inkl. leverandørfinansiering av kurs, møter og konferanser 4. OUS Retningslinje: Roller og ansvar i kliniske legemiddelutprøvinger Versjon
HVORFOR, AV HVEM OG HVORDAN
 MONITORERING HVORFOR, AV HVEM OG HVORDAN MONITORER VED HAUKELAND UNIVERSITETSSYKEHUS Forsknings- og utviklingsavdelingen Seksjon for pasientsikkerhet Epost: monitor@helse-bergen.no Ingunn Heie Anundskås
MONITORERING HVORFOR, AV HVEM OG HVORDAN MONITORER VED HAUKELAND UNIVERSITETSSYKEHUS Forsknings- og utviklingsavdelingen Seksjon for pasientsikkerhet Epost: monitor@helse-bergen.no Ingunn Heie Anundskås
Ahus Roller og ansvar i kliniske legemiddelutprøvinger og utprøving av medisinsk utstyr. Gyldig fra: Revisjonsfrist:
 Ahus Roller og ansvar i kliniske legemiddelutprøvinger og utprøving av medisinsk utstyr 1. Hensikt Hensikten med denne prosedyren (Standard Operating Procedure - SOP) er å beskrive den overordnede rolle,
Ahus Roller og ansvar i kliniske legemiddelutprøvinger og utprøving av medisinsk utstyr 1. Hensikt Hensikten med denne prosedyren (Standard Operating Procedure - SOP) er å beskrive den overordnede rolle,
Hensikten med SOP-en (Standard Operating Procedure/retningslinje) er å beskrive hvordan legemiddelhåndtering i kliniske studier bør gjennomføres.
 1 HENSIKT Hensikten med SOP-en (Standard Operating Procedure/retningslinje) er å beskrive hvordan legemiddelhåndtering i kliniske studier bør gjennomføres. Retningslinjen skal sikre at legemiddelhåndtering
1 HENSIKT Hensikten med SOP-en (Standard Operating Procedure/retningslinje) er å beskrive hvordan legemiddelhåndtering i kliniske studier bør gjennomføres. Retningslinjen skal sikre at legemiddelhåndtering
Med forskningsbiobank forstås en samling humant biologisk materiale som anvendes eller skal anvendes til forskning.
 Biobankinstruks 1. Endringer siden siste versjon 2. Definisjoner Biobank Med diagnostisk biobank og behandlingsbiobank (klinisk biobank) forstås en samling humant biologisk materiale som er avgitt for
Biobankinstruks 1. Endringer siden siste versjon 2. Definisjoner Biobank Med diagnostisk biobank og behandlingsbiobank (klinisk biobank) forstås en samling humant biologisk materiale som er avgitt for
Innføring i Good Clinical Practice (GCP) og hva er spesielt hos barn?
 Innføring i Good Clinical Practice (GCP) og hva er spesielt hos barn? Martha Colban, Avdelingsleder Avdeling for klinisk forskningsstøtte Virksomhetsområde forskningsstøtte Oslo universitetssykehus HF
Innføring i Good Clinical Practice (GCP) og hva er spesielt hos barn? Martha Colban, Avdelingsleder Avdeling for klinisk forskningsstøtte Virksomhetsområde forskningsstøtte Oslo universitetssykehus HF
Heidi Glosli Vårseminaret 2. juni 2015. Klinisk legemiddelforskning - i spesialisthelsetjenesten
 Heidi Glosli Vårseminaret 2. juni 2015 Klinisk legemiddelforskning - i spesialisthelsetjenesten Nasjonalt kompetansenettverk for legemidler til barn St.meld. nr. 18 (2004-2005) (Legemiddelmeldingen) Stortinget
Heidi Glosli Vårseminaret 2. juni 2015 Klinisk legemiddelforskning - i spesialisthelsetjenesten Nasjonalt kompetansenettverk for legemidler til barn St.meld. nr. 18 (2004-2005) (Legemiddelmeldingen) Stortinget
1. Endringer siden siste versjon. 2. Hensikt og omfang
 Oslo universitetssykehus HF Dokument-ID: 62 Versjon: 0 Retningslinjer Intern godkjenning for Medisinsk og Helsefaglig forskning, og Kvalitetssikring Virksomhetsomfattende Utarbeidet av: Stab FoU Godkjent
Oslo universitetssykehus HF Dokument-ID: 62 Versjon: 0 Retningslinjer Intern godkjenning for Medisinsk og Helsefaglig forskning, og Kvalitetssikring Virksomhetsomfattende Utarbeidet av: Stab FoU Godkjent
Heidi Glosli Etterutdanning for Barnesykepleiere 20. oktober 2015. Legemiddelutprøving på barn
 Heidi Glosli Etterutdanning for Barnesykepleiere 20. oktober 2015 Legemiddelutprøving på barn Bruk av legemidler utenfor godkjenning til barn og ungdom på sykehus Arna Teigens masteroppgave 2 sengeposter
Heidi Glosli Etterutdanning for Barnesykepleiere 20. oktober 2015 Legemiddelutprøving på barn Bruk av legemidler utenfor godkjenning til barn og ungdom på sykehus Arna Teigens masteroppgave 2 sengeposter
Helseforskningsloven konsekvenser for ansvarsdeling mellom UNN og UiT
 Helseforskningsloven konsekvenser for ansvarsdeling mellom UNN og UiT Anne Husebekk Fag- og forskningssjef, UNN Professor, UiT 2003 2005 2007 2009 Formål; Lovens formål er å fremme god og etisk forsvarlig
Helseforskningsloven konsekvenser for ansvarsdeling mellom UNN og UiT Anne Husebekk Fag- og forskningssjef, UNN Professor, UiT 2003 2005 2007 2009 Formål; Lovens formål er å fremme god og etisk forsvarlig
UiO : Universitetet i Oslo Universitetsdirektøren
 UiO : Universitetet i Oslo lav Gyldig fra: l 15.05.2012 Gj k K ^/^vt r4 ' Gunn-Elin Aa. Bjomeboe MEDISINSK OG HELSEFAGLIG FORSKNING Virksomhet som utføres med vitenskapelig metodikk for å skaffe til veie
UiO : Universitetet i Oslo lav Gyldig fra: l 15.05.2012 Gj k K ^/^vt r4 ' Gunn-Elin Aa. Bjomeboe MEDISINSK OG HELSEFAGLIG FORSKNING Virksomhet som utføres med vitenskapelig metodikk for å skaffe til veie
Forskrift om klinisk utprøving: Hva betyr begrepene og hva er annerledes enn helseforskningsloven
 Forskrift om klinisk utprøving: Hva betyr begrepene og hva er annerledes enn helseforskningsloven Ingvild Aaløkken Seksjon for preklinikk og klinisk utprøving Statens legemiddelverk Hensynet til forsøkspersonenes
Forskrift om klinisk utprøving: Hva betyr begrepene og hva er annerledes enn helseforskningsloven Ingvild Aaløkken Seksjon for preklinikk og klinisk utprøving Statens legemiddelverk Hensynet til forsøkspersonenes
Ledelse og personvern. Forenklet sammendrag av de styrende dokumenter for personvern og informasjonssikkerhet ved Oslo universitetssykehus
 Ledelse og personvern Forenklet sammendrag av de styrende dokumenter for personvern og informasjonssikkerhet ved Oslo universitetssykehus Stab fag og pasientsikkerhet Seksjon for personvern og informasjonssikkerhet
Ledelse og personvern Forenklet sammendrag av de styrende dokumenter for personvern og informasjonssikkerhet ved Oslo universitetssykehus Stab fag og pasientsikkerhet Seksjon for personvern og informasjonssikkerhet
1/19/2015. From Science to Business. Inven2, kontraktsprosess og visjon. Ole Kristian Hjelstuen Adm dir
 1/19/2015 From Science to Business Inven2, kontraktsprosess og visjon Ole Kristian Hjelstuen Adm dir 1 Inven2: Betjener ca 6000 forskere 1/19/2015 2 Turning Top Science into Products Innovasjonstall 2014
1/19/2015 From Science to Business Inven2, kontraktsprosess og visjon Ole Kristian Hjelstuen Adm dir 1 Inven2: Betjener ca 6000 forskere 1/19/2015 2 Turning Top Science into Products Innovasjonstall 2014
NorCRIN. Norwegian Clinical Research Infrastructure Network. Norsk Biotekforum, 26. november 2013
 NorCRIN Norwegian Clinical Research Infrastructure Network Norsk Biotekforum, 26. november 2013 Sigrun K. Sæther NorCRIN nettverkskoordinator St. Olavs Hospital, Trondheim Bestilling Fra Helse- og Omsorgsdepartementet
NorCRIN Norwegian Clinical Research Infrastructure Network Norsk Biotekforum, 26. november 2013 Sigrun K. Sæther NorCRIN nettverkskoordinator St. Olavs Hospital, Trondheim Bestilling Fra Helse- og Omsorgsdepartementet
NorCRIN. Norwegian Clinical Research Infrastructure Network Nettverk mellom forskningsstøtteenheter ved de 6 universitetssykehusene i Norge
 NorCRIN Norwegian Clinical Research Infrastructure Network Nettverk mellom forskningsstøtteenheter ved de 6 universitetssykehusene i Norge Bakgrunn Ønske om bedre klinisk behandling Ønske om forskningsbasert
NorCRIN Norwegian Clinical Research Infrastructure Network Nettverk mellom forskningsstøtteenheter ved de 6 universitetssykehusene i Norge Bakgrunn Ønske om bedre klinisk behandling Ønske om forskningsbasert
Avslutning av studie: Rapporteringer Data Closure underveis Intrimanalyser
 Avslutning av studie: Rapporteringer Data Closure underveis Intrimanalyser Gøril Knutsen Country Clinical Operations Manager Abbvie Clinical Data Lifecycle Gøril Knutsen. Kurs om kliniske studier, Haukeland
Avslutning av studie: Rapporteringer Data Closure underveis Intrimanalyser Gøril Knutsen Country Clinical Operations Manager Abbvie Clinical Data Lifecycle Gøril Knutsen. Kurs om kliniske studier, Haukeland
Statens legemiddelverks rolle i kliniske studier og hva skal det søkes om?
 Statens legemiddelverks rolle i kliniske studier og hva skal det søkes om? Ingvild Aaløkken Seksjon for preklinikk og klinisk utprøving Statens legemiddelverk AGENDA Regelverket Søknader og rapporter til
Statens legemiddelverks rolle i kliniske studier og hva skal det søkes om? Ingvild Aaløkken Seksjon for preklinikk og klinisk utprøving Statens legemiddelverk AGENDA Regelverket Søknader og rapporter til
1. Endringer siden siste versjon. 2. Hensikt og omfang. 3. Ansvar. Instruks Forskningsinstruks. Oslo universitetssykehus HF
 Oslo universitetssykehus HF Dokument-ID: 60 Versjon: 0 Utarbeidet av: Stab FoU Instruks Forskningsinstruks Virksomhetsomfattende Godkjent av: Siri Hatlen Dato: 24.06.2010 Gyldig fra: 24.06.2010 Gyldig
Oslo universitetssykehus HF Dokument-ID: 60 Versjon: 0 Utarbeidet av: Stab FoU Instruks Forskningsinstruks Virksomhetsomfattende Godkjent av: Siri Hatlen Dato: 24.06.2010 Gyldig fra: 24.06.2010 Gyldig
Logistikk, etikk og sikkerhet. Gardermoen 14. september 2015 Ingvild Kjeken
 Logistikk, etikk og sikkerhet Gardermoen 14. september 2015 Ingvild Kjeken Logistikk, etikk og sikkerhet BRO-prosjektet er en multisenterstudie hvor mange personer er involvert i rekruttering av pasienter
Logistikk, etikk og sikkerhet Gardermoen 14. september 2015 Ingvild Kjeken Logistikk, etikk og sikkerhet BRO-prosjektet er en multisenterstudie hvor mange personer er involvert i rekruttering av pasienter
Veileder for registrering av kvalitets- og forskningsprosjekter i eskjema for internkontroll på Ahus
 Veileder for registrering av kvalitets- og forskningsprosjekter i eskjema for internkontroll på Ahus Vedlegg: Viktig informasjon om kliniske behandlingsstudier 1 Veileder til registrering av kvalitets-
Veileder for registrering av kvalitets- og forskningsprosjekter i eskjema for internkontroll på Ahus Vedlegg: Viktig informasjon om kliniske behandlingsstudier 1 Veileder til registrering av kvalitets-
Veileder til registrering av kliniske studier i ClinicalTrials.gov
 Veileder til registrering av kliniske studier i ClinicalTrials.gov 04.12.2018 Versjon 1.0 1 Fremgangsmåte 1. Opprettelse av individuell konto ClinicalTrials.gov bruker Protocol Registration and Results
Veileder til registrering av kliniske studier i ClinicalTrials.gov 04.12.2018 Versjon 1.0 1 Fremgangsmåte 1. Opprettelse av individuell konto ClinicalTrials.gov bruker Protocol Registration and Results
Sykehusfarmasøytens rolle i kliniske studier. Siri Mork Sykehusapoteket Oslo, Radiumhospitalet Farmasidagene 2013
 Sykehusfarmasøytens rolle i kliniske studier Siri Mork Sykehusapoteket Oslo, Radiumhospitalet Farmasidagene 2013 Apotekets rolle Utprøver har ansvaret for legemiddelhåndteringen Utprøver delegerer oppgaven
Sykehusfarmasøytens rolle i kliniske studier Siri Mork Sykehusapoteket Oslo, Radiumhospitalet Farmasidagene 2013 Apotekets rolle Utprøver har ansvaret for legemiddelhåndteringen Utprøver delegerer oppgaven
Forskningsprosedyre. Prosedyre. Oslo universitetssykehus HF
 Oslo universitetssykehus HF Dokument-ID: 61 Versjon: 0 Utarbeidet av: Stab FoU Prosedyre Forskningsprosedyre Virksomhetsomfattende Godkjent av: Siri Hatlen Dato: 24.06.2010 Gyldig fra: 24.06.2010 Gyldig
Oslo universitetssykehus HF Dokument-ID: 61 Versjon: 0 Utarbeidet av: Stab FoU Prosedyre Forskningsprosedyre Virksomhetsomfattende Godkjent av: Siri Hatlen Dato: 24.06.2010 Gyldig fra: 24.06.2010 Gyldig
Status og videre arbeid med kliniske studier
 Helse- og omsorgsdepartementet Status og videre arbeid med kliniske studier Maiken Engelstad, Ph.D. MPH, Spesialisthelsetjenesteavdelingen Kliniske studier i Norge, DM, Arendalsuka 17. august 2017 Hva
Helse- og omsorgsdepartementet Status og videre arbeid med kliniske studier Maiken Engelstad, Ph.D. MPH, Spesialisthelsetjenesteavdelingen Kliniske studier i Norge, DM, Arendalsuka 17. august 2017 Hva
Skjemaet skal ikke benyttes for forskningsstudier som skal godkjennes av REK.
 Meldeskjema for forskningsstudier, kvalitetssikring og annen aktivitet som medfører behandling av personopplysninger som er melde- eller konsesjonspliktig i henhold til helseregisterloven og personopplysningsloven
Meldeskjema for forskningsstudier, kvalitetssikring og annen aktivitet som medfører behandling av personopplysninger som er melde- eller konsesjonspliktig i henhold til helseregisterloven og personopplysningsloven
Retningslinjen er veiledende for alle kliniske legemiddelutprøvinger som gjennomføres ved Oslo universitetssykehus HF.
 Versjn nr. 1.1 1 HENSIKT Hensikten med SOP-en (Standard Operating Prcedure/retningslinje) er å beskrive den verrdnede rlle, ansvar g ppgavefrdeling i kliniske legemiddelutprøvinger. Retningslinjen skal
Versjn nr. 1.1 1 HENSIKT Hensikten med SOP-en (Standard Operating Prcedure/retningslinje) er å beskrive den verrdnede rlle, ansvar g ppgavefrdeling i kliniske legemiddelutprøvinger. Retningslinjen skal
UiO: Universitetet i Oslo Universitetsdirektøren
 UiO: Universitetet i Oslo Versjon: 1 Gyldigfra: l _ 15.02.2012 MEDISINSKOG HELSEFAGLIG FORSKNING Virksomhet som utføres med vitenskapelig metodikk for å skaffe til veie ny kunnskap om helse, og sykdom.
UiO: Universitetet i Oslo Versjon: 1 Gyldigfra: l _ 15.02.2012 MEDISINSKOG HELSEFAGLIG FORSKNING Virksomhet som utføres med vitenskapelig metodikk for å skaffe til veie ny kunnskap om helse, og sykdom.
Personvernerklæring Stendi
 Personvernerklæring Stendi Ditt personvern er viktig for oss. Nedenfor kan du lese mer om hvordan vi aktivt jobber med å ivareta ditt personvern. Her vil vi forklare hvordan og hvorfor vi samler inn og
Personvernerklæring Stendi Ditt personvern er viktig for oss. Nedenfor kan du lese mer om hvordan vi aktivt jobber med å ivareta ditt personvern. Her vil vi forklare hvordan og hvorfor vi samler inn og
Utprøvende behandling noe for deg? Informasjon om deltakelse i kliniske studier
 Novartis Norge AS Utprøvende behandling noe for deg? Informasjon om deltakelse i kliniske studier Innledning Å velge om du skal delta i utprøvende behandling eller ikke, er et viktig og personlig valg.
Novartis Norge AS Utprøvende behandling noe for deg? Informasjon om deltakelse i kliniske studier Innledning Å velge om du skal delta i utprøvende behandling eller ikke, er et viktig og personlig valg.
Om å samarbeide for pasientens beste
 Om å samarbeide for pasientens beste Nyttige råd med utgangspunkt i Helse Sør-Østs antikorrupsjonsprogram og samarbeidsavtalene mellom HSØ/LFH, HSL/LFH Grete Solli, spesialrådgiver Helse Sør-Øst RHF Samfunnsansvar;
Om å samarbeide for pasientens beste Nyttige råd med utgangspunkt i Helse Sør-Østs antikorrupsjonsprogram og samarbeidsavtalene mellom HSØ/LFH, HSL/LFH Grete Solli, spesialrådgiver Helse Sør-Øst RHF Samfunnsansvar;
Helseforskningsloven konsekvenser i skjæringspunktet mellom universitet og helseforetak
 Helseforskningsloven konsekvenser i skjæringspunktet mellom universitet og helseforetak Anne Husebekk Fag- og forskningssjef, UNN Professor, UiT Norske lover Straffeloven Forvaltningsloven Patentloven
Helseforskningsloven konsekvenser i skjæringspunktet mellom universitet og helseforetak Anne Husebekk Fag- og forskningssjef, UNN Professor, UiT Norske lover Straffeloven Forvaltningsloven Patentloven
Forespørsel om deltakelse i forskningsprosjektet: <Sett inn tittel, prosjektnummer>
 Forespørsel om deltakelse i forskningsprosjektet: Bakgrunn og hensikt Dette er et spørsmål til deg om å delta i en forskningsstudie ved Helse Bergen HF/Haukeland universitetssykehus.
Forespørsel om deltakelse i forskningsprosjektet: Bakgrunn og hensikt Dette er et spørsmål til deg om å delta i en forskningsstudie ved Helse Bergen HF/Haukeland universitetssykehus.
Kvalitetssystem for medisinsk og helsefaglig forskning. Delegering av oppgaver i kvalitetssystemets rutiner Bakgrunn
 1 FRAMLEGGSNOTAT TIL FAKULTETSSTYRET Til: Det medisinske fakultets styre Fra: Forskningsadministrasjonen, seniorrådgiver Katrine Ore Sakstype: O Arkivsaksnr: Vedlegg: Rutine for håndtering av avvik som
1 FRAMLEGGSNOTAT TIL FAKULTETSSTYRET Til: Det medisinske fakultets styre Fra: Forskningsadministrasjonen, seniorrådgiver Katrine Ore Sakstype: O Arkivsaksnr: Vedlegg: Rutine for håndtering av avvik som
Nettverksarbeidet ved OUS
 Nettverksarbeidet ved OUS Nettverksleder/prosjektkoordinator Carin Granlund Enhet for utprøvende kreftbehandling Seksjon for klinisk kreftforskning og kompetanseutvikling Agenda Bakgrunn Formål og organisering
Nettverksarbeidet ved OUS Nettverksleder/prosjektkoordinator Carin Granlund Enhet for utprøvende kreftbehandling Seksjon for klinisk kreftforskning og kompetanseutvikling Agenda Bakgrunn Formål og organisering
Kvalitetssikring av forskningsprosjekter Normer og regelverk. Introduksjonskurs Doktorgradsprogrammet Det medisinske fakultet, Universitetet i Oslo
 Kvalitetssikring av forskningsprosjekter Normer og regelverk Introduksjonskurs Doktorgradsprogrammet Det medisinske fakultet, Universitetet i Oslo Sagt om doktorgradsprogrammet: Forskerutdanning som en
Kvalitetssikring av forskningsprosjekter Normer og regelverk Introduksjonskurs Doktorgradsprogrammet Det medisinske fakultet, Universitetet i Oslo Sagt om doktorgradsprogrammet: Forskerutdanning som en
F o r e t a k s n i v å. Godkjent dato:
 F o r e t a k s n i v å Dokument ID: Gyldig til: 12.01.2017 Skjema Side 1 av 6 Årlig framdriftsrapport for forskningsprosjekter ved SSHF År: OBS: Sendes elektronisk til postmottak@sshf.no A. Grunnopplysninger
F o r e t a k s n i v å Dokument ID: Gyldig til: 12.01.2017 Skjema Side 1 av 6 Årlig framdriftsrapport for forskningsprosjekter ved SSHF År: OBS: Sendes elektronisk til postmottak@sshf.no A. Grunnopplysninger
Forespørsel om deltakelse i forskningsprosjektet
 [Sett inn korttittel på studien Hoveddel - sett inn dato] Forespørsel om deltakelse i forskningsprosjektet [Fjern den merkede teksten og hakeparentesen og sett inn din egen tekst: Bruk minimum 12 pkt.
[Sett inn korttittel på studien Hoveddel - sett inn dato] Forespørsel om deltakelse i forskningsprosjektet [Fjern den merkede teksten og hakeparentesen og sett inn din egen tekst: Bruk minimum 12 pkt.
Utprøvende behandling noe for deg? Informasjon om deltakelse i kliniske studier
 Novartis Norge AS Utprøvende behandling noe for deg? Informasjon om deltakelse i kliniske studier Innledning Å velge om du skal delta i utprøvende behandling eller ikke, er et viktig og personlig valg.
Novartis Norge AS Utprøvende behandling noe for deg? Informasjon om deltakelse i kliniske studier Innledning Å velge om du skal delta i utprøvende behandling eller ikke, er et viktig og personlig valg.
Forskningsdefinisjoner (vedlegg til styrende dokument nr 60, 61 og 62) Utarbeidet av: Stab FoU Ajour pr: 24.06.2010
 Forskningsdefinisjoner (vedlegg til styrende dokument nr 60, 61 og 62) Utarbeidet av: Stab FoU Ajour pr: 24.06.2010 Anonyme helse- og personopplysninger: Opplysninger der navn, fødselsnummer og andre personentydige
Forskningsdefinisjoner (vedlegg til styrende dokument nr 60, 61 og 62) Utarbeidet av: Stab FoU Ajour pr: 24.06.2010 Anonyme helse- og personopplysninger: Opplysninger der navn, fødselsnummer og andre personentydige
Inven2 Klinikk - bidrag til klinisk forskning. Regionalt forskningsutvalg HSØ, 11.05.15 Siri Kolle, VP Clinical
 Inven2 Klinikk - bidrag til klinisk forskning Regionalt forskningsutvalg HSØ, 11.05.15 Siri Kolle, VP Clinical Pasienten i fokus Aftenposten 3. februar 2015: Norges i verdenstoppen i behandling av lymfekreft
Inven2 Klinikk - bidrag til klinisk forskning Regionalt forskningsutvalg HSØ, 11.05.15 Siri Kolle, VP Clinical Pasienten i fokus Aftenposten 3. februar 2015: Norges i verdenstoppen i behandling av lymfekreft
Forespørsel om deltakelse i forskningsprosjektet: <Sett inn tittel, prosjektnummer>
 Forespørsel om deltakelse i forskningsprosjektet: Bakgrunn og hensikt Dette er et spørsmål til deg om å delta i en forskningsstudie ved Universitetet i. [Sett inn informasjon
Forespørsel om deltakelse i forskningsprosjektet: Bakgrunn og hensikt Dette er et spørsmål til deg om å delta i en forskningsstudie ved Universitetet i. [Sett inn informasjon
1. Endringer siden forrige versjon Instruksen er revidert i samarbeid med UiO. Ny mal for annonse i Webcruiter og kortversjon av prosessen er vedlagt.
 Instruks Ansettelse i nye og ledige stillinger som professor II eller førsteamanuensis ved UiO, kombinert med samtidig ansettelse i hovedstilling ved OUS OUS nivå 1 / Personal Dokument-ID: 2671 Versjon:
Instruks Ansettelse i nye og ledige stillinger som professor II eller førsteamanuensis ved UiO, kombinert med samtidig ansettelse i hovedstilling ved OUS OUS nivå 1 / Personal Dokument-ID: 2671 Versjon:
Helseforskningsloven - lovgivers intensjoner
 Helseforskningsloven - lovgivers intensjoner Sverre Engelschiøn Oslo, 30. mars 2011 Intensjonen Fremme god og etisk forsvarlig medisinsk og helsefaglig forskning Ivareta hensynet til forskningsdeltakere
Helseforskningsloven - lovgivers intensjoner Sverre Engelschiøn Oslo, 30. mars 2011 Intensjonen Fremme god og etisk forsvarlig medisinsk og helsefaglig forskning Ivareta hensynet til forskningsdeltakere
Hvilken rolle har REK (NEM), Personvernombudene, Datatilsynet og Helsetilsynet i henhold til klinisk oppdragsforskning og helseforskningsloven?
 Jacob C Hølen Hvilken rolle har REK (NEM), Personvernombudene, Datatilsynet og Helsetilsynet i henhold til klinisk oppdragsforskning og helseforskningsloven? Sekretariatsleder Den nasjonale forskningsetiske
Jacob C Hølen Hvilken rolle har REK (NEM), Personvernombudene, Datatilsynet og Helsetilsynet i henhold til klinisk oppdragsforskning og helseforskningsloven? Sekretariatsleder Den nasjonale forskningsetiske
Compassionate use ---og kliniske studier. Ingvild Aaløkken Seksjon for preklinikk og klinisk utprøving
 Compassionate use ---og kliniske studier Ingvild Aaløkken Seksjon for preklinikk og klinisk utprøving Compassionate use - grenseområder Compassionate use: Til en gruppe pasienter Til pasienter som har
Compassionate use ---og kliniske studier Ingvild Aaløkken Seksjon for preklinikk og klinisk utprøving Compassionate use - grenseområder Compassionate use: Til en gruppe pasienter Til pasienter som har
Helseforskningsloven - intensjon og utfordringer
 Helseforskningsloven - intensjon og utfordringer Sverre Engelschiøn Gardermoen, 25. oktober 2010 Intensjonen Fremme god og etisk forsvarlig medisinsk i og helsefaglig forskning Ivareta hensynet til forskningsdeltakere
Helseforskningsloven - intensjon og utfordringer Sverre Engelschiøn Gardermoen, 25. oktober 2010 Intensjonen Fremme god og etisk forsvarlig medisinsk i og helsefaglig forskning Ivareta hensynet til forskningsdeltakere
Én helseforskninglov. Ny helseforskningslov 010710. Medisinsk og helsefaglig forskning
 UNH1 Medisinsk og helsefaglig forskning Ny helseforskningslov 010710 Sameline Grimsgaard Leder Klinisk forskningssenter Anne Husebekk Fag- og forskningssjef, UNN Professor, UiT virksomhet som utføres med
UNH1 Medisinsk og helsefaglig forskning Ny helseforskningslov 010710 Sameline Grimsgaard Leder Klinisk forskningssenter Anne Husebekk Fag- og forskningssjef, UNN Professor, UiT virksomhet som utføres med
hva betyr loven for den enkelte forsker?
 Helseforskningsloven --- hva betyr loven for den enkelte forsker? Karin C. Lødrup Carlsen Professor dr med Forskningsleder OUS/UiO Kvinne- og barneklinikken Daglig leder av ORAACLE, (Oslo Research group
Helseforskningsloven --- hva betyr loven for den enkelte forsker? Karin C. Lødrup Carlsen Professor dr med Forskningsleder OUS/UiO Kvinne- og barneklinikken Daglig leder av ORAACLE, (Oslo Research group
Anette Hylen Ranhoff, overlege dr med, leder Kavli senter 24. November 2008 HDS - Bergen
 Anette Hylen Ranhoff, overlege dr med, leder Kavli senter 24. November 2008 HDS - Bergen Kavli senter er et samarbeidsprosjekt mellom Kavlifondet, Haraldsplass Diakonale Sykehus, Universitetet i Bergen
Anette Hylen Ranhoff, overlege dr med, leder Kavli senter 24. November 2008 HDS - Bergen Kavli senter er et samarbeidsprosjekt mellom Kavlifondet, Haraldsplass Diakonale Sykehus, Universitetet i Bergen
De lokale rutinene må sikre at:
 3. Regionale studier som kan ta i mot pasienter fra hele landet. For slike studier må det avklares om studien finansierer reise og evt opphold for deltakere fra andre helseregioner, og det må informeres
3. Regionale studier som kan ta i mot pasienter fra hele landet. For slike studier må det avklares om studien finansierer reise og evt opphold for deltakere fra andre helseregioner, og det må informeres
Forskrift om organisering av medisinsk og helsefaglig forskning
 Forskrift om organisering av medisinsk og helsefaglig forskning Fastsatt av Helse- og omsorgsdepartementet 1. juli 2009 med hjemmel i lov 20. juni 2008 nr. 44 om medisinsk og helsefaglig forskning 6 tredje
Forskrift om organisering av medisinsk og helsefaglig forskning Fastsatt av Helse- og omsorgsdepartementet 1. juli 2009 med hjemmel i lov 20. juni 2008 nr. 44 om medisinsk og helsefaglig forskning 6 tredje
Lovlig journalbruk Oppslag i og bruk av pasientjournalen
 Lovlig journalbruk Oppslag i og bruk av pasientjournalen Stab fag og pasientsikkerhet Seksjon for personvern og informasjonssikkerhet OPPSLAG I OG BRUK AV PASIENTJOURNALEN Journalen er et viktig verktøy
Lovlig journalbruk Oppslag i og bruk av pasientjournalen Stab fag og pasientsikkerhet Seksjon for personvern og informasjonssikkerhet OPPSLAG I OG BRUK AV PASIENTJOURNALEN Journalen er et viktig verktøy
Forespørsel om deltakelse i klinisk studie
 Forespørsel om deltakelse i klinisk studie The Stop-GIST trial; Avslutning av Glivec behandling hos pasienter med begrenset spredning fra GIST som har hatt stabil sykdom i over fem år på Glivec og hvor
Forespørsel om deltakelse i klinisk studie The Stop-GIST trial; Avslutning av Glivec behandling hos pasienter med begrenset spredning fra GIST som har hatt stabil sykdom i over fem år på Glivec og hvor
Oslo universitetssykehus
 i universitetssykehus Hvordan støtte opp om kliniske forskning? Peder Heyerdahl Utne Avdeling for forskningsadministrasjon, Oslo universitetssykehus Administrerende direktør Bjørn Erikstein Økonomi, juridisk
i universitetssykehus Hvordan støtte opp om kliniske forskning? Peder Heyerdahl Utne Avdeling for forskningsadministrasjon, Oslo universitetssykehus Administrerende direktør Bjørn Erikstein Økonomi, juridisk
7. Omfatter prosjektet bruk av identifiserbare/avidentifiserte personopplysninger slik Ja som helseopplysninger, inkludert kodede opplysninger?
 Prosjektnr. SI: Fylles ut av SI ved 1. gangs registrering Registreringsskjema for: Ved førstegangsregistrering: Ved endrings- årlig statusmelding: 1. Prosjektets tittel All forskning Utviklings- kvalitetsprosjekter
Prosjektnr. SI: Fylles ut av SI ved 1. gangs registrering Registreringsskjema for: Ved førstegangsregistrering: Ved endrings- årlig statusmelding: 1. Prosjektets tittel All forskning Utviklings- kvalitetsprosjekter
Forskningsjus og forskningsetikk i et nøtteskall
 Forskningsjus og forskningsetikk i et nøtteskall Grunnkurs D, Våruka 2016 Professor Elin O. Rosvold Uetisk forskning og forskningsjuks Historier om uetisk forskning Helsinkideklarasjonen Lover som regulerer
Forskningsjus og forskningsetikk i et nøtteskall Grunnkurs D, Våruka 2016 Professor Elin O. Rosvold Uetisk forskning og forskningsjuks Historier om uetisk forskning Helsinkideklarasjonen Lover som regulerer
REK og helseforskningsloven
 REK og helseforskningsloven Øystein Lundestad Rådgiver, REK Midt-Norge REK Sekretariat: Komité: Bindeleddet mellom komité og søker FATTER VEDTAK Hvorfor må dere forholde dere til REK? REKs mandat 1. Forhåndsgodkjenne
REK og helseforskningsloven Øystein Lundestad Rådgiver, REK Midt-Norge REK Sekretariat: Komité: Bindeleddet mellom komité og søker FATTER VEDTAK Hvorfor må dere forholde dere til REK? REKs mandat 1. Forhåndsgodkjenne
Kompetansesenter for personvern og sikkerhet
 Sykehusene og internkontrollansvaret i legemiddelstudier Helge Grimnes Personvernrådgiver Kompetansesenter for personvern og sikkerhet Oslo universitetssykehus HF Kompetansesenter for personvern og sikkerhet
Sykehusene og internkontrollansvaret i legemiddelstudier Helge Grimnes Personvernrådgiver Kompetansesenter for personvern og sikkerhet Oslo universitetssykehus HF Kompetansesenter for personvern og sikkerhet
FORESPØRSEL OM DELTAKELSE I FORSKNINGSPROSJEKTET BETA-BLOCKER TREATMENT AFTER ACUTE MYOCARDIAL INFARCTION (BETAMI) STUDIEN
 FORESPØRSEL OM DELTAKELSE I FORSKNINGSPROSJEKTET BETA-BLOCKER TREATMENT AFTER ACUTE MYOCARDIAL INFARCTION (BETAMI) STUDIEN Dette er en forespørsel til deg om å delta i forskningsprosjektet BETAMI som har
FORESPØRSEL OM DELTAKELSE I FORSKNINGSPROSJEKTET BETA-BLOCKER TREATMENT AFTER ACUTE MYOCARDIAL INFARCTION (BETAMI) STUDIEN Dette er en forespørsel til deg om å delta i forskningsprosjektet BETAMI som har
Lovlig journalbruk Oppslag i og bruk av Pasientjournalen
 Lovlig journalbruk Oppslag i og bruk av Pasientjournalen 1 Oppslag i og bruk av pasientjournalen Journalen er et viktig verktøy for tilgang til og deling av informasjon mellom samhandlende helsepersonell.
Lovlig journalbruk Oppslag i og bruk av Pasientjournalen 1 Oppslag i og bruk av pasientjournalen Journalen er et viktig verktøy for tilgang til og deling av informasjon mellom samhandlende helsepersonell.
Er det felles forståelse om hvem som har ansvar/myndighet i forhold til industriinitierte kliniske studier?
 Er det felles forståelse om hvem som har ansvar/myndighet i forhold til industriinitierte kliniske studier? Steinar Østerbø Thoresen Professor dr med Head of Medical and Scientific Affairs GSK Norway Presentasjon
Er det felles forståelse om hvem som har ansvar/myndighet i forhold til industriinitierte kliniske studier? Steinar Østerbø Thoresen Professor dr med Head of Medical and Scientific Affairs GSK Norway Presentasjon
KONKURRANSEGRUNNLAG FOR ANSKAFFELSE AV
 KONKURRANSEGRUNNLAG FOR ANSKAFFELSE AV Immunmodulerende (sykdomsmodifiserende) medikamenter med indikasjonen multippel sklerose (MS) LIS-MS 1103 LIS på vegne av de regionale helseforetakene Helse Sør-Øst
KONKURRANSEGRUNNLAG FOR ANSKAFFELSE AV Immunmodulerende (sykdomsmodifiserende) medikamenter med indikasjonen multippel sklerose (MS) LIS-MS 1103 LIS på vegne av de regionale helseforetakene Helse Sør-Øst
REK-vurderinger etter GDPR
 REK-vurderinger etter GDPR Anders Strand Rådgiver, REK sør-øst C anders.strand@medisin.uio.no Plan Litt bakgrunnsinformasjon om REK, GDPR og fritak fra taushetsplikt for forskningsformål. Case til diskusjon;
REK-vurderinger etter GDPR Anders Strand Rådgiver, REK sør-øst C anders.strand@medisin.uio.no Plan Litt bakgrunnsinformasjon om REK, GDPR og fritak fra taushetsplikt for forskningsformål. Case til diskusjon;
Helseforskningsloven - oppfølging ved universiteter og høyskoler Seminar om helseforskningsloven 25. oktober 2010 Trine B. Haugen
 Helseforskningsloven - oppfølging ved universiteter og høyskoler Seminar om helseforskningsloven 25. oktober 2010 Trine B. Haugen Høgskolen i Oslo Helseforskningsloven 1. juli 2009 Bakgrunn UHR oppfølging
Helseforskningsloven - oppfølging ved universiteter og høyskoler Seminar om helseforskningsloven 25. oktober 2010 Trine B. Haugen Høgskolen i Oslo Helseforskningsloven 1. juli 2009 Bakgrunn UHR oppfølging
NORSK LOVTIDEND Avd. I Lover og sentrale forskrifter mv. Utgitt i henhold til lov 19. juni 1969 nr. 53.
 NORSK LOVTIDEND Avd. I Lover og sentrale forskrifter mv. Utgitt i henhold til lov 19. juni 1969 nr. 53. Kunngjort 2. mai 2018 kl. 13.55 PDF-versjon 14. mai 2018 27.04.2018 nr. 645 Forskrift om befolkningsbaserte
NORSK LOVTIDEND Avd. I Lover og sentrale forskrifter mv. Utgitt i henhold til lov 19. juni 1969 nr. 53. Kunngjort 2. mai 2018 kl. 13.55 PDF-versjon 14. mai 2018 27.04.2018 nr. 645 Forskrift om befolkningsbaserte
PROSEDYRE FOR Tjenesteområde:
 PROSEDYRE FOR Tjenesteområde: Kategori: 3. Omsorgstjenester 3.2 Medikamenthåndtering Side 1 av 3 ANSVARSFORDELING OG NØDVENDIG BRUKERINFORMASJON Vedlegg: 2 Ansvarlig: Rådmannen Godkjent den: 17.12.2012
PROSEDYRE FOR Tjenesteområde: Kategori: 3. Omsorgstjenester 3.2 Medikamenthåndtering Side 1 av 3 ANSVARSFORDELING OG NØDVENDIG BRUKERINFORMASJON Vedlegg: 2 Ansvarlig: Rådmannen Godkjent den: 17.12.2012
Hvordan få tilgang til kvalitetsregisterdata for forskningsformål?
 Hvordan få tilgang til kvalitetsregisterdata for forskningsformål? Helse- og kvalitetsregister konferansen 2014 Oslo 14. mars 2014 Torild Skrivarhaug overlege dr.med. barnelege, leder Barnediabetesregisteret
Hvordan få tilgang til kvalitetsregisterdata for forskningsformål? Helse- og kvalitetsregister konferansen 2014 Oslo 14. mars 2014 Torild Skrivarhaug overlege dr.med. barnelege, leder Barnediabetesregisteret
Elektronisk pasientjournal -
 Elektronisk pasientjournal - Tilgangsregulering internt, men hva med økende krav om utlevering? Heidi Thorstensen IKT-sikkerhetssjef /Personvernombud Hvorfor sikkerhet/personvern? 1 Elektroniske journalopplysninger
Elektronisk pasientjournal - Tilgangsregulering internt, men hva med økende krav om utlevering? Heidi Thorstensen IKT-sikkerhetssjef /Personvernombud Hvorfor sikkerhet/personvern? 1 Elektroniske journalopplysninger
Møtereferat. Nettverk for studiepersonell i HSØ Møtedeltakere. Kopi:
 Møtereferat Møtetema: Til: Kopi: Nettverk for studiepersonell i HSØ Møtedeltakere Dato dok: 8.4.2019 Dato møte: 2.4.2019 Referent: Tilstede: Forfall: Ellen Johnsen / Anne Marie Halstensen Line Samuelsen
Møtereferat Møtetema: Til: Kopi: Nettverk for studiepersonell i HSØ Møtedeltakere Dato dok: 8.4.2019 Dato møte: 2.4.2019 Referent: Tilstede: Forfall: Ellen Johnsen / Anne Marie Halstensen Line Samuelsen
Prosjektinformasjonen må oppdateres
 Det er kun prosjektleder, forskningsansvarliges representant og saksbehandlere som har tilgang til filene. Prosjektinformasjonen må oppdateres Prosjekter som ikke har behov for -godkjenning er etter helseforskningsloven
Det er kun prosjektleder, forskningsansvarliges representant og saksbehandlere som har tilgang til filene. Prosjektinformasjonen må oppdateres Prosjekter som ikke har behov for -godkjenning er etter helseforskningsloven
Pasientreiser ANS - Offentlig journal
 I,, N, X, S tgående internt produsert, 11/00277-26 Lønnsjustering - mappe - Dok. dato: 26.10.2016 Arkivdel: arkiv Arkivkode: 221 Inngående eksternt produsert, 11/00339-218 Ønske om å tilsendt dokumenter
I,, N, X, S tgående internt produsert, 11/00277-26 Lønnsjustering - mappe - Dok. dato: 26.10.2016 Arkivdel: arkiv Arkivkode: 221 Inngående eksternt produsert, 11/00339-218 Ønske om å tilsendt dokumenter
Rapport Revisjon forskning Revmatismesykehuset AS
 Rapport Revisjon forskning Revmatismesykehuset AS Internrevisjonen Helse Øst 10.01.2007 Rapport nr. 21-2006 Revisjonsperiode August-oktober 2006 Virksomhet Rapportmottaker Kopi Rapportavsender Oppdragsgiver
Rapport Revisjon forskning Revmatismesykehuset AS Internrevisjonen Helse Øst 10.01.2007 Rapport nr. 21-2006 Revisjonsperiode August-oktober 2006 Virksomhet Rapportmottaker Kopi Rapportavsender Oppdragsgiver
Klinisk utprøving i praksis. Paal Fr Brunsvig Enhetsleder
 Klinisk utprøving i praksis Paal Fr Brunsvig Enhetsleder 10.04.2018 New drugs in development Statens legemiddelverk 2017 Aftenposten fredag 2. mars 2018 Høyrepolitiker vil vite hvilke kreftpasienter som
Klinisk utprøving i praksis Paal Fr Brunsvig Enhetsleder 10.04.2018 New drugs in development Statens legemiddelverk 2017 Aftenposten fredag 2. mars 2018 Høyrepolitiker vil vite hvilke kreftpasienter som
UNIVERSITETET I BERGEN Regional komité for medisinsk og helsefaglig forskningsetikk, Vest-Norge (REK Vest)
 UNIVERSITETET I BERGEN Regional komité for medisinsk og helsefaglig forskningsetikk, Vest-Norge (REK Vest) Randi Rolvsjord randi.rolvsjord@grieg.uib.no Griegakademiet - Institutt for musikk Universitetet
UNIVERSITETET I BERGEN Regional komité for medisinsk og helsefaglig forskningsetikk, Vest-Norge (REK Vest) Randi Rolvsjord randi.rolvsjord@grieg.uib.no Griegakademiet - Institutt for musikk Universitetet
Ansvar og organisering
 Utgitt med støtte av: Norm for www.normen.no Ansvar og organisering Støttedokument Faktaark nr 1 Versjon: 3.0 Dato: 12.2.2015 Formål Ansvar Gjennomføring Omfang Målgruppe Dette faktaarket er spesielt relevant
Utgitt med støtte av: Norm for www.normen.no Ansvar og organisering Støttedokument Faktaark nr 1 Versjon: 3.0 Dato: 12.2.2015 Formål Ansvar Gjennomføring Omfang Målgruppe Dette faktaarket er spesielt relevant
Standard: Organisasjonsoppsett
 Helse Sør-Øst RHF Teknologi og ehelse/regionale standarder, prosedyrer, brukerveiledninger og opplæring for DIPS/Regionale Standardområder DIPS Standard: Organisasjonsoppsett Utgave: 1.00 Utarbeidet/revidert
Helse Sør-Øst RHF Teknologi og ehelse/regionale standarder, prosedyrer, brukerveiledninger og opplæring for DIPS/Regionale Standardområder DIPS Standard: Organisasjonsoppsett Utgave: 1.00 Utarbeidet/revidert
Oslo universitetssykehus HF
 Oslo universitetssykehus HF Styresak Dato møte: 20. september 2012 Saksbehandler: Vedlegg: Viseadministrerende direktør medisin, helsefag og utvikling Stabsdirektør pasientsikkerhet og kvalitet 1. Prosjektmandat
Oslo universitetssykehus HF Styresak Dato møte: 20. september 2012 Saksbehandler: Vedlegg: Viseadministrerende direktør medisin, helsefag og utvikling Stabsdirektør pasientsikkerhet og kvalitet 1. Prosjektmandat
Styresak 131-2015/3 Samarbeid om felles journal i Helse Nord - informasjon
 Møtedato: 25. november 2015 Arkivnr.: Saksbeh/tlf: Sted/Dato: H. Talsethagen Bodø, 13.11.2015 Styresak 131-2015/3 Samarbeid om felles journal i Helse Nord - informasjon Bakgrunn I forbindelse med konsolidering
Møtedato: 25. november 2015 Arkivnr.: Saksbeh/tlf: Sted/Dato: H. Talsethagen Bodø, 13.11.2015 Styresak 131-2015/3 Samarbeid om felles journal i Helse Nord - informasjon Bakgrunn I forbindelse med konsolidering
PERSONVERNERKLÆRING FOR ADVOKATFIRMAET EVEN SOLBRAA-BAY (ORG.NR )
 PERSONVERNERKLÆRING FOR ADVOKATFIRMAET EVEN SOLBRAA-BAY (ORG.NR.994 236 016) (Sist endret 05.07.2018) Denne personvernerklæringen gjelder for Advokatfirmaet Even Solbraa-Bay. Jeg er behandlingsansvarlig
PERSONVERNERKLÆRING FOR ADVOKATFIRMAET EVEN SOLBRAA-BAY (ORG.NR.994 236 016) (Sist endret 05.07.2018) Denne personvernerklæringen gjelder for Advokatfirmaet Even Solbraa-Bay. Jeg er behandlingsansvarlig
Medinnova. Utfordringer ved Klinisk legemiddelutprøving - Oppdragsforskning ved helseforetak i Helse Sør-Øst
 Utfordringer ved Klinisk legemiddelutprøving - Oppdragsforskning ved helseforetak i Helse Sør-Øst Møte i Norsk Biotekforum - Møteplass kliniske studier 1. juni 2010 Kari Borch direktør klinisk forskning,
Utfordringer ved Klinisk legemiddelutprøving - Oppdragsforskning ved helseforetak i Helse Sør-Øst Møte i Norsk Biotekforum - Møteplass kliniske studier 1. juni 2010 Kari Borch direktør klinisk forskning,
«[prosjektnavn]» Kontrakt for innvilgelse av tilskudd til gjennomføring av kvalitetsforbedringsprosjektet
![«[prosjektnavn]» Kontrakt for innvilgelse av tilskudd til gjennomføring av kvalitetsforbedringsprosjektet «[prosjektnavn]» Kontrakt for innvilgelse av tilskudd til gjennomføring av kvalitetsforbedringsprosjektet](/thumbs/59/43522895.jpg) Kontrakt for innvilgelse av tilskudd til gjennomføring av kvalitetsforbedringsprosjektet «[prosjektnavn]» Oppdragsgiver: Prosjektansvarlig: Prosjektstart: Prosjektslutt: Overlevering sluttrapport: Nasjonalt
Kontrakt for innvilgelse av tilskudd til gjennomføring av kvalitetsforbedringsprosjektet «[prosjektnavn]» Oppdragsgiver: Prosjektansvarlig: Prosjektstart: Prosjektslutt: Overlevering sluttrapport: Nasjonalt
Aktuelle temaer. Forskningsetikk & juss hva veier tyngst? - Roller og ansvarsfordeling?
 Forskningsetikk & juss hva veier tyngst? - Roller og ansvarsfordeling? Peder Heyerdahl Utne Avdeling for forskningsadministrasjon og biobank Oslo universitetssykehus Aktuelle temaer Fra etikk til juss
Forskningsetikk & juss hva veier tyngst? - Roller og ansvarsfordeling? Peder Heyerdahl Utne Avdeling for forskningsadministrasjon og biobank Oslo universitetssykehus Aktuelle temaer Fra etikk til juss
Statens legemiddelverk '
 ' Helse- og omsorgsdepartementet Postboks 8011 Dep 0030 OSLO Deres dato Deres referanse Vår dato Vår referanse Seksjon/saksbehandler 2005-01-28 200405164 2005-05-11 200501909 DI/JU/PTT HØRING NOU 2005:1
' Helse- og omsorgsdepartementet Postboks 8011 Dep 0030 OSLO Deres dato Deres referanse Vår dato Vår referanse Seksjon/saksbehandler 2005-01-28 200405164 2005-05-11 200501909 DI/JU/PTT HØRING NOU 2005:1
16. januar 2019 kl 13:30 17:00 Forskningsparken
 16. januar 2019 kl 13:30 17:00 Forskningsparken Oslo Imaging Technology Research and Innovation Centre, ImTECH Avdeling for endokrinologi, sykelig overvekt og forebyggende medisin Seksjon for preventiv
16. januar 2019 kl 13:30 17:00 Forskningsparken Oslo Imaging Technology Research and Innovation Centre, ImTECH Avdeling for endokrinologi, sykelig overvekt og forebyggende medisin Seksjon for preventiv
NORSK LOVTIDEND Avd. I Lover og sentrale forskrifter mv. Utgitt i henhold til lov 19. juni 1969 nr. 53.
 NORSK LOVTIDEND Avd. I Lover og sentrale forskrifter mv. Utgitt i henhold til lov 19. juni 1969 nr. 53. Kunngjort 21. juni 2019 kl. 17.35 PDF-versjon 2. juli 2019 21.06.2019 nr. 789 Forskrift om medisinske
NORSK LOVTIDEND Avd. I Lover og sentrale forskrifter mv. Utgitt i henhold til lov 19. juni 1969 nr. 53. Kunngjort 21. juni 2019 kl. 17.35 PDF-versjon 2. juli 2019 21.06.2019 nr. 789 Forskrift om medisinske
Inven2 - status for klinisk utprøving - Inven2 tiltak
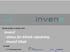 Kliniske studier 9. oktober 2013 Inven2 - status for klinisk utprøving - Inven2 tiltak Siri Kolle www.inven2.com Antall innmeldte studier per år YTD 10/16/2013 www.inven2.com 2 Hvem melder inn : 73% Sponsor
Kliniske studier 9. oktober 2013 Inven2 - status for klinisk utprøving - Inven2 tiltak Siri Kolle www.inven2.com Antall innmeldte studier per år YTD 10/16/2013 www.inven2.com 2 Hvem melder inn : 73% Sponsor
iavi Rutinebeskrivelse 04 Versjon: Gyldig fra:
 iavi Versjon: Gyldig fra: 1 IM6602.2012 SPONSORS OG HOVEDUTPRØRS y^fgl^v1^9^^/ Gunn-Elin Aa. Bjomeboe MEDISINSKOG HELSEFAGLIG FORSKNING Virksomhet som utføres med vitenskapelig metodikk for å skaffe til
iavi Versjon: Gyldig fra: 1 IM6602.2012 SPONSORS OG HOVEDUTPRØRS y^fgl^v1^9^^/ Gunn-Elin Aa. Bjomeboe MEDISINSKOG HELSEFAGLIG FORSKNING Virksomhet som utføres med vitenskapelig metodikk for å skaffe til
Vitenskapelig og etisk vurdering av design og kontrollgruppe
 Vitenskapelig og etisk vurdering av design og kontrollgruppe Stein A. Evensen Tidl leder REK Sør-Øst D Soria Moria 29 august 2013 Hva karakteriserer legemiddelstudier? At de oftest kommer fra legemiddelindustrien
Vitenskapelig og etisk vurdering av design og kontrollgruppe Stein A. Evensen Tidl leder REK Sør-Øst D Soria Moria 29 august 2013 Hva karakteriserer legemiddelstudier? At de oftest kommer fra legemiddelindustrien
Samarbeidsavtaler mellom de regionale helseforetakene, Legemiddelindustrien (LMI) og Medtek Norge
 Helse Sør-Øst RHF Gode og likeverdige helsetjenester til alle som trenger det, når de trenger det, uavhengig av alder, bosted, etnisk bakgrunn, kjønn og økonomi. Samarbeidsavtaler mellom de regionale helseforetakene,
Helse Sør-Øst RHF Gode og likeverdige helsetjenester til alle som trenger det, når de trenger det, uavhengig av alder, bosted, etnisk bakgrunn, kjønn og økonomi. Samarbeidsavtaler mellom de regionale helseforetakene,
Denne er kun til gjennomlesning. Rapportering av forskningsprosjekter må gjøres elektronisk.
 QuestBack https://response.questback.com/isa/qbv.dll/showquest?questid=4368891&sid=fml... Norwegian (Bokmål) English OK Copyright www.questback.com. All Rights Reserved. https://response.questback.com/isa/qbv.dll/showquest
QuestBack https://response.questback.com/isa/qbv.dll/showquest?questid=4368891&sid=fml... Norwegian (Bokmål) English OK Copyright www.questback.com. All Rights Reserved. https://response.questback.com/isa/qbv.dll/showquest
Personvernerklæring for Cristin (Current Research Information System in Norway)
 Personvernerklæring for Cristin (Current Research Information System in Norway) Sist endret: 15.06.2018 Innhold: 1) Kort om Cristin (Current Research Information System in Norway) 2) Hva er en personvernerklæring?
Personvernerklæring for Cristin (Current Research Information System in Norway) Sist endret: 15.06.2018 Innhold: 1) Kort om Cristin (Current Research Information System in Norway) 2) Hva er en personvernerklæring?
Meldeplikt når og hvor?
 Meldeplikt når og hvor? KAI VICTOR HANSEN, PHD, MSC NORSK HOTELLHHØGSKOLE UNIVERSITETET I STAVANGER KVH 2015 Innhold Hvilke prosjekter er meldepliktige? Når skal en søknad til NSD og når skal den til Regionaletisk
Meldeplikt når og hvor? KAI VICTOR HANSEN, PHD, MSC NORSK HOTELLHHØGSKOLE UNIVERSITETET I STAVANGER KVH 2015 Innhold Hvilke prosjekter er meldepliktige? Når skal en søknad til NSD og når skal den til Regionaletisk
Noe om forskningsetikk
 Noe om forskningsetikk Dag Bruusgaard Professor emeritus Institutt for helse og samfunn Avdeling for allmennmedisin Leder av Den nasjonale forskningsetiske komite for medisin og helsefag Tidl. fastlege
Noe om forskningsetikk Dag Bruusgaard Professor emeritus Institutt for helse og samfunn Avdeling for allmennmedisin Leder av Den nasjonale forskningsetiske komite for medisin og helsefag Tidl. fastlege
Gjennomføring av studier - fra planlegging til avslutning. Line Bjørge
 Gjennomføring av studier - fra planlegging til avslutning Line Bjørge Flere pasienter i kliniske studier!... ønsker regjeringen at pasienter skal gis økte muligheter til å delta i utprøvende behandling.
Gjennomføring av studier - fra planlegging til avslutning Line Bjørge Flere pasienter i kliniske studier!... ønsker regjeringen at pasienter skal gis økte muligheter til å delta i utprøvende behandling.
Opplæringsbehov etter helseforskningsloven
 Opplæringsbehov etter helseforskningsloven Juridisk seniorrådgiver Jannicke Hudson Seksjon for forskningstjenester Det helsevitenskapelige fakultet Universitetet i Tromsø Kort om helseforskningsloven Legger
Opplæringsbehov etter helseforskningsloven Juridisk seniorrådgiver Jannicke Hudson Seksjon for forskningstjenester Det helsevitenskapelige fakultet Universitetet i Tromsø Kort om helseforskningsloven Legger
Godkjenning av prosjekter og kliniske utprøvinger på barn hvordan er SLV s rolle?
 Godkjenning av prosjekter og kliniske utprøvinger på barn hvordan er SLV s rolle? Ingvild Aaløkken Seksjon for preklinikk og klinisk utprøving Statens legemiddelverk AGENDA Regelverket Søknader til Legemiddelverket
Godkjenning av prosjekter og kliniske utprøvinger på barn hvordan er SLV s rolle? Ingvild Aaløkken Seksjon for preklinikk og klinisk utprøving Statens legemiddelverk AGENDA Regelverket Søknader til Legemiddelverket
I Forskning som involverer personopplysninger særlig forholdet til personopplysningsloven og helseforskningsloven
 INTERNT BAKGRUNNSNOTAT I Forskning som involverer personopplysninger særlig forholdet til personopplysningsloven og helseforskningsloven Bakgrunn En rekke forskningsprosjekter ved fakultetet håndterer
INTERNT BAKGRUNNSNOTAT I Forskning som involverer personopplysninger særlig forholdet til personopplysningsloven og helseforskningsloven Bakgrunn En rekke forskningsprosjekter ved fakultetet håndterer
Hva er personopplysninger og hvem er ansvarlig for dem?
 Personvernerklæring Divisjon Aleris Omsorg Norge Ditt personvern er viktig for oss. Nedenfor kan du lese mer om vordan vi aktivt jobber med å ivareta ditt personvern. Her vil vi forklare vordan og vorfor
Personvernerklæring Divisjon Aleris Omsorg Norge Ditt personvern er viktig for oss. Nedenfor kan du lese mer om vordan vi aktivt jobber med å ivareta ditt personvern. Her vil vi forklare vordan og vorfor
Gjennomføring av europaparlaments- og rådsforordning (EU) nr. 536/2014 om klinisk utprøving av legemidler til mennesker i norsk rett.
 1 Høringsnotat Gjennomføring av europaparlaments- og rådsforordning (EU) nr. 536/2014 om klinisk utprøving av legemidler til mennesker i norsk rett. 1 Innledning. EØS-komiteen vedtok ved beslutning nr.
1 Høringsnotat Gjennomføring av europaparlaments- og rådsforordning (EU) nr. 536/2014 om klinisk utprøving av legemidler til mennesker i norsk rett. 1 Innledning. EØS-komiteen vedtok ved beslutning nr.
