Tema Vaksinasjon.
|
|
|
- Bengt Fredriksen
- 10 år siden
- Visninger:
Transkript
1 I Tidsskriftet nr /2006 publiseres flere artikler om vaksinasjon. Artiklene er redigert av Preben Aavitsland og Petter Gjersvik. Bildet illustrerer sentrale celler ved slimhinneimmunitet: Dendrittiske celler med sine utløpere i tarmlumen «snorkler» etter vaksineantigener eller patogene tarmbakterier og tar med seg antigener til nærmeste lymfeknute, der immunresponsen igangsettes. Illustrasjon Ludvig André Munthe Nr. 19/2006 Kua, gutten og lymfeknuten immunologiske prinsipper for vaksinasjon Ludvig André Munthe Side Det norske vaksinasjonsprogrammet Hanne Nøkleby, Berit Feiring Side Uønskede hendelser etter vaksinering Hanne Nøkleby, Marianne A. Riise Bergsaker Side Nr. 20/2006 Vaksinering er det verdt pengene? Torbjørn Wisløff, Tore G. Abrahamsen, Marianne A. Riise Bergsaker, Øistein Løvoll, Ivar Sønbø Kristiansen Side Vaksinasjon i et utviklingsperspektiv Halvor Sommerfelt, Tore Godal Side Vaksiner mot tuberkulose Harald G. Wiker, Gunnar Bjune Side Nr. 21/2006 Reisevaksinasjon Synne Sandbu Side Influensavaksinering hvorfor, for hvem og med hvilken vaksine? Marianne Bergsaker, Olav Hungnes, Bjørn Iversen Side Slimhinnevaksiner i utvikling Hilde Bakke, Bjørn Haneberg Side Nr. 22/2006 DNA fremtidens vaksine? Rune Kjeken, Bjarne Bogen, Iacob Mathiesen Side Kreftvaksiner Jon Amund Kyte Side Vaksiner mot rusmidler Jørg Mørland Side Tidsskr Nor Lægeforen nr. 22, 2006;
2 Medisin og vitenskap tema Vaksinasjon Kua, gutten og lymfeknuten immunologiske prinsipper for vaksinasjon Sammendrag Vaksiner stimulerer immunsystemet ved å aktivere profesjonelle antigenpresenterende celler, deriblant dendrittiske celler. Dendrittiske celler uttrykker en rekke mønstergjenkjennelsesreseptorer (MGR) på overflaten, reseptorer som gjenkjenner strukturer på virus og bakterier. Disse reseptorene stimulerer til modning av dendrittiske celler, som deretter migrerer til lymfeknuter og presenterer vaksineantigen til T-celler. Vaksinens MGR-ligander er bestemmende for om man får en hensiktsmessig immunrespons, og effektiv langvarig immunitet. I denne artikkelen gjennomgås cellulære prinsipper og mekanismer for vaksineresponser, inkludert antigennedbrytning, antigenpresentasjon, T-celleresirkulering, Th1-, Th2- og CTL- T-celleresponser og T-B-cellesamarbeid, samt primære og sekundære B-celleresponser. Engelsk sammendrag finnes i artikkelen på Oppgitte interessekonflikter: Ingen > Se også side 2504 Ludvig André Munthe [email protected] Immunologisk institutt Fakultetsdivisjon Rikshospitalet Universitetet i Oslo og Rikshospitalet-Radiumhospitalet 0027 Oslo Edward Jenner ( ) beskrev vaksineringsprinsippet i 1796 (1). Koppeepidemier var et stort problem i Jenners samtid, kopper var en infeksjon som forårsaket stor barnedødelighet og i tillegg vansiret en betydelig del av verdens befolkning. Letaliteten var over 30 % (2). Ved sitt forsøk der han vaksinerte gutten James Phipps (fig 1), viste Jenner at kroppen kunne utvikle en motstand mot koppeinfeksjon dersom man tidligere hadde gjennomgått en immunrespons mot det nær beslektede kukoppeviruset. Uten å vite det, hadde Jenner oppdaget ervervet immunitet og immunologisk hukommelse, og tatt det første skrittet mot utryddelsen av kopper. Koppeviruset var også det første viruset som ble erklært utryddet av WHO i I det følgende omtales immunologiske prinsipper for vaksinasjon, først ved gjennomgang av celler og ervervet immunitet, deretter beskrives igangsettelsen av immunresponser med utgangspunkt i antigenpresenterende celler, og det trekkes linjer til vaksinasjonsstrategier. Medfødt og ervervet immunitet Kroppens hud og slimhinner danner barrierer som utgjør første forsvarsverk i medfødt (non-adaptiv) immunitet. I tillegg har vi proteiner i sekreter og i plasma som beskytter oss mot bakterier og virus. En rekke plasmaproteiner inngår i komplementsystemet, en kaskade som er spesielt viktig i den tidlige fasen av infeksjoner. Bakterier aktiverer komplementfaktorer, og det dannes komplementfaktorfragmenter: Opsoniner (C3b) binder reseptorer på fagocytter, anafylatoksiner (C5a, C3a) aktiverer mastceller, kjemotaksiner (C5a) rekrutterer leukocytter til inflammasjonen. Det dannes også terminalt komplementkompleks (C5b-C9) som laserer bakterier (3). Leukocytter inndeles i lymfocytter (T-celler, B-celler, NK-celler (naturlige drepeceller)), monocytter, dendrittiske celler og granulocytter (e-fig 2). Ervervet (adaptiv) infeksjonsforsvar, som utvikles som en følge av kontakt med mikroorganismer, er avhengig av lymfocyttresponser og har tre kjennetegn: spesifisitet, hukommelse og toleranse (3). En spesifikk reaksjon betegnes ved at lymfocytter reagerer med ett antigen (og ikke et annet ubeslektet antigen). Immunologisk hukommelse innebærer at lymfocytter som er spesifikke for et antigen, gjennomgår celledeling for å bli langlivede hukommelsesceller. Toleranse omtales ikke nærmere her, men krever at lymfocytter ikke reagerer på kroppens egne celler og proteiner. Opplasting av antigenpresenterende celler La oss se på hvordan et moderne immunologisk perspektiv ville forklare funnene til Jenner. Gutten James Phipps (fig 1) ble immunisert subkutant med et inokulat av kukoppevirus. I huden og i subkutant vev finnes spesialiserte antigenpresenterende celler kalt dendrittiske celler. Disse er oftest hvilende og kalles da umodne. I hvilefasen tar dendrittiske celler opp ekstracellulærvæske tilsvarende flere ganger deres eget volum hvert døgn. Denne prosessen, makropinocytose, gjør at dendrittiske celler lastes opp med de antigenene som til enhver tid finnes i det aktuelle vevet (3), for eksempel kukoppeantigener etter vaksineringen. Proteinantigener brytes ned til peptider, som så binder gropen til MHC-klasse II-molekyler (ramme 1), for videre transport ut til cellens overflate (fig 3) (3, 4). Mønstergjenkjennelsesreseptorer Dendrittiske celler har en lang rekke reseptorer som aktiverer cellen ved kontakt med bakterie- og virusprodukter. Slike mønstergjenkjennelsesreseptorer (MGR) (5) er helt nødvendig for det medfødte immunforsvarets gjenkjennelse av patogener. Den største gruppen av mønstergjenkjennelsesreseptorer er Toll-liknende reseptorer (TLR, en gruppe som har fått navnet sitt etter toll-reseptor oppdaget i bananflue) (5). Mønstergjenkjennelsesreseptorer aktiverer og modner monocytter, makrofager og dendrittiske celler. Tabell 1 inneholder en liste av bakterieantigener og deres MGR-ligander, med sentrale referanser (6 21). Ved infeksjoner, eller som i gutten James Phipps tilfelle, etter subkutan vaksinering med virus, vil dendrittiske celler meget effektivt modnes ved hjelp av mønstergjenkjennelsesreseptorer. De vil deretter vandre til lymfeknutens paracortex, hvor de presenterer et antigent «øyeblikksbilde» til T-celler (fig 4).! Hovedbudskap Vaksiner setter i gang immunresponser som beskytter organismen mot infeksjoner Vaksiner aktiverer antigenproduserende celler, som gjennom reseptorer på overflaten er i stand til å gjenkjenne strukturer på virus og bakterier De antigenproduserende cellene migrerer til lymfeknuter og presenterer vaksineantigen overfor T-celler, en immunrespons settes i gang og langvarig immunitet etableres 2532 Tidsskr Nor Lægeforen nr. 19, 2006; 126:
3 MEDISIN OG VITENSKAP For optimalisering av vaksiner er det nødvendig å simulere den aktivering som antigenpresenterende celler får fra mikroorganismer (22). Kunnskap om mønstergjenkjennelsesreseptorer og om hvordan man kan få den ønskede aktiveringen av dendrittiske celler, står derfor sentralt. Tradisjonelle vaksiner benytter gjerne svekkede eller drepte mikroorganismer og drar nytte av patogenets egne ligander for mønstergjenkjennelsesreseptorer. Eksempelvis aktiverer den levende attenuerte gulfebervirusvaksinen (YF-17D) en rekke toll-liknende reseptorer (TLR2, 7, 8 og 9) (21). En utfordring for moderne vaksineutvikling er å skreddersy vaksiner til å optimalisere igangsettingen av immunresponsen og å fremprovosere den ønskede typen av immunrespons som initieres av dendrittiske celler, jf. omtale av TLR og Th1/Th2-balansen nedenfor. T-cellereseptor og B-cellereseptor T-cellereseptor og B-cellereseptor er grunnlaget for immunologisk hukommelse og ervervet immunitet. Én reseptor på én dendrittisk celle er lik den som finnes på nabocellen. Dette er ikke tilfellet for lymfocytter, hvor T-cellereseptor (TCR) eller B-cellereseptor (BCR, membranbundet antistoff) kan være helt unike for den aktuelle cellen. For å forstå hvordan immunsystemet klarer å gjenkjenne et bredt repertoar av antigene determinanter, kreves det en kort gjennomgang av mekanismen for mangfold av T- og B-lymfocyttenes reseptorer. Prinsipielt er mekanismen for danningen av lymfocyttreseptormangfold lik for B- og T- celler. B-celler gjennomgår en såkalt rearrangering av BCR-gener i utviklingen i beinmargen (23). Ett V-gensegment, ett D-gensegment (for tungkjeder) og ett J-gensegment settes tilfeldig sammen, og mellomliggende gensegmenter klippes bort (e-fig 5). Det samme skjer for T-lymfocytter og T-cellereseptor (TCR), men da i thymus. T-cellereseptor har to kjeder, rearrangeringen av TCR-α-kjedegensegmentene tilsvarer lettkjedegensegmentene, mens TCRβ-locus tilsvarer tungkjedelokus. Denne tilfeldige rearrangeringen resulterer i cirka potensielt unike reseptorer for T- og B-celler, noe som forklarer hvordan det er mulig å danne reseptorer som kan binde nesten alle tenkelige antigener (3). Merk at det ikke ligger noen antigenseleksjon i lymfocyttmodningen. B-celler som kommer fra beinmargen er altså ikke selektert for å kunne binde et antigen, og cellene har ingen viten om eksistensen av antigen (de kalles derfor naive lymfocytter). Bare tilfeldigheter avgjør om deres B-cellereseptor kan binde mikroorganismer i kroppen (3). Seleksjon, emigrasjon og resirkulering I beinmargen fjernes B-celler som reagerer på kroppens egne antigener (selvantigener). Det samme skjer for T-celler i thymus. Denne prosessen kalles negativ seleksjon (3). De Figur 1 Det første vaksinasjonsforsøket i Budeia Sarah Nelmes hadde utviklet blemmer i håndflatene etter å ha melket kua Blossom (ordet vaksine er avledet fra vacca, latin, ku). Edward Jenner tok eksudat fra blemmene, et inokulat som han ga åtteåringen James Phipps. Seks uker senere fikk James ekstrakt fra en koppeinfisert pasient, en behandling som normalt ville resultere i koppesykdom, en livstruende sykdom, men han forble frisk. Forsøket demonstrerte at resistens kan erverves ved vaksinering, men kan trygt sies ikke å tilfredsstille dagens forskningsetiske krav gjenværende lymfocyttene har reseptorer som ikke reagerer på kroppsegne proteiner. Godkjente B-celler og T-celler emigrerer deretter ut i blodbanen som naive lymfocytter og vandrer til lymfeknuter og annet sekundært lymfoid vev. I lymfeknuter ekstravaserer både T- og B-lymfocyttene gjennom spesialiserte høyendotelvenyler i paracortex (fig 6A). Presentasjon til hjelpeceller og cytotoksiske celler T-celler inndeles i to hovedgrupper, etter uttrykk av enten CD4-koreseptor eller CD8- koreseptor (3). CD4-positive (CD4 + ) T-celler kalles hjelpeceller, mens CD8-positive (CD8 +) T-celler kalles cytotoksiske T-lymfocytter (CTL). I motsetning til B-celler, som med sine B-cellereseptorer kan binde konformasjonsdeterminanter på hele proteiner, gjenkjenner T-cellereseptor antigent peptid som ligger i gropen på MHC- klasse I- eller II-molekyler. Nukleære og cytosolære proteiner brytes konstitutivt ned, og peptider fraktes over den endoplasmatiske retikulummembranen for å havne i gropen på MHC-klasse I-molekyler (3). Nedbrutte virusproteinfragmenter som uttrykkes av infiserte celler, havner altså som peptider på MHC-klasse I-molekyler. MHC klasse I/peptidkomplekset kan gjenkjennes av T-cellereseptor på cytotoksiske T-lymfocytter. CD8-koreseptoren benyttes av T-cellen til å stabilisere bindingen til MHC-klasse I-molekyler. MHC-klasse I- molekyler finnes på nesten alle kjerneholdige celler, som dermed kan presentere viruspeptidantigen til CD8-positive T-celler (3). MHC klasse II uttrykkes bare av såkalte profesjonelle antigenpresenterende celler (dendrittiske celler, makrofager, B-celler). Proteinfragmenter derivert fra ekstracellulærvæsken, eller fra det sekretoriske apparatet, havner som peptider i gropen på MHCklasse II-molekyler. Dermed vil de aller fleste vaksineantigener presenteres på MHC-klasse II-molekyler, via endocytose Figur 3 Opplasting av peptider i gropen på MHC-molekyler. A. Profesjonelle antigenpresenterende celler (APC) endocytterer antigener, endosomer fusjonerer med MHC klasse II inneholdende vesikler, ph reduseres, og enzymer bryter ned proteiner til peptidfragmenter som lastes opp i gropen av MHC klasse II. MHC klasse II/peptidkomplekset fraktes deretter til overflaten av cellen, og kan gjenkjennes av T-cellereseptor (TCR) på overflaten av T-lymfocytter. B. Krystallstrukturen til MHC-klasse II-molekylet (3, 4). MHC klasse II består av en α- og en β-kjede. Den peptidbindende gropen ligger mellom to såkalte α-helikser fra α 1- og β 1- domenene. Figuren er modifisert fra (3) Tidsskr Nor Lægeforen nr. 19, 2006;
4 Ramme 1 Antigenpresenterende celle (APC) Slike celler kan være profesjonelle APC, da uttrykker cellene både MHC klasse I og klasse II i tillegg til kostimulerende molekyler. B-cellereseptor (BCR) Membranbundet antistoff (kalles også membranbundet immunglobulin). I utskilt form: Immunglobulin, antistoff. CD-antigener Fra «cluster of differentiation», markører som benyttes til å karakterisere celler og vev. CD4-koreseptor Markør for T-hjelpeceller, CD4-positive T-celler er spesialisert til å samarbeide med monocytter/makrofager/dendrittiske celler eller B-celler. CD8-koreseptor Markør for cytotoksiske T-celler. CD8- positive T-celler dreper virusinfiserte celler. Dendrittisk celle (DC) Den mest effektive profesjonelle antigenpresenterende cellen. MHC-komplekset (major histocompatibility complex) Vevsforlikelighetsantigener. Disse benyttes av antigenpresenterende celler til å presentere antigene peptider til T-celler. MHC klasse I bindes av CD8, som finnes på cytotoksiske T-celler. MHC klasse II på overflaten av antigenpresenterende celler bindes av CD4 på T-hjelpeceller. HLA (human leukocyte antigen) MHC hos mennesket. Mønstergjenkjennelsesreseptorer (MGR) Samlebetegnelse på reseptorer, for eksempel TLR, som har som funksjon å binde patogene agenser, bakterier, virus og sopp. Kalles på engelsk pattern recognition receptors (PRR). Toll-liknende reseptorer (TLR) Mønstergjenkjennelsesreseptorer som finnes på antigenpresenterende celler hos pattedyr. Toll-reseptorer ble først oppdaget hos bananfluer, og liknende reseptorer ble siden funnet hos en rekke arter, deriblant hos mennesket. Tabell 1 Antigenbinding til mønstergjenkjennelsesreseptorer (MGR) Mikroorganisme og endosomal prosessering av proteinantigener (fig 3). CD4 + -koreseptoren binder MHC klasse II, og øker dermed aviditeten. Attenuerte virale vaksiner vil ved transkripsjon og translasjon uttrykke cytosolære eller nukleære proteinantigener som havner i gropen på MHC klasse I. Derimot vil drepte vaksiner endocytteres og presenteres på MHC klasse II. Hvordan får man da aktivering av CD8-positive T-celler ved vaksiner som inneholder ikke-viable virus? Ved kraftig aktivering av antigenpresenterende celler skjer krysspresentasjon (cross priming) av ekstracellulære proteiner på MHC klasse I. Den nøyaktige mekanismen for dette er fortsatt uklar, men TLR3 ser ut til å spille en rolle (24). Aktivering av T-celler Dersom en naiv CD4-positiv T-celle tilfeldigvis har en T-cellereseptor (TCR) som kan binde et peptid presentert i gropen på MHCklasse II-molekyler (for eksempel et peptid fra kukoppeviruset), mottar den både stimulering via T-cellereseptor og kostimulering via overflateproteiner som CD28 (som ligeres av CD80, CD86; fig 4B). Det dannes da en tett synapse mellom cellene og signaleringsapparatet polariseres inn mot synapsen (3). Etter flere timer har den naive T-cellen fått tilstrekkelig stimulering for å lage både vekstfaktoren IL-2 og IL-2-reseptorer. T- cellen gjennomgår så en kraftig celledeling som i løpet av noen uker kan resultere i titusenvis av datterceller, alle med samme spesifisitet, nå kalt effektorceller eller hukommelsesceller. Det er to viktige forskjeller mellom den naive T-cellen og effektorcellen. For det første har effektorceller et annet sett med Binding til MGR Bakterieantigen LPS Gramnegative bakterier LPS binder plasmaproteinet LPS-bindende protein (LBP) og deretter TLR4 1 (6) LTA, lipoproteiner Peptidoglykan Grampositive bakterier Gruppe B-streptokokker, Staphylococcus aureus CpG-DNA 2 Bakterier og mykobakterier TLR9 (10) Flagellin Flagellate bakterier TLR5 (11) TLR2 (7), TLR6/TLR2/TLR1 (8, 9) Lipoarabinomannan Mykobakterier TLR2, Dectin-1, (TLR4) (12) Triacylerte lipoproteiner Mycobacterium leprae TLR1/TLR2 (13) Mannose Bakterier Mannosereseptor Virusantigen CpG-DNA Virus, f.eks. HSV-1, HSV-2, og musecytomegalovirus (MCMV) TLR9 (14, 15) Dobbelttrådet (ds)rna Virus TLR3 (16), retinoic-acid-inducible protein I (RIG-I) (17) Enkelttrådet (ss)rna RNA-virus TLR7, TLR8 (18) F(fusjons)-protein RSV TLR4 (19) Hemagglutininprotein Meslingvirus TLR2 (20) YF-17D-vaksine Gulfeber TLR2, 7, 8 og 9 (21) 1 Følgende toll-liknende reseptorer (TLR) uttrykkes på celleoverflaten: TLR1, 2, 4, 5, 6. TLR danner ofte heterodimerer, f.eks. TLR2/TLR6. TLR3, 7, 8, 9 uttrykkes nesten bare intracellulært, og patogene antigener må derfor endocytteres. TLR benytter felles signaleringsvei, som deles med IL-1-reseptoren 2 Bakterielt DNA inneholder ofte sekvenser med kombinasjoner av C- og G-nukleotidene, som i motsetning til hos pattedyr ikke er metylert. Pattedyrceller har TLR9 som har affinitet for bestemte sekvenser av slike CpG-motiver. TLR9 uttrykkes i endosomer, og bakterielt DNA må derfor endocytteres, eller hele bakterien fagocytteres kjemokinreseptorer (fig 6B) som lokker cellen ut i betent vev og ikke bare til lymfeknuter. Effekten av en vaksine er dermed å mangfoldiggjøre spesifikke hukommelsesceller, som umiddelbart kan dra til det infiserte stedet ved en infeksjon (fig 6B). Effektorceller utskiller dessuten inflammatoriske cytokiner som aktiverer en rekke celler, slik som monocytter, makrofager og dendrittiske celler (fig 6B, e-tab 2). Effektorcellen kan drepe virusinfiserte celler (og for eksempel kreftceller) ved å indusere aktivert celledød (apoptose) i målcellene. Alternativt kan effektorceller gi hjelp til B-celler og aktivere dem til å utskille antistoff. Polarisering av effektorfunksjon CD4-positive T-hjelperceller kan inndeles i to grupper med vidt forskjellige effektorfunksjoner, Th1- og Th2-celler. CD4-positive Th1-celler, som ofte kalles inflammatoriske hjelperceller, utskiller interferon-γ (IFN-γ, i tillegg til for eksempel IL-2 og TNF) (e-tab 2). Th1-celler er meget potente til å aktivere monocytter, makrofager og dendrittiske celler. Th1-celler er også helt nødvendige for eliminering av intracellulære bakterier som Mycobacterium leprae og Mycobacterium tuberculosis. I tillegg er Th1-celler spesielt effektive i kampen mot virusinfeksjoner. Videre er det vist at Th Tidsskr Nor Lægeforen nr. 19, 2006; 126
5 MEDISIN OG VITENSKAP celler effektivt kan eliminere kreftceller (25, 26). Th1-celler kan også indusere apoptose i målceller ved at Fas-ligand (FasL) på Th1- cellens overflate binder Fas (CD95) på målcellen (26). For de fleste formål er det derfor ønskelig å indusere Th1-responser ved vaksinering. CD4-positive Th2-celler er dårlige hjelpere av dendrittiske celler og makrofager, men er meget gode hjelpere av B-celler, utskiller IL-4 og IL-13 og er nødvendig for bekjempelse av helmintinfeksjoner. Et viktig poeng er at Th1- og Th2-celler gjensidig hemmer hverandre (tab 2). Dessuten kan dendrittiske celler aktiveres av patogener til å favorisere den ene eller andre responstypen. Lipopolysakkarid (LPS) fra patogene og mindre patogene bakterier induserer henholdsvis Th1- og Th2-responser, sannsynligvis grunnet forskjellig TLR4-signalering (27). Det er vist at selekterte TLR-ligander kan polarisere responsen mot Th1-celler ved stimulering av humane dendrittiske celler (28, 29). Legering av TLR2 kan indusere Th2- responser (30 32). En effektiv virusvaksine mot gulfeber (YF-17D) resulterer i både Th1- og Th2-responser (med Th1-overvekt) (21). Dersom YF-17D-vaksinerte mus mangler TLR2, utvikles en kraftig Th1-respons (21). I lys av slike resultater, pågår en aktiv forskning for å utvikle vaksiner som favoriserer Th1-responser. Eksempelvis induserer Hiv- Gag-protein koblet til TLR7/9-agonister en kraftig og vedvarende Th1-respons i tillegg til CD8-positiv T-cellerespons hos aper (33). Lisensiering av dendrittiske celler CD4-positive T-celler potenserer antigenpresentasjonsfunksjonen av dendrittiske celler ved hjelp av membranbundet CD40-ligand (CD40L), som binder CD40 på de dendrittiske cellene. Dermed bedres cellens evne til å presentere til naive CD8-positve T- celler, en mekanisme som kalles lisensiering av dendrittiske celler (34). I tillegg utskiller CD4-positive T-celler cytokiner, for eksempel IL-2 og IL-15, som parakrint tilfører vekstfaktorer for CD8-positive T-celler (etab 2). CD8-positive cytotoksiske T-lymfocytter (CTL) har som hovedfunksjon å drepe virusinfiserte celler. Det er altså en stor fordel for virale vaksineantigener at det finnes epitoper som aktiverer både CD4-positive (med lisensiering av dendrittiske celler) og CD8-positive celler. Etter aktivering vil virusspesifikke CD4- positive T-celler og CD8-positive T-celler endre sine kjemokinreseptorer på overflaten og erverve evnen til å vandre til betent vev (fig 6B). Når gutten James Phipps igjen fikk en inokulering, denne gangen med koppevirus, hadde han T-celler som kunne dra direkte til det aktuelle virusinfiserte vevet. Koppevirusinfiserte celler ble dermed angrepet av koppespesifikke CD8-positive T-celler, som induserte apoptose i målcellene. Som støtte til CD8-positive T-celleresponser vil Figur 4 Vaksinering, aktivering og migrering av dendrittiske celler. A. Dendrittiske celler, eksempelvis langerhansceller i huden og subkutane umodne dendrittiske celler, tar opp ekstracellulærvæsken ved makropinocytose. Proteiner som tas opp, brytes ned til peptidfragmenter, og peptidene binder seg til gropen av MHC-molekyler (HLA-molekyler). Dendrittiske celler har en lang rekke med mønstergjenkjennelsesreseptorer (MGR). Når MGR binder bakterie eller virus, aktiveres cellen. MGR kan også føre til reseptormediert opptak av det bundne antigenet. På tilsvarende måte, kan antigener som påheftes komplementfaktorer (for eksempel C3b), aktivere og modne dendrittiske celler via komplementreseptorer (CR1, CD35) og føre til fagocytose. Dette kalles opsonisering. B. På umodne dendrittiske celler er det få MHC-molekyler på overflaten, da MHC- molekyler i løpet av mindre enn en time resirkuleres inn i cellen. Ved modning fraktes MHC-molekyler med peptid i gropen til overflaten og forblir der. Modningen medfører også at cellen begynner å uttrykke såkalte kostimulerende molekyler (CD80, CD86), som er viktig for effektiv aktivering av T-celler. C. I løpet av modningen uttrykker cellen kjemokinreseptorer som CCR7. CCR7 gjør at cellen kan binde kjemokinet CCL21 (tidligere kalt SLC). Dette gjør den dendrittiske cellen følsom for CCL21- kjemokingradienter slik at den kan vandre inn i vevsdrenerende lymfekar. D. Dendrittiske celler vandrer med lymfekaret ned til første drenerende lymfeknute. Her tar den seg ned gjennom lymfeknutens trabekelverk av retikulære fibroblaster, hvor den ekstravaserer og vandrer til lymfeknutens T-celleområde, paracortex. På denne måten frakter dendrittiske celler et antigent «øyeblikksbilde», tatt under en infeksjon eller ved en vaksinering, til en av immunsystemets kontrollstasjoner. Her møter den dendrittiske cellen T-celler. T-celler ankommer paracortex ved å ekstravasere gjennom spesialisert endotel, på såkalt høyendotelvenyler (HEV) i lymfeknutens paracortex. Dersom T-cellene gjenkjenner viruspeptider i gropen på MHC-klasse II-molekyler på overflaten til dendrittiske celler, vil T-cellen aktiveres, utskille cytokiner og gjennomgå celledeling. Figuren er modifisert fra (3) Th1-celler utskille cytokiner, som så aktiverer makrofager og bidrar til drap av virusinfiserte celler. Når virusinfiserte celler drepes, hindres videre mangfoldiggjøring av viruset. CD4-positive T-celler hjelper B-celler T- og B-celler samarbeider ved å gjensidig stimulere hverandre. T-cellen hjelper B-cellen til å differensiere til hukommelsesceller eller plasmaceller. Ved en infeksjon eller ved vaksinasjon vil antigener drenere fra vevet til lymfeknuter med den efferente lymfen. B-celler, som hovedsakelig befinner seg i lymfeknutens kortikale follikler, har derfor mulighet til å binde antigener fra et infeksjonsfokus. Dersom en B-celle har en egnet B-cellereseptor med spesifisitet for antigen, binder denne reseptoren antigenet, komplekset internaliseres og antigenet brytes ned til peptidfragmenter. Peptidene lastes deretter opp i gropen på MHC-klasse II-molekyler og fraktes til overflaten av B-cellen. En slik BCR-ligering aktiverer B-cellen til å dra dypere inn i lymfeknuten, hvor den vil kunne treffe CD4-positive T-celler i randsonen rundt follikkelen (3). Dersom B-cellen i utkanten av folliklene finner en CD4- positiv T-celle som gjenkjenner det samme antigenet (nå presentert i form av peptid/ MHC klasse II kompleks), aktiveres T-cellen. T-cellen stimulerer B-cellen både med cytokiner (for eksempel IL-2, IL-4, IL-5, IL- 6, eller IFN-γ (tab 2), og ved CD40L-ligering av B-cellens CD40 (3). Avhengig av kvaliteten og kvantiteten av de mottatte signalene, vil B-cellen enten dele seg utenfor follikkelen og så differensiere til kortlivede IgM-utskillende plasmaceller (primærrespons), eller vende tilbake til follikkelen for å danne et kimsenter og gjennomgå såkalt Tidsskr Nor Lægeforen nr. 19, 2006;
6 Figur 6 Resirkulering av naive T-celler og effektor-t-celler. A. Naive T-celler sirkulerer i blodbanen og passerer ut i lymfeknuters paracortex gjennom spesialiserte venyler kalt høyendotelvenyler (HEV). T-cellene fester seg til HEV-endotelet med selektiner, kjemokinreseptorer (for eksempel CCR7, som binder CCL21), integriner, og ekstravaserer gjennom endotelet ved diapedese. Dermed kommer T-cellene inn i det ekstravaskulære paracortexvevet og kan reagere på dendrittiske celler lastet opp med antigener fra kroppens mange vev. T-cellene migrerer deretter innover i lymfeknuten til margsinuser som samles til efferente lymfekar. Lymfekarene samles i ductus thoracicus, som tømmer seg i v. subclavia. B. Effektor-T-celler erverver et annet sett med kjemokinreseptorer på overflaten. I infisert vev aktiveres makrofager til å utskille kjemokiner (som for eksempel CCL2, tidligere kalt MIP-1α, CCL2, tidligere MCP-1. T-celler som har kjemokinreseptorer som kan binde disse kjemokinene (henholdsvis CCR1, 4, 5; CCR2, 4, 9), vil stanse opp ved infeksjonsfokus og ekstravasere. I vevet kan T-cellene aktiveres og utøve sin effektorfunksjon, interagere med DC og makrofager (CD40L-CD40, m.fl.), utskille inflammatoriske cytokiner, som IFN-γ, TNF, og drepe målceller (via FasL-Fas-interaksjon). Etter at infeksjonen er bekjempet, kan T-celler migrere tilbake via lymfekar, til blodbanen. Figuren er modifisert fra (3) Figur 7 Peyerske plakk og mucosaassosiert lymfoid vev (MALV). A. I tynntarm finnes peyerske plakk, strukturer som konseptuelt likner lymfeknuter ved å ha B-cellefollikler, T-celleområder og høyendotelvenyler (3). B. Det er imidlertid ingen efferent lymfe, men spesialiserte epitelceller (M-celler) som frakter antigener over epitelet til T-cellene, B-cellene og dendrittiske celler i submucosa (3). Det finnes også spredte dendrittiske celler, både her og i andre slimhinner, som har lange utløpere som strekker seg ut i lumen. Dersom slike dendrittiske celler treffer på patogener som binder MGR, vil den dendrittiske cellen fagocyttere patogenet, aktiveres og dra til drenerende lymfeknuter hvor antigener presenteres. Flesteparten av B-celler, og en stor andel av T-celler i kroppen finnes i mucosaassosiert lymfoid vev (MALV), både i fokale områder, som peyerske plakk eller tonsiller, eller diffust i submucosa. Plasmaceller utskiller IgA-dimerer med J-kjede, som binder poly-ig-reseptor PIgR på overflaten av epitelceller (37). Komplekset transcytteres og PIgR kuttes av proteolyttiske enzymer. Den delen av PIgR som er bundet til IgA etter proteolyse, kalles sekretorisk komponent og beskytter mot proteolyse. Luminalt IgA vil kunne binde bakterier og forhindre at bakterier kan binde seg til epitelceller. Ved tilstedeværelse av patogener i tarmen ligeres MGR på epitelceller, uttrykket av PIgR oppreguleres, og uttransportering av IgA effektiviseres (38). Vaksiner som får tilgang til MALV gjennom M-celler, eller via aktiverte dendrittiske celler, vil kunne aktivere T- og B-celler. Som for andre vaksiner spiller sannsynligvis MGR en stor rolle for kvaliteten av immunresponsen. Figuren er modifisert fra (3) somatisk hypermutasjon (sekundærrespons) (3). De kortlivede plasmacellene står for den såkalte primærresponsen, hvor lavaffinitets IgM-antistoffer utskilles. IgM består av fem (eller seks) antistoffmonomerer (H 2 L 2 ) 5/(6) (35) og er en meget effektiv komplementaktivator. På tross av en lav affinitet finnes ti (eller 12) antigenbindingssteder. Man sier derfor at IgM har høy bindingsaviditet. Kimsenterreaksjonen er grunnlaget for den såkalte sekundærresponsen. I B-cellefollikler finnes en spesialisert celle kalt follikulærdendrittisk celle (FDC). Denne celletypen har et annet opphav enn dendrittiske celler og mangler MHC-klasse II-molekyler, men har rikelig med komplementreseptorer og Fc-reseptorer (3). Antigener som aktiverer komplement eller som binder IgG, dekker derfor follikulærdendrittiske celler. B- celler som aktiveres, gjennomgår en meget kraftig celledeling hvor deres antistoffreseptorgener muteres i en aktiv prosess der AIDproteinet (activation-induced deaminase) er sentralt (36). B-celler med hensiktsmessige mutasjoner binder bedre antigen på overflaten av follikulærdendrittisk celler. De klarer derfor mer effektivt å ta opp antigenet og presentere til CD4-positive T-celler og selekteres dermed for videre overlevelse. T- celle CD40L ligerer CD40 på B-cellens overflate og induserer isotypeskifte, for eksempel fra IgM til IgG. Det er deretter to differensieringsmuligheter: B-cellen kan enten vandre til beinmargen og bli langlivede plasmaceller, eller bli hukommelsesceller klare til å reagere på en reinfeksjon (3). Plasmaceller utskiller 100 millioner antistoffmolekyler per sekund og overlever flere år i beinmargen. På denne måten får man en langvarig humoral immunitet der høyaffinitets isotypeskiftede antistoffer er ferdig fremstilt til neste smitteeksponering (3). Den vaksinerte James hadde altså sannsynligvis høyaffinitets IgG-antistoffer med spesifisitet for kukoppevirus i plasma og ekstracellulærvæsken. Når han så ble eksponert for koppevirus, kunne slike antistoffer kryssreagere med viruset og hindre videre spredning. I forhold til moderne vaksinestrategier er det mulig at B-celler er sekundære i forhold til hensynet til optimal DC-aktivering. Det er likevel vist at B-celler reagerer meget godt på MGR-ligander som CpG og LPS, og at B-celler uttrykker en rekke TLR. Antigener som aktiverer komplement er også ganger mer effektive til å fremkalle antistoffer i sekundærresponsen enn antigen som ikke er bundet til komplementfaktorer. Denne kraftige effekten forklares ved at B-celler har reseptor for komplementfaktor C3d og interaksjon med antigen-c3d komplekser på follikulærdendrittiske celler (3). Altså er det slik at B-celleresponser optimaliseres i nærvær av patogener eller deres produkter (CpG, o.l.), et fenomen som det er mulig å simulere ved vaksinering Tidsskr Nor Lægeforen nr. 19, 2006; 126
7 MEDISIN OG VITENSKAP Antistoffeffektorfunksjoner Antistoffisotyper varierer i evne til å igangsette biologiske effektorfunksjoner. Dette gjelder komplementaktivering, opsonisering (via Fc-reseptorer) og antistoffavhengig cellulær cytotoksisitet. Som en grov hovedregel kan man si at CD4-positive Th1-celler hjelper B-celler til å gjennomgå isotypeskifte til isotyper som er mer effektive ved disse tre prosessene. CD4-positive Th2-celler induserer IgE, som er nødvendig for immunresponser mot helminter. I tillegg induseres andre isotyper og subklasser av IgG. Også for B-celleresponser er det altså hensiktsmessig at dendrittiske celler igangsetter Th1-responser. Virussmittede celler vil også kunne uttrykke enkelte virusproteiner på sin overflate som antistoffer kan binde. Antistoffbinding til celleoverflater resulterer både i komplementaktivering og i antistoffavhengig cellulær cytotoksisitet. I dette siste angripes antistoffmerkede celler av Fc-reseptorbærende celler som NK-celler (3). MHC-peptidbindingslommer MHC-molekyler har meget stor interindividuell variasjon (3). Dette har konsekvenser for vaksinasjonsstrategier da MHC-molekyler varierer sterkt i evnen til å binde definerte peptider. I den peptidbindende gropen finnes lommer hvor bestemte aminosyrer eller sidekjeder kan feste seg. Slike lommer varierer i stor grad mellom personers HLA-molekyler. Det er derfor også oftest forskjellige peptider som presenteres fra et antigent protein hos forskjellige personer. På befolkningsnivå er det dermed som regel mer effektivt å vaksinere med preparater som inneholder hele proteiner, for å sikre at hver enkelt vaksinerte person blir immunisert med et protein som inneholder peptider det er mulig å binde og presentere. Immunitet i slimhinner Slimhinner og mucosaassosiert lymfoid vev (MALV) er meget viktig i vårt forsvar mot patogener (fig 7) (3, 37, 38). Det er ikke hensiktsmessig å reagere immunologisk mot matantigener, kroppen må altså klare å skille bakterier/virus fra for eksempel hveteproteiner (39). Dette kalles oral toleranse. Vaksiner som leveres gjennom slimhinner må altså fremstå som patogent. Mye tyder på at mønstergjenkjennelsesreseptorer har stor betydning for effektiviteten av slike vaksiner. Terapeutiske vaksiner og kreft Kreftceller kan overuttrykke proteiner, uttrykke muterte eller posttranslasjonelt modifiserte proteiner eller uttrykke helt unike tumor spesifikke proteiner, for eksempel hos kreftceller i B-cellerekken, som kan presentere BCR V-region- peptidsekvenser på MHC klasse II. Det er vist at både CD4-positive T-celler og CD8-positive T-celler kan spesifikt angripe kreftceller, et konsept som kalles immunovervåking (25, 26). På samme måte som for mikroorganismer, er optimal immunaktivering nødvendig for adekvate immunresponser mot kreftcellen. Resultater fra vaksineringsforsøk og immunterapi er noe blandet, men lovende. Det pågår en utstrakt internasjonal forskning for å utvikle og optimalisere effektive terapeutiske vaksiner. Jeg takker Hilde Omholt, Gro Tunheim og Hege Bunkholt Elstrand for kommentarer til manuskriptet. e-tab 2, e-fig 2 og e-fig 5 finnes i artikkelen på Litteratur 1. Jenner E. An inquiry into the causes and effects of the variolae vaccinae. London, Stewart AJ, Devlin PM. The history of the smallpox vaccine. J Infect 2005; 52: Bogen B, Munthe LA. Immunologi. Oslo: Universitetsforlaget, Brown JH, Jardetzky TS, Gorga JC et al. Threedimensional structure of the human class II histocompatibility antigen HLA-DR1. Nature 1993; 364: Akira S, Uematsu S, Takeuchi O. Pathogen recognition and innate immunity. Cell 2006; 124: Poltorak A, He X, Smirnova I et al. Defective LPS signaling in C3H/HeJ and C57BL/10ScCr mice: mutations in Tlr4 gene. Science 1998; 282: Ozinsky A, Underhill DM, Fontenot JD et al. The repertoire for pattern recognition of pathogens by the innate immune system is defined by cooperation between toll-like receptors. Proc Natl Acad Sci U S A. 2000; 97: Takeuchi O, Hoshino K, Akira S. Cutting edge: TLR2-deficient and MyD88-deficient mice are highly susceptible to Staphylococcus aureus infection. J Immunol 2000; 165: Takeuchi O, Kawai T, Muhlradt PF et al. Discrimination of bacterial lipoproteins by Toll-like receptor 6. Int Immunol 2001; 13: Hemmi H, Takeuchi O, Kawai T et al. A Toll-like receptor recognizes bacterial DNA. Nature 2000; 408: Alexopoulou L, Holt AC, Medzhitov R et al. Recognition of double-stranded RNA and activation of NF-kappaB by Toll-like receptor 3. Nature 2001; 413: Hayashi F, Smith KD, Ozinsky A et al. The innate immune response to bacterial flagellin is mediated by Toll-like receptor 5. Nature : Gantner BN, Simmons RM, Canavera SJ et al. Collaborative induction of inflammatory responses by dectin-1 and Toll-like receptor 2. J Exp Med 2003; 197: Krutzik SR, Ochoa MT, Sieling PA et al. Activation and regulation of Toll-like receptors 2 and 1 in human leprosy. Nat Med 2003; 9: Hochrein H, Schlatter B, O Keeffe M et al. Herpes simplex virus type-1 induces IFN-alpha production via Toll-like receptor 9-dependent and -independent pathways. Proc Natl Acad Sci USA. 2004; 101: Krug A, French AR, Barchet W et al. TLR9-dependent recognition of MCMV by IPC and DC generates coordinated cytokine responses that activate antiviral NK cell function. Immunity 2004; 21: Yoneyama M, Kikuchi M, Matsumoto K et al. Shared and unique functions of the DExD/H-box helicases RIG-I, MDA5, and LGP2 in antiviral innate immunity. J Immunol 2005; 175: Heil F, Hemmi H, Hochrein H et al. Species-specific recognition of single-stranded RNA via tolllike receptor 7 and 8. Science 2004; 303: Kurt-Jones EA, Popova L, Kwinn L et al. Pattern recognition receptors TLR4 and CD14 mediate response to respiratory syncytial virus. Nat Immunol 2000; 1: Bieback K, Lien E, Klagge IM et al. Hemagglutinin protein of wild-type measles virus activates tolllike receptor 2 signaling. J Virol 2002; 76: Querec T, Bennouna S, Alkan S et al. Yellow fever vaccine YF-17D activates multiple dendritic cell subsets via TLR2, 7, 8, and 9 to stimulate polyvalent immunity. J Exp Med 2006; 203: Pulendran B, Ahmed R. Translating innate immunity into immunological memory: implications for vaccine development. Cell 2006; 124: Tonegawa S. Somatic generation of antibody diversity. Nature 1983; 302: Schulz O, Diebold SS, Chen M et al. Toll-like receptor 3 promotes cross-priming to virus-infected cells. Nature 2005; 433: Corthay A, Skovseth DK, Lundin KU et al. Primary antitumor immune response mediated by CD4+ T cells. Immunity 2005; 22: Dunn GP, Old LJ, Schreiber RD. The three Es of cancer immunoediting. Annu Rev Immunol 2004; 22: Pulendran B, Kumar P, Cutler CW et al. Lipopolysaccharides from distinct pathogens induce different classes of immune responses in vivo. J Immunol 2001; 167: Napolitani G, Rinaldi A, Bertoni F et al. Selected Toll-like receptor agonist combinations synergistically trigger a T helper type 1-polarizing program in dendritic cells. Nat Immunol 2005; 6: Roelofs MF, Joosten LA, Bdollahi-Roodsaz S et al. The expression of toll-like receptors 3 and 7 in rheumatoid arthritis synovium is increased and costimulation of toll-like receptors 3, 4, and 7/8 results in synergistic cytokine production by dendritic cells. Arthritis Rheum 2005; 52: Pulendran B, Kumar P, Cutler CW et al. Lipopolysaccharides from distinct pathogens induce different classes of immune responses in vivo. J Immunol 2001; 167: Dillon S, Agrawal A, Van Dyke T et al. A Toll-like receptor 2 ligand stimulates Th2 responses in vivo, via induction of extracellular signal-regulated kinase mitogen-activated protein kinase and c-fos in dendritic cells. J Immunol 2004; 172: Netea MG, Sutmuller R, Hermann C et al. Toll-like receptor 2 suppresses immunity against candida albicans through induction of IL-10 and regulatory T cells. J Immunol 2004; 172: Wille-Reece U, Flynn BJ, Lore K et al. HIV Gag protein conjugated to a Toll-like receptor 7/8 agonist improves the magnitude and quality of Th1 and CD8+ T cell responses in nonhuman primates. Proc Natl Acad Sci USA 2005; 102: Ridge JP, Di RF, Matzinger P. A conditioned dendritic cell can be a temporal bridge between a CD4+ T-helper and a T-killer cell. Nature 1998; 393: Sorensen V, Rasmussen IB, Sundvold V et al. Structural requirements for incorporation of J chain into human IgM and IgA. Int Immunol 2000; 12: Honjo T, Nagaoka H, Shinkura R et al. AID to overcome the limitations of genomic information. Nat Immunol 2005; 6: Brandtzaeg P, Johansen FE. Mucosal B cells: phenotypic characteristics, transcriptional regulation, and homing properties. Immunol Rev 2005; 206: Schneeman TA, Bruno ME, Schjerven H et al. Regulation of the polymeric Ig receptor by signaling through TLRs 3 and 4: linking innate and adaptive immune responses. J Immunol 2005; 175: Sollid LM, Jabri B. Is celiac disease an autoimmune disorder? Curr Opin Immunol 2005; 17: Manuskriptet ble mottatt og godkjent Medisinsk redaktør Petter Gjersvik. Tidsskr Nor Lægeforen nr. 19, 2006;
8 Det norske vaksinasjonsprogrammet Sammendrag Vaksineutviklingen har på mange måter vært «det muliges kunst», der man hele tiden har fulgt opp dagens kunnskap om infeksjoner og mikrober med nye preparater. Enhver vaksinasjon har som formål å forebygge sykdom. Vaksiner som brukes i et vaksinasjonsprogram, har dessuten et mål utover å beskytte enkeltindividet, nemlig å endre epidemiologien for den aktuelle sykdommen. I løpet av de kommende ti år vil vi få tilgang til flere vaksiner, men det er lite sannsynlig at det norske vaksinasjonsprogrammet blir radikalt forandret. På lengre sikt kan man tenke seg at økte kunnskaper om immunapparatet gjør det mulig å bygge opp vaksinasjonsprogrammet på en helt ny måte. Kanskje kan vaksiner hjelpe oss til å styre immunforsvaret slik at vi oppnår god generell beskyttelse mot sykdom, lite allergi og lite autoimmune sykdommer i tillegg til beskyttelse mot spesifikke infeksjoner. Engelsk sammendrag finnes i artikkelen på Oppgitte interessekonflikter: Ingen > Se også side 2504 Hanne Nøkleby [email protected] Berit Feiring Nasjonalt folkehelseinstitutt Postbok 4404 Nydalen 0403 Oslo Moderne vaksinehistorie begynner med koppevaksinen i Starten bygger på kombinasjonen av en skarp observasjon og flaks (1). Først omkring 100 år senere, da verden fikk forståelse for bakterienes rolle i infeksjonssammenheng, kom grunnlaget for et systematisk arbeid. En rekke bakterier ble dyrket, drept og forsøkt som vaksiner. Vellykket behandling av difteri og tetanus med antitoksin fra hest ga grunnlag for utvikling av toksoidvaksiner. Med virologien kom virusvaksinene. Genteknologiens fremvekst ga store forhåpninger om nye vaksinemuligheter, men de er til nå bare i beskjeden grad innfridd. Slik har vaksineutviklingen på en måte vært «det muliges kunst», der man hele tiden fulgte opp dagens kunnskap med nye preparater. Noen vaksiner har overlevd nærmest uendret i nær 100 år, andre har gått i glemmeboken. De som er valgt ut til vaksinasjonsprogrammer, har likevel hatt spesielle egenskaper. Vaksinasjonsprogrammets utvikling Samlet sett er bruk av vaksiner sannsynligvis vår viktigste strategi i kampen mot sykdommer. Enhver vaksinasjon har som formål å forebygge sykdom. Men vaksinasjonsprogrammer har større siktemål: ikke bare å beskytte enkeltindividet, men å endre epidemiologien for sykdommen. Det mest ambisiøse målet er å utrydde sykdommen. Det har verden klart med kopper, og vi er nær målet for poliomyelitt (2). Mer beskjedne mål er å hindre smitte innen et land eller et større geografisk område (meslinger), eller å redusere forekomsten så mye at det også gir en viss beskyttelse av dem som ikke er vaksinert (kikhoste). Slike mål forutsetter at man når frem til store deler av målgruppen. Hvilken vaksinasjonsdekning som må til, sannsynligheten for å oppnå tilstrekkelig høy dekning og hva man risikerer hvis målet ikke nås, er spørsmål som må tas opp til vurdering før programmet startes. Risikoen ved et dårlig gjennomført program kan være at sykdommen forskyves til en annen aldersgruppe, der skadene blir langt større (3). Også vaksinasjonsprogrammet begynte med koppevaksine. I Danmark-Norge ble vaksinen påbudt i 1810, selv om påbudet neppe ble særlig strengt håndhevet. Vaksinen inngikk i vårt vaksinasjonsprogram i over 160 år, hele tiden som påbudt vaksine (tab 1). Tuberkulose var en fryktet sykdom på og 1900-tallet. Bedre levekår er den viktigste grunnen til tuberkulosen nesten har forsvunnet i vårt land. Men i 1947 var frykten for sykdommen fortsatt så stor at BCGvaksine ble tatt inn i vaksinasjonsprogrammet. I motsetning til de fleste andre land valgte Norge ikke å vaksinere spedbarn, men derimot tenåringer, på vei fra den obligatoriske skolen til «det virkelige livet», fordi det var da smitterisikoen var størst hos oss. BCG-vaksinen var påbudt de første årene, mens alle vaksiner som senere er tatt inn i programmet har vært frivillige. Da smittevernloven kom i 1995, ble også BCG-vaksinering frivillig. I dagens situasjon vurderes det om BCG-vaksine bør tas ut av det generelle programmet og bare tilbys grupper med økt risiko for tuberkulosesmitte. Difteriepidemiene herjet under den annen verdenskrig, og mange barn og voksne ble vaksinert. Vaksinen ble imidlertid ikke en del av et allment program før ti år senere, da den ble tilgjengelig som kombinasjonsvaksine sammen med vaksine mot tetanus og kikhoste (DTP-vaksine). Det siste var nok en fryktet sykdom. Den ble regnet blant barnesykdommene, som alle barn skulle gjennom, men var likevel årsak til mye lidelse, flere tilfeller av varige hjerneskader og noen dødsfall hvert år. Etter de store polioepidemiene i begynnelsen av 1950-årene, var poliomyelitt den store skrekken for mange foreldre. Poliovaksinen ble derfor tatt imot med stor glede i! Hovedbudskap Vaksinasjon har gjort alvorlige og tidligere vanlige sykdommer sjeldne Kravene til sikkerhet må være høyere for vaksiner enn for andre legemidler, fordi vaksine gis til et stort antall friske individer På lengre sikt kan modifisering av immunforsvaret gjennom vaksinering også gi gevinster utover beskyttelse mot bestemte sykdommer 2538 Tidsskr Nor Lægeforen nr. 19, 2006; 126:
9 MEDISIN OG VITENSKAP Vaksinasjonsdekningen var høy. Problemet var å skaffe vaksine til alle som ville ha (4). Innføring av vaksine mot meslinger var kanskje den første delen av programmet som skapte betydelig debatt her i landet (5). Meslinger hadde da alle hatt, det kunne vel ikke være farlig? For første gang var det vanskelig å få vaksinasjonsdekningen for en programvaksine opp mot 80 %, med den risikoen det innebærer for forskyvning av sykdommen til en aldersgruppe der konsekvensene kunne være mer alvorlige. Derimot var det ingen uenighet om at røde hunder var en meget alvorlig sykdom for gravide. Det var derfor liten motstand da vaksine mot røde hunder ble tilbudt jenter i ungdomsskolen i Større var usikkerheten da kombinasjonsvaksinen mot meslinger, kusma og røde hunder kom inn i programmet (6). Var det virkelig riktig å gi vaksine mot røde hunder til alle småbarn? Erfaring fra Norge og andre land har vist at dette var nødvendig og tilstrekkelig til å gjøre medfødt rubellasyndrom til historie (tab 1). Vaksinasjonsprogrammet i 2006 Muligheten til å forebygge en alvorlig sykdom med stor utbredelse har vært forutsetningen for å innlemme en vaksine i det norske vaksinasjonsprogrammet. Frem til 1990 var alle vaksiner i programmet (unntatt tetanusvaksine) rettet mot sykdommer som rammet de aller fleste, selv om langt fra alle fikk alvorlige forløp med komplikasjoner. Dette bildet ble annerledes da Hib-vaksinen ble innført. Haemophilus influenzae serotype b var uten tvil den bakterien som ga flest tilfeller av alvorlig invasive infeksjoner hos barn i de første fem leveårene, men det var bare et par hundre barn som ble rammet hvert år (7). Vaksinen virker kun mot type b, ikke mot de typene som er vanlig årsak til mer banale luftveisinfeksjoner. Det var likevel enighet om at sykdommen var så alvorlig for dem som ble rammet, at det var riktig å gi vaksinen til alle norske spedbarn (tab 2). Det samme argumentet kommer inn i enda sterkere grad når vi nå innfører sjuvalent pneumokokkonjugatvaksine. Det er ingen tvil om at alvorlige, invasive pneumokokkinfeksjoner forekommer hyppigere i de første to leveårene enn hos eldre barn. Det er heller ikke tvil om at vaksinen er effektiv (8). Den har også en viss effekt mot pneumoni og otitt (9), men bare en mindre del av disse infeksjonene er forårsaket av de pneumokokktypene som inngår i vaksinen. Totalt vil bare et fåtall av barna ha direkte nytte av pneumokokkvaksinen. Sykdommens konsekvenser gjør det likevel riktig å vaksinere alle. Vaksiner gis til tusenvis av barn for å hindre alvorlig sykdom som bare rammer en prosent eller enda færre. Det skiller vaksiner fra terapeutiske legemidler. Derfor er kravene til grundige utprøvninger på forhånd, Tabell 1 Innføring av vaksiner i vaksinasjonsprogrammet i Norge Vaksine Tatt i bruk Kommentarer Koppevaksine 1810 Påbudt. I programmet til 1976 BCG-vaksine 1947 Tenåringer. Påbudt til 1995, deretter frivillig DTP-vaksine 1952 Spedbarn. Frivillig Poliovaksine 1956 Skolebarn og spedbarn. Frivillig. Meslinger måneder. Frivillig. Erstattet av MMR Røde hunder 1978 Jenter i ungdomsskolen. Erstattet av MMR MMR måneder og 12 år. Frivillig Hib 1992 Spedbarn. Frivillig Pneumokker 2006 Spedbarn. Frivillig Tabell 2 Vaksinasjonsprogrammet i Norge i 2006 Alder Vaksine mot 3, 5 og 12 måneder Difteri, tetanus, kikhoste, poliomyelitt, Hib, pneumokokkinfeksjon 15 måneder Meslinger, kusma og røde hunder 7 8 år Difteri, stivkrampe, kikhoste, poliomyelitt 12 år Meslinger, kusma og røde hunder Ungdomsskolealder Tuberkulose, difteri, stivkrampe, poliomyelitt Tabell 3 Mulige nye vaksiner i vaksinasjonsprogrammet i 2016 Sykdommer det kan bli aktuelt å vaksinere mot Vaksinens status Kommentarer Hepatitt B Tilgjengelig Epidemiologi og behov i Norge må vurderes løpende. Kan bli aktuelt ved endringer. Tenåringsprogram? Vannkopper Tilgjengelig Behov og ventet effekt må vurderes løpende. Tilbud til ikke-immune tenåringer? Meningokokker gruppe C (eller ACYW) Tilgjengelig først og fremst med tanke på sikkerhet, strengere for vaksiner enn for noe annet legemiddel. En vaksine er som en forsikring, noe alle trenger fordi vi ikke vet hvem som blir rammet. Så langt det på noen måte er mulig, må det derfor sikres at vi ikke risikerer uventede, alvorlige reaksjoner med varige følger (10). Sikkerheten for vaksinene i dagens vaksinasjonsprogram er underbygd av erfaring fra bruk av mange millioner doser. Kan bli aktuelt hvis forekomsten i Norge øker Hepatitt A Tilgjengelig Fortsatt en reisevaksine? Influensavaksine til småbarn Tilgjengelig Måtte gis årlig til definerte aldersgrupper. Vil trolig bli vurdert HPV-virus Tilgjengelig 2006/2007 Vil trolig bli innført når dokumentasjonen vurderes som tilstrekkelig Rotavirus Tilgjengelig 2006 Epidemiologi og behov i Norge er under vurdering Herpes simplex Kliniske utprøvninger pågår Vurderes når den blir tilgjengelig RSV Hiv Utvikling pågår, men går langsomt. Neppe tilgjengelig før 2016 Terapeutiske vaksiner er kommet langt, men generell, profylaktisk vaksine er vanskelig. Neppe tilgjengelig før 2016 Bør innføres til spedbarn når den blir tilgjengelig Vil sannsynligvis bli innført når den kommer Om ti år nye vaksiner, men ingen revolusjon Da genteknologien gjorde sitt inntog i årene, var forventningene til nytten av slike teknikker i vaksinesammenheng skyhøye. Hittil har resultatene imidlertid vært moderate. Vaksinetilbudet domineres av «gammeldagse» vaksiner. Alle vaksiner i programmet er laget med tradisjonelle teknikker. De består av inaktiverte mikrober (hele eller deler), levende svekkede mikrober eller Tidsskr Nor Lægeforen nr. 19, 2006;
10 avgiftede toksiner. I global sammenheng har likevel én genteknologisk fremstilt vaksine vært et meget viktig fremskritt, vaksine mot hepatitt B. Det er imidlertid signaler som tyder på at dette nå er i ferd med å endre seg. Flere nye vaksiner, utviklet ved hjelp av genteknologiske metoder, er på trappene. Vaksine mot humant papillomvirus (HPV-vaksine) og rotavirus er her allerede (11, 12). Vaksine mot herpesinfeksjoner er ikke kommet så langt, men også her er det gjort fremskritt. Det er fortsatt vanskelig å komme frem til en vaksine mot RS-virus. De katastrofale forsøkene med slik vaksine i 1960-årene, der de vaksinerte fikk langt mer alvorlig sykdom enn de ikke-vaksinerte (13), gjør at forsøkene går langsomt fremover. Samtidig er dette en av de vaksinene barnemedisinen venter mest utålmodig på. Lokale epidemiologiske forhold er medvirkende til at vaksinasjonsprogrammet er forskjellig fra land til land. I Norge inngår ikke vaksine mot hepatitt B, meningokokk gruppe C og vannkopper i vaksinasjonsprogrammet, fordi sykdommene og/eller deres komplikasjoner er sjeldne i vårt land. Endringer i epidemiologi eller nye vurderinger kan føre til at vi velger å innføre generell vaksinasjon mot disse sykdommene også her i landet. I de nærmeste årene vil det sannsynligvis bli utviklet flere kombinasjonsvaksiner. Det vil være nødvendig for å få gitt de vaksiner vi ønsker uten å komme opp i et uakseptabelt antall stikk. Men det har flere ganger vist seg vanskelig å oppnå samme effekt som av enkeltvaksinene når flere vaksiner kombineres i én injeksjon. Så lenge hver vaksine må lages for seg og deretter blandes med de andre, er utvikling og produksjon av kombinasjonsvaksiner arbeids- og kostnadskrevende, og antall komponenter i hver vaksine vil være begrenset. Det arbeides også med å utvikle vaksiner som kan gis på andre måter enn ved injeksjon, først og fremst på slimhinner (peroralt, nesedråper), men også transkutant (plaster). Vaksineutvikling er så kostnadskrevende at man neppe vil bruke mye ressurser på å omformulere godt fungerende vaksiner til slike presentasjonsformer, men for nye vaksiner gir dette flere muligheter. I vaksinasjonsprogrammet frem mot 2016 kan vi vente flere nye vaksiner, kanskje nye vaksinasjonsregimer og kanskje bruk i andre aldersgrupper. Det mest sannsynlige er likevel at det ikke blir noen prinsipielle endringer i programmet slik vi kjenner det i dag (tab 3). Vaksinasjonsprogram for eldre? Hittil har «vaksinasjonsprogram» i praksis vært synonymt med barnevaksinasjonsprogrammet. Flere sykdommer slår imidlertid først og fremst til i livets ytterfaser, dvs. hos de yngste og de eldste. Vaksinering av eldre dukker derfor opp som et aktuelt og viktig tema. Årlig vaksinering mot influensa er anbefalt for alle over 65 år. Helse- og omsorgsdepartementet sendte våren 2006 på høring et forslag til en ny forskrift, som gjør dette til en del av det nasjonale vaksinasjonsprogrammet. Generell vaksinering av eldre mot pneumokokkinfeksjon er også anbefalt. Det kan bli en del av samme program. En vaksine mot herpes zoster er under utvikling, først og fremst beregnet på eldre. Den kan bli særlig viktig hvis vi velger å ta i bruk generell vaksinering mot vannkopper. Redusert forekomst av vannkopper gir mindre mulighet for naturlig boostring av immuniteten. Risikoen for å utvikle herpes zoster i høyere alder vil sannsynligvis øke (14). Det kan derfor være nyttig å se disse to vaksinene i sammenheng, når vi skal vurdere deres rolle i vaksinasjonsprogrammet. Om 20 år nye måter å tenke på? I de senere år er vi blitt klar over at vaksiner kan ha andre og mer uspesifikke effekter i tillegg til å beskytte mot en konkret sykdom. Det viste seg første gang da en meslingvaksine utviklet for å ha effekt allerede fra tre måneders alder, ble utprøvd i Afrika. Vaksinen var effektiv mot meslinger. Men da barna var fulgt opp til tre års alder, hadde jenter som hadde fått den nye vaksinen en total overdødelighet i forhold til dem som var vaksinert på tradisjonell måte (15). Epidemiologiske oppfølgingsundersøkelser tyder på at det ikke skyldtes problemer med den nye vaksinen, men en generell positiv effekt på overlevelse av den konvensjonelle meslingvaksinen. En tilsvarende positiv effekt er vist av BCG-vaksine til nyfødte, mens resultatene knyttet til DTP-vaksine er langt mer tvilsomme (16). Dette viser først og fremst at det er mye vi ikke vet om effekten av vaksiner, og for den saks skyld av infeksjoner, i tidlig barnealder. Sannsynligvis henger slike effekter sammen med hvordan stimuli spiller på det medfødte infeksjonsforsvaret (17), eller hvordan de er med på å styre immunapparatet i forskjellige retninger. Foreløpig må vi først og fremst ha dette i tankene hvis gamle vaksiner skal byttes ut med nye. Det er stort behov for en bedre vaksine mot tuberkulose i store deler av verden, men utprøvninger av nye vaksiner til spedbarn må sikre at vi ikke bare får effekt mot tuberkulose, men også opprettholder den gunstige effekten på generell overlevelse. I løpet av de neste 20 år vil vår viten om immunsystemet kanskje bli så stor at vi kan bruke den til å bygge opp det ideelle vaksinasjonsprogrammet. Gjennom bruk av de rette antigenene, og ikke minst riktig adjuvans (stoff som tilsettes for å øke responsen mot vaksineantigenene), på riktig tidspunkt, kan et vaksinasjonsprogram bidra til å målrette vårt immunforsvar. Målet vil være god generell beskyttelse mot sykdom, lite allergi og lite autoimmune sykdommer i tillegg til de spesifikke vaksineeffektene vi drar nytte av allerede i dag. Det er neppe noen som i dag tør å si hvordan et slikt program vil se ut. Men det er spennende utsikter, og mulighetene overgår sannsynligvis det vi kan forestille oss. Litteratur 1. Jenner E. An inquiry into the causes and effects of the variolae vaccinae, a disease discovered in some of the western counties in England, particularly Gloucestershire and known by the name of cow pox. London Trykt i: Camac CNB, red. Classics of medicine and surgery. New York: Dover, Progress towards global poliomyelitis eradication: preparation for the oral poliovirus vaccine cessation era. WHO WER 2004; 79: Panagiotopoulos T, Antoniadou I, Valassi-adam E. Increase in congenital rubella occurrence after immunisation in Greece: retrospective survey and systematic review. BMJ 1999; 319: Ørstavik I, Jakobsen E. Vaksinasjon mot poliomyelitt. Tidskr Nor Lægeforen 1971; 91: Lerche C. Bør vi vaksinere mot meslinger? Tidsskr Nor Lægeforen 1972; 92: Rønne T, Kaaber K, Petersen I. Kendskab og holdninger samt tilslutning de to første år til de nye vaccinationer mod mæslinger, fåresyge og røde hunde. Ugeskr Læger1989; 151: Claesson BA. Epidemiology of invasive Haemophilus influenzae type b disease in Scandinavia. Vaccine 1993; (suppl 1): Black S, Shinefield H, Fireman B et al. Efficacy, safety and immunogenicity of heptavalent pneumococcal conjugate vaccine in children. Northern California Kaiser Permanente Vaccine Study Center Group. PIDJ 2000; 19: Kilpi T, Ahman H, Jokinen J et al. Protective efficacy of a second pneumococcal conjugate vaccine against pneumococcal acute otitis media in infants and children: randomized controlled trial of a 7-valent pneumococcal polysaccharide-meningococcal outer membrane protein complex conjugate vaccine in 1666 children. Clin Infect Dis 2003; 37: Chen RT, Glasser JW, Rhodes PH et al. Vaccine Safety Datalink Project: a new tool for improving vaccine safety monitoring in the United States. Pediatrics 1997; 99: Lowndes CM, Gill ON. Cervical cancer, human papillomavirus, and vaccination. BMJ 2005; 331: Glass RI, Parashar UD. The promise of new rotavirus vaccines. N Engl J Med 2006; 345: Kim HW, Canchola JG, Brandt CD et al. Respiratory syncytial virus disease in infants despite prior administration of antigenic inactivated vaccine. Am J Epidemiol 1969; 89: Oxman MN, Levin MJ, Johnson GR et al. A vaccine to prevent herpes zoster and postherpetic neuralgia in older adults. N Engl J Med 2005; 352: Aaby P, Knudsen K, Whittle H et al. Long-term survival after Edmonston Zagreb measles vaccination in Guinea-Bissau: increased female mortality rate. J Pediatr 1993; 122: Kristensen I, Aaby P, Jensen H. Routine vaccinations and child survival: follow up study in Guinea- Bissau, West Africa. BMJ 2000; 321: Siegrist CA. Neonatal and early life vaccinology. Vaccine 2001; 19: Manuskriptet ble mottatt og godkjent Medisinsk redaktør Petter Gjersvik Tidsskr Nor Lægeforen nr. 19, 2006; 126
11 MEDISIN OG VITENSKAP Uønskede hendelser etter vaksinering Sammendrag Det er lett å rette oppmerksomheten mot risikoen ved vaksiner når de sykdommene vi vaksinerer mot blir svært sjeldne. Vaksiner har tidligere ført til utilsiktede skader på grunn av produksjonsfeil og mangelfull kontroll. I dag er kravene til vaksinekontroll så strenge at risikoen for slike hendelser er nær null. Lokalreaksjoner og lette systemiske vaksinereaksjoner er relativt vanlig, og er som regel godt beskrevet når en vaksine blir godkjent. Vaksiner kan imidlertid medføre sjeldne reaksjoner, som bare kan avsløres ved overvåking av reaksjoner etter at vaksinen er tatt i bruk. Mistanke om slike hendelser kommer i dag oftest gjennom meldesystemer. Avklaring av mulig årsakssammenheng krever oftest store, epidemiologisk undersøkelser. Registrering av og åpenhet om vaksinereaksjoner er avgjørende for å opprettholde vaksinenes troverdighet. Engelsk sammendrag finnes i artikkelen på Oppgitte interessekonflikter: Se til slutt i artikkelen > Se også side 2504 Hanne Nøkleby [email protected] Marianne A. Riise Bergsaker Divisjon for smittevern Nasjonalt folkehelseinstitutt Postboks 4404 Nydalen 0403 Oslo Vaksiner er et klassisk eksempel på det såkalte forebyggingsparadokset. Vellykket forebygging gjør den forebyggede tilstanden usynlig. Vi glemmer at den eksisterer. Dermed blir eventuelle negative effekter av det midlet som benyttes, dominerende i folks oppfatning av problemstillingen. Samtidig må vi innse at de første vaksinene langt fra var ufarlige. Da koppevaksinen ble tatt i bruke i 1796, foregikk det ingen systematisert produksjon og slett ikke noen kvalitetskontroll. Vaksinen ble bokstavelig talt overført fra arm til arm og kunne medføre overføring av andre sykdommer, som hepatitt B, difteri og meslinger. Selv om produksjonen ble noe bedre kontrollert omkring 100 år senere, kunne den levende vaksinen forårsake generaliserte infeksjoner, med encefalitt som den mest alvorlige. Så sent som i 1960-årene forekom encefalitt (1 : ved vaksinering i spedbarnsalder) og enkelte dødsfall på grunn av koppevaksine i Norge (1). Så lenge kopper ble opplevd som en stor trussel, var dette en akseptabel pris å betale sett fra samfunnets side. Etter at kopper ble en svært sjelden sykdom, raste det forståelig nok sterke diskusjoner om hvor lenge det var riktig å fortsette med koppevaksinen (2) før den ble tatt ut av det norske vaksinasjonsprogrammet i Også andre vaksiner har gitt store skader i situasjoner der produksjonen ikke har vært underlagt tilstrekkelig kontroll. I 1902 døde 13 barn i USA etter å ha blitt vaksiner med difterivaksine forurenset med tetanustoksin (3). Hendelsen førte til en ny lov om kravene til kontroll av vaksiner i USA. Det forhindret likevel ikke den såkalte Cutter-hendelsen i 1955, der ufullstendig inaktivering av poliovaksine førte til mer enn 200 tilfeller av paralytisk poliomyelitt. Vaksiner har således gjennom årene ført til alvorlige, uønskede hendelser. Som en følge av dette er kravene til vaksinekontroll og oppfølgingen av at kravene blir fulgt, i dag så strenge at risikoen for at en slik hendelse skal gjenta seg er svært nær null. I dag er spørsmålet derfor i hvilken grad vaksiner kan ha uforutsette uheldige virkninger, selv om produksjon og kontroll har foregått etter alle kunstens regler. Problemstillingen er aktuell for alle legemidler, men vaksiner skiller seg fra andre legemidler ved at de gis til store grupper av friske personer, oftest barn. Derfor må kravene til balanse mellom effekt og bivirkninger, og kravene til kunnskap om dette før preparatet tas i bruk, være høyere for vaksiner enn for andre legemidler. Vanlige vaksinereaksjoner På engelsk brukes i dag uttrykket «adverse events following immunisation», AEFI. I dette begrepet ligger det en tidsmessig, men ikke noen årsaksmessig, sammenheng. Uttrykket oversettes best med «uønskede hendelser etter vaksinering». Siden dette er et langt og tungt uttrykk, brukes på norsk oftest, og i denne artikkelen, vaksinereaksjoner om begrepet AEFI. Vaksinereaksjoner deles i lokale og systemiske reaksjoner. Lokalreaksjoner forekommer etter vaksinering med alle vaksiner, selv om hyppigheten varierer. Etter poliovaksine er lokalreaksjoner en raritet. Etter vaksinering med vaksiner som inneholder aluminiumssalter som adjuvans, slik som difteriog stivkrampevaksiner, vil minst 10 % oppleve rubor, hevelse og smerte på injeksjonsstedet i større eller mindre grad. Feilaktig injeksjonsteknikk, f.eks. subkutan injeksjon i stedet for intramuskulær, øker risikoen for lokalreaksjoner. Reaksjonen kommer gjerne først etter en dag eller to, og kan vare opptil en ukes tid (4). Reaksjonen på Hib-vaksine er annerledes, i det den kommer i løpet av få timer, dekker et stort område og oftest er over til neste dag (5). Lokalreaksjoner er så vanlig at både type og hyppighet kan fastslås i tidlige kliniske utprøvninger, og vil være godt beskrevet når vaksinen tas i vanlig bruk.! Hovedbudskap Alvorlige vaksinereaksjoner eller varige skader etter vaksiner forekommer uhyre sjelden Den største risikoen ligger i at alvorlige infeksjonssykdommer blir oversett fordi man tror symptomene skyldes en vaksine Registrering og oppfølging av vaksinereaksjoner og åpenhet om funnene er helt nødvendig for å opprettholde vaksinenes troverdighet Tidsskr Nor Lægeforen nr. 19, 2006; 126:
12 Ramme 1 Den første vaksinen mot rotavirusinfeksjon ble godkjent i 1998 og straks innført i vaksinasjonsprogrammetprogrammet i USA. I løpet av de første åtte månedenes bruk mottok det amerikanske medlesystemet for vaksinereaksjoner VAERS ni meldinger om invaginasjon kort tid etter vaksinering. Dette førte til at det straks ble gjennomført en større pasient-kontrollundersøkelse, med utgangspunkt i 429 barn innlagt for invaginasjon og kontrollpersoner. Studien konkluderte med at risikoen for å få invaginasjon var nesten 30 ganger høyere i løpet av de første dagene etter første vaksinedose enn ellers (7). Vaksinen ble straks trukket fra markedet. Det er ingen tvil om at dette var riktig for USA og andre vestlige land. Samtidig mistet land der rotavirusinfeksjoner er årsak til mange dødsfall hos spedbarn, tilgang til vaksinen, til tross for at en slik vaksine sannsynligvis ville reddet mange liv. Systemiske reaksjoner er langt sjeldnere (tab 1). Grader av uvelfølelse og feber regnes imidlertid blant de vanlige reaksjonene Tabell 1 Vaksinereaksjoner som kan skape bekymringer Vaksine Reaksjonstype Kommentar Difteri- og tetanusvaksine MMR-vaksine 1 MMR-vaksine 1 Store lokalreaksjoner (rubor, hevelse, ømhet), ofte av flere dagers varighet. Av og til feber Lette tilfeller av de aktuelle sykdommene etter 5 12 dager Trombocytopeni hos 1 av vaksinerte etter de fleste vaksiner. Hvor vanlig det angis å være, vil bl.a. avhenge av måten studiene er gjort. En rekke studier konkluderer med at % av alle småbarn får feber etter MMR-vaksine. Lette infeksjoner med feber er imidlertid meget vanlig i annet leveår, også hos dem som ikke blir vaksinert. I en finsk tvillingundersøkelse fikk den ene tvillingen MMR-vaksine og den andre placebo. Foreldrene førte «bivirkningsdagbok» for begge. Etter tre uker ble vaksinasjonen gjentatt på omvendt måte. Resultatene viste at det bare var 5 % høyere forekomst av feber hos den tvillingen som hadde fått ekte vaksine (6). Resten representerte vanlige infeksjoner for et barn i den alderen. De samme forfatterne har også vist at fordi man velger å vaksinere barna i en frisk periode, og småbarn mellom ett og to år er mye småsyke, vil forekomsten av vanlige forkjølelsessymptomer etc. øke hos så vel vaksinerte som hos barn som har fått placebo, i de første 7 9 dagene etter vaksinering. Barna går simpelthen tilbake fra å være uvanlig friske til sin vanlige helsetilstand. Dette beskrives gjerne som «den friske vaksineeffekten» (the healthy vaccinee effect) og kan ifølge forfatterne forklare mange av de symptomer som tilskrives vaksiner (7). En vanlig oppfatning, også blant helsepersonell, er at vaksiner kan føre til den sykdommen det vaksineres mot. De aller fleste vaksiner inneholder imidlertid ikke levende komponenter og kan således ikke forårsake Kan likne erysipelas, men gir bare lett forhøyet CRP. Ikke grunnlag for antibiotikabehandling Ufarlig. Smitte til ikke-immune aldri beskrevet Oftest forløp som mild ITP 2. Trombocytopeni ses hos ca. 1 av etter rubella Rubella Leddsymptomer Ikke økt forekomst av kroniske leddlidelser 1 Vaksine mot meslinger, kusma og røde hunder 2 Idiopatisk trombocytopenisk purpura Tabell 2 Noen mistenkte alvorlige vaksinereaksjoner Vaksine Reaksjon Mulig årsakssammenheng Kopper Encefalitt Ja Helcellevaksine mot kikhoste Encefalopati Sannsynligvis ikke MMR 1 Autisme Nei Hepatitt B Multippel sklerose Sannsynligvis ikke Influensa Guillain-Barrés syndrom 1: ved svineinfluensavaksine, benyttet i USA :1 mill ved senere vaksiner Vaksiner med thiomersal Autisme, hjerneskade Ingen holdepunkter til nå 1 Vaksine mot meslinger, kusma og røde hunder infeksjonssykdommer. Unntakene er de få vaksinene som består av levende, svekkede agenser, som vaksine mot meslinger, kusma, røde hunder og vannkopper. Hvis disse vaksinene forårsaker sykdom, har «vaksinesykdommen» en inkubasjonstid som andre infeksjoner. «Minimeslinger» eller tilsvarende røde hunder og kusma, forekommer etter en inkubasjonstid på 5 12 dager. Vaksineinfeksjonene er imidlertid alltid mindre alvorlige enn infeksjoner med «vilt» virus av meslinger, kusma og røde hunder vil være. Vaksinereaksjoner som er nevnt her, er aldri farlige i seg selv. Derimot kan det være farlig å oppfatte vaksine som årsak til en febersykdom og derfor unnlate å gjøre de undersøkelser og vurderinger man ellers ville gjort. Det kan få dramatiske følger hvis en meningitt blir oversett i tidlig fase, fordi personen fikk vaksine en dag eller to tidligere. Sjeldne vaksinereaksjoner Reaksjoner som i vaksinesammenheng kalles sjeldne, opptrer hos mindre enn én av vaksinerte. Så sjeldne reaksjoner kan være vanskelige å avsløre før vaksinen tas i vanlig bruk, selv om de kliniske utprøvingene omfatter svært mange personer gjerne langt flere enn I dag er man klar over denne risikoen. Legemiddelmyndighetene vil derfor vanligvis kreve meget detaljert overvåking av mulige reaksjoner i den første tiden etter at vaksiner er tatt i bruk. En slik overvåking førte til at man ble klar over en mulig sammenheng mellom vaksine mot rotavirus og invaginasjon (7) (ramme 1). Vaksinen ble trukket fra markedet så fort det forelå data for at årsakssammenheng var sannsynlig. Ytterligere undersøkelser kan tyde på at vaksinen var årsak til mange tilfeller av tarminfeksjoner, og at invaginasjon nærmest var «toppen av isfjellet» (8). Situasjonen er vanskeligere når det dukker opp mistanke om at en vaksine som er brukt i mange år, er årsak til alvorlige hendelser som hittil ikke er erkjent. Mistanken kan oppstå på forskjellige måter hos forskere, publikum eller leger. Utgangspunktet for mistanken er gjerne enkeltepisoder der det er tidsmessig sammenheng med vaksineringen. Ofte dreier det seg om en tilstand som opptrer spontant i den aktuelle aldersgruppen, men der pårørende eller andre lurer på hvorfor akkurat dette barnet ble rammet (tab 2). I dag oppstår slike mistanker ved registre som tar imot meldinger om vaksinereaksjoner. Det amerikanske vaksinereaksjonsregistret (Vaccine Adverse Event Registration System; VAERS) har vist seg særlig nyttig i denne sammenhengen. Systemet tar imot meldinger fra pasienter, helsepersonell og apotek og stiller ikke store krav til dokumentasjon (9). Hensikten er å gjøre systemet så lett tilgjengelig at det oppfanger eventuelle signaler, ikke å påvise årsakssammenheng eller samle informasjon om alle hendelser. Slike signaler må følges opp, raskt og grun Tidsskr Nor Lægeforen nr. 19, 2006; 126
13 MEDISIN OG VITENSKAP dig. Det første skritt vil ofte være en pasientkontroll-undersøkelse, der man finner ut om personer med den aktuelle tilstanden i større grad har fått vaksine enn en tilfeldig valgt kontrollgruppe. Oftest begrenses studien til en bestemt tidsperiode etter vaksinering, avhengig av hva man ser som mulig mekanisme for utløsning av reaksjonen. Mange mistanker kan avkreftes på denne måten (10). Hvis en begrenset pasient-kontroll-undersøkelse styrker hypotesen om en årsakssammenheng, kan det være nødvendig med større epidemiologiske undersøkelser med forskjellig metodikk for å nå frem til et sikkert svar. Men en tilstrekkelig stor undersøkelse kan i seg selv si noe om forekomsten av problemet, slik man gjennom en intervjuundersøkelse fastslo forekomsten av Guillain-Barrés syndrom etter influensavaksinering til ca. én på 1 million vaksinerte (11). Vaksinene i barnevaksinasjonsprogrammet gis i en alder der alvorlig tilstander debuterer eller oppdages (krampetilstander, krybbedød, autisme m.m.). Det kan ikke unngås at sykdomsdebut i en del tilfeller faller sammen med vaksineringen i tid. Da er grundig klinisk undersøkelse viktig. Vaksinereaksjoner gir imidlertid svært sjelden spesifikke funn. Det eneste unntaket vil være hendelser som skyldes infeksjon med levende agens fra vaksinen, der spesifikke mikrobiologiske undersøkelser kan vise at det dreier seg om infeksjon med vaksinevirus eller BCG-bakterier, ikke infeksjon med naturlige bakterier eller virus. Det gjør det vanskelig å avgjøre om vaksinen er (medvirkende) årsak til sykdommen i det enkelte tilfellet. Mistenkte vaksinereaksjoner bør derfor utredes på bakgrunn av symptomene som om pasienten ikke var blitt vaksinert, så andre mulige årsaker og behandlingsmuligheter ikke blir oversett. Mangelen på spesifikke funn gjør at sammenstilling av tilgjengelig viten er nødvendig for å skille mellom tilfeldig sammenfall i tid og årsakssammenheng (ramme 2) (12, 13). I enkelte situasjoner får en hypotesen om sammenheng mellom vaksine og alvorlig sykdom fotfeste hos publikum så fort mistanken er reist. Mistanken kan da være vanskelig å tilbakevise, selv om store og godt gjennomførte undersøkelser taler sterkt imot årsakssammenheng. Det er aldri mulig å vise med 100 % sikkerhet at noe ikke henger sammen. Mistanken om at MMR-vaksine kunne føre til autisme er et eksempel på dette (ramme 3) (14 17). Mistanken har ført til vaksinasjonsmotstand og lav vaksinasjonsdekning gjennom flere år, særlig i engelsktalende land, og er en medvirkende årsak til at det nå stadig er utbrudd av meslinger i forskjellige europeiske land (18, 19). Behov for registrering og åpenhet Blant alle som arbeider med vaksiner er det i dag enighet om at registrering av vaksinereaksjoner og åpenhet om det man finner er viktig. Her samarbeider vaksineprodusenter, legemiddelmyndigheter og de som har ansvar for sykdomsforebygging og vaksinasjonsprogrammer. Nye vaksiner får av og til markedsføringstillatelse på betingelse av at bruken de første årene blir fulgt opp med spesiell overvåking av vaksinereaksjoner, enten i form av kliniske utprøvninger (fase 4) eller som overvåkingsprogram. Vaksineprodusentene er pådrivere og hjelper til å sette opp overvåkingsprogram i samarbeid med den myndighet som har ansvaret for registrering av vaksinereaksjoner. Dette er nødvendig for å opprettholde vaksinenes troverdighet og dermed den forebyggingsmuligheten vaksinene innebærer. Overvåking i Norge Alvorlige reaksjoner knyttet til programvaksiner har vært meldingspliktig til System for vaksinasjonskontroll (SYSVAK) siden 2003 (før dette til Meldesystem for infeksjonssykdommer). Årlig meldes ca. 350 reaksjoner i Norge. For å gjøre systemet best mulig i stand til å fange opp signaler, har Helse- og omsorgsdepartementet bestemt at også mistanke om vaksinereaksjoner skal meldes (20). Meldingsplikten er lagt til helsepersonell (leger og helsesøstre). Systemet registrerer ikke meldinger fra privatpersoner. Hvis privatpersoner henvender seg til SYSVAK og forteller om mulige vaksinereaksjoner, blir de oppfordret til å ta det opp med helsestasjon eller lege og be om at hendelsen blir meldt. Hvis hendelsen har ført til konsultasjon hos lege eller sykehusinnleggelse, har Folkehelseinstituttet, som ansvarlig for SY- SVAK, tillatelse etter forskriften til å innhente tilleggsopplysninger slik at informasjonen om hendelsen blir så fullstendig som mulig. Alvorlige og uventede vaksinereaksjoner er også meldingspliktige til Legemiddelverket, på samme måte som alle andre legemiddelreaksjoner. Et dobbelt meldingssystem kan imidlertid være uheldig og føre til at begge systemene blir mindre fullstendige enn ønskelig. Legemiddelverket og Folkehelseinstituttet har derfor utviklet samarbeidsrutiner som skal sikre utveksling av meldinger etter nærmere regler. Veien fremover Oppfatningen om et «risikofritt samfunn» har i noen grad fått fotfeste i vår del av verden. I det ligger det at egentlig bør det aldri skje noe galt for noen av oss. Hvis personer rammes av alvorlige sykdommer eller hendelser, skyldes det at noen har gjort noe de ikke burde. I denne tankegangen kommer vaksiner, som et valgt tiltak, lett i søkelyset. Samtidig er fortsatt stor oppslutning om vaksinasjonsprogrammet en forutsetning for å beholde gevinstene ved allmenn vaksinasjon. Derfor er kravene til sikkerhetsdokumentasjon før vaksiner tas i bruk i dag sannsynligvis så strenge som de kan være, hvis det i det hele tatt skal være mulig å få tatt i bruk nye vaksiner. Ramme 2 Institute of Medicine (IOM) i USA har gjort en viktig jobb med å gå gjennom foreliggende litteratur på vaksinefeltet og gi klare vurderinger av hva foreliggende kunnskap sier om årsakssammenheng (12, 13). Her konkluderes det bl.a. med at det ikke er holdepunkter for årsakssammenheng mellom helcelle kikhostevaksine og krybbedød eller afebrile kramper. The Brighton Collaboration består av en gruppe fagpersoner på vaksinefeltet som har påtatt seg oppgaven med å utvikle kasusdefinisjoner og vurdere årsakssammenheng for en rekke tilstander som opptrer etter vaksinering. Stoffet finnes på deres hjemmeside Ramme 3 En beskrivelse av 12 barn med symptomkomplekset inflammatorisk tarmsykdom og autisme reiste en hypotese om at bildet kunne være forårsaket av MMR-vaksine (14). På bakgrunn av hypotesen ble det startet en rekke store, epidemiologisk undersøkelser (15, 16). Ingen av disse studiene bekreftet mistanken om årsakssammenheng. Særlig viktig var en dansk undersøkelse, der man på grunnlag av registerdata kunne vise at det ikke var høyere forekomst av autisme hos vaksinerte enn hos uvaksinerte (16). Hypotesen fikk imidlertid stor publisitet, særlig i engelsktalende land, men også i Norge (17). Publisiteten førte til betydelig usikkerhet rundt MMR-vaksinen, fallende vaksinasjonsdekning i mange land og utbrudd av meslinger med komplikasjoner og dødsfall (18, 19). Det tok mer enn fem år før situasjonen roet seg så mye at vaksinasjonsdekningen igjen nærmet seg utgangsnivået Som helsepersonell kan vi bidra ved å være åpne, fortelle om hva som blir gjort og hva vi vet, både av positiv og negativ art. Alt helsepersonell må gjøre det som er mulig for å unngå mistanker om en «skjult agenda» eller ønsker om å holde informasjon borte fra publikum. Det krever kunnskap om hva vaksiner består av og hvilke hendelser de kan eller ikke kan utløse. Det krever ikke minst tid, innlevelse og vilje til å ta foreldrenes bekymringer på alvor ved å diskutere deres problemer og oppfatninger på en åpen måte. Tidsskr Nor Lægeforen nr. 19, 2006;
14 Oppgitte interessekonflikter: Hanne Nøkleby har ingen oppgitte interessekonflikter. Marianne A. Riise Bergsaker har deltatt i en helseøkonomisk evaluering av pneumokokkvaksine, initiert av Wyeth Lederle, og på et rådgivningsmøte arrangert av samme firma. Litteratur 1. Gaustad V. Koppevaksinasjon. Tidsskr Nor Lægeforen 1971; 91: Lahelle O. Virusvaksiner (rundebordskonferanse). Tidsskr Nor Lægeforen 1971; 91: Ball LK, Evans G, Bostrom A. Risky business: challenges in vaccine risk communication. Pediatrics 1888; 101: Carlsson RM, Claesson BA, Kayhty H et al. Studies on a Hib-tetanus toxoid conjugate vaccine: effects of co-administered tetanus toxoid vaccine, of administration route and of combined administration with an inactivated polio vaccine. Vaccine 1999; 18: Peltola H, Heinonen OP. Frequency of true adverse reactions to measles-mumps-rubella vaccine. Lancet 1986; 1: Virtanen M, Peltola H, Paunio M et al. Day-to-day reactogenicity and the healthy vaccinee effect of measles-mumps-rubella vaccination. Pediatrics 2000; 106: E Murphy TV, Garguillo GM, Massoudi MS et al. Intussusception among infants given an oral rotavirus vaccine. N Engl J Med 2001; 344: Haber P, Chen RT, Zanardi LR et al. An analysis of rotavirus vaccine reports to the Vaccine Adverse Event Reporting System: more than intussusception alone? Pediatrics 2004; 113: Singleton JA, Lloyd JC, Mootrey GT et al. An overview of the vaccine adverse event reporting system (VAERS) as a surveillance system. VAERS Working Group. Vaccine 1999; 17: Ascherio A, Zhang SM, Hernán MA et al. Hepatits B vaccination and the risk of multiple sclerosis. N Engl J Med 2001; 344: Lasky T, Terracciano GJ, Magder R et al. The Guillain-Barre syndrome and the and Influenza vaccines. N Engl J Med 1998; 339: Howson CP, Howe CJ, Fineberg HV, red. Adverse effects of pertussis and rubella vaccines. Institute of Medicine. Washington, D.C.: National Academy Press, Stratton KR, Howe CJ, Johnston RB, red. Adverse effects associated with childhood vaccines. Evidence bearing on causality. Institute of Medicine. Washington, D.C.: National Academy Press, Wakefield AJ, Murch SH, Anthony A et al. Ileallymphodi-nodular hyperplasia, non-specific colitis, and pervasive developmental disorder in children. Lancet 1998; 351: Tilbaketrukket Lancet 1998; 351: Taylor B, Miller E, Farrington CP et al. Autism and measles, mumps and rubella vaccine: no epidemiological evidence for a causal association. Lancet 1999; 353: Madsen KM, Hviid A, Vestergaard M et al. A population-based study of measles, mumps, and rubella vaccination and autism. N Engl J Med 2002; 347: Nøkleby H. Vaksinasjon, inflammatorisk tarmsykdom og autisme er det noen sammenheng? Tidsskr Nor Lægeforen 2001; 121: McBrien J, Murphy J, Gill D et al. Measles outbreak in Dublin, Pediatr Infect Dis J 2003; 22: Ianazzio S, Ciofi M, Huberty-Krau P et al. Measles Surveillance annual report ( ). 20. Om SYSVAK-register-forskriften. Forskrift av 20. juni 2003 nr Rundskriv I-12/2003. Oslo: Helsedepartementet, Manus ble mottatt og godkjent Medisinsk redaktør Petter Gjersvik Tidsskr Nor Lægeforen nr. 19, 2006; 126
15 Medisin og vitenskap tema Vaksinasjon Vaksinering er det verdt pengene? Sammendrag Moderne vaksiner kan være meget kostbare, og samfunnet må vurdere vaksinasjon i forhold til annen forebygging og behandling. Økonomisk evaluering innebærer å kvantifisere kostnader og effekter av helsetiltak for å gi bedre grunnlag for prioriteringer. Hovedutfordringen er å få valide mål på helseeffektene, herunder bivirkninger og konsekvenser av flokkimmunitet og serotypeskifte. I denne artikkelen omtales metoder og metodevansker ved økonomisk evaluering av vaksinasjonsprogrammer, med vaksinasjon mot kikhoste og pneumokokksykdom som eksempler. Engelsk sammendrag finnes i artikkelen på Oppgitte interessekonflikter: Se til slutt i artikkelen Torbjørn Wisløff [email protected] Nasjonalt kunnskapssenter for helsetjenesten Postboks 7004 St. Olavs plass 0130 Oslo Tore G. Abrahamsen Rikshospitalet-Radiumhospitalet og Universitetet i Oslo Marianne A. Riise Bergsaker Øistein Løvoll Nasjonalt folkehelseinstitutt Ivar Sønbø Kristiansen Institutt for helseledelse og helseøkonomi Universitetet i Oslo og Institut for Sundhedstjenesteforskning Syddansk Universitet Odense Hensikten med denne artikkelen er å peke på de spesielle utfordringer som reiser seg i forbindelse med evaluering av vaksinasjonsprogrammer. I artikkelen vil vi først beskrive hovedprinsippene i økonomisk evaluering, vise to eksempler der metoden er blitt anvendt på vaksiner og deretter drøfte noen av de metodeproblemer man står overfor i økonomisk evaluering av vaksiner. Et gjennomgående element vil være en norsk økonomisk evaluering av pneumokokkvaksine (1). Økonomisk evaluering Det sentrale ved økonomisk evaluering er å kvantifisere kostnader og helseeffekter ved ulike behandlinger. Metodene har vært omtalt i Tidsskriftet tidligere (2 7). Vi vil her konsentrere oss om det som er spesifikt for vaksinasjonsprogrammer og drøfte enkelte sentrale begreper. En økonomisk evaluering er oftest relevant bare for ett enkelt land eller én enkelt problemstilling. I praksis er det umulig å gjøre en ny klinisk effektstudie for hver ny økonomisk analyse. Man er derfor henvist til å analysere kostnader og effekter ved å simulere ulike behandlinger. Dette gjøres i en modell der man henter data om kostnader og effekter fra ulike kilder. Man utvikler typisk et beslutningstre der hver gren i treet representerer mulige beslutninger (f.eks. nytt behandlingsopplegg og tidligere behandlingsopplegg). Etter hver beslutning beskrives det kliniske hendelsesforløpet hos dem intervensjonene gjelder for (e-fig 1). Ved sykdommer som følges over lengre tid, vil et beslutningstre bli uoversiktlig pga. de mange grenene. I slike tilfeller benytter man heller en såkalt Markov-modell (8). Dette er i prinsippet en modell hvor pasienter over tid beveger seg mellom forskjellige medisinske tilstander. Det spesielle med en Markov-modell er at den ikke har minne, hvilket betyr at sannsynligheten for å bevege seg til en ny tilstand er uavhengig av det som har skjedd tidligere. Figur 2 viser prinsippet for en Markov-modell som simulerer forløpet av pneumokokksykdom i en populasjon. Alle individer i populasjonen er på ethvert tidspunkt i én av flere helsetilstander som er gjensidig utelukkende. Hver helsetilstand er representert ved en rombe. Alle individer starter i tilstanden «frisk», hvilket i denne forbindelse betyr at man ikke har eller har hatt pneumokokksykdom. Individene følges år for år til alle er døde 100 år senere. Til hvert leveår knyttes kostnader. Hvert eneste år er individene utsatt for risiko for pneumokokksykdom og dessuten for alminnelig dødelighet. Ved å følge dem med og dem uten vaksine kan man tallfeste merkostnader og unngått pneumokokksykdom. Valg av analysemetode, perspektiv, nåverdiberegning, effektmål og kostnadsberegning kan ha stor innflytelse på resultatet av økonomiske analyser. Det er derfor nødvendig at man for hver usikker variabel både velger en punktverdi (base-case value) og innhenter et estimat for usikkerheten i punktverdien. Det er standard for økonomiske evalueringer å utføre enveis sensitivitetsanalyser for alle usikre variabler i modellen ved å variere hver enkelt opp og ned innenfor nevnte grenser. I tillegg er det de seneste årene også blitt vanlig å gjøre såkalte probabilistiske sensitivitetsanalyser med Monte Carlo-simuleringer (9). Dette vil si at man tilegner en sannsynlighetsfordeling til de angitte variablene basert på anslag på punktestimater og grenser for variasjon. Man trekker så ett tilfeldig tall fra angitt sannsynlighetsfordeling for hver variabel og regner ut kostnader og effekter for de alternativene man sammenlikner. Denne operasjonen utføres typisk ganger for å finne frem til et anslag for hvilke verdier kostnader og effekter kan variere innenfor. Diskontering kan være et vanskelig begrep, og vi har derfor forsøkt å illustrere dette med eksempler (e-ramme 1, e-ramme 2, e-fig 3) (10, 11). To eksempler på økonomisk evaluering finnes i ramme 3 (12) og ramme 4 (e-fig 4) (13). Tabell 1 og tabell 2 illustrerer helsegevinster og kostnader per vunnet leveår fra eksemplet i ramme 4. Betydningen av gode kliniske data Kvaliteten på en økonomisk evaluering er helt avhengig av gode grunnlagsdata om blant annet forekomst av den aktuelle infeksjonen, smittsomhet og forholdet mellom bærerskap og sykdom, sykdomsvarighet og forekomst av sekveler og død. I Europa har! Hovedbudskap Økonomisk evaluering av vaksiner krever kvantifisering av helseeffekter og kostnader i simuleringsmodeller Store og langvarige randomiserte studier er nødvendig for å få gode effektestimater Muligheten for serotypeskifte og flokkimmunitet kan ha stor innflytelse på resultatene Diskontering og tidspreferanser har stor innflytelse på resultatene av vaksineevaluering 2670 Tidsskr Nor Lægeforen nr. 20, 2006; 126:
16 MEDISIN OG VITENSKAP det vært vanlig å utføre nasjonale evalueringer av nye vaksiner. I de fleste landene er det relativt homogene populasjoner og egne tradisjoner for diagnose og behandling. Ikke minst er de infeksjonsfremkallende mikrobenes epidemiologi rimelig begrenset når det gjelder forekomst av subgrupper, virulens og antibiotikafølsomhet. Generelt sett synes det som om oppfølgingsdata, slik som forekomst av sekveler, er vanskelig å få frem selv i såkalt utviklede land i Vest-Europa og Nord-Amerika. Norge burde være et foregangsland når det gjelder epidemiologiske data som bakgrunn for innføring av vaksiner. Vi har et godt utbygd og oversiktlig helsevesen med gode muligheter for infeksjonsregistrering. Meldingssystem for smittsomme sykdommer (MSIS) har ført oss et stykke på vei, men det er et vell av infeksjonsdata som ikke registreres der. Ved evalueringen av den sjuvalente pneumokokkvaksinen (1) manglet det nasjonale data over forekomst av pneumonier og otitter og over fordeling på etiologiske agenser. I stedet ble det brukt henholdsvis sykehusdata og resultater fra en dansk epidemiologisk undersøkelse (14). Enda mer problematisk var forekomst av senfølger av systemiske pneumokokkinfeksjoner, der det verken fantes nasjonale eller internasjonale data. Løsningen ble å få anslag fra et panel av nasjonale eksperter på området. Betydningen av serotypeskifte En forutsetning for at en vaksine skal ha beskyttende effekt mot en sykdom, er at de antistoffer og B- og T-celler som dannes, er rettet mot den mikroben som forårsaker sykdom. For enkelte sykdommer kan det være flere ulike varianter av mikroben, f.eks. ulike influensavirusstammer eller ulike serotyper av pneumokokker. De ulike variantene av mikroben kan være så forskjellige at vaksine rettet mot én variant ikke gir beskyttelse mot en annen. Dersom en vaksine bare er effektiv mot en viss andel av de ulike serotypene av f.eks. pneumokokker, kunne man vente at serotyper som ikke dekkes av vaksinen, blir mer vanlige (serotypeskifte). Dette ville gjøre vaksinen mindre klinisk effektiv. Etter innføringen av vaksine mot Haemophilus influenzae type b (Hib) i det norske barnevaksinasjonsprogrammet kom det et sterkt fall i antall meldte tilfeller av invasiv Haemophilus influenzae-infeksjon. I ettertid har det ikke kommet en økning av infeksjoner forårsaket av andre typer Haemophilus influenzae, og et serotypeskifte synes ikke å ha skjedd. Etter innføringen av pneumokokkonjugatvaksine i det amerikanske barnevaksinasjonsprogrammet er det observert et sterkt fall i antall rapporterte tilfeller av invasiv pneumokokksykdom innenfor de serotyper som inngår i vaksinen. Imidlertid har man observert en viss økning i tilfeller av pneumokokksykdom forårsaket av andre serotyper (15, 16). Noen studier kan imidlertid tyde på at serotypeskiftet var i gang allerede før vaksinen ble innført. Det er vanskelig å kvantifisere betydningen av serotypeskifte fordi endringer i sykdomsforekomst kan ha mange andre årsaker enn vaksinering. Serotypeskifte kan imidlertid ha en markert negativ effekt på vaksiners effekt og dermed deres kostnadseffektivitet. Flokkimmunitet Etter innføring av vaksinasjon mot en smittsom sykdom i en befolkning har man sett at fallet i forekomsten av sykdommen i befolkningen er større enn vaksinasjonsdekningen skulle tilsi. Forklaringen synes å være at sykdommen sprer seg dårligere i en befolkning jo flere som er immune. Dette fenomenet kalles flokkimmunitet (herd immunity), og det er til stede enten immuniteten skyldes gjennomgått sykdom eller vaksinasjon. Før innføring av vaksinasjon forløp sykdommer som meslinger og kikhoste i epidemier med få års mellomrom. De aller fleste barna fikk sykdommene som små, og etter en epidemi måtte man ha en viss tilvekst av nye mottakelige barn for at en ny epidemi skulle kunne bre seg. Sykdommens evne til å spre seg i en befolkning kan uttrykkes i det såkalte basale reproduksjonsantallet, R 0. R 0 er det gjennomsnittlige antallet nye sykdomstilfeller Ramme 3 Kikhostevaksine I en svensk artikkel vurderte forfatterne hvorvidt det var kostnadseffektivt å gjeninnføre kikhostevaksinasjon i det svenske barnevaksinasjonsprogrammet (12). Denne modellanalysen hadde effektestimater fra én svensk studie. I tillegg bygde modellen på diverse epidemiologiske og demografiske data. Modellen baserte seg på at effekten av vaksinen varer i fem år. Hovedresultatene i analysen var at antall tilfeller av kikhoste i Sverige ville gå ned fra til over en seksårsperiode. Man forventet at dette samtidig skulle føre til 147 millioner svenske kroner i «forbedret samfunnsøkonomisk resultat». Fordi analysen ga positive resultater for både helsegevinster og kostnader, sier vi at vaksinasjonen representer en dominant strategi. Dersom analyseresultatet er korrekt, er det ingen tvil om at kikhostevaksinering bør innføres. som hver syk person smitter i sin smittsomme periode i en stor populasjon av smittemottakelige individer. R 0 bestemmes av smittsomheten, kontakthyppigheten og smittevarigheten. Den vil variere fra sykdom Figur 2 Markov-modell som beskriver forløpet for en fødselskohort med tanke på pneumokokksykdom Tidsskr Nor Lægeforen nr. 20, 2006;
17 Ramme 4 Pneumokokkvaksine I analysen ble kostnader og helseeffekter ved å innføre pneumokokkvaksinering av alle norske spedbarn beregnet. Vi sammenliknet her livstidsforløpet for en vaksinert fødselskohort ( fødte) med en tilsvarende kohort uten vaksinering (1). Simuleringsmodellen fanget opp effekter på forekomst av pneumoni, invasiv pneumokokksykdom, otitt og sekvele etter disse sykdommene. Effektestimatene ble hentet fra studier i Finland (otitt) og USA (pneumoni og invasiv pneumokokksykdom). Estimatene fra USA ble justert med tanke på norsk serotypefordeling. Data for forekomst av invasiv pneumokokksykdom ble hentet fra MSIS, mens forekomst av pneumonier og otitter ble basert på henholdsvis sykehusdata og resultater fra en dansk epidemiologisk undersøkelse. Livskvalitet ved sekveler ble verdsatt med tall fra en amerikansk database (13). Modellen fanget også opp muligheten for at vaksinering av barn reduserer forekomsten av invasiv pneumokokksykdom hos voksne (flokkimmunitet). Modellanalysen viste at vaksinasjon av én fødselskohort gir 69 vunne leveår eller 142 kvalitetsjuserte leveår (diskontert 4 %: henholdsvis 23,5 år og 52,1 år) (tab 1). Dersom man også inkluderte flokkimmunitet, ble den samlede leveårsgevinst 101 leveår (udiskontert) Vaksinasjon av spedbarn koster ca. 100 millioner kroner (med fire doser per barn). De samlede livstidskostnader for pneumokokkrelatert sykdom var i gjennomsnitt kroner per barn uten vaksine og kroner med vaksine (indirekte kostnader ikke inkludert). Tabell 2 viser merkostnad per vunnet (kvalitetsjustert) leveår ved å innføre spedbarnsvaksinering (både kostnader og helseeffekter diskontert). Kostnad-effekt-forholdet er mer gunstig om man trekker inn indirekte kostnader, dvs. at vaksinasjon reduserer produksjonsbortfallet ved pneumokokkrelatert sykdom og død. Dette forholdet blir også mer gunstig om man kvalitetsjusterer leveårene, fordi vaksinering forebygger otitter og alvorlige sekvele. Vaksinasjon er også mer kostnadseffektiv dersom man antar at tre vaksinedoser gir samme beskyttelse som fire. Ved probabilistisk sensitivitetsanalyse var det mindre enn 1 % sannsynlighet for at vaksinering er kostnadseffektivt under forutsetning av fire doser vaksine og at man ser bort fra indirekte kostnader og flokkimmunitet (e-fig 4). til sykdom og også noe fra befolkning til befolkning. Eksempelvis er R 0 ca. 15 for meslinger, men bare 2 3 for influensa. For at en sykdom skal kunne bre seg og øke i forekomst, må R 0 være større enn 1. Dersom R 0 er mindre enn 1, vil spredningen begrenses og sykdommen dø ut. Dersom R 0 er lik 1, har vi en endemisk situasjon. Man kan ut fra R 0 beregne hvilken vaksinasjonsdekning, eller rettere sagt hvilken grad av immunitet, man må ha i befolkningen for at man skal kunne få kontroll med en sykdom, den såkalte flokkimmunitetsterskel (herd immunity threshold). Denne er definert som 1 1/R 0. Jo høyere R 0 for en sykdom er, desto høyere flokkimmunitetsterskel eller vaksinasjonsdekning må man ha for å få kontroll. I denne beregningen må man også ta med vaksinenes effektivitet, som aldri vil være 100 %. For å oppnå kontroll med meslinger i en befolkning må man ha et flokkimmunitetsnivå på over 90 %. Når man gjør økonomisk evaluering av vaksiner, vil flokkimmuniteten kunne komme inn som en ekstra bonus med stor betydning for vaksinens kostnadseffektivitet. Innføringen av sjuvalent konjugert pneumokokkvaksine hos spedbarn i USA har, foruten betydelig fall i forekomst i de vaksinerte gruppene, ført til et fall i forekomsten av invasiv pneumokokksykdom hos grupper av voksne. Effekten har vært størst i aldersgrupper som kan passe med foreldre- og besteforeldregenerasjonen. Vi vet at for denne sykdommen er det et stort antall friske bærere, særlig gjelder det små barn. Mindre sykdom og færre bærere blant barn gir mindre smittepress mot voksne. Den norske analysen av pneumokokkvaksine viste at flokkimmunitet hadde avgjørende betydning for om vaksinen kan betraktes som kostnadseffektiv (1). Diskusjon Pasientrettighetsloven slår fast at «retten (til helsehjelp) gjelder bare dersom pasienten kan ha forventet nytte av helsehjelpen, og kostnadene står i rimelig forhold til tiltakets effekt». Den siste bisetningen betyr i praksis at samfunnet har behov for å kvantifisere kostnader og nytte av helsetiltak. Foreløpig er det bare for blåreseptordningen at dette prinsippet er satt i system. Når man tar i betraktning at vaksinering av et årskull for én sykdom kan koste 100 millioner kroner, er det naturlig at økonomisk evaluering også benyttes for vaksiner og annen behandling for den saks skyld. To spørsmål blir påtrengende når samfunnet bruker økonomisk evaluering for prioritering i helsepolitikken. For det første: Hva er helsevesenets målsetting? Her finner man for det meste uforpliktende og upresise formuleringer i offentlige dokumenter. Politiske diskusjoner om for eksempel nedlegging av sykehus bærer bud om at målsettingen er meget mer enn å maksimere befolkningens helse. Fordi økonomiske analyser av helsetiltak måler kostnadene ved å øke livskvalitet og livslengde, er de til lite eller ingen nytte dersom beslutningstakere skulle ha andre mål med helsevesenet. For det andre: Hvor mye skal samfunnet være villig til å betale for helseforbedringer? Dersom samfunnet ikke vil eller tør sette en grense her, vil økonomisk evaluering i praksis få liten praktisk betydning. I Norge er det foreslått at samfunnet i utgangspunktet ikke skal være villig til å betale mer enn kroner eller kroner for et (godt) leveår (11, 17). Det gjenstår å se hva norske helsemyndigheter mener om dette kjernespørsmålet. Da regjeringen høsten 2005 foreslo å innføre pneumokokkvaksinering av spedbarn, kunne det virke som om medieoppmerksomhet snarere enn økonomisk evaluering var utslagsgivende. Etter vår oppfatning ville det være ønskelig at økonomisk evaluering fungerer som premissleverandør for helsepolitikken snarere enn som unnskyldning for beslutninger som i realiteten har en annen begrunnelse. Verdien av metoden må likevel vurderes i lys av den usikkerheten de økonomiske analyser er basert på (7). Med moderne dataprogrammer er det forholdsvis enkelt å utvikle analyser som er svært kompliserte. Resultatene blir likevel ikke mer pålitelige enn forutsetningene de hviler på. Økonomiske evalueringer av vaksiner innebærer samme typer usikkerhet som evaluering av andre helsetiltak. I de fleste tilfeller er usikkerhet med henblikk på helseeffekt det viktigste enkeltbidrag til den samlede usikkerhet. Store, langvarige randomiserte studier med måling av både effekt og eventuelle bivirkninger står sentralt. Den norske evalueringen av pneumokokkvaksine (1) var i hovedsak bygd på tre kliniske studier av relativt kort varighet. Det er sterkt ønskelig at kliniske studier er bedre enn det som her var tilfellet. Ansvaret ligger hos så vel produsenter som myndigheter. Myndighetene bør stille strengere krav til klinisk dokumentasjon og i sterkere grad enn hittil selv finansiere studier for å sikre uavhengighet og relevans. Her spiller publikums legitime krav på dokumentasjon av bivirkninger en viktig rolle. Verdien av å unngå symptomer og plager står sentralt i økonomisk evaluering. Kvalitetsjustering av leveår har hittil vært den mest anvendbare metoden, men måling av livskvalitet er en vanskelig og omstridt aktivitet (3). I likhet med det som er tilfellet i andre land mangler vi i Norge gode data om ressursforbruk i medisinsk behandling. Ofte er man henvist til å benytte ekspertanslag i kostnadsanalysen, men heldigvis betyr ikke dette så mye for den samlede usikkerhet i analysen. Flokkimmunitet og serotypeskifte representerer spesielle utfordringer i økonomisk evaluering av vaksinasjonsprogrammer. Disse fenomenene kan ha betydelig innflytelse på resultatene når man evaluerer vaksiner og 2672 Tidsskr Nor Lægeforen nr. 20, 2006; 126
18 MEDISIN OG VITENSKAP Tabell 1 Helsegevinster (udiskonterte) ved å vaksinere en norsk fødselskohort (n = ) Uten flokkimmunitet Med flokkimmunitet Unngåtte hjernehinnebetennelser blant vaksinerte barn 7,2 7,2 Unngåtte blodforgiftninger blant vaksinerte barn 5,2 5,2 Unngåtte lungebetennelser blant vaksinerte barn 49,7 49,7 Unngåtte mellomørebetennelser blant vaksinerte barn 3 063, ,1 Unngåtte dødsfall blant vaksinerte barn 0,8 0,8 Unngåtte hjernehinnebetennelser blant voksne 0 10,4 Unngåtte blodforgiftninger blant voksne 0 24,3 Vunne leveår Vunne kvalitetsjusterte leveår (QALY) Tabell 2 Kostnad (i norske kroner) per (kvalitetsjustert) leveår avhengig av forutsetninger om flokkimmunitet, indirekte kostnader og hvorvidt tre eller fire doser vil være like effektivt. Både kostnader og helseeffekter er diskontert 4 % per år Kostnad per vunnet leveår (kr) Kostnad per QALY 1 (kr) Indirekte kostnader Flokkimmunitet Fire doser Tre doser Fire doser Tre doser Ikke inkludert Ikke inkludert Ikke inkludert Inkludert Inkludert Ikke inkludert Kostnadsbesparende Inkludert Inkludert Kostnadsbesparende 1 Kvalitetsjustert leveår (quality adjusted life years) Kostnadsbesparende Kostnadsbesparende andre tiltak mot infeksjonssykdommer (18). For å fange opp disse fenomenene bør man fortrinnsvis benytte dynamiske simuleringsmodeller, som er mer kompliserte enn de statiske modellene som er omtalt foran. Når langtidseffektene av flokkimmunitet bygges inn i dynamiske modeller, blir de samlede helseeffekter større enn i statiske modeller og behandlingen i virkeligheten mer kostnadseffektiv enn de statiske modeller skulle tilsi (19). Økonomisk evaluering av vaksiner er preget av usikkerhet. Betyr dette at det er mer usikkerhet i økonomisk evaluering enn i de kliniske vurderinger? Svaret er nei. Hvis klinikere anfører at de har god dokumentasjon for en vaksine, tenker de i praksis på kliniske effekter i et korttidsperspektiv, ikke på kostnadsaspektet. Dersom man skulle velge å treffe beslutninger på dette grunnlaget, har man utelatt potensielt essensielle elementer i beslutningsgrunnlaget. Vi mener at økonomisk evaluering av vaksiner tilfører en ny dimensjon i evalueringen av vaksineprogrammer, både fordi den fanger opp flere av de elementer som bør inngå i beslutningene om vaksinering, og fordi økonomisk evaluering håndterer usikkerhet på en mer systematisk måte enn kliniske vurderinger alene. Dette betyr ikke at en økonomisk evaluering kan eller skal diktere beslutninger. Enten det er helsemyndigheter eller politikere som fatter beslutninger, vil det alltid inngå et viktig element av verdivurderinger. Målsettingen med økonomisk evaluering av vaksiner er ikke å diktere beslutninger, men å sørge for et bedre grunnlag for å fatte de riktige beslutningene. Oppgitte interessekonflikter: Forfatterne bruker pneumokokkvaksine som ett av eksemplene på økonomisk evaluering, og studien ble initiert av Wyeth Lederle. Torbjørn Wisløff mottok honorar for statistiske analyser, og Ivar Sønbø Kristiansen og Torbjørn Wisløff har fått reisestøtte for å presentere studien på internasjonale konferanser. e-fig 1, e-fig 3, e-fig 4, e-ramme 1 og e-ramme 2 finnes i artikkelen på Litteratur 1. Wisløff T, Abrahamsen TG, Bergsaker MA et al. Cost effectiveness of adding 7-valent pneumococcal conjugate (PCV-7) vaccine to the Norwegian childhood vaccination program. Vaccine 2006; 24: Kristiansen IS. Økonomiske analyser av helsetiltak: om kostnad-nytte- og kostnad-effekt-analyser som hjelpemiddel for bedre ressursbruk. Tidsskr Nor Lægeforen 1990; 110: Nord E. Kvalitetsjusterte leveår muligheter, begrensninger, alternativer. Tidsskr Nor Lægeforen 1992; 112: Nord E. Veiledende verditall for kostnad-nytte-analyser av helsetjenester. Tidsskr Nor Lægeforen 1996; 116: Kristiansen IS, Andersen CK. Bør samfunnet prioritere kostbare sykdommer? Tidsskr Nor Lægeforen 2001; 121: Nord E. Helseøkonomi kort innføring i nyttekostnads-analyser. Tidsskr Nor Lægeforen 2002; 122: Kristiansen IS, Stavem K, Linnestad K et al. Evaluering av medisinske metoder kan vi stole på kostnad-effekt-analyser? Tidsskr Nor Lægeforen 2003; 123: Sonnenberg FA, Beck JR. Markov models in medical decision making: a practical guide. Med Decis Making 1993; 13: Ades AE, Claxton K, Sculpher M. Evidence synthesis, parameter correlation and probabilistic sensitivity analysis. Health Econ 2006; 15: Olsen JA. Time preferences for health gains: an empirical investigation. Health Econ 1993; 2: Veileder i samfunnsøkonomiske analyser. Oslo: Finansdepartementet, Nordlund A, Kornfalt R, Lithman T. Vaccination mot kikhosta en hãlsoeconomisk vinst. Läkartidningen 1996; 93: Harvard Centre for Risk Analysis. harvard.edu/cearegistry/ ( ). 14. Stangerup SE, Tos M. Epidemiology of acute suppurative otitis media. Am J Otolaryngol 1986; 7: Black S, Shinefield H, Fireman B et al. Efficacy, safety and immunogenicity of heptavalent pneumococcal conjugate vaccine in children. Northern California Kaiser Permanente Vaccine Study Center Group. Pediatr Infect Dis J 2000; 19: Black SB, Shinefield HR, Hansen J et al. Postlicensure evaluation of the effectiveness of seven valent pneumococcal conjugate vaccine. Pediatr Infect Dis J 2001; 20: Kristiansen IS. Hvor mye bør samfunnet være villig til å betale for helseforbedringer? Verdien av liv og helse. Oslo: Helseøkonomisk forskningsprogram, Universitetet i Oslo, 2003: Brisson M, Edmunds WJ. Economic evaluation of vaccination programs: the impact of herdimmunity. Med Decis Making 2003; 23: Welte R, Postma M, Leidl R et al. Costs and effects of chlamydial screening: dynamic versus static modeling. Sex Transm Dis 2005; 32: Manuskriptet ble mottatt og godkjent Medisinsk redaktør Petter Gjersvik. Tidsskr Nor Lægeforen nr. 20, 2006;
19 Vaksinasjon i et utviklingsperspektiv Sammendrag Vaksinering er et effektivt virkemiddel, men produksjon og distribusjon av vaksiner er en utfordring. Mer enn tre firedeler av alle verdens barn blir vaksinert, men vi må nå flere. Helse generelt og vaksinasjon spesielt spiller en viktig rolle for den økonomiske veksten i fattige land. Vaksinasjon av barn har i de senere år fått en sentral plass i utviklingen av nye samarbeidsformer, strategier og finansiering av helserettet og annen utviklingshjelp. Norge har stått sentralt i dette arbeidet. Mange nye og lovende vaksiner er under utvikling. Forutsatt rettferdig distribusjon vil disse vaksinene bli kjærkomne tilbud til store befolkningsgrupper, også til dem som fortsatt ikke har tilgang til adekvat kurativ medisin. Det er mange utfordringer i arbeidet med å nå marginaliserte befolkningsgrupper, dvs. de som trenger vaksinebeskyttelse aller mest. Oppgitte interessekonflikter: Se til slutt i artikkelen Halvor Sommerfelt [email protected] Senter for internasjonal helse Universitetet i Bergen Armauer Hansens hus 5021 Bergen og Divisjon for smittevern Nasjonalt folkehelseinstitutt Tore Godal Statsministerens kontor Vår egen historie har vist at økonomisk utvikling, mindre fattigdom og en jevnere fordeling av godene bidrar vesentlig til bedret folkehelse. Sengene som vikingtidens og middelalderens folk sov i, var korte ikke fordi de sovende «halvsatt med sverdet i hånd, klare til kamp», men fordi folk flest var kortvokste, et resultat av den onde sirkelen av gjentatte infeksjoner og dårlig ernæring. Man antar at bedret folkehelse i vår del av verden først og fremst var en konsekvens av den sosioøkonomiske utviklingen. Holdningen til helse og utvikling i fattige land i og 70-årene var i stor grad basert på denne historiske forståelsen. Man mente at folkehelsen i utviklingsland mest effektivt kunne bedres ved å bedre de sosioøkonomiske kår blant folk flest. Forskning gjennom de siste 15 år har vist at det også er en effekt den andre veien bedret helse kan bidra vesentlig til økonomisk utvikling (1). Denne forståelsen kulminerte i et viktig dokument i 2001, kalt Report of the Commission on Macroeconomics and Health (2). Det ble bestilt av daværende generaldirektør for Verdens helseorganisasjon (WHO), Gro Harlem Brundtland. I rapporten staket man ut en strategi der spesifikke helseintervensjoner står sentralt i bekjempelsen av fattigdom og i utviklingslandenes økonomiske utvikling. Parallelt med denne rapporten utviklet FN sine tusenårsmål (3), der spesifikke helseintervensjoner, særlig rettet mot mødre- og barnehelse og mot bekjempelse av de store infeksjonssykdommene, sidestilles med andre utviklingstiltak, slik som bedret utdanning og fattigdomsbekjempelse. Det er ikke tilfeldig at disse to prosessene var koblet begge ble ledet av økonomen Jeffrey D. Sachs. Bloom & Canning har påvist sammenhengen mellom redusert barnedødelighet, lavere fertilitet og økonomisk vekst. De innførte begrepet «den demografiske gave» (the demographic gift), en aldersdistribusjon der en større del av befolkningen er i produktiv alder (1). Basert på denne forståelsen er det iverksatt en rekke målrettede tiltak for å bedre barns helsetilstand og gi dem større overlevelsessjanser (4 7). Det fjerde tusenårsmålet sier at dødeligheten blant barn under fem år skal reduseres med to tredeler fra 1990 til 2015, et ambisiøst mål der full dekning med de seks basisvaksinene (BCG, stivkrampe, difteri, kikhoste, polio og meslinger) er en viktig komponent. Etter at dekningen med disse vaksinene falt i løpet av 1990-årene, kom det mot slutten av dette tiåret en ny giv, ikke bare for å øke basisvaksinasjonsdekningen, men også for å introdusere nye vaksiner mot andre viktige infeksjonssykdommer. Man innså raskt at ingen organisasjon alene i vesentlig grad kunne styrke vaksinasjonsprogrammene i den tredje verden og at man trengte en allianse av partnere. The Global Alliance for Vaccines and Immunization (GAVI) ble skapt. I september 1999 donerte Bill Gates 750 millioner dollar for en femårsperiode. Dette sprengte den vanlige oppfatning av utviklingshjelp som et offentlig anliggende. Samarbeid med privat sektor ble nå ansett som grunnleggende. GAVI ble formelt lansert på Verdens økonomiske forum (World Economic Forum) i Davos i januar 2000 og har som målsetting å beskytte barn og voksne i alle verdens land, uavhengig av sosioøkonomisk status, mot vaksineforebyggbare sykdommer (ramme 1). Fem år senere kunne WHO og UNICEF vise til resultatene av GAVIs satsing. Vaksinedekningen med basisvaksiner var på vei oppover igjen (fig 1), over 1,7 millioner liv var reddet, og nesten 100 millioner barn var blitt vaksinert mot hepatitt B. Femårsprosjektet ble forlenget til 15 år, og GAVI blir modell for utprøvning av nye finansieringsmekanismer. Innsatsen vil bli tre ganger så stor. Bill Gates bidrar med nye 750 millioner, og sammen med solide bevilgninger fra vestlige land, først Norge og Nederland, deretter Storbritannia, USA, Frankrike, Sverige og Danmark, blir det gitt muligheter for langsiktig satsing. For første gang blir det gitt bindende tiårsrammer for u-hjelp. GAVI konsentrerte seg om de 75 fattigste landene i verden. For å komme raskt i gang og for å sikre en omfattende tilnærming bestemte man at alle land skulle stå fritt til å sende inn søknader om støtte. Mange var nervøse for at GAVI gapte over for mye for raskt. Ville det ikke være bedre å satse på en håndfull «demonstrasjonsland»? Argumentet om at man gikk for fort frem og at man ikke visste i hvilke land GAVI mest effektivt kunne bidra, vant frem. Siden det dreide seg om nye penger, var det viktig at man satset! Hovedbudskap Vaksinasjon er en effektiv intervensjon, men med komplisert produksjon og distribusjon Helse og vaksinasjon spiller en viktig rolle for økonomisk vekst i fattige land I de senere år er det utviklet nye samarbeidsformer, strategier og finansieringsformer Nye og lovende vaksiner kan, forutsatt rettferdig distribusjon, være et vesentlig bidrag til bedre folkehelse i fattige land 2674 Tidsskr Nor Lægeforen nr. 20, 2006; 126:
20 MEDISIN OG VITENSKAP på noe nytt og ikke subsidierte eller erstattet pågående arbeid. I GAVI bestemte man seg for også å satse på vaksiner som ennå ikke var innført i den fattigste del av verden, nemlig vaksiner mot gulfeber, hepatitt B og Haemophilus influenzae type b (Hib). GAVI kom også til den konklusjon at for å sikre økt vaksinedekning måtte man satse på å støtte helsetjenesten. Men hvordan kunne man gjøre dette på en måte som harmonerte med bred sektorstøtte, som var blitt rådende politikk for utviklingssamarbeid? Ideen om å betale for oppnådde resultater slo rot. Fordi betalingen var basert på innsats, skulle det være opp til landet selv å bestemme hvordan midlene skulle brukes. Dette ville være forenlig med sektorstøtteprinsippet. De tre første årene ble landene gitt forskudd på bagrunn av planer om økt vaksinasjonsdekning. Det var stor optimisme rundt tusenårsskiftet. Brundtlands høyre hånd i WHO, Jonas Gahr Støre, tok initiativ til en massiv innsats mot aids, malaria og tuberkulose, med GAVI som mal. G8 tok opp ideen, og et globalt fond mot aids, malaria og tuberkulose ble skapt. Hittil har man skaffet til veie i overkant av 10 milliarder dollar, og resultatene er i ferd med å komme. Motforestillinger Innovasjon stimulerer til motforestillinger. Kort tid etter at GAVI ble etablert, ble det reist en rekke kritiske spørsmål, som kort kan oppsummeres slik: Er det tilrådelig at filantropiske organisasjoner som Bill and Melinda Gates Foundation (BMGF) og mer eller mindre bindende gaver fra enkelte lands myndigheter blir viktige pilarer når det gjelder vaksinering av verdens barn? Hvor bærekraftig blir et globalt vaksinasjonsprogram som er basert på slike gaver? Risikerer vi at verdens vaksinasjonsprogrammer blir for avhengig av GAVI og bryter sammen når alliansen etter planen skulle opphøre etter fem år? GAVI er heller ikke underlagt demokratisk kontroll, slik som WHO, hvor hvert enkelt land har en stemme. I GAVIs styre på 15 medlemmer er mottakerlandene underrepresentert i forhold til giverorganisasjonene og giverlandene. Vaksineindustrien har to representanter, en fra industrialiserte land og en fra utviklingsland. En annen motforestilling er at en av GAVIs forutsetninger for å støtte introduksjon av nye vaksiner er at søkerlandet kan dokumentere at det har oppnådd minst 50 % dekning med den siste dosen av difteri-stivkrampe-kikhoste-vaksinen. 50 % dekning er lavt, langt under det man oppnådde i de aller fleste land på slutten av 1980-årene. Det er også fremholdt at GAVI i de første årene brukte omtrent to tredeler av sine midler på introduksjon av hepatitt B-vaksinen og den vesentlig dyrere Hib-vaksinen, mens bare en tredel gikk til å styrke helsesektortiltak, primært for å øke dekningsgraden av basisvaksinene. Dette står i kontrast til målsettingen om at 80 % av landene med GAVIstøtte innen rimelig tid skulle oppnå 80 % dekning med basisvaksinene i samtlige distrikter. Argumentet var at vaksinasjon med «dollarvaksinene» bør iverksettes først når nesten alle landets barn får «pennyvaksinene». Hvis ikke, risikerer vi at land med suboptimal basisvaksinasjonsdekning satser på de nye vaksinene. Dersom midlene fra GAVI og andre kortsiktige programmer blir borte, risikerer man i disse landene å stå igjen med et svekket vaksinasjonsprogram. Et argument har vært at suboptimal dekning skyldes et for svakt helsesystem, inkludert mangel på utdannet personell, at vaksiner går tapt pga. mangel på muligheter til kjølig lagring og dårlig utnyttelse av multidoseampuller. GAVI burde derfor i større grad satse på styrking av helsevesenet i det enkelte land slik at man får et bærekraftig system for å få basisvaksinene ut til flere. Hvordan kritikken kan håndteres Vi vil her ta for oss hvert av disse punktene for å forsøke å illustrere hvordan GAVI og dens partnere forsøker å håndtere denne konstruktive kritikken. Bærekraft for vaksinasjonsprogrammer i utviklingsland er et springende punkt. For å sitere Jeffrey Sachs, nå direktør ved The Earth Institute (8) og spesialrådgiver for FNs generalsekretær: «Det er ikke hjelp i ett eller to år, det er hjelp i 20 år vi trenger. Det Gates har gjort er fantastisk, men Gates kan ikke ta ansvaret for dette alene.» Ideelt sett bør hvert land, med støtte fra WHO, ha tilstrekkelige økonomiske og menneskelige ressurser til full dekning med samtlige tilgjengelige vaksiner mot de store infeksjonssykdommene. Situasjonen er imidlertid en annen, og GAVI forsøker sammen med nasjonale og internasjonale partnere å bidra til å øke den langsiktige vaksinasjonsdekningen. Flere prinsipper benyttes for å bidra til implementeringseffektivitet og langsiktighet. Prestasjonsbaserte bevilgninger Frem til 2005 kunne land med under 80 % basisvaksinasjonsdekning søke om midler til å styrke kapasiteten. Begrensningen på 80 % er nå hevet med den hensikt å bidra til å styrke helsesystemene ytterligere, også i land med forholdsvis god dekningsgrad. Landene bestemmer selv hvordan helsesystemene best bygges opp for å øke dekningsgraden. Senere tilskudd er betinget av at landene kan dokumentere økt vaksinasjonsdekning. Bill og Melinda Gates har bidratt med betydelige midler til The Global Alliance for Vaccines and Immunization (GAVI). Foto Adrian Wyld, AP/SCANPIX Innkjøpsfond Land med over 50 % dekning med basisvaksinene kan altså søke om midler til vaksinasjon med de nyere og mindre brukte vaksinene mot hepatitt B og Haemophilus influenzae type b, som kan gis sammen med difteri-stivkrampe-kikhoste-vaksinen og gulfebervaksinen. Ved å koordinere innkjøp av disse vaksinene gjennom UNICEF er etterspørselen økt betydelig og blitt mer stabil og forutsigbar. Da GAVI ble opprettet, var det bare én produsent, nå er det blitt flere, særlig i utviklingsland. Dette vil stabilisere produksjonen og ventelig føre til betydelig prisreduksjon. Langsiktige bevilgninger Så langt har Brasil, Frankrike, Italia, Norge, Spania, Sverige, Storbritannia og Sør-Afrika gått sammen om å etablere International Finance Facility for Immunization (IFFIm) (9), som gir langsiktige og forpliktende bevilgninger til GAVI til innkjøp av både basisvaksiner og de nyere vaksinene. Midlene skal også gå til å styrke helsesystemene. GAVI arbeider i et tiårsperspektiv, Ramme 1 De strategiske målsettingene for GAVI, Global Alliance for Vaccines and Immunization, kan oppsummeres slik: Øke tilgangen til bærekraftige vaksinasjonstilbud Øke bruken av sikre og kostnadseffektive vaksiner og fremme andre egnede helsefremmende tiltak ved vaksinasjonskontaktene Støtte nasjonale og internasjonale tiltak for akselerert kontroll av vaksineforebyggbare sykdommer Akselerere utvikling og introduksjon av nye vaksiner og relevante teknologier Akselerere forsknings- og utviklingstiltak for vaksiner rettet primært mot bruk i utviklingsland Bidra til at bedret vaksinasjonsdekning står sentralt i internasjonalt utviklingsarbeid Tidsskr Nor Lægeforen nr. 20, 2006;
21 Figur 1 Utviklingen av vaksinedekningen på verdensbasis etter ifølge WHOs og UNICEFs estimater. Globalt var dekningen 75 % i 1990 og 78 % i 2003 til 2015, og ressursfordelingen er nå femtifemti mellom vaksiner og helsetjenestestøtte. Partnerskap om produktutvikling Partnerskap mellom offentlig og privat sektor om produktutvikling er ment å takle problemet med at det ikke finnes et tilstrekkelig sterkt marked for og dermed incentiver til å forske på utvikling av vaksiner mot sykdommer som primært forekommer i utviklingsland. Disse partnerskapene bruker en porteføljetilnærming ved å investere i eller støtte forskjellige selskaper og andre instanser som utfører forskningen. Eksempler er blant annet International AIDS Vaccine Initiative (IAVI) (10) og Malaria Vaccine Initiative (MVI) (11). Forpliktende garantier Giverlandene vil gi forpliktende garantier (advance market commitments) om at dersom en effektiv vaksine mot en gitt sykdom blir utviklet, vil de kjøpe inn tilstrekkelig store kvanta til bruk i utviklingsland. Dette er ment som et viktig incitament for vaksineutviklere som ellers ikke vil prioritere utvikling av vaksiner primært rettet mot befolkningsgrupper med lav eller ingen kjøpekraft. Denne mekanismen er fortsatt under diskusjon i G8-landene (12). Erfaringen fra GAVI tyder på at det er mye lettere å sikre langsiktig finansiering når man kan vise til konkrete resultater Demokratisk kontroll Som allianse var det svært viktig for GAVI å sikre at de viktigste aktørene var representert i styret og å sikre stor grad av åpenhet. Noen av aktørene, slik som WHO, har en styringsstruktur der de fleste land er med. Det diskuteres fortsatt om landene og befolkningsgruppene som skal nyte godt av vaksinene, bør være sterkere representert (12). Dekningsgrad En dekningsgrad på minimum 50 % er altså en forutsetning for å få støtte til introduksjon av nye vaksiner. GAVI har nylig styrket sin prioritering av støtte til rutinevaksinasjon som en integrert del av en bedret helsesektor i mottakerlandene (13). Tiden vil vise hvor vellykket denne satsingen er. Diskusjon om prioritering Da GAVI ble opprettet, forventet man en sterk økning i helsebudsjettene i de fattigste landene gjennom sektorstøtteprogrammene. Denne økningen har dessverre ikke funnet sted. Hvilke kanaler kan benyttes mest effektivt for å støtte helsesektoren: de globale helsefondene, tradisjonell bilateral bistand eller multilaterale bevilgninger, for eksempel gjennom WHO og UNICEF? Tendensen synes å være at alle skal være med på alt. Dermed får vi et stort koordineringsproblem (14). Er det en fare for at en for sterk satsing på flere sykdomsspesifikke programmer, slik som vaksinasjon og målrettet bekjempelse av hivinfeksjon og tuberkulose, kan gå på bekostning av den langsiktige, integrerte satsingen på preventive og terapeutiske helsetilbud som fremmer folkehelsen mer effektivt? Vi mener at verden har råd til både å øke dekningsgraden av eksisterende vaksiner og å utvikle nye vaksiner mot de store folkesykdommene i utviklingsland og samtidig styrke helsesystemene for å fremme folkehelsen effektivt. Spørsmålet er om det er politisk vilje til å investere bredt og styrke alle disse aspektene på en integrert måte. En slik integrering vil kunne øke kostnad-nytteeffekten betydelig (4, 5). Integrering krever både økonomiske ressurser, politisk vilje og faglig kompetanse til å gjennomføre helseintervensjoner som tjener folk flest, særlig de mest ressurssvake. Det er viktig at det blir tilstrekkelig attraktivt for kompetente helsearbeidere å arbeide i helsesystemer der det gjennomføres essensielle helsetiltak, slik som vaksinering og tidlig gjenkjennelse og behandling av vanlige og alvorlige sykdommer. Ved innføring av nye vaksiner kan vaksinasjonsprogrammene i fremtiden bidra betydelig til bekjempelse av sykdommer både hos barn og voksne. Blant de som er kommet lengst i utviklingen, er vaksiner rettet mot pneumokokklungebetennelse og rotavirusdiaré. Før pneumokokkkonjugatvaksiner kan implementeres i fattige utviklingsland, må de bli billigere. Vi trenger også mer informasjon om deres effektivitet i utviklingsland (15). Hib-vaksinene må også bli billigere før de kan innføres på bred basis, og vi trenger mer informasjon om sykdomsbyrden forårsaket av Hib-infeksjoner, spesielt i Asia. Vaksiner mot diarésykdommer Utviklingen av nye vaksiner mot den andre store sykdomsgruppen hos barn, diarésykdommene, er kommet kortere. Detaljerte studier av sykdomsbyrden er gjennomført i noen få utviklingsland (16). De viser at rotavirus er den viktigste årsak til alvorlig akutt diaré. Den relative betydning av de andre agensene, inkludert dem som bidrar til langvarig og underernærende diaré, er fortsatt omdiskutert. Dette er grunnen til at BMGF nylig finansierte et stort internasjonalt prosjekt med 27 millioner dollar for å kartlegge både diarésykdomsbyrden og bidraget fra hvert enkelt diarépatogen til denne byrden (tilskrivbar risiko). Senter for internasjonal helse ved Universitetet i Bergen og Folkehelseinstituttet er representert i dette ambisiøse prosjektet. I 2000 trakk Wyeth tilbake den meget effektive rotavirusvaksinen Rotashield fra det amerikanske markedet pga. en økning i forekomsten av tarminvaginasjon hos vaksinerte barn. På tross av dette tilbakesteget gikk GAVI, legemiddelindustrien og WHO videre med utvikingen av nye rotavirusvaksiner, og GSK og Merck lanserte nylig sine to vaksiner, som i store studier i Europa, Latin-Amerika og deler av Asia viste seg å gi høy grad av beskyttelse mot rotavirusdiaré uten å øke invaginasjonsforekomsten (17, 18). Problemet er at effekten ennå ikke er dokumentert i de fattigste utviklingsland, hvor koinfeksjoner med andre mikrober er hyppige. Prisen på rotavirus- og pneumokokkvaksinene er for høy og produksjonskapasi Tidsskr Nor Lægeforen nr. 20, 2006; 126
22 MEDISIN OG VITENSKAP teten for liten til at disse vaksinene kan gis i global skala i overskuelig fremtid. Takket være GAVI øker konkurransen mellom vaksineprodusentene, og produksjonen legges i stigende grad til lavkostnadsland. Det er grunn til å tro at de omtalte strategiene kan bidra til å senke prisen og øke produksjonsvolumet, også når det gjelder disse vaksinene. Særlig diaré, men også infeksjoner i de nedre luftveier, bidrar i stor grad til underernæring, noe som igjen øker risikoen for alvorlige infeksjoner og død. Vaksiner mot slike infeksjoner vil derfor kunne være et vesentlig bidrag til bedring av ernæringsstatus, helsestatus, utviklingsmuligheter og overlevelsessjanser hos barn. En forutsetning er at slike vaksiner når dem som trenger dem mest. Av smittsomme sykdommer er diaré og luftveisinfeksjoner de viktigste årsakene til at barn i utviklingsland dør. Siden det globale samfunn ennå ikke er villig til å betale for helseintervensjoner basert på kostnadnytte-effekt-beregninger, er det økonomiske incitamentet for å utvikle vaksiner mot en rekke viktige diaré- og luftveisinfeksjoner begrenset. Vi trenger å gjennomføre flere slike studier som er beskrevet over, studier der man beregner hvor mye hvert enkelt agens bidrar til sykdomsbyrden, for å kunne prioritere innen vaksineutvikling. Norges bidrag Norge har i de senere år stått sentralt i arbeidet for å bedre vaksinasjonsdekningen i utviklingsland. Under Jens Stoltenbergs forrige regjeringsperiode var Norge det første landet til å følge opp med solid støtte til GAVI, etter Bill Gates. I juni 2000 ble det her i landet bevilget en milliard kroner for en femårsperiode. Under Stoltenbergs nåværende regjering er dette beløpet økt til over 400 millioner kroner per år. Norge er også en aktiv pådriver for nye finansieringsmekanismer, slik som IFFIm. I tillegg har regjeringen nylig bevilget 50 millioner kroner årlig til et ambisiøst program som gir norske forskningsmiljøer vesentlig bedre muligheter til å bidra til vaksinearbeidet i utviklingsland. Programmet, som Forskningsrådet håndterer, legger vekt på de sykdommer som rammer de fattigste i fattige land hardest. Samarbeid med enkeltland, slik som India, er spesielt interessant, fordi det gir betydelige muligheter for norske miljøer: Oppdagelser kan forbli i norsk eie helt frem til produksjon hos og global markedsføring av for eksempel indiske produsenter. Forebygging av sykdom hos voksne Selv om de omtalte vaksinene gis til barn, er hensikten med noen av dem å forebygge sykdom hos voksne. Et eksempel er hepatitt B-vaksinen, som med GAVI-støtte gis til millioner av barn i utviklingsland. Denne vaksinen er primært rettet mot forebygging av de om lag en halv million årlige dødsfall som skyldes kronisk hepatitt og hepatom hos voksne. Det arbeides intenst med utvikling av vaksiner også mot andre sykdommer hos voksne, blant annet hivinfeksjon og tuberkulose. Lengst er vaksinen mot humant papillomvirus kommet. Dette viruset forårsaker årlig om lag en halv million dødsfall pga. livmorhalskreft hos kvinner, de aller fleste i utviklingsland. I 2002 bidro sykdommer som kan forebygges med de seks basisvaksinene, samt Hib-infeksjon og hepatitt B-infeksjon, med omtrent to millioner dødsfall. Dersom de nye rotavirus- og pneumokokkvaksinene viser seg å gi god beskyttelse også i utviklingsland, og de implementeres bredt, vil barnevaksinasjon alt i alt kunne forebygge om lag 3,5 millioner dødsfall årlig (19) og således bidra vesentlig til tusenårsmålene. En viktig forutsetning er altså at vi samtidig med introduksjonen av de nye vaksinene greier å opprettholde og øke dekningsgraden av basisvaksinene. Dette er en stor utfordring som både krever økonomiske ressurser, koordinering og betydelig oppgradering av helsesystemene. Tilgang på menneskelige ressurser er et kritisk aspekt. I mange land skjer det en stor intern forflytning og eksport av helsearbeidere vekk fra folkehelseoppgaver. Videre er hiv/aids og tuberkulose blitt en stor belastning for mange afrikanske land, både ved at mange helsearbeidere blir syke og fordi behandlingsprogrammene er meget ressurskrevende. Oppsummering Vaksinasjon er i seg selv en svært effektiv intervensjon, men det er store produksjonsog distribusjonsmessige utfordringer. Vaksinering når ut til mer enn tre firedeler av alle verdens barn, men vi må nå ut til enda flere. Dette vil redusere sykdomsbyrden og dermed bidra til økonomisk vekst i fattige land. Vaksinasjon av barn har i de senere år fått en sentral plass i utviklingen av nye samarbeidsformer, strategier og finansiering av helserettet og annen utviklingshjelp. Det er gledelig at et lite land som Norge spiller en så viktig rolle i dette arbeidet. Mange nye og lovende vaksiner er under utvikling. Hvis vi får etablert systemer som gjør at de når ut også til dem som trenger dem mest, og at de ikke blir gitt på bekostning av, men som et viktig tillegg til andre essensielle helsefremmende tiltak, vil vi kunne bidra til bedret helse, ernæring, overlevelse og dermed økonomisk utvikling og politisk stabilitet i utviklingsland. Det trengs mer forskning på hvordan vi på en effektiv, rettferdig og bærekraftig måte kan gjennomføre vaksinasjonstiltak og andre målrettede helsetiltak for å fremme folkehelsen. For å sitere Mexicos helseminister, Julio Frenk, på et møte i Bergen i februar 2006: «We have the magic bullets, but we need the magic guns.» Oppgitte interessekonflikter: Tore Godal var leder for GAVI i organisasjonens første fem år og har vært konsulent for BMGF. Halvor Sommerfelt har ingen oppgitte interessekonflikter. Litteratur 1. Bloom DE, Canning D. Policy forum: public health. The health and wealth of nations. Science 2000; 287: Commission on macroeconomics and health. Genève: WHO, en/ ( ). 3. Millennium development goals. millenniumgoals/. ( ). 4. Black RE, Morris SS, Bryce J. Where and why are 10 million children dying every year? Lancet 2003; 361: Lawn JE, Cousens S, Zupan J. 4 million neonatal deaths: when? Where? Why? Lancet 2005; 365: Bryce J, Black RE, Walker N et al. Can the world afford to save the lives of 6 million children each year? Lancet 2005; 365: Knippenberg R, Lawn JE, Darmstadt GL et al. Systematic scaling up of neonatal care in countries. Lancet 2005; 365: Jeffrey M. Sachs. who/sachs ( ). 9. International Finance Facility for Immunization. ( ). 10. International AIDS Vaccine Initiative. ( ). 11. Malaria Vaccine Initiative ( ). 12. WHO s in charge. Lobal health remains firmly on the G8 agenda for better or worse. Nature 2006; 442: General principles for use of GAVI Alliance/GAVI Fund resources General_Information/About_alliance/GAVI/ Principles.php ( ). 14. Godal T. Opinion: do we have the architecture for health aid right? Increasing global aid effectiveness. Nat Rev Microbiol 2005; 3: Cutts, FT, Zaman SM, Enwere G et al. Efficacy of nine-valent pneumococcal conjugate vaccine against pneumonia and invasive pneumococcal disease in The Gambia: randomised, double-blind, placebo-controlled trial. Lancet. 2005; 365: Valentiner-Branth P, Steinsland H, Fischer TK et al. Cohort study of Guinean children: incidence, pathogenicity, conferred protection, and attributable risk for enteropathogens during the first 2 years of life. J Clin Microbiol 2003; 41: Ruiz-Palacios GM, Perez-Schael I, Velazquez FR et al. Safety and efficacy of an attenuated vaccine against severe rotavirus gastroenteritis. N Engl J Med 2006; 354: Vesikari T, Matson DO, Dennehy P et al. Safety and efficacy of a pentavalent human-bovine (WC3) reassortant rotavirus vaccine. N Engl J Med 2006; 354: Annual deaths in 2002 from vaccine-preventable diseases Information/Immunization_informa/index.php ( ). Manuskriptet ble mottatt og godkjent Medisinsk redaktør Petter Gjersvik. Tidsskr Nor Lægeforen nr. 20, 2006;
23 Vaksiner mot tuberkulose Sammendrag Til tross for omfattende BCG-vaksinering siden 1970-årene er tuberkulose fortsatt et betydelig problem på verdensbasis. De siste årene har det vært utført en stadig mer målrettet forskningsinnsats for å utvikle nye vaksiner, og flere vaksinekandidater er nå i klinisk fase 1/fase 2-utprøvning og planlegges å gå til fase 3 i Etter dette vil det fortsatt ta flere år før man får endelig svar på om en ny vaksine vil gi redusert forekomst av tuberkulose. Selv om flere av vaksinekandidatene er lovende, er det betydelig usikkerhet knyttet til om de kan løse tuberkuloseproblemet. Grunnen er at man ikke har tilstrekkelig kjennskap til hva som gir beskyttende immunitet. Dagens vaksinekandidater er utviklet for å gi beskyttelse mot noen få laboratoriestammer av tuberkelbasiller og vil ikke nødvendigvis gi beskyttelse mot hele spekteret. Beregninger viser at en effektiv vaksine mot latent tuberkulose vil gi en snarlig og kraftig reduksjon i forekomsten av sykdommen, men dagens vaksinekandidater er utviklet i dyremodeller som måler effekt mot primær tuberkulose, ikke mot reaktivert latent tuberkulose. Det har derfor stor betydning å sikre at det eksperimentelle grunnlaget for en eller flere nye tuberkulosevaksiner er best mulig. Det er også viktig å få informasjon om hvilke av de mange vaksinekandidatene som er best. Engelsk sammendrag finnes i artikkelen på Oppgitte interessekonflikter: Se til slutt i artikkelen Harald G. Wiker [email protected] Seksjon for mikrobiologi og immunologi Gades Institutt Universitetet i Bergen og Avdeling for mikrobiologi og immunologi Haukeland Universitetssjukehus 5021 Bergen Gunnar Bjune Seksjon for internasjonal helse Institutt for allmenn- og samfunnsmedisin Universitetet i Oslo Mycobacterium tuberculosis er en av de mest utbredte sykdomsfremkallende mikrobene vi kjenner. Omtrent en tredel av verdens befolkning er smittet. Mellom to og tre millioner mennesker dør av tuberkulose hvert år, mens det er ca millioner nye tilfeller av aktiv sykdom (1). HIV-smittede med latent tuberkulose utvikler aktiv sykdom på et tidlig stadium av immunsvekkelsen, og dette er en viktig årsak til at tuberkuloseproblemet øker. I tillegg er det enorme utfordringer i behandlingen, som involverer bruk av 3 4 legemidler samtidig over lang tid. Dette krever mye av både pasient og helsevesen. Korrekt gjennomført diagnostikk og behandling representerer effektiv bekjempelse av tuberkulose. Dårlig gjennomført kjemoterapi fører til utvikling av resistente basiller. Vaksinering er den andre grunnpilaren i bekjempelsen av tuberkulose, men dessverre har ikke massevaksinering med BCG hatt den ønskede effekten. Det er derfor et sterkt behov for nye, mer effektive vaksiner mot sykdommen. Vanlige markedsmekanismer har fungert dårlig for utvikling av nye vaksiner. Private produsenter har bare i begrenset omfang funnet det interessant å investere på dette området. Internasjonalt har det vært en klar økning i interessen for tuberkuloseproblemet de siste årene, og offentlige og filantropiske initiativer spiller en viktig rolle. StopTBpartnerskapet har nedsatt flere arbeidsgrupper, blant annet en vaksinegruppe. Global alliance for vaccines and immunizations (GAVI) arbeider også for å bidra til vaksineutviklingen. Den internasjonale tuberkuloseunionen (IUATLD) og Landsforeningen for hjerte- og lungesyke (LHL) i Norge engasjerer seg nå fordi multiresistent tuberkulose er i ferd med å bli et svært alvorlig problem i mange land. Det norske tuberkulosekontrollarbeidet og tuberkuloseregisteret nyter vid internasjonal anerkjennelse, og her i landet har vi en sterk tradisjon når det gjelder karakterisering av tuberkelbasillens antigener og immunresponser mot disse. Kort historikk om dagens BCG-vaksine BCG-vaksinen ble utviklet fra et klinisk isolat (lait Nocard) av Mycobacterium bovis fra en tuberkuløs ku (2). Calmette og Guérin startet i 1908 å svekke lait Nocard på et potet-galle-medium. De observerte ganske tidlig morfologiske endringer i koloniene, noe som i dag gjerne settes i forbindelse med at et større genelement (region of difference 1, RD1) ble eliminert. Dette var sannsynligvis også årsak til svekkelsen (3). I løpet av 1920-årene ble stammen, nå kalt bacille Calmette-Guérin (BCG), tatt i bruk. BCG-vaksinasjon vant raskt innpass i mange land og vant ry for sin beskyttende evne (2). Her i Norge tok dr. Heimbeck vaksinen i bruk ved Ullevål sykehus. Han fant en klar beskyttende effekt av vaksinering av tuberkulinnegative sykepleierstudenter som begynte ved infeksjonsavdelingen, der det var et betydelig smittepress (fig 1) (4). Heimbeck observerte også at vaksinen måtte være viabel for å være effektiv (5). BCG-vaksinen ble brukt i stort omfang etter den annen verdenskrig. Det ble gjennomført kampanjer over mesteparten av verden i regi av Verdens helseorganisasjon. Dekningen ble imidlertid forbedret da BCG-vaksinering ble en del av i de utvidede vaksinasjonsprogrammene, som økte i omfang fra 1970-årene. Dagens bruk av BCG-vaksinen BCG-vaksinen er den eneste levende bakterievaksinen i det norske barnevaksinasjons-! Hovedbudskap Utvikling av nye vaksiner mot tuberkulose har høy prioritet Det finnes flere konkurrerende vaksinekandidater for utvelgelse til klinisk fase 3-utprøvning Hvilken vaksine som skal velges diskuteres mye, men prosedyren for utvelgelse er ikke bestemt Det hefter usikkerhet ved om vaksinekandidatene er gode nok fordi man ikke har tilstrekkelig kunnskap om beskyttende immunitet 2678 Tidsskr Nor Lægeforen nr. 20, 2006; 126:
24 MEDISIN OG VITENSKAP programmet. Den gir sjelden alvorlige bivirkninger. Risikoen for klinisk BCG-infeksjon er til stede hos personer med nedsatt immunitet. De vanligste bivirkningene er lokale reaksjoner (sår på injeksjonsstedet) og lymfeknutesvulst. I Norge og England vaksineres barn ved 14 års alder. I de fleste land vaksinerer man i tilknytning til fødselen, i samsvar med WHOs anbefaling. I Norge følges denne anbefalingen hos barn fra miljøer der det er høyere forekomst av tuberkulose. Det har aldri vært innført allmenn BCG-vaksinering i USA, og i flere vestlige land har man sluttet med allmenn vaksinering, men vaksine er et tilbud til utsatte grupper. I Norge var det inntil ca obligatorisk BCG-vaksinering. Vi har nå så lite tuberkulose at den forebyggende effekten av å fortsette å vaksinere er helt marginal (6). Vaksinering er gjort til en frivillig sak. Uklarheter om effekt av BCG-vaksinen Den mest anerkjente effekten av BCG-vaksine er beskyttelse mot tuberkuløs meningitt og andre disseminerte former for tuberkulose hos barn. Utover dette er det betydelig usikkerhet. Det er en klar nord-sør-gradient av vaksineeffekten. Vaksinasjonsstudier i USA, Storbritannia og Norge har vist opp mot 80 % beskyttelse (5, 7, 8). En nyere studie har oppsiktsvekkende vist effektiv beskyttelse i mer enn 60 år (9), mens studier fra sørligere breddegrader tyder på at vaksineeffekten er helt marginal (8). Dette er blitt forklart med mer atypiske mykobakterier i tropiske land og at tilleggseffekten reduseres ved preeksisterende antimykobakteriell immunitet. Sannsynligvis er det en grense for hvor sterk immunitet en levende mykobakterievaksine kan gi. Det er en vanlig oppfatning at BCG-vaksinen må gi en «miniinfeksjon», der tilstrekkelige mengder av relevante antigener kan sensibilisere immunsystemet. M tuberculosis har vært regnet for å være enhetlig, med lite stamme-til-stamme-variasjon. Nyere undersøkelser viser at isolater av M tuberculosis er forskjellige. Fremveksten av den såkalte W-Beijing-varianten gir grunn til bekymring. Enkelte stammer av denne progredierer oftere til aktiv sykdom, de er mer assosiert med primær resistens mot kjemoterapi (10) og de er mer virulente. Virulensen knyttes til ekspresjon av et unikt fenolisk glykolipid (11). W-Beijing-varianten sprer seg hurtigere enn andre tuberkelbasiller. Man arbeider med hypoteser om at den har vokst frem under et selektivt press fra BCG-vaksinering og at den representerer en unnslippelsesvariant (12 14). Hvorfor er det så vanskelig å lage en god tuberkulosevaksine? Tuberkelbasillene vokser langsomt, og det er et stort reservoar av personer med latent tuberkulose en kilde til nysmitte. Det er Figur 1 Gjengivelse av figur 4 fra dr. J. Heimbecks artikkel i Tidskriftet fra 1928 om BCG-vaksinering av sykepleierstudenter ved infeksjonsavdelingen ved Ullevål sykehus (4). Søylene merket «+» og viser henholdsvis antall tuberkulinpositive og antall tuberkulinnegative studenter som begynte ved infeksjonsavdelingen. Skravert felt med antall viser hvor mange som fikk tuberkulose i de to gruppene. De tuberkulinpositive hadde svært lav risiko for å få sykdommen. I 1927 og 1928 ble de tuberkulinnegative tilbudt BCG-vaksinering (søyle merket «Vac»). Kun én av de 88 vaksinerte studentene ble syke, mens blant dem som avslo tilbudet, ble åtte av 30 syke derfor nødvendig med en svært langsiktig strategi for å utrydde sykdommen. BCGvaksinen har ikke effekt mot reaktivering av tuberkulose. Den viktigste årsaken til at det er så vanskelig å lage en god vaksine er likevel at vi ikke har tilstrekkelig kunnskap om hva beskyttende immunitet ved tuberkulose representerer. Feltet har vært preget av sterke dogmer. Man har derfor ikke hatt en tilstrekkelig bredt anlagt strategi for å klarlegge beskyttende immunitet. Cellulær immunitet er definitivt viktigst. Tuberkulinreaksjonen er et mål på cellulær immunitet, men personer med særlig kraftige tuberkulinreaksjoner har høyere risiko for aktiv sykdom enn dem med moderate tuberkulinreaksjoner. IFN-γ er det cytokinet som korrelerer best med beskyttelse, men også her har man eksempler på at kraftige IFN-γ-responser mot enkelte antigener er assosiert med økt risiko for tuberkuløs sykdom. Antistoffer er tradisjonelt blitt regnet å være uten betydning. Nyere data og revisjon av litteraturen tyder imidlertid på at antistoffer kan ha en gunstig effekt. Det er håp om at fremskritt hva gjelder karakterisering av tuberkelbasillens antigene komponenter og mer kunnskap om hvordan tuberkelbasillene unnslipper gjenkjennelse av immunsystemet vil gi oss én eller flere nye vaksiner som vil være effektive både hos personer med latent tuberkulose og mot sykdom etter nysmitte. Mange leter etter en kombinasjon av spesifiserte antigener sammen med et adjuvans som kan ha ønsket effekt. Adjuvantia er hjelpestoffer i vaksinen som skal bidra til kraftig og rett immunrespons. Et hovedproblem ligger i regulatoriske forhold. Det er få godkjente adjuvantia. De som er godkjent, gir fortrinnsvis antistoffresponser, ikke T-celleresponser. Det forventes imidlertid at pågående forskning og utvikling av nye adjuvantia skal føre frem til en ny effektiv subenhetsvaksine. Det er viktig å huske at vevsdestruksjonen ved tuberkulose er immunmediert. Nye tuberkulosevaksiner må derfor ikke stimulere til vevsskade. Dette gjelder særlig for vaksiner mot latent infeksjon. Dyreforsøk tyder på at forskjellige stammer av tuberkelbasiller har varierende evne til å kolonisere og til å etablere infeksjon, og at det er et inverst forhold mellom disse egenskapene. Slik variasjon er sannsynligvis knyttet til uttrykket av spesifikke virulensfaktorer og koloniseringsfaktorer. Nye vaksiner bør antakelig inneholde disse faktorene for å ha effekt i ulike faser av infeksjonsforløpet og mot hovedvariantene av tuberkelbasiller som sprer seg i verden. Spredning av nye basillvarianter representerer en stor utfordring både for behandling og for utvikling av nye og bedre vaksiner. Aktuelle vaksinekandidater Vaksinekandidatene kan deles inn i levende vaksiner og komponentvaksiner. Noen vaksiner tenkes brukt som grunnvaksinering mot primær tuberkulose, andre skal forsterke eksisterende immunitet. Det er ikke vist at revaksinering med BCG gir noen ytterligere effekt (15), og vaksinering av tuberkulinpositive personer er også uten nytte. Dyreeksperimenter tyder imidlertid på at komponentvaksiner vil kunne gi en tilleggseffekt og dermed også beskytte personer med latent infeksjon. Utvikling av slike vaksiner møter spesielle utfordringer fordi arbeid med musemodeller for latent tuberkulose er meget tidkrevende (16). Tidsskr Nor Lægeforen nr. 20, 2006;
25 Figur 2 Analyse av antigener i mykobakterier. Krysset immunelektroforese av M bovis-bcg. Antigener fra bakteriene reagerer med antistoffer og danner buede presipitasjonslinjer i en agarosegel. Antistoffer spesifikt rettet mot antigen 85 presipiterer de tre mest beslektede antigen 85-komponentene 85A, 85B og 85C. Disse proteinene er løselige utskilte proteiner (20), og 85A og 85B er viktige kandidater i nye vaksiner mot tuberkulose Flere vaksinekandidater er nå kommet til klinisk fase 1- og fase 2-utprøvning (tab 1). Hvis denne utprøvningen går etter planen, vil vaksinene komme til fase 3 i Fase 3-utprøvning er meget ressurskrevende og vil ta flere år å gjennomføre. Hensikten er å få solide bevis for at vaksinen virker. Mye tyder på at immunitet mot aktivt utskilte proteiner er særlig viktig for beskyttelse mot tuberkulose. De fleste subenehetsvaksiner inneholder derfor slike antigener. I den senere tid har vi ved den nasjonale proteomikkplattformen i Bergen (PROBE) arbeidet med karakterisering av utskilte proteiner ved hjelp av moderne proteomikkmetoder, og vi har funnet et stort antall nye proteiner (Wiker HG, Målen H, Berven F Tabell 1 Ledende vaksinekandidater et al. Late breaker: revealing the secreted proteome of Mycobacterium tuberculosis H37Rv. TB Vaccines for the World, Wien april 2006). Dette gir et helt nytt syn på repertoaret av proteiner som tuberkelbasillene kan spille på i infeksjonsforløpet. Noen av disse proteinene kan ha spesiell betydning i patogenesen ved tuberkulose og vil i prinsippet kunne indusere ulike former for beskyttende immunitet, men det er for tidlig å peke på spesifikke kandidater. Levende vaksiner I og med at BCG-vaksinen er effektiv i visse sammenhenger, er utvikling av nye levende vaksiner en viktig strategi som forfølges av flere forskningsgrupper. Slike vaksiner er basert på forbedret BCG eller svekket M tuberculosis eller M bovis. Disse vaksinene er ment å erstatte dagens BCG-vaksine. Forbedret BCG Tuberkelbasillene har strategier for å unnslippe immunmediert destruksjon i makrofager (17), og bakteriene overlever ved å hemme fagolysosomal fusjon. Dette hindrer også bakteriene i å entre cytosol, og aktiveringen av CD8-positive T-lymfocytter blir redusert. For å motvirke dette er det utviklet en rekombinant BCG med listeriolysin fra Listeria monocytogenes. I tillegg er også genet for urease ødelagt for å fremme surgjøring av fagosomet (18). Denne vaksinen gir klart bedre beskyttelse enn BCG i musemodeller. Det er også laget rekombinante BCGstammer hvor gener for viktige antigener er duplisert for å gi ekstra stor ekspresjon. Det mest kjente eksemplet er BCG30, som uttrykker store mengder antigen 85B (19). Antigen 85B er en komponent av antigen 85-komplekset (fig 2) og representerer de Vaksine Type Utviklingstrinn Utvikler MtbPhoP rbcgδurec: Hly rbcg30 MVA85A Ag85B-TB10,4 (HyVac4) Mtb72f-AS02A HBHA Levende svekket M tuberculosis Levende forbedret BCG med rekombinant listeriolysin og uten ureasefunksjon Levende forbedret BCG med rekombinant antigen 85B Vacciniavirus med rekombinant antigen 85A Komponentvaksine med rekombinant fusjonsprotein av antigen 85B og TB10,4 Komponentvaksine med rekombinant fusjonsprotein av en protease og et overflateprotein Komponentvaksine med rekombinant uttrykt heparinbindende hemagglutinin Preklinisk Fase 1, klinisk utprøvning Fase 1, klinisk utprøvning Fase 2, klinisk utprøvning Fase 1, klinisk utprøvning Fase 2, klinisk utprøvning Preklinisk Universidad de Zaragoza, Spania Vakzine Project Management GmbH Aeras Wellcome Trust Aeras/Crucell GlaxoSmithKline Institut Pasteur, Lille kvantitativt viktigste utskilte antigenene (20). Dette antigenet forekommer i alle mykobakterier og er mykolsyretransferaser (21), essensielle enzymer for syntesen av celleveggen. Andre varianter av rekombinante BCG uttrykker humane cytokiner (22) som skal bidra til å stimulere immunsystemet. Svekket M tuberculosis En strategi tar utgangspunkt i svekkelse av virulente M tuberculosis- eller M bovisstammer ved å inaktivere gener som styrer sentrale metabolske reaksjoner. Transkripsjonsfaktoren phop regulerer ekspresjonen av flere virulensassosierte gener, og det er laget en mutant hvor phopgenet i M tuberculosis er ødelagt. Den har svært redusert virulens, men gir bedre beskyttelse enn BCG-vaksine i dyreforsøk (23). Rekombinante virale vektorer Antigener kan også settes rekombinant inn i andre vektorer. Vaccinia- og adenovirus brukes til dette formålet. MVA85A (24) består av vacciniavirus som uttrykker antigen 85A (fig 2), og den gir meget kraftige IFN-γ-responser. Noen mener at denne effekten er mer uttalt hos mennesker enn i musemodeller. Forsterkningseffekten er betydelig, fordi svært mange allerede er sensibilisert for antigen 85. Komponentvaksiner Komponentvaksiner, eller subenhetsvaksiner, baseres på utvalgte antigener som formuleres med et adjuvans. Mtb72f (25) inneholder et fusjonsprotein. Den ene delen er en utskilt protease, den andre delen et PE-protein. Det representerer en ny klasse av overflateproteiner som ble oppdaget ved sekvenseringen av M tuberculosis-genomet. Statens Serum Institut i Danmark utvikler en vaksine med et fusjonsprotein av antigen 85B og en ESAT-6-homolog som kalles TB10,4 (26). Denne vaksinekandidaten var lenge basert på antigen 85B og ESAT-6. ESAT-6 brukes i nye diagnostiske metoder, og det er viktig at man ikke kompromitterer de diagnostiske mulighetene gjennom vaksineringen. Dette har alltid vært et viktig ankepunkt mot BCG-vaksineringen. ESAT-6 var lenge en sentral del av vaksineutviklingen, fordi proteinet måtte antas å spille en viktig patogenetisk rolle. Det er imidlertid sannsynlig at andre antigener kan gi tilsvarende immunitet. Hensynet til diagnostikken tilsier derfor at ESAT-6 ikke bør brukes i vaksiner, siden det finnes få diagnostiske antigenkandidater (27). En ny vaksinekandidat inneholder et metylert overflateprotein, heparinbindende hemagglutinin (HBHA) (28). Cellulær immunitet mot dette proteinet forebygger spredning av tuberkulose fra lungene til andre organer i en tidlig fase etter infeksjon (29) Tidsskr Nor Lægeforen nr. 20, 2006; 126
26 MEDISIN OG VITENSKAP ANNONSE Veien videre Kritikken mot vaksinene som er under utvikling, er at de har vært laget med tanke på å indusere så kraftige IFN-γ-responser som mulig. Man vet at dette ikke er tilstrekkelig. Den ideelle tuberkulosevaksinen bør stimulere ulike former for immunitet. Sannsynligvis bør en vaksine ikke stimulere for kraftige IL- 4-responser, og det bør være en balanse mellom IFN-γ- og TNF-α-responser. Stimulering av regulatoriske T-celler har også betydning. Det er viktig å arbeide med et bredere og mer representativt repertoar av ferske kliniske isolater i dyremodellene for å sikre at nye vaksiner får den ønskede effekten. Fase 3-utprøvning er meget ressurskrevende, og det vil være lite hensiktsmessig å starte med en slik utprøvning før man har et tilfredsstillende eksperimentelt grunnlag. På samme måte som man er avhengig av en allsidig tilnærming når det gjelder kjemoterapi ved behandling av tuberkulose, er det nødvendig å ha en bred tilnærming i vaksinefeltet. Når man bestemmer seg for å gå videre, vil det være klokt å fortsette det prekliniske arbeidet med andre vaksinekandidater. Oppgitte interessekonflikter: Harald Wiker har fått honorar for to foredrag på et infeksjonsmedisinsk møte som var støttet av GlaxoSmith- Kline. Gunnar Bjune har ingen oppgitte interessekonflikter. Litteratur 1. Dye C, Scheele S, Dolin P et al. Consensus statement. Global burden of tuberculosis: estimated incidence, prevalence, and mortality by country. WHO Global Surveillance and Monitoring Project. JAMA 1999; 282: Osborn TW. Changes in BCG strains. Tubercle 1983; 64: Behr MA, Wilson MA, Gill WP et al. Comparative genomics of BCG vaccines by whole-genome DNA microarray. Science 1999; 284: Heimbeck J. Tuberkuloseinfektion og tuberkulosevakcination. Tidsskr Nor Lægeforen 1928; 48: Heimbeck J. BCG vaccination of nurses. Tubercle 1948; 29: Eskild A. Massevaksinasjon mot tuberkulose trenger vi det i Norge? Tidsskr Nor Lægeforen 1994; 114: Bjartveit K, Waaler H. Some evidence of the efficacy of mass BCG vaccination. Bull World Health Organ 1965; 33: Fine PE. Variation in protection by BCG: implications of and for heterologous immunity. Lancet 1995; 346: Aronson NE, Santosham M, Comstock GW, et al. Long-term efficacy of BCG vaccine in American Indians and Alaska natives: a 60-year follow-up study. JAMA 2004; 291: Toungoussova OS, Mariandyshev AO, Bjune G et al. Resistance of multidrug-resistant strains of Mycobacterium tuberculosis from the Archangel oblast, Russia, to second-line anti-tuberculosis drugs. Eur J Clin Microbiol Infect Dis 2005; 24: Reed MB, Domenech P, Manca C et al. A glycolipid of hypervirulent tuberculosis strains that inhibits the innate immune response. Nature 2004; 431: Bjune G. Tuberculosis in the 21st century: an emerging pandemic? Norsk Epidemiologi 2006; 15: Abebe F, Bjune G. The emergence of Beijing family genotypes of Mycobacterium tuberculosis and low-level protection by bacille Calmette- Guerin (BCG) vaccines: is there a link? Clin Exp Immunol 2006; 145: Surikova OV, Voitech DS, Kuzmicheva G et al. Efficient differentiation of Mycobacterium tuberculosis strains of the W-Beijing family from Russia using highly polymorphic VNTR loci. Eur J Epidemiol 2005; 20: Rodrigues LC, Pereira SM, Cunha SS et al. Effect of BCG revaccination on incidence of tuberculosis in school-aged children in Brazil: the BCG-REVAC cluster-randomised trial. Lancet 2005; 366: Phyu S, Mustafa T, Hofstad T et al. A mouse model for latent tuberculosis. Scand J Infect Dis 1998; 30: Hernandez-Pando R, Jeyanathan M, Mengistu G et al. Persistence of DNA from Mycobacterium tuberculosis in superficially normal lung tissue during latent infection. Lancet 2000; 356: Eddine AN, Kaufmann SE. Improved protection by recombinant BCG. Microbes Infect 2005; 7: Horwitz MA, Harth G, Dillon BJ et al. Recombinant bacillus Calmette-Guerin (BCG) vaccines expressing the Mycobacterium tuberculosis 30- kda major secretory protein induce greater protective immunity against tuberculosis than conventional BCG vaccines in a highly susceptible animal model. Proc Natl Acad Sci USA 2000; 97: Wiker HG, Harboe M. The antigen 85 complex: a major secretion product of Mycobacterium tuberculosis. Microbiol Rev 1992; 56: Belisle JT, Vissa VD, Sievert T et al. Role of the major antigen of Mycobacterium tuberculosis in cell wall biogenesis. Science 1997; 276: Murray PJ, Aldovini A, Young RA. Manipulation and potentiation of antimycobacterial immunity using recombinant bacille Calmette-Guerin strains that secrete cytokines. Proc Natl Acad Sci USA 1996; 93: Martin C, Williams A, Hernandez-Pando R et al. The live Mycobacterium tuberculosis phop mutant strain is more attenuated than BCG and confers protective immunity against tuberculosis in mice and guinea pigs. Vaccine 2006; 24: McShane H, Hill A. Prime-boost immunisation strategies for tuberculosis. Microbes Infect 2005; 7: Skeiky YA, Alderson MR, Ovendale PJ et al. Differential immune responses and protective efficacy induced by components of a tuberculosis polyprotein vaccine, Mtb72F, delivered as naked DNA or recombinant protein. J Immunol 2004; 172: Dietrich J, Aagaard C, Leah R et al. Exchanging ESAT6 with TB10.4 in an Ag85B fusion moleculebased tuberculosis subunit vaccine: efficient protection and ESAT6-based sensitive monitoring of vaccine efficacy. J Immunol 2005; 174: Wiker HG. Nytt spesifikt tuberkulin forventes å bedre diagnostikken av tuberkulose. Tidsskr Nor Lægeforen 2001; 121: Pethe K, Alonso S, Biet F et al. The heparin-binding haemagglutinin of M. tuberculosis is required for extrapulmonary dissemination. Nature 2001; 412: Temmerman S, Pethe K, Parra M et al. Methylation-dependent T cell immunity to Mycobacterium tuberculosis heparin-binding hemagglutinin. Nat Med 2004; 10: Manuskriptet ble mottatt og godkjent Medisinsk redaktør Petter Gjersvik. Tidsskr Nor Lægeforen nr. 20, 2006;
27 Medisin og vitenskap tema vaksinasjon Reisevaksinasjon Sammendrag Vaksinasjon gir god og langvarig beskyttelse mot en rekke infeksjonssykdommer og anbefales nesten alltid før reiser til land med høy smitterisiko. I tillegg til oppdatering av barnevaksinene er hepatitt A-vaksine viktig. Gulfebervaksine og meningokokkvaksine er obligatorisk ved innreise i visse land. Ved lengre opphold i endemiske områder må det også vurderes å vaksinere mot hepatitt B, rabies, tyfoidfeber og kanskje kolera. Det er smitterisiko for japansk encefalitt i store deler av Sørøst-Asia og skogflåttencefalitt i visse områder av Europa. Engelsk sammendrag finnes i artikkelen på Oppgitte interessekonflikter: Ingen Synne Sandbu [email protected] Avdeling for vaksine Divisjon for smittevern Nasjonalt folkehelseinstitutt Postboks 4404 Nydalen 0403 Oslo Reisevaksinasjon kan betraktes som en forsikring for den enkelte og bidrar i tillegg til redusert spredning av smittsomme sykdommer fra land til land. Det er neppe mulig å beregne risikoen for å få en gitt infeksjonssykdom for en uvaksinert person som reiser til et gitt område (1), og sykdomsrisikoen i lokalbefolkningen kan ikke uten videre overføres til besøkende. Det kan være betydelige sesongvariasjoner, og lokalbefolkningen kan gjennom sine barnevaksinasjonsprogrammer være beskyttet mot sykdommer som gulfeber, japansk encefalitt eller skogflåttencefalitt. Vanligvis har turister lavere sykdomsrisiko enn lokalbefolkningen, fordi de i mindre grad eksponeres for de lokale omgivelsene. De færreste turister vil f.eks. tilbringe dager med hardt arbeid i jungelen, bade i synlig forurensede dammer eller overnatte uten myggnett i bambushytter ved kanten av en rismark. Reisevaksinasjon gir anledning til å planlegge livslang beskyttelse, selv om hensikten i første omgang er beskyttelse for en aktuell reise. I Norge er det tilgjengelig vaksiner mot litt over 20 sykdommer (tab 1). De fleste kan være aktuelle som reisevaksiner, men det er usannsynlig at en enkeltperson noen gang har behov for alle vaksinene samtidig. Vaksinasjon mot tetanus, poliomyelitt, hepatitt A, gulfeber og rabies gir langvarig og tilnærmet fullstendig beskyttelse. Noen vaksiner gir bare kortvarig og delvis beskyttelse, men bidrar likevel betydelig til å redusere forekomsten av alvorlige sykdommer. Basistilbudet for ikke-vestlige reisemål er rådgivning, oppdatering av programvaksiner og hepatitt A-vaksine. Andre vaksiner i tillegg er aktuelle for dem som skal oppholde seg lenge i et område og ha nær kontakt med lokalbefolkningen eller ferdes langt fra byer og bilveier. Det er vanskelig å fastsette grensen mellom kortvarig og langvarig opphold. Gjøremål kan være viktigere enn oppholdets varighet for smitteeksponering. Individuell smitterisiko påvirkes av vaksinasjonsstatus, alder, kronisk sykdom, livsstil og erfaring fra tidligere reiser. Den som vaksineres og betaler for vaksinasjonen, bør selv være med på å vurdere risiko og vaksinasjonsbehov. Forskjellige vaksinatører kan gi ulike råd for samme reise, og alle kan ha rett. Ulikhetene beror dels på at det alltid må brukes skjønn i slike vurderinger, og dels på ulike opplysninger fra den som skal reise. De som skal besøke slekt og venner i et fjerntliggende opprinnelsesland, og som ikke selv er klar over at de mangler immunitet mot mange infeksjoner som er vanlige i området, har høyest risiko for smittsomme sykdommer. En annen gruppe med høy risiko er ungdom som skal oppleve verden og planlegge deler av reisen underveis. De bør vanligvis vaksineres forholdsvis grundig. De bør dessuten anbefales å ta med myggnett, siden de ofte bor på billige overnattingssteder med begrensede bekvemmeligheter. Det er viktig å formidle informasjon om hvilke vaksiner som gir ufullstendig beskyttelse og at vaksinasjon beskytter mot en svært begrenset andel av de risikofaktorene den reisende møter. Trafikk, alkohol og tilfeldig sex innebærer høyere risiko i mange andre land enn det vi vanligvis regner med i Norge. Vanlige vaksinasjonsanbefalinger Alle bør være vaksinert mot tetanus, difteri og poliomyelitt. Disse sykdommene er vanskelige å behandle, og de tilgjengelige vaksinene gir nær 100 % beskyttelse, som er langvarig. Tidligere fullvaksinerte trenger bare en enkelt forsterkningsdose etter ti år. Vaksinasjon av uvaksinerte voksne krever flere doser. Grunnvaksinering med barnedoser gir bedre antistoffrespons enn forsterkningsdoser med redusert antigeninnhold (2). Uvaksinerte bør ha to doser difteri-, stivkrampe- (ev. kikhoste-) og poliovaksine med minimumsintervall på fire uker. Rekker de ikke det, bør de minst få én dose før avreise. Eldre individer responderer ofte langsomt og ufullstendig på nye vaksineantigener og kan ha god nytte av gjentatt dose, også etter avsluttet reise. Kikhostevaksine til forsterkningsvaksinasjon av voksne finnes som kombinasjonsvaksiner med difteri-tetanus(-polio)-vaksine og kan anbefales, selv om risikoen for kikhoste neppe er høyere i utlandet enn hjemme. Det er aldri feil å oppdatere poliovaksinasjonsstatus selv om reisen går til et poliofritt område. En polioepidemi som i spredte seg fra Nigeria til en rekke tidligere poliofrie land med utilstrekkelig vaksinasjonsdekning, viser at høy vaksinasjonsdekning fortsatt er nødvendig. Hepatitt A-vaksinasjon anbefales fra ettårsalder for alle ikke-vestlige reisemål. En dose hepatitt A- eller to doser hepatitt A+Bvaksine gir innen to uker full beskyttelse mot hepatitt A i ett år hos nesten alle. Det er ikke kjent hvor langvarig beskyttelsen er etter en forsterkningsdose, siden det foreløpig bare er vel 15 års erfaring med vaksinen.! Hovedbudskap Reisevaksinasjon kan betraktes som en forsikring for den enkelte, og bidrar i tillegg til redusert smittespredning fra land til land Basistilbudet for ikke-vestlige reisemål er rådgivning, oppdatering av programvaksiner og hepatitt A-vaksine Behov for andre vaksiner vurderes på bakgrunn av hvem som reiser, hvor reisen går, oppholdets karakter og reisens varighet 2810 Tidsskr Nor Lægeforen nr. 21, 2006; 126:
28 MEDISIN OG VITENSKAP Krav om vaksinasjonssertifikat Gulfeber Gulfeber forekommer i store deler av tropisk Afrika og tropisk Sør-Amerika og overføres med myggstikk. Sykdommen er aldri registrert i Asia, men vektormyggen forekommer der. Ved innreise til de fleste tropiske og subtropiske land utenfor gulfeberområdene kreves gyldig vaksinasjonssertifikat for gulfeber for personer som kommer fra gulfeberendemisk område, men ikke for personer som kommer direkte fra Europa. Vaksinasjon før innreise i gulfeberområde anbefales, selv om ikke alle land krever det. Gulfebervaksine gir minst 99 % beskyttelse som er langvarig. Gyldig vaksinasjonssertifikat for gulfeber kan bare utstedes av autorisert gulfebervaksinatør. Meningokokksykdom Myndighetene i Saudi-Arabia krever at alle pilegrimer til landet er vaksinert mot meningokokk gruppe A og W135, altså med meningokokk A+C+W+Y-vaksine, minst ti dager og maksimum tre år før innreise. I perioder kan kravet gjelde alle som reiser inn i landet. Ingen andre land krever meningokokkvaksinasjon for innreise. I «meningokokkbeltet» tvers over Afrika sør for Sahara er det høy grunnforekomst av meningokokksykdom og jevnlige epidemier, oftest forårsaket av gruppe A-meningokokker. De siste årene har det vært påvist flere serogrupper i samme epidemi, og i noen epidemier har gruppe W135-meningokokker dominert. Fra tid til annen er det tidsbegrensede utbrudd av meningokokksykdom i andre deler av verden. Opplysninger om utbrudd pleier å bli publisert av WHO ( Det er sjeldnere informasjon om når utbrudd slutter. Meningokokk A+C-polysakkaridvaksine produseres ikke lenger, men firevalent meningokokk A+C+W+Y-vaksine kan fås på spesielt godkjenningsfritak. Dessverre medfører polysakkaridvaksiner risiko for lavere antistoffrespons ved gjentatt vaksinasjon enn ved førstegangsvaksinasjon. Vaksinasjon er aktuelt for barn og unge mennesker ved langtidsopphold og kan også vurderes ved kortere opphold og for voksne, avhengig av den epidemiologiske situasjonen. Konjugert meningokokk C-vaksine bør gis til barn og ungdom som skal gå på skole eller studere i vestlige land med høy forekomst av meningokokk C-sykdom. Ofte vil de aktuelle lærestedene anbefale vaksinen. Andre vaksiner ved lengre opphold Vaksiner som er indisert ved lengre opphold i visse områder (tab 2) omtales her i alfabetisk rekkefølge. Hepatitt B-vaksinasjon Hepatitt B-vaksinasjon anbefales først og fremst til helsepersonell som skal arbeide med direkte pasientkontakt i land utenfor Tabell 1 Vaksiner som er tilgjengelige i Norge. Alle tilgjengelige vaksineprodukter finnes i prislisten på Fullstendige preparatomtaler for vaksiner med markedsføringstillatelse finnes på Vaksine mot lavendemiske områder. Vaksinasjon bør vurderes for alle før lengre opphold i høyendemisk område, bl.a. fordi det er risiko for smitte gjennom helsevesenet mange steder. Personer med livsstil som medfører økt risiko for seksuell eller blodbåren smitte, bør tilbys vaksinasjon. Det er også økt smitterisiko for ungdom som skal være lenge nok i endemisk område til å kunne få en kjæreste. Vaksinen gir omkring 80 % beskyttelse etter to doser og over 95 % etter tre doser. De fleste land utenfor Nordvest-Europa har hepatitt B-vaksine i barnevaksinasjonsprogram. Japansk encefalitt Japansk encefalitt er en viral zoonose som overføres til mennesker ved myggstikk. Ca. én av 200 smittede utvikler sykdom. Sykdommen forekommer i alle land i Sørøst-Asia og er den alvorligste av virusencefalittene, med ca. 25 % letalitet og nevrologiske sekveler hos ca. 50 %. Den ble først erkjent som et folkehelseproblem i Japan, hvor vaksinen siden 1954 har inngått i barnevaksinasjonsprogrammet. Sykdommen kan neppe utryddes, fordi smittereservoaret er vadefugler og gris. Forekomsten hos turister er under 1: per måned ved kortvarige reiser Tabell 2 Vaksiner som kan være aktuelle for reise til ulike deler av verden Basisanbefaling Tillegg for visse områder, visse tider av året, langtidsopphold Europa DT(P) 1, Polio, MMR 2 Hepatitt A, hepatitt B, skogflåttencefalitt, meningokokk C Nord-Amerika DT(P) 1, Polio, MMR 2 Hepatitt A, hepatitt B, meningokokk C Mellom- og Sør-Amerika DT(P) 1, Polio, MMR 2 Hepatitt A Gulfeber, tyfoidfeber, rabies, hepatitt B Nord-Afrika DT(P) 1, Polio, MMR 2, Hepatitt A Tyfoidfeber, rabies, hepatitt B Afrika sør for Sahara DT(P) 1, Polio, MMR 2, Hepatitt A Gulfeber, Meningokokk A+C+W+Y, tyfoidfeber, rabies, hepatitt B Sentral- og Øst-Asia DT(P) 1, Polio, MMR 2, Hepatitt A Tyfoidfeber, rabies, hepatitt B, (skogflåttencefalitt) Sørøst-Asia og indiske subkontinent DT(P) 1, Polio, MMR 2, Hepatitt A Tyfoidfeber, hepatitt B, rabies, japansk encefalitt, Stillehavsområdet DT(P) 1, Polio, MMR 2, Hepatitt A Hepatitt B, tyfoidfeber 1 difteri, tetanus, (pertussis), poliomyelitt 2 meslinger, kusma, røde hunder Inngår i barnevaksinasjonsprogrammet Aktuelle for reisevaksinasjon Aktuelle for spesielle risikogrupper Difteri X X Stivkrampe X X Kikhoste (bare i kombinasjonsvaksine) X X Hib (Haemophilus influenzae type b) X Polio (inaktivert poliovaksine) X X Mesling-kusma-røde hunder (MMR) X X Varicella X Pneumokokksykdom (konjugatvaksine) X Pneumokokksykdom (polysakkaridvaksine) X Tuberkulose (BCG) X (X) X Influensa (X) X Gulfeber X Kolera/ETEC-diaré X Hepatitt A X X Hepatitt B X X Meningokokk C (konjugatvaksine) X X Meningokokk A+C+W+Y (polysakkaridvaksine)* X Japansk encefalitt* X Rabies X Skogflåttencefalitt X Tyfoidfeber X * spesielt godkjenningsfritak Tidsskr Nor Lægeforen nr. 21, 2006;
29 Tabell 3 Laveste alder det medisinsk er tilrådelig å gi visse vaksiner Vaksinetype BCG Hepatitt B Polio (OPV og IPV) Difteri-stivkrampe-kikhoste Haemophilus influenzae type b Mesling-kusma-rubella (MMR) Gulfeber Hepatitt A Rabies Kolera/ETEC-diaré Tyfoid polysakkarid Tyfoid levende oral Meningokokk C-konjugat Meningokokk polysakkarid A+C/A+C+W+Y Japansk encefalitt Skogflåttencefalitt Influensa Varicella Pneumokokk polysakkarid 23-valent Pneumokokk konjugat 7-valent til byer og turiststeder (3, 4). Risikoen varierer imidlertid betydelig med årstid, sted og varighet av oppholdet og er høyest for dem som bor i lengre perioder på landsbygda i områder der sykdommen er endemisk eller epidemisk. I forhold til sykdommens alvorlighet er vaksinasjonsanbefalingene restriktive. Den tilgjengelige vaksinen består av virus dyrket på musehjerne, og medfører en viss risiko for alvorlige nevrologiske bivirkninger. Vaksinasjon mot japansk encefalitt bør tilbys dem som skal oppholde seg fire ukers tid eller mer på landsbygda i sykdomssesongen. Kolera Kolera forekommer i Afrika, Sør-Amerika, Asia og noen av de tidligere sovjetrepublikkene. Det kreves stor smittedose for å få typisk kolerasykdom. Viktigste beskyttende tiltak er rent drikkevann. Ved reise til koleraendemiske områder anbefales vaksinasjon for personer som skal leve under dårlige hygieniske og sanitære forhold, personer som mangler magesyre eller bruker antacida, personer med kronisk tarmsykdom, hivpositive og hjelpepersonell ved krig eller naturkatastrofer. I Norge brukes den orale koleravaksinen i Laveste anbefalte alder 1. levedøgn 1. levedøgn 6 uker (tre doser med minst fire ukers intervall og forsterkningsdose senere) 8 uker i vanlig norsk program Ikke-tellende dose kan gis 1. levedøgn 6 uker (tre doser med minst fire ukers intervall og forsterkningsdose etter minst ett år) 8 uker i vanlig norsk program 6 uker (tre doser med minst fire ukers intervall og forsterkningsdose etter ett års alder) 8 uker i vanlig norsk program (antall doser avhenger av barnets alder) 9 måneder (bør gjentas ved alder 15 måneder) 9 12 måneder 1 år Ingen nedre grense for posteksposisjonell bruk 2 år 2 år 5 år 8 uker (antall doser avhenger av barnets alder) 2 år (A-komponent virksom fra 3 måneder) 1 år 1 år 6 måneder 9 måneder 2 år 8 uker (antall doser avhenger av barnets alder) stor utstrekning til forebygging av infeksjon med enterotoksindannende E Coli (ETEC), som er årsak til % av tilfellene av turistdiaré. Vaksinen gir rundt 60 % beskyttelse mot ETEC-diaré i 3 6 måneder. Den kan være nyttig for personer med grunnsykdommer som gjør at de bør unngå diaré, og kan tilbys andre. Rabies Rabies er en zoonose som forekommer i alle verdensdeler. Moderne rabiesvaksiner er sikre og effektive og bør vurderes før lengre opphold i Afrika, Asia eller Sør-Amerika. Vaksinasjon anbefales for personer som skal oppholde seg på avsidesliggende steder uten mulighet for rask medisinsk behandling eller i deler av verden der tilgangen på vaksine kan være dårlig, for helsepersonell som kommer i nær kontakt med rabiespasienter og for personell i utlandet som har økt risiko i arbeidssituasjonen (fangstmenn på Svalbard, veterinærer, zoologer). Spesielt anbefales rabiesvaksinasjon for barn som skal bo i endemisk område og er store nok til å bevege seg uten tilsyn, men for unge til å rapportere pålitelig om de har hatt kontakt med rabiessuspekt dyr. Etter mulig smitteeksponering skal både vaksinerte og uvaksinerte ha posteksponeringsbehandling med flere vaksinedoser. For vaksinerte er regimet enklere, spesifikt rabiesimmunglobulin unødvendig og tidsfristen på 24 timer før behandling mindre kritisk. Vaksinen skal injiseres intramuskulært, idet subkutan injeksjon kan gi dårlig immunrespons. Korrekt utført rabiesvaksinasjon gir tilnærmet full beskyttelse, og de fleste har påvisbare antistoffer i årtier. Det er noe uenighet om hvor ofte forsterkningsdoser skal gis etter fjerde dose. Informasjon om risikoen for rabiessmitte er viktigere enn vaksinen. Både barn og voksne bør lære å holde seg unna ukjente dyr, både levende og døde. Alle som skal til rabiesområder, må få nok informasjon til å gjenkjenne en smitterisikosituasjon: bitt, slikking på åpent sår eller kloremerke av mistenkt rabid dyr, oftest hund. I slike tilfeller må lokal helsetjeneste og veterinærhelsetjeneste straks kontaktes for posteksponeringsbehandling og håndtering av dyret. Skogflåttencefalitt Skogflåttencefalitt (tick borne encephalitis, TBE) skyldes TBE-viruset, som overføres ved flåttbitt i deler av Mellom-Europa og områder ved Østersjøen. Vaksinen gir en viss beskyttelse mot russisk vår- og sommerencefalitt (Russian spring-summer encephalitis, RSSE). Tyfoidfeber Tyfoidfeber er endemisk i Afrika, Asia, Mellom-Amerika, Sør-Amerika og enkelte steder i Sørøst-Europa, spesielt der det er dårlig drikkevannshygiene eller dårlig hygiene blant dem som håndterer matvarer. Smitterisikoen øker med oppholdets varighet og nærkontakt med lokalbefolkningen og er høyest for dem som besøker slekt og venner i familiens opphavsland på det indiske subkontinentet (inkludert Bangladesh, Bhutan, Nepal, Pakistan og Sri Lanka). Vaksinasjonen bør være fullført 14 dager før innreise i det aktuelle området. Det finnes to vaksinetyper. Den orale vaksinen, som ikke alltid er tilgjengelig, består av levende, svekkede Salmonella typhi i enterokapsler. Injeksjonsvaksinen består av kapselpolysakkarid fra S typhi, og revaksinasjon kan gi lavere antistoffrespons en førstegangsvaksinasjon (5). Begge vaksinene gir beskyttelse i størrelsesorden 70 %, og ingen av dem kan brukes til de yngste barna (tab 2). Personen som skal vaksineres Vaksinatøren må spørre om den som skal vaksineres, er frisk, har noen sykdom eller bruker noe legemiddel som kan påvirke effekten av eller indikasjonen for vaksine, er gravid eller planlegger å bli det, nylig har fått andre vaksiner eller immunglobuliner, tidligere har hatt kraftige vaksinereaksjoner eller har noen allergi. Alvorlig straksaller Tidsskr Nor Lægeforen nr. 21, 2006; 126
30 MEDISIN OG VITENSKAP gisk reaksjon på tidligere vaksinedose utgjør vanligvis kontraindikasjon mot gjentatt bruk av samme vaksine, men det er få kontraindikasjoner som er absolutte. Vaksinasjon under utvidet beredskap kan innebære en mindre risiko enn det å være uvaksinert. Levende vaksiner er vanligvis kontraindisert ved immunsvikttilstander. Eldre reisende Eldre utenlandsreisende er en stor og voksende gruppe. De mangler ofte grunnvaksinering. I tillegg medfører aldersbetingede endringer av immunsystemet dårligere antistoffrespons på nye vaksineantigener (6). De bør likevel tilbys reisevaksiner etter samme retningslinjer som befolkningen ellers. Dødeligheten av hepatitt A øker med alderen. Hepatitt A-vaksine bør derfor tilbys når reisemålet tilsier at det er indisert. Mange personer født før 1945 er naturlig immune mot hepatitt A. Anamnese på gjennomgått gulsott vil fange opp de fleste av dem. Hepatitt A-antistoffundersøkelse kan tilbys mistenkt immune for å spare utgifter til vaksine. Personer over 65 år bør tilbys pneumokokkvaksine hvis det ikke er gitt i løpet av de siste ti årene, og influensavaksine hvis det er tilgjengelig. Gravide og ammende Få vaksiner er benyttet til gravide i større utstrekning. Derfor er kunnskapen om mulig risiko for fosterskade begrenset (7). Teoretisk kan både levende og ikke-levende vaksiner være teratogene. Difteri-, tetanus-, polio- og hepatitt B-vaksine har i stor utstrekning vært gitt til gravide, og det er økende erfaring med hepatitt A-vaksine. Levende virusvaksiner kan gi viremi hos mor og barn og er som hovedregel kontraindisert. Det er imidlertid aldri beskrevet fosterskade etter vaksinasjon, ikke engang etter rubellavaksinasjon som teoretisk sett skulle være den mest risikable (8). Gulfeber, rubella- eller MMR-vaksinasjon like før eller i begynnelsen av et svangerskap er derfor ikke indikasjon for abort (9). Immunglobulinpreparater kan gis til gravide på samme indikasjoner som til andre. I hvert enkelt tilfelle må smitterisiko vurderes mot den mulige risikoen ved vaksinasjon. For de fleste vaksiner foreligger liten dokumentasjon om overgang til morsmelk, men det kan vanskelig tenkes at små mengder vaksine i morsmelken skulle kunne skade barnet. Som hovedregel er amming derfor ikke kontraindikasjon mot noen vaksine til mor. Barn og ungdom Når spedbarn skal ha langvarig opphold utenfor Norge, kan vaksinasjon begynne før avreise og eventuelt legges opp etter programmet i det landet de flytter til (7). Forskjellene i vaksinasjonsprogram er ikke større enn at spedbarn kan få de viktigste vaksinene hvor som helst i verden, med litt justeringer når de er tilbake i hjemlandet. Imidlertid kan det ofte være vanskelig å finne frem i helsetjenesten i et fremmed land. Mange steder vil ikke det offentlige vaksinasjonsprogrammet yte tjenester til turisters barn, og privat sektor har ikke nødvendigvis samme tilgang på de riktige vaksinene med god kvalitet. Det kan være aktuelt å forsere vaksinasjonsprogrammet i spedbarnsalder ved å gi tre doser difteri-stivkrampe-kikhoste-polio-hib-vaksine med korte intervaller (ned til fire uker) og første dose så tidlig som ved seksukersalder (tab 3). Dette regimet krever en fjerde dose, som vanligvis gis minst ett års tid etter tredje dose. Selv for opphold på bare 1 2 måneder kan det være aktuelt å begynne vaksinasjon tidligere enn tremånedersalder for å unngå store forsinkelser i programmet. Det er viktig å sende med skriftlig dokumentasjon på gjennomførte vaksinasjoner. De siste somrene har det vært økt oppmerksomhet om MMR-vaksine pga. meslingutbrudd i nærliggende ferieland som Danmark (2002), Italia (2002) og Tyskland ( ). Vaksinen kan anbefales til uvaksinerte voksne som ikke vet at de har hatt meslinger. For opphold på noen uker i land med lavere vaksinasjonsdekning kan en dose mesling-kusma-rubella-vaksine være aktuelt så tidlig som ved ni måneders alder for barn som skal ha nærkontakt med barn i lokalbefolkningen. Vanlige «reisevaksiner» gis stort sett som til voksne, men indikasjonen for rabiesvaksine og hepatitt B-vaksine er mer liberal for barn. Det er mange vaksiner som ikke anbefales i første leveår, og noen har enda høyere aldersgrenser (tab 3). For barn og ungdom kan i tillegg følgende vaksiner være aktuelle: BCG-vaksinasjon ved fødselen for barn som skal bo mer enn et par måneder i land der risikoen for tuberkulosesmitte er mye høyere enn i Norge. BCG er ellers lite egnet som reisevaksine, fordi det tar 6 12 uker før vaksineindusert beskyttelse inntrer. Rotavirusvaksine, som nylig er blitt tilgjengelig, bør vurderes for spedbarn i første levehalvår hvis det i løpet av småbarnsalder planlegges å ta dem med til reisemål der helsetjenestene har lavere standard enn i Norge (10). Meningokokk C-konjugatvaksine anbefales til barn og ungdom som skal bo i land med høy forekomst av meningokokk C- sykdom. For tiden gjelder det flere europeiske land, Australia, og deler av Canada. Pneumokokkonjugatvaksine er aktuelt for småbarn som skal flytte til visse vestlige land. Spesielt i USA er det vanlig at barnehager og skoler ved inntak krever attestasjon for visse vaksiner. Vannkoppevaksine er aktuelt for barn som skal på skole eller i barnehage i USA. Vaksinasjon ved sykdom Ved akutt febersykdom utsettes vanligvis vaksinasjon. Pasienter med kompliserte kroniske tilstander bør tas hånd om av lege som kjenner pasienten og sykehistorien, gjerne i samarbeid med lege som kan mye om vaksiner og vaksinasjon. Enkelte kroniske sykdommer og tilstander påvirker behovet for eller utgjør kontraindikasjon mot visse vaksiner. Det er begrenset kunnskap om effekten av vaksiner under sykdom, men mistanke om dårlig respons på vaksine utgjør ikke kontraindikasjon hvis vaksinen ellers er indisert. Det bør så vidt mulig avklares om vaksinen kan skade pasienten, om den forventes å virke, om det er aktuelt å bruke avvikende doseringsskjema, om det er indisert å gi spesielle vaksiner og om det er risikabelt å utsette vaksinasjonen. Det er få legemidler som interfererer med vaksiner. Levende vaksiner skal ikke gis under behandling med immunmodulerende legemidler i doser som svekker immunforsvaret. Antibiotika og kjemoterapeutika kan inaktivere levende bakterievaksiner, blodprodukter kan nøytralisere levende virusvaksiner. Litteratur 1. Steffen R, Connor BA. Vaccines in travel health: from risk assessment to priorities. J Travel Med 2005; 12: Bartels I, Jungert J, Lugauer S et al. Immunogenicity and reactogenicity of a single dose of a diphtheria--tetanus--acellular pertussis component vaccine (DTaP) compared to a diphtheria--tetanus toxoid (Td) and a diphtheria toxoid vaccine (d) in adults. Vaccine 2001; 19: Tiroumourougane SV, Raghava P, Srinivasan S. Japanese viral encephalitis. Postgrad Med J 2002; 78: Shlim DR, Solomon T. Japanese encephalitis vaccine for travelers: exploring the limits of risk. Clin Infect Dis 2002; 35: Overbosch D, Peyron F, Picot N et al. Combined typhoid fever and hepatitis A vaccine: comparison of immunogenicity and safety to concomitant monovalent vaccine over 3 years. J Travel Med 2005; 12: Ginaldi L, Loreto MF, Corsi MP et al. Immunosenescence and infectious diseases. Microbes Infect 2001; 3: Sandbu S, Nøkleby H. Småbarn, gravide og utenlandsreiser. Tidsskr Nor Lægeforen 2002; 122: Hofmann J, Kortung M, Pustowoit B et al. Persistent fetal rubella vaccine virus infection following inadvertent vaccination during early pregnancy. J Med Virol 2000; 61: Suzano CES, Amaral E, Sato HK et al. The effects of yellow fever immunization (17DD) inadvertently used in early pregnancy during a mass campaign in Brazil. Vaccine 2006; 24: Sandbu S, Sivesind S. Nye vaksiner mot rotavirusinfeksjon. MSIS-rapport 2006; 34. Oslo: Nasjonalt folkehelseinstitutt, Manuskriptet ble mottatt og godkjent Medisinsk redaktør Petter Gjersvik. Tidsskr Nor Lægeforen nr. 21, 2006;
31 Influensavaksinering hvorfor, for hvem og med hvilken vaksine? Sammendrag Årlig blir 5 10 % av alle nordmenn syke av influensa. Enkelte grupper, som eldre og personer med alvorlig bakenforliggende sykdom, har økt risiko for alvorlig forløp, komplikasjoner og død. Årlig influensavaksinasjon reduserer risikoen for pneumoni, sykehusinnleggelser og død hos risikogruppene. For pasienten fører vaksinasjon av helsearbeidere til redusert dødelighet i løpet av vintersesongen. I Norge tilhører rundt personer en risikogruppe og bør få tilbud om vaksinasjon. For sesongen 2005/06 var vaksinasjonsdekningen på ca. 45 % i risikogruppene. Målet er 75 % innen Egenopplevd behov for vaksinasjon er ofte avgjørende for om en person lar seg vaksinere eller ei. Helsepersonell spiller en viktig rolle i å øke bevisstheten og formidle kunnskap om influensa og vaksinasjon. Bruk av personlig invitasjon og arrangering av massevaksinasjonsdager er effektive metoder for å få opp vaksinasjonsdekningen. Engelsk sammendrag finnes i artikkelen på Oppgitte interessekonflikter: Ingen Marianne Bergsaker [email protected] Olav Hungnes Bjørn Iversen Divisjon for smittevern Nasjonalt folkehelseinstitutt Postboks 4404 Nydalen 0403 Oslo Hvert år blir 5 10 % av alle nordmenn syke av influensa, og kanskje like mange smittes uten å vite om det. Influensa er en av hovedårsakene til luftveisinfeksjoner og en viktig årsak til sykehusinnleggelse og død, spesielt blant eldre mennesker. Vaksine er et viktig redskap i å forebygge sykdommen. Mange land, deriblant Norge, har anbefalinger for bruk av vaksine, men det distribueres langt færre doser enn det anbefalingene skulle tilsi. Influensavirus forandres stadig, det er derfor nødvendig å endre vaksinen hvert år. Neste gang et dramatisk forandret virus oppstår og utløser en ny influensapandemi, vil behovet for vaksine bli ekstra stort. Sykdommen Influensa er forårsaket av influensavirus og gir typisk plutselig innsettende allmennsymptomer med feber, hodepine, muskelverk og nedsatt allmenntilstand samt tørrhoste. Det kliniske bildet varierer sterkt blant annet avhengig av virus, smittedose, pasientens alder, bakenforliggende sykdommer og immunitet etter tidligere kontakt med beslektede influensavirus. Enkelte grupper som eldre og personer med alvorlig bakenforliggende sykdom, har økt risiko for alvorlig forløp, komplikasjoner, særlig bakteriell pneumoni, og død. En svensk undersøkelse har beregnet overdødeligheten under en gjennomsnittlig influensasesong til personer (1). Tilsvarende beregninger er ikke gjort for Norge. Gjennomgått influensa eller vaksinasjon gir delvis beskyttende immunitet, best mot samme eller et liknende virus. Siden barn har vært eksponert for færre influensavirus, er de mer mottakelig for smitte. Spredning av influensa kan derfor lettere skje blant barn, for eksempel i skoler. Epidemiologi Vanlig influensa har en inkubasjonstid på 1 3 dager, og en person er vanligvis smitteførende fra tiden rundt symptomdebut og 3 5 dager fremover, barn ofte noe lenger (2). Asymptomatiske individer kan også være smittsomme. Epidemiologisk forekommer sykdommen i tre hovedformer hos mennesker: Sesonginfluensa Hver vinter, vanligvis i desember eller januar (aldri før uke 46 eller etter uke 10), starter influensautbrudd av varierende omfang. Utbruddet varer i 6 8 uker og domineres gjerne av ett av våre tre vanlige influensavirus. Sporadiske importtilfeller kan forekomme hele året. Neste sesongs utbrudd har sitt utspring i beslektede virus som sirkulerer i andre deler av verden. Således varierer gjerne virus fra sesong til sesong, mens det oftest er lite variasjon mellom virus forskjellige steder i verden i én og samme periode. Influensa som zoonose Mennesker kan i sjeldne tilfeller smittes av ikke-mennesketilpassede influensavirus fra dyr, hovedsakelig fugl (3) og svin (4). Slike infeksjoner fører som regel ikke til videre smitte blant mennesker. Etter 1997 har et høypatogent fugleinfluensavirus av subtype H5N1 forårsaket en stor epizooti blant fugler over store deler av Eurasia og Afrika med 244 bekreftede humantilfeller per 8. september 2006 (5). De få som smittes, har meget høy risiko for alvorlige sykdomsforløp. 143 dødsfall er bekreftet. Pandemisk influensa Med noen tiårs mellomrom forekommer influensapandemier (6). Dette er epidemier forårsaket av et influensa A-virus med et nytt hemagglutinin som hele eller størstedelen av befolkningen fullstendig mangler immunitet mot. Tidligere pandemier er blitt utløst ved at det har oppstått krysninger mellom influensavirus fra fugl og mennesker (i 1957 og 1968) (7), eller ved at et fuglevirus gradvis har ervervet tilpasninger som til slutt har gitt de nødvendige egenskapene (i 1918) (8). Det er stor variasjon i pandemienes alvorlighet, men nesten alle fører med seg overbelastning av helsetjenester, økt dødelighet og svikt i viktige samfunnsfunksjoner grunnet høyt sykefravær. Pandemier har som regel kommet i flere påfølgende bølger og kan komme når som helst på året. Det nye influensa A-viruset går i de påfølgende sesongene over til å bli vanlig sesonginfluensa, mens det forrige A-viruset gjerne fortrenges. De siste hundre årene har pandemier introdusert influensa av subtypene H1N1 ( ), H2N2 ( ), H3N2 (1968 og senere). I 1977 ble subtypen H1N1 reintrodusert uten at dette førte til pandemisk utbrudd og uten å utkonkurrere den eksisterende H3N2-subtypen.! Hovedbudskap Stadig forandring i influensavirus nødvendiggjør årlig vaksinering Høy vaksinasjonsdekning blant risikogrupper reduserer alvorlig sykdom og død Massevaksinasjon er et effektivt tiltak for å oppnå høy vaksinasjonsdekning 2814 Tidsskr Nor Lægeforen nr. 21, 2006; 126:
32 MEDISIN OG VITENSKAP Folkehelseinstituttet kjøper inn og distribuerer influensavaksinen til risikogruppene. I år sendes det ut over doser til kommunehelsetjenesten som står for vaksineringen. Under en kort og hektisk periode på høsten pakkes og sendes influensavaksinen ut fra Folkehelseinstituttets lager. Foto Anne Lene Solbakken/Folkehelseinstituttet Overvåking I Norge overvåkes influensa for å påvise begynnelse, slutt og størrelse av utbruddet, hvilke grupper som rammes og hvilke virus som sirkulerer. Totalt 201 fastlegekontorer og legevakter rapporterer forekomsten av klinisk influensa hver vinter til Folkehelseinstituttet. Om lag 70 leger sender også nasopharynxprøver til Folkehelseinstituttet for undersøkelse på influensavirus. I tillegg rapporterer landets medisinsk-mikrobiologiske avdelinger alle funn de gjør av influensavirus som ledd i klinisk diagnostikk. Mange virusprøver sendes også inn fra disse laboratoriene. Virus detaljkarakteriseres blant annet for å fastslå likhet med virusstammer som inngår i influensavaksinen. Alt foregår i nært internasjonalt samarbeid gjennom Verdens helseorganisasjon og European Influenza Surveillance Scheme (EISS). Influensavaksiner Influensavaksiner inneholder immunologisk viktige deler av drepte influensavirus (inaktivert vaksine). Vanligvis inngår tre forskjellige virus, to A-stammer og én B-stamme. Virus dyrkes i all hovedsak på befruktede hønseegg eller i cellekultur og inaktiveres vanligvis med formalin. Vaksinen kan være laget av hele virus (helvirusvaksine), viruspartikler som er kuttet opp (splittvaksine) eller av overflateantigener (subenhetsvaksine). Vaksinen gis subkutant eller intramuskulært og er godkjent til bruk hos alle personer over seks måneder. I Norge brukes splittog subenhetsvaksiner. En vaksine som gis intranasalt og som består av levende, svekkede influensavirus er foreløpig ikke tilgjengelig i Norge. Fordi influensavirus stadig endrer seg, vil immunitet etter gjennomgått sykdom eller vaksinasjon være begrenset mot nye virus. Det er foreløpig ikke funnet konserverte deler av viruset som er immunogene nok til å gi beskyttelse mot alle influensavirus. Bivirkninger Opptil 10 % av influensavaksinerte beskriver reaksjoner som rødhet, ømhet og hevelse på stikkstedet og lette allmennsymptomer med feber og generell uvelfølelse. Forekomsten av alvorlige, nevrologiske bivirkninger er svært sjeldne og overvåkes nøye. Under massevaksinasjon mot «svineinfluensa» i USA i 1976/77 ble forekomsten av Guillain-Barrés syndrom beregnet til å være i underkant av ett tilfelle per vaksinerte (9). I den siste store studien av alvorlige, nevrologiske komplikasjoner til sesonginfluensavaksinasjon fant man en overhyppighet av Guillain-Barrés syndrom på ca. ett tilfelle per en million vaksinerte (10). Dette er langt færre enn det antall dødsfall man unngår ved å vaksinere. I løpet av årene ble det totalt utlevert nær 3,5 millioner doser influensavaksine her i landet. For denne perioden mottok Folkehelseinstituttet i alt 83 meldinger om uønskede hendelser etter influensavaksinasjon. De aller fleste uønskede hendelsene var lette og kortvarige. Fire av hendelsene førte til sykehusinnleggelse. Ved et av disse tilfellene døde personen i tilslutning til influensavaksineringen. Det var ingen holdepunkter for sammenheng med selve vaksinen, men vasovagalt blodtrykksfall med påfølgende hjertestans i tilslutning til stikkprosedyren kan ha vært medvirkende årsak til dødsfallet. Med unntak av denne hendelsen, ga ingen varig skade. Effekt Antall tilfeller av ukomplisert influensa er vanligvis høyest blant barn under skolealder. Hos eldre og personer med kronisk hjerteog lungesykdom, nedsatt immunforsvar, nyresvikt og metabolske sykdommer har sykdommen oftere et mer alvorlig forløp med økt risiko for sykehusinnleggelse og død (11 15). Disse, samt nærkontakter til personer som ikke bør få influensa, anbefales vaksinasjon (ramme 1). Den målte effekten av vaksinasjon varierer en god del, og mange studier er gjort på risikogrupper. Gjennomgående funn er at vaksinasjon reduserer risikoen for pneumoni, sykehusinnleggelse og død hos eldre under en influensaepidemi. I en metaanalyse av 20 kohortstudier var den estimerte vaksineeffekten for å forebygge luftveissykdom, pneumoni, sykehusinnleggelse og død henholdsvis 56 %, 53 %, 50 % og 68 % (12). Effekten av å forebygge bekreftet influensa Ramme 1 Personer som spesielt vil ha nytte av vaksinasjon Voksne og barn med: alvorlige lungesykdommer kronisk hjerte- og karsykdommer sykdommer som gir nedsatt infeksjonsresistens personer med diabetes mellitus type 1 og 2 Beboere på alders- og sykehjem Alle personer over 65 år Nærkontakter til personer som ikke bør få influensa: helsepersonell som tar hånd om personer i risikogrupper/syke husstandsmedlemmer til personer med risikosymptomer Tidsskr Nor Lægeforen nr. 21, 2006;
33 Ramme 2 Noen grunner til at folk ikke lar seg vaksinere Ikke behov Tror ikke de tilhører en risikogruppe Tror de har tilstrekkelig motstand mot influensa Anser ikke influensa som en alvorlig sykdom Føler seg friske Ikke fått råd om vaksinasjon Frykt for bivirkninger Helsepersonell har frarådet dem å la seg vaksinere Manglende tilgjengelighet Pris og influensaliknende symptomer varierer fra ingen til delvis beskyttelse og er svært avhengig av om personen er hjemmeboende eller bor i sykehjem (16, 17). I en Cochraneoversikt fra 2004 som inkluderte 25 undersøkelser med totalt friske voksne i aldersgruppen år, var effekten av inaktivert vaksine mot serologisk påvist influensa og klinisk influensa henholdsvis 70 % og 25 % (18). Noen enkeltstudier En stor amerikansk studie inkluderte over hjemmeboende eldre hvert år over to sesonger (1998/99 og 1999/2000) (13). Korrelasjon mellom vaksinestamme og sirkulerende virus var god begge sesonger. Vaksinasjonsdekningen var på %. Det var færre innleggelser blant de vaksinerte enn blant de uvaksinerte. For pneumoni/ Ramme 3 Faktorer som har vist seg nyttige for å øke vaksinasjonsdekningen Sende personlig brev Ha spesielle vaksinasjonstider Retningslinjer for allmennpraktikerens rolle vedrørende influensavaksinasjon Økt bevissthet og kunnskap om influensa og vaksinasjon hos målgruppen ved bruk av helsepersonell og andre informasjonskilder som: video informasjonsbrosjyrer artikler i ikke-faglig presse nettside pressekonferanse informasjon via lokal TV- eller radiostasjon influensasykdom var reduksjonen 32 % og 29 % i de to sesongene, for hjertesykdom 19 % for begge sesonger og for hjerneslag 16 % og 23 %. Dødelighet uansett årsak var 48 % og 50 % lavere hos vaksinerte. For å forhindre ett dødsfall måtte man vaksinere ca. 100 personer (95 og 118 i de to sesongene). For å forhindre enten sykehusinnleggelse eller død var antallet som måtte vaksinere ca. 65 personer. I en stor studie fra Sverige ble nesten personer over 65 år invitert til å delta i en vaksinasjonskampanje i 1998/99 og 1999/2000 (14, 15). Henholdsvis 39 % og 48 % ble vaksinert med influensavaksine eller 23-valent pneumokokkvaksine eller begge. Det ble påvist lavere forekomst av influensasykdom, pneumoni og invasiv pneumokokksykdom hos de vaksinerte enn hos de uvaksinerte. Ved sykehusinnleggelse var gjennomsnittlig liggetid for vaksinerte 5,2 dager for influensa og 9,9 dager for pneumoni, mens den for uvaksinerte var henholdsvis 7,5 og 11,3 dager. Færre sykehusinnleggelser og kortere liggetid for dem som var vaksinert, førte til at totalt antall sykehusdager ble redusert med henholdsvis 56 % for personer med influensa, 38 % for pneumoni og 48 % ved invasiv pneumokokksykdom. Som i den amerikanske undersøkelsen fant man lavere dødelighet pga. pneumoni, hjertesykdom, kronisk obstruktiv lungesykdom og lavere generell dødelighet blant vaksinerte. Samtidig vaksinering med begge vaksiner ga forsterket effekt. Det var ingen økt dødelighet blant de vaksinerte i perioden etter influensasesongen. I en studie fra Nederland undersøkte man om influensavaksinasjon av høyrisikopasienter førte til redusert antall pasientkontakter for allmennpraktikere (november 1999 mars 2002) (19). I år med en «mild» influensasesong var det ingen reduksjon i antall kontakter. Ved en «normal» influensasesong var det en klar nedgang i antall kontakter. For pasienter med kardiovaskulær sykdom og diabetes mellitus var denne reduksjonen statistisk signifikant. I en annen nederlandsk studie ble vel personer over 65 år fulgt gjennom seks år (20). Vaksinasjonsdekningen var på %. Knapt 20 % ble aldri vaksinert i løpet av studieperioden. Ved studiestart hadde vel 50 % risikofaktorer som høyt blodtrykk og kronisk kardiovaskulær sykdom. Første vaksinedose førte til en ikke-signifikant reduksjon i dødsrisiko på 10 %. Ved revaksinasjon ble dødsrisiko redusert med om lag en firedel og ved avbrudd i vaksinasjonen økte den tilsvarende. Den positive effekten av vaksinasjon ble gjenvunnet hvis man gjenopptok vaksinasjonen. I hele populasjonen forhindret man ett dødsfall for hver 302 som ble vaksinert, og ett dødsfall for hver 195. person som ble revaksinert. Andre faktorer Immunresponsen etter vaksinasjon er bedre hos unge enn hos eldre, men moderat trening hos eldre kan bedre immunresponsen ved influensavaksinasjon (21). Vaksinasjon av risikogrupper Det er anslått at om lag en femdel av en befolkning tilhører en risikogruppe og derfor bør tilbys influensavaksine (22). For Norge skulle det bety rundt mennesker. Folkehelseinstituttet har gjennom flere år sendt ut om lag doser til bruk i risikogruppene, svarende til en vaksinasjonsdekning på ca. 33 %. For de siste sesongene har anvendelsen økt noe. For sesongen 2005/06 ble det på landsbasis totalt solgt nærmere doser. Av disse distribuerte Folkehelseinstituttet knapt doser til risikogruppene, dvs. en vaksinasjonsdekning på ca. 45 % i risikogruppene. Likevel er vaksinasjonsdekningen i Norge langt dårligere enn de fleste andre land, både i Norden og i resten av Europa (23). Det er også et stykke frem til Verdens helseorganisasjons mål med 75 % dekning innen Et av tiltakene myndighetene har iverksatt for å bedre dekningen i Norge, er bevilgninger for innkjøp av influensavaksine til risikogruppene for sesongen 2006/07. I tillegg er forslag til ny vaksineforskrift sendt ut på høring. Her foreslås det at kommunene skal ha plikt til å tilby influensavaksine til risikogruppene. Flere studier har sett på hva som er avgjørende for om en person lar seg vaksinere mot influensa eller ikke (24, 25). Et fellestrekk for disse undersøkelsene er betydningen av egenopplevd behov for vaksinasjon (ramme 2). I en studie fra Sverige med 210 personer over 75 år var vaksinasjonsdekningen 30 %, og halvparten av de uvaksinerte oppga som grunn at de ikke hadde behov for å bli vaksinert. Hos ca. en firedel av de uvaksinerte var manglende anbefaling fra helsepersonell årsaken, 5 % av de uvaksinerte var anbefalt ikke å la seg vaksinere (24). Bruk av personlig invitasjon til vaksinasjon og massevaksinasjon har vist seg å være svært effektivt for å øke vaksinasjonsdekningen (ramme 3). Videre er det viktig å skape økt bevissthet og kunnskap om influensa og vaksinasjon hos målgruppen gjennom bruk av helsepersonell. Det er også viktig å ha retningslinjer for allmennpraktikerens rolle, ikke minst for å identifisere høyrisikopasienter gjennom bruk av dataprogram. Helsepersonellets egne holdninger til influensavaksinasjon og formidling av disse spiller også en ikke ubetydelig rolle (26, 27). Vaksinasjon av helsepersonell Helsearbeidere er mer utsatt for influensasmitte enn mange andre arbeidstakere og får ofte økt arbeidsbelastning i influensaperioder, både pga. økt sykelighet blant pasienter og økt sykefravær blant kolleger. I tillegg omgås de personer i risikogruppene og bør derfor ikke være smittespredere. I etterkant av en influensasesong har ofte langt flere vært utsatt for viruset enn dem 2816 Tidsskr Nor Lægeforen nr. 21, 2006; 126
34 MEDISIN OG VITENSKAP som kan huske å ha gjennomgått sykdom (28). I år med større utbrudd er det vist at uvaksinerte helsearbeidere som arbeider med risikopasienter, hadde 35 % høyere fravær enn i resten av året og at fraværet lå høyere enn for resten av sykehuset. For dem som var vaksinert, var det ingen signifikant forskjell i fraværet gjennom året (29). Andre studier bekrefter disse funnene og viser i tillegg at helsearbeidere har en tendens til å gå på jobb til tross for influensa med feber (30). Ved vaksinasjon av en gruppe i befolkningen kan en for visse sykdommer, som influensa, oppnå beskyttelse av andre grupper i befolkningen (flokkimmunitet). Det skyldes redusert sirkulasjon av smittestoffet og redusert smittepress (31). For pasienter fører influensavaksinasjon av helsearbeidere til redusert dødelighet i løpet av vintersesongen. Hvis pasienten også er vaksinert, ser man i tillegg redusert forekomst av influensaliknende sykdom (32). Vaksinasjon ved pandemi Verdens helseorganisasjon har oppfordret alle land til å ha en nasjonal beredskapsplan mot pandemisk influensa. Hovedmålsettingen i den norske pandemiplanen, siste versjon fastsatt i februar 2006, er å forebygge smittespredning og redusere sykelighet og død under en pandemi (33, 34). For helsetjenesten er hovedutfordringen å kunne møte et kraftig økt behov for helsetjenester i en periode hvor de som arbeider i helsetjenesten selv er syke. Et viktig moment i en pandemiplan er raskt å få tilgang på en virksom vaksine og få iverksatt massevaksinering av prioriterte grupper. Vaksine til bruk under en pandemi vil inneholde én virusstamme. Hvor mange doser som er nødvendig for å oppnå beskyttelse ved bruk av en pandemivaksine i en immunologisk naiv populasjon, er ikke avklart. Immunrespons vil blant annet avhenge av mengden antigen, bruk av adjuvans og vaksinetype. Ved starten på en pandemi der man står overfor en immunologisk helt naiv befolkning, vil sannsynligvis to doser gi best effekt. Det diskuteres om såkalt priming vil kunne gjøre en befolkning mindre sårbar i en pandemisituasjon. Priming går ut på å vaksinere før pandemiutbruddet med en allerede produsert vaksine som inneholder et virus man tror vil være nært beslektet med pandemiviruset. Det er vanskelig å velge virus til produksjon av en primingvaksine, siden viruset gjennomgår stadig endringer. En slik vaksine vil sannsynligvis ikke være optimalt tilpasset det aktuelle pandemiske viruset, men vil muligens kunne gi en kryssimmunitet som innebærer noen grad av beskyttelse mot alvorlig influensasykdom. I tillegg kommer dilemmaet med å vaksinere mange mennesker med en vaksine hvor graden av beskyttelse er usikker, men hvor man må forvente at bivirkninger av ulik grad vil forekomme. Norge har inngått avtale om vaksineleveranse av fire millioner doser i en pandemisituasjon. Avtalen gjelder primært en splittvaksine med vanlig antigenmengde (15 μg) tilpasset den aktuelle stammen. Ved behov for større antigeninnhold i vaksinen vil vi få levert et tilsvarende mindre antall doser. For at en pandemivaksine raskt skal kunne godkjennes hos legemiddelmyndighetene, lager de ulike produsentene på forhånd såkalte modellvaksiner. Disse vaksinene kan man så gjøre utprøvninger med og søke om godkjenning for før det endelige pandemiviruset er kjent. Flere slike studier foregår eller er i ferd med å starte opp, også i Norge. Helseog omsorgsministeren har gitt signaler om at Norge stiller seg positivt til et nordisk samarbeid for produksjon av pandemisk influensavaksine. Konklusjon Omfanget av vinterens influensasesong vet vi først når sesongen er over. Høy vaksinasjonsdekning blant eldre og personer med kroniske sykdommer vil være med på å redusere følgene av sykdommen. For å nå målet er det viktig med felles innsats både fra helsepersonell, helsemyndigheter og mediene. Ved å arrangere massevaksinasjondager i kommunene vil flere kunne nås. Samtidig skaffer kommunene seg erfaring og kunnskap slik at de kan stå bedre rustet til å møte en pandemi. Utfordringen ligger i at dette må gjentas hvert år. Litteratur 1. Linde A, Ekdahl K, Lindbäck J et al. Aktuellt om influensa och RS i Sverige. Smittskydd 1999; 5: Smittevernhåndbok for kommunehelsetjenesten. 3. utgave. Oslo: Nasjonalt folkehelseinstitutt, Alexander DJ. Avian influenza viruses and human health. I: OIE/FAO International Scientific Conference on Avian Influenza, Basel. Dev Biol 2006: 124: Brown IH. The epidemiology and evolution of influenza viruses in pigs. Vet Microbiol 2000; 74: country/cases_table_2006_09_08/en/index.html ( ). 6. Potter CW. Chronicle of influenza pandemics. I: Nicholson KG, Webster RG, Hay AJ, red. Textbook of influenza. Oxford: Blackwell Science, Kawaoka Y, Krauss S, Webster RG. Avian-tohuman transmission of the PB1 gene of influenza A viruses in the 1957 and 1968 pandemics. J Virol 1989; 63: Taubenberger JK, Reid AH, Lourens RM et al. Characterization of the 1918 influenza virus polymerase genes. Nature 2005; 437: Schonberger LB, Bergman DJ, Sullivan-Bolyai SZ et al. Guillain-Barre syndrome following vaccination in the national influenza immunization program, United States, Am J Epidemiol 1979; 110: Lasky T, Terraciano GJ, Magder L et al. The Guillain-Barré syndrome and the and the influenza vaccines. N Engl J Med 1998; 339: WHO. The Weekly Epidemiological Record 2002; 77: Gross PA, Hermogenes AW, Sacks HS et al. The efficacy of influenza vaccine in elderly persons. A meta-analysis and review of the literature. Ann Intern Med 1995; 123: Nichol KL, Nordin J, Mullooly J et al. Influenza vaccination and reduction in hospitalizations for cardiac disease and stroke among the elderly. N Engl J Med 2003; 348: Hedlund J, Christenson B, Lundbergh P et al. Effects of a large-scale intervention with influenzae and 23-valent pneumococcal vaccines in elderly people: a 1-year follow-up. Vaccine 2003; 21: Christenson B, Hedlund J, Lundgren P et al. Additive preventive effect of influenza and pneumococcal vaccines in elderly persons. Eur Respir J 2004; 23: Jefferson T, Rivetti D, Rivetti A et al. Efficacy and effectiveness of influenza vaccines in elderly people: a systematic review. Lancet 2005; 366: Vu T, Farish S, Jenkins M et al. A meta-analysis of effectiveness of influenza vaccine in persons aged 65 years and over living in the community. Vaccine 2002; 20: Demicheli V, Rivetti D, Deeks JJ et al. Vaccines for preventing influenza in healthy adults (review). Cochrane Database Syst Rev 2004: CD Tacken MA, Braspenning JC, Berende A et al. Vaccination of high-risk patients against influenza: impact on primary care contact rates during epidemics. Analysis of routinely collected data. Vaccine 2004; 22: Voordouw AC, Sturkenboom MC, Dieleman JP et al. Annual revaccination against influenza and mortality risk in community-dwelling elderly persons. JAMA 2004; 292: Kohut ML, Arntson BA, Lee W et al. Moderate exercise improves antibody response to influenza immunization in older adults. Vaccine 2004; 22: Hak E, van Essen GA, Stalman WA et al. Improving influenza vaccination coverage among highrisk patients: a role for computer-supported prevention strategy? Fam Pract 1998; 2: Macroepidemiology of Influenza Vaccination (MIV) Study Group. The macro-epidemiology of influenza vaccination in 56 countries, Vaccine 2005; 23: Dannetun E, Tegnell A, Normann B et al. Influenza vaccine coverage and reasons for non-vaccination in a sample of people above 65 years of age, in Sweden, Scand J Infect Dis 2003; 35: Kroneman M, van Essen GA, Paget JW. Influenza vaccination coverage and reasons to refrain among high-risk persons in four European countries. Vaccine 2006; 24: Hak E, Hermens RP, Hoes AW et al. Effectiveness of a co-ordinated nation-wide programme to improve influenza immunisation rates in The Netherlands. Scand J Prim Health Care 2000; 18: Hofmann F, Ferracin C, Marsh G et al. Influenza vaccination of healthcare workers: a literature review of attitudes and beliefs. Infection 2006; 34: Elder AG, O Donnell B, McCruden EA et al. Incidence and recall of influenza in a cohort of Glasgow healthcare workers during the epidemic: results of serum testing and questionnaire. BMJ 1996; 313: Yassi A, Kettner J, Hammond G et al. Effectiveness and cost-benefit of an influenza vaccination program for health care workers. Can J Infect Dis 1991; 2: Wilde JA, McMillan JA, Serwint J et al. Effectiveness of influenza vaccine in health care professionals: a randomized trial. JAMA 1999; 281: Reichert TA, Sugaya N, Fedson DS et al. Japanese experience with vaccinating schoolchildren against influenza. N Engl J Med 2001; 344: Thomas RE, Jefferson TO, Demicheli V et al. Influenza vaccination for health-care workers who work with elderly people in institutions: a systematic review. Lancet Infect Dis 2006; 6: World Health Organization. Assessing the pandemic threat. WHO_CDS_2005_29/en/index.html ( ). 34. Nasjonal beredskapsplan for pandemisk influensa. Versjon 3.0. Oslo: Helse- og omsorgsdepartementet, Manuskriptet ble mottatt og godkjent Medisinsk redaktør Petter Gjersvik. Tidsskr Nor Lægeforen nr. 21, 2006;
35 Slimhinnevaksiner i utvikling Sammendrag Den levende poliovaksinen som gis oralt, representerer den første slimhinnevaksinen i allmenn bruk. Senere er det utviklet liknende vaksiner mot tyfoidfeber, kolera og rotavirusinfeksjon, og en nasal vaksine mot influensa er nylig registrert i USA. Den eneste ikke-levende slimhinnevaksinen på markedet i dag er en oral koleravaksine som består av inaktiverte Vibrio cholerae og B-subenheten av koleratoksin. Flere forskningsgrupper arbeider imidlertid med å utvikle andre slimhinnevaksiner basert på inaktiverte mikrober eller deler av dem. Ved Folkehelseinstituttet er det gjort forsøk med dyr som tyder på at ikkelevende nasale vaksiner kan gi opphav til beskyttende immunitet og at de kan kombineres med tilsvarende vaksiner til injeksjon. Kliniske forsøk med nasale vaksiner bestående av betapropiolaktoninaktiverte influensapartikler viste at det kunne oppnås konsentrasjoner av antistoff i serum som regnes som beskyttende mot influensa. Det ble også dannet IgA-antistoff i nesesekret spesifikt rettet mot influensa, noe som kan tenkes å hemme utbredelse av sykdommen. Ved å optimalisere immuniseringsregimene slik at den immunologiske hukommelsen blir utnyttet bedre, og eventuelt legge til adjuvans i formuleringene, er det sannsynlig at ikkelevende slimhinnevaksiner kan bli et realistisk alternativ til flere vaksiner som nå gis ved injeksjon. Hilde Bakke [email protected] Bjørn Haneberg Nasjonalt folkehelseinstitutt Divisjon for smittevern Postboks 4404 Nydalen 0403 Oslo De som opplevde 1950-årene og tiden før det, husker med gru angsten for å få poliomyelitt. Alle kjente noen som var rammet, og flere av disse ble merket for livet. Håpet kom i 1956 med den første poliovaksinen, en inaktivert vaksine som måtte gis ved injeksjon. Men det var først da den såkalte levende vaksinen kom på markedet ti år senere den som ble gitt som dråper rett i munnen at det ble mulig å vaksinere store deler av verdens befolkning. I dag er poliomyelitt sjelden og regnes som utryddet i Europa og på det amerikanske kontinentet (1). Hensikten med å gi poliovaksinen oralt, direkte på slimhinnene, var at det svekkede virus i vaksinen skulle nå tarmen hvor det, som andre enterovirus, har sitt naturlige habitat. Denne smitten skulle så gjøre den vaksinerte immun mot det nært beslektede «ville» viruset ved å aktivere det slimhinneassosierte immunapparatet (fig 1). Det viste seg imidlertid at også vaksineviruset en sjelden gang kunne være årsak til alvorlig sykdom, og at det lett ble overført fra den vaksinerte til et ikke-vaksinert familiemedlem, som så kunne bli syk (2). Dette førte til at man i mange land gikk tilbake til den inaktiverte poliovaksinen som må injiseres. Men hvis det er tale om å nå ut til store befolkningsgrupper, spesielt i områder hvor polio ennå forekommer, blir den orale vaksinen fortsatt foretrukket. Andre levende slimhinnevaksiner Det samme prinsippet med å gi en levende, men svekket mikrobe peroralt, som slimhinnevaksine, kan også benyttes for å forebygge andre sykdommer, blant annet tyfoidfeber og rotavirusinfeksjon (3). Til tross for at disse vaksinene er både effektive og enkle å administrere, har det store gjennombruddet latt vente på seg. Vaksinen mot tyfoidfeber har for eksempel ikke fortrengt bruken av tilsvarende vaksine som består av inaktiverte salmonellakomponenter og som må injiseres. Produksjonen av slike levende vaksiner er også komplisert. De må lagres kjølig, og prisen blir derfor høy noe som gjør dem mindre anvendelige i den fattige del av verden (4). Dessuten har det vært knyttet en viss skepsis til slike vaksiner, spesielt siden den første perorale vaksinen mot rotavirusinfeksjon ble trukket fra markedet etter bare få måneders Engelsk sammendrag finnes i artikkelen på Oppgitte interessekonflikter: Se til slutt i artikkelen Slimhinnevaksiner er enkle å administrere. Vaksiner gitt som nesedråper er et godt eksempel. Vaksinanden kan selv ta vaksinen under tilsyn 2818 Tidsskr Nor Lægeforen nr. 21, 2006; 126:
36 MEDISIN OG VITENSKAP bruk på grunn av mistanke om at den kunne forårsake invaginasjon hos barn. Beskyttelsen mot sykdom i de mest utsatte deler av verden har ikke alltid vært så god som de første forsøkene kunne gi håp om (4, 5). Den levende vaksinen mot influensa som kom på markedet i USA for et par år siden og som gis som nesespray, er heller ikke blitt den suksessen som var forventet. Muligens kan dette forklares ved at de etablerte injeksjonsvaksinene mot influensa er både billige og effektive. Det har dessuten vært antydet at det svekkede virus i den nasale influensavaksinen kunne tenkes å revertere til mer patogene former. Det blir derfor anbefalt å fortsette arbeidet med å utvikle alternative, ikke-levende slimhinnevaksiner mot influensa (6). Ikke-levende slimhinnevaksiner Ved Folkehelseinstituttet har det inntil nylig vært arbeidet med å undersøke hvilke faktorer som var bestemmende for at ikke-levende slimhinnevaksiner skulle kunne bli effektive og praktiske i bruk (7). Forsøk fra årene etter 1940 hadde nemlig vist at det var mulig å oppnå en viss antistoffrespons i serum etter å ha gitt den tradisjonelle, inaktiverte influensavaksinen intranasalt, men ikke på langt nær det som måtte til for å utfordre injeksjonsvaksinene (8). I en tidligere studie som ser ut til å ha gått i glemmeboken, var imidlertid resultatene av intranasal vaksinering mer oppløftende; barn som hadde fått bare én subkutan injeksjon med difterivaksine, og som deretter ble revaksinert intranasalt, hadde like god effekt på antitoksinnivået i serum som etter revaksinering subkutant (9). Dette til tross for at det ikke ble gitt større doser intranasalt enn subkutant og at den nasale vaksinen heller ikke inneholdt tradisjonell adjuvans, mens den subkutane vaksinen var absorbert til Al(OH) 3. Hvis man i dag skulle forsøke å forklare denne gode effekten av nasal vaksine mot difteri, måtte det være at den hadde beholdt noe av difteritoksinets egenskaper som muligens kunne ha virket som et slimhinneadjuvans på linje med andre bakterielle toksiner, som forklart nedenfor, og som kunne ha bidratt til at vaksinen klarte å trenge igjennom den barrieren som slimhinnene representerer. Slimhinneadjuvans Normalt vil kroppen tåle å bli utsatt for store molekyler som presenteres på slimhinnene i form av fødemidler eller inhalerte substanser. Det utvikles som regel redusert immunreaksjon eller immunologisk toleranse etter gjentatt inntak av slike komponenter med antigene egenskaper (10). I dyreforsøk er det! Hovedbudskap Flere levende slimhinnevaksiner er utviklet Én ikke-levende oral vaksine mot kolera er i salg Flere ikke-levende slimhinnevaksiner kan være på markedet i løpet av få år imidlertid vist at enkelte toksiner som utskilles fra V cholerae og Escherichia coli, kan bryte denne toleransen og virke som adjuvans, slik at det blir utviklet immunitet mot proteiner som gis direkte på slimhinner (11). Grunnlaget for denne virkningen er ikke helt klarlagt, men kan delvis forklares ved at de aktiverer og setter slimhinnen i en tilstand av alarmberedskap (3). På denne måten kan virkningen av et antigen bli forsterket ved å gis samtidig med adjuvans, men uten at antigenet nødvendigvis er koblet til adjuvans. Det har vist seg at verken kolera- eller E coli-toksinene er egnet til bruk i mennesker, men ikke-toksiske derivater av dem kan ha sin immunologiske effekt i behold, noe som er utnyttet i den svenskutviklede vaksi- Figur 1 Opptak av vaksineantigener gjennom slimhinner. a) I mange slimhinner finnes dendrittiske celler (Dc) med lange utløpere (dendritter). Utløperne kan strekke seg gjennom epitelet, såkalt snorklende dendrittiske celler, og ta opp antigener på overflaten, bryte dem ned til peptidfragmenter og så presentere disse på HLA-klasse 2-molekyler til T-celler. Dersom dendrittiske celler aktiveres av vaksinen eller adjuvans, vil de vandre til lymfeknuter og sette i gang T-celleresponser der. Det er også mulig at antigener kan tas opp av epitelceller. b) I tarm finnes M-celler som kan frakte antigener over epitellaget til underliggende vev, der T- og B-celleresponser igangsettes i spesialisert lymfoid vev (Peyersk plakk). Dendrittiske celler finnes også her og kan ta med vaksineantigener til drenerende lymfeknuter. B-celler vil utvikles til IgG- eller IgA-produserende plasmaceller. IgA kan transporteres til overflaten ved reseptormediert transcytose og der binde patogener slik at de ikke trenger inn i vevet. Immunologisk hukommelse etter vaksinering er resultat av langlivede T- og B-celler. Illustrasjon Ludvig A. Munthe Tidsskr Nor Lægeforen nr. 21, 2006;
37 Tabell 1 Antall deltakere (n) med serum-hai-titer 40 i prosent av totalt antall vaksinerte (N), før og etter to og fire doser med inaktivert influensa helvirusvaksine mot A/New Caledonia/20/99 (H1N1), gitt enten som nesespray med spesialinnretning (OptiMist), som konvensjonell nesespray, som nesedråper eller som munnspray Før vaksine Etter to doser Etter fire doser Administrasjonsmåte n/n % n/n % n/n % Nesespray (OptiMist) 6/ / / Nesespray (konvensjonell) 6/ / /16 94 Nesedråper 5/ / / Munnspray 5/ / /15 87 nen mot kolera bestående av hele, inaktiverte V cholerae pluss B-subenheten av koleratoksin som slimhinneadjuvans (10). Denne vaksinen, som gis peroralt sammen med bikarbonat for å hindre nedbrytning i ventrikkelen, har erstattet en lite effektiv injiserbar koleravaksine og er i dag den eneste ikkelevende slimhinnevaksinen på markedet. Til alt overmål virker den mot vanlig turistdiaré forårsaket av tarmpatogene E coli, om enn bare i noen få uker. Immunglobulin A De første forsøkene med ikke-levende slimhinnevaksiner på 1900-tallet hadde til hensikt å unngå ulemper av gjentatte injeksjoner, både lokale og generelle reaksjoner (9). Først senere ble immunapparatet kartlagt. Man erkjente da slimhinnenes evne til å skape en immunologisk barriere ved sekresjon av robuste IgA-molekyler til slimhinnenes overflate (fig 1) og at dette kunne ha betydning for senere vaksineutvikling (12). Selv om B-celler som er aktivert av vaksineantigener i ett slimhinneområde, kan nå sirkulasjonen og slå seg ned i slimhinner fjernt fra opprinnelsesstedet og gi opphav til IgA-produserende plasmaceller, har norske forskere nylig funnet holdepunkter i mennesker for at denne «homingen» av B-celler fra ett område er begrenset til visse organer (13). Dessuten diskuteres det fortsatt hvilken betydning sekresjonen av IgA-antistoffer kan ha, sammenliknet med IgG-antistoffer, som også lekker fra serum ut til slimhinnenes overflate (3, 12). Resultater av dyreforsøk her ved instituttet tyder på at lokalt produserte IgA-antistoffer som forekommer i marginale konsentrasjoner, kan ha effekter som skiller seg fra tilsvarende IgG-antistoffer i serum (14). Undersøkelsen viste at IgA i sekreter fra øvre luftveier hemmet lokal replikasjon av influensavirus etter nasal smitte, mens IgG i serum så mest ut til å ha betydning for dyrets evne til å motstå klinisk sykdom. Det kan derfor tenkes at ikke-levende slimhinnevaksiner vil kunne hindre spredningen av virus i befolkningen i større grad enn det som kan oppnås med tilsvarende injeksjonsvaksiner. Egne undersøkelser bekrefter tidligere observasjoner i forsøksdyr som har vist at slimhinnevaksiner kan brukes som et supplement til injiserbare vaksiner, idet immunresponsen i serum etter en injeksjonsvaksine ble forsterket av en tilsvarende nasal vaksine og vice versa (15). Det var overraskende å oppdage at injeksjonene, som selv ikke førte til økt sekresjon av IgA, kunne sensibilisere slimhinnene til økt IgA-produksjon ved senere revaksinering intranasalt. Partikulære formuleringer Noen av dyrene i studien som er beskrevet ovenfor (14), var immunisert intranasalt med en vaksine bestående av hele, formalininaktiverte influensavirus i saltvann uten tilsetning av adjuvans. Forut for dette var det her ved instituttet og andre steder vist at enkle formuleringer av hele, inaktiverte mikrober eller deler av dem kunne virke som slimhinnevaksiner både hos dyr og mennesker (8). I forsøksdyr var det åpenbart at slike formuleringer ikke induserte toleranse, som man kunne frykte, men immunologisk hukommelse, som ofte er en forutsetning for å oppnå tilstrekkelig immunitet ved gjentatte immuniseringer (15). Denne positive effekten av ikke-levende slimhinnevaksiner kan sannsynligvis forklares ved at mikrobenes partikkelnatur så vel som antigene egenskaper er av betydning for evnen til å skape immunitet, for eksempel ved at de imiterer tilsvarende infeksiøse partikler. Det er holdepunkter for at slike partikler på slimhinnenes overflate bringes i kontakt med immunapparatet, enten ved at de transporteres gjennom såkalte M-celler, eller ved at de fanges opp av dendrittiske celler beliggende i slimhinnens epitel (fig 1) (3, 12). Resultater av forsøk med forskjellige partikulære vaksineantigener tydet på at det ikke var noe å oppnå verken på antistoffdanning eller beskyttelse mot infeksjon ved å tilsette koleratoksin, som regnes å være den mest effektive slimhinneadjuvans (16, 17). Koleratoksin som i seg selv har antigene egenskaper, kunne til og med hemme induksjonen av antistoffer mot vaksineantigenet, noe som så ut til å representere en form for interaksjon eller konkurranse mellom koleratoksin og det partikulære antigenet (18). De partikulære antigenene kunne også virke som adjuvans for andre slimhinnevaksiner i partikulær form (16, 19) og som adjuvans for vaksine bestående av løselige proteiner (18). Nye kliniske studier Muligheten for at enkelte partikulære komponenter kunne virke som adjuvans for en ikke-levende, eller mer korrekt ikke-replikerende, nasal vaksine mot influensa, ble testet i en klinisk studie her ved instituttet (20). Det viste seg at formalininaktiverte Bordetella pertussis brukt som adjuvans ikke hadde større effekt på immunitetsutviklingen enn den enkle formuleringen bestående av bare betapropiolaktoninaktiverte influensaviruspartikler og som ble gitt fire ganger intranasalt. Disse alene førte til systemisk immunitet på linje med det som oppnås ved injeksjon. Muligens kan dette forklares ved at den enkle vaksineformuleringen er tilstrekkelig immunogen til å utnytte den immunologiske kapasiteten der hvor vaksinen er deponert, og at det ikke oppnås ytterligere effekt ved bruk av adjuvans. Dessuten har andre forskere vist at partikler med yttermembranproteiner fra meningokokker kunne virke som adjuvans for deler av influensavirus, såkalt splittvaksine, som er mindre immunogen enn hele viruspartikler (21). Men effekten på antistoffkonsentrasjonen i serum med denne vaksinen var ikke på langt nær så god som etter intramuskulær immunisering med en tilsvarende vaksine. Heller ikke tilsetning av en celluloseforbindelse registrert til bruk i nasale medikamenter for å øke klebrigheten til slimhinnen hadde noen positiv virkning på immuniteten mot influensaantigenet (20). Dette er i tråd med de observasjonene som vi tidligere har gjort i dyr, og som viste at gjentatte applikasjoner i løpet av få timer ikke hadde noen forsterkende virkning på immunresponsen (22). Observasjonene taler derfor mot at det har noe for seg å forlenge applikasjonstiden på slimhinnens overflate, for eksempel ved bruk av komponenter som øker vaksineantigenets adheranse til slimhinnens overflate (3). Andre forskningsgrupper har også kunnet påvise at enkle formuleringer av hele, ikkereplikerende influensaviruspartikler kan være immunogene i seg selv og lede til både lokal og systemisk antistoffrespons når de gis intranasalt, selv etter bare én til to immuniseringer i doser som tilsvarer dem som gis intramuskulært (23). Men for å oppnå et antistoffnivå i serum som regnes som beskyttende mot sykdom, dvs. et hemagglutinasjonshemmende (HAI) titer 40, ser det ut til at dosen må være en god del større (24). I denne siste studien fra Folkehelseinstituttet hvor det ble brukt seks ganger større doser enn ved injeksjon, kunne det oppnås et beskyttende serumnivå hos ca. 90 % av de vaksinerte etter to intranasale immuniseringer (tab 1). En liknende andel oppnådde signifikant titerstigning uavhengig av tidligere antistoffnivå. Ved å ta hensyn til at immunologisk hukommelse og eventuell boosterreaksjon kan oppnås i serum ved å øke intervallet mellom de nasale dosene til mer enn fire uker, er det mulig at denne 2820 Tidsskr Nor Lægeforen nr. 21, 2006; 126
38 MEDISIN OG VITENSKAP effekten kan økes eller at dosen kan reduseres (22). I tillegg til induksjon av antistoff i serum og sekreter førte den sistnevnte studien til en markert cellulær immunrespons målt som cytotoksiske T-celler (24). Disse funnene tyder på at nasale vaksiner ikke bare vil kunne forhindre en infeksjon, men også bidra til å bekjempe viruset etter at smitten er etablert (3). Nasal versus oral administrering I dyreforsøk var det åpenbart at intranasal immunisering med pneumokokkantigen hadde større effekt enn ved å gi vaksinen peroralt eller intragastrisk, også på IgA-produksjonen i tarmen (17). For å avklare om noe av effekten av nasale vaksiner kunne bero på stimulering av lymfoid vev tilhørende Waldeyers ring og ikke bare neseslimhinnen og lymfoid vev på bakre pharynxvegg, fikk noen forsøkspersoner i den tidligere nevnte studien (24) influensavaksinen som oral spray. Disse vaksinandene ble bedt om å åpne munnen på vidt gap, og vaksinen ble forsøkt deponert på slimhinnene i den orale delen av pharynx, inkludert tonsilleregionene. Det viste seg da at en stor del av dem som fikk vaksinen på denne måten, oppnådde serum-hai-titer 40, men som forventet kom det ikke til noen målbar antistoffrespons i nasalsekretet. De beste resultatene lokalt på slimhinnene ble oppnådd ved bruk av en egen administrasjonsinnretning utviklet av OptiNose AS, som sikret utelukkende intranasal deponering av vaksinen med lukket gane. Likevel kan det tenkes at oral deponering av vaksine vil ha en viss berettigelse fordi denne administrasjonsmåten gjør det mulig å benytte seg av formuleringer med slimhinneadjuvans som ikke kan brukes intranasalt, for eksempel derivater av de tidligere nevnte bakterielle toksinene (25). Fremtidsutsikter Fordelene ved slimhinnevaksiner er åpenbare, spesielt i forbindelse med verdensomspennende infeksjoner. Ved å utnytte potensialet for at også ikke-levende slimhinnevaksiner kan bli praktiske og økonomiske i bruk, er det sannsynlig at flere infeksjoner kan bringes under kontroll uten større risiko for individuelle eller miljømessige ulemper. Selv om omkostningene ved å satse på utviklingen av slike vaksiner vil være relativt beskjedne sett i forhold til hva som kan oppnås for store deler av verdens befolkning, er det lite trolig at industrien finner dette økonomisk interessant. I tillegg er også offentlige institusjoner i dag nødt til å prioritere ut ifra kortsiktige økonomiske vurderinger. Drivkraften i utviklingen av nye vaksiner er sannsynligvis avhengig av angst for at den rike del av verden skal rammes av alvorlige infeksjoner. Forfatterne takker Ludvig A. Munthe for bruk av figur 1. Oppgitte interessekonflikter: Bjørn Haneberg har mottatt foredragshonorar fra GlaxoSmith- Kline. Hilde Bakke har ingen interessekonflikter. Litteratur 1. Smith J, Leke R, Adams A et al. Certification of polio eradication: process and lessons learned. Bull World Health Organ 2004; 82: Haneberg B, Ørstavik I. Poliomyelitis associated with oral poliovaccine. Report on two cases. Acta Paediatr Scand 1972; 61: Neutra MR, Kozlowski PA. Mucosal vaccines: the promise and the challenge. Nat Rev Immunol 2006; 6: von Seidlein L. The need for another typhoid fever vaccine (editorial). J Infect Dis 2005; 192: Glass RI, Parashar UD. The promise of new rotavirus vaccines (editorial). N Engl J Med 2006; 354: Beyer WEP, Palache AM, de Jong JC et al. Coldadapted live influenza vaccine versus inactivated vaccine: systemic vaccine reactions, local and systemic antibody response, and vaccine efficacy. A meta-analysis. Vaccine 2002; 20: Bakke H. Strategies for making non-replicating mucosal vaccines suitable for use in humans. Doktoravhandling. Oslo: Det matematisk-naturvitenskapelige fakultet, Universitetet i Oslo, Haneberg B, Holst J. Can nonliving nasal vaccines be made to work? Expert Rev Vaccines 2002; 1: Jensen C. Active immunization against diphtheria by the combined subcutaneous and intranasal method. Proc Royal Soc Med 1937; 30: Holmgren J, Czerkinski C. Mucosal immunity and vaccines. Nat Med 2005; 11: S Ogra PL. Mucosal immunoprophylaxis: an introductory overview. I: Kiyono H, Ogra PL, McGhee JR, red. Mucosal vaccines. San Diego: Academic Press, 1996: Brandtzaeg P. Role of secretory antibodies in the defence against infections. Int J Med Microbiol 2003; 293: Johansen F-E, Baekkevold ES, Carlsen HS et al. Regional induction of adhesion molecules and chemokine receptors explains disparate homing of human B cells to systemic and mucosal effector sites: dispersion from tonsils. Blood 2005; 106: Bizanov G, Janakova L, Knapstad SE et al. Immunoglobulin A-antibodies in upper airway secretions may inhibit intranasal influenza virus replication in mice but not protect against clinical illness. Scand J Immunol 2005; 61: Bakke H, Lie K, Haugen IL et al. Meningococcal outer membrane vesicle vaccine given intranasally can induce immunological memory and booster responses without evidence of tolerance. Infect Immun 2001; 69: Berstad AKH, Andersen SR, Dalseg R et al. Inactivated meningococci and pertussis bacteria are immunogenic and act as mucosal adjuvants for nasal inactivated influenza virus vaccine. Vaccine 2000; 18: Hvalbye BKR, Aaberge IS, Løvik M et al. Intranasal immunisation with heat-inactivated Streptococcus pneumoniae protects against systemic pneumococcal infection. Infect Immun 1999; 67: Haugan A, Dao PXT, Glende N et al. Bordetella pertussis can act as adjuvant as well as inhibitor of immune responses to non-replicating nasal vaccines. Vaccine 2003; 22: Dalseg R, Holst J, Tangen T et al. Outer membrane vesicles from group B meningococci can act as mucosal adjuvant for influenza virus antigens. I: Brown F, Norrby E, Burton D et al, red. Vaccines 96: Molecular approaches to the control of infectious diseases. Cold Spring Harbor: Cold Spring Harbor Laboratory Press, 1996: Samdal HH, Bakke H, Oftung F et al. A non-living nasal influenza vaccine can induce major humoral and cellular immune responses in humans without the need for adjuvants. Human Vaccines 2005; 1: Treanor J, Nolan C, O Brien D et al. Intranasal administration of a proteosome-influenza vaccine is well-tolerated and induces serum and nasal secretions influenza antibodies in healthy human subjects. Vaccine 2006; 24: Bakke H, Setek TN, Huynh PN et al. Immunisation schedules for non-replicating nasal vaccines can be made simple by allowing time for development of immunological memory. Vaccine 2004; 22: Greenbaum E, Engelhard D, Levy R et al. Mucosal (SIgA) and serum (IgG) immunologic responses in young adults following intranasal administration of one or two doses of inactivated, trivalent antiinfluenza vaccine. Vaccine 2004; 22: Bakke H, Samdal HH, Holst J et al. Oral spray immunization may be an alternative to intranasal vaccine delivery to induce systemic antibodies but not nasal mucosal or cellular immunity. Scand J Immunol 2006; 63: van Ginkel FW, Jackson RJ, Yuki Y et al. Cutting edge: the mucosal adjuvant cholera toxin redirects vaccine proteins into olfactory tissues. J Immunol 2000; 165: Manuskriptet ble mottatt og godkjent Medisinsk redaktør Petter Gjersvik. Tidsskr Nor Lægeforen nr. 21, 2006;
39 Medisin og vitenskap tema vaksinasjon DNA fremtidens vaksine? Sammendrag Genbaserte vaksiner, såkalte DNAvaksiner, representerer en ny og lovende vaksineteknologi, der man istedenfor å inokulere med attenuerte eller inaktiverte mikrober eller deler av disse, anvender DNA som koder for ett eller flere antigener. Produksjon av antigen skjer i kroppens egne celler på en måte som likner en normal virusinfeksjon. Denne måten å vaksinere på kan indusere sterke cellulære immunresponser og muliggjør dermed beskyttelse mot, eventuelt behandling av sykdommer der tradisjonelle vaksiner har vist seg lite effektive. Imidlertid har DNA-vaksiner, til tross for lovende resultater i mus, vist seg langt mindre potente i mennesker. De første kliniske studiene på slutten av årene ga svært skuffende resultater. Denne artikkelen gir en enkel innføring i virkningsmekanismer for DNA-vaksiner og omtaler muligheter, begrensninger og strategier for å løse problemene med å overføre teknologien fra mus til menneske. Engelsk sammendrag finnes i artikkelen på Oppgitte interessekonflikter: Se til slutt i artikkelen Rune Kjeken [email protected] Inovio Biomedical Corporation Sorrento Valley Road San Diego, CA, USA Bjarne Bogen Immunologisk institutt Rikshospitalet-Radiumhospitalet og Universitetet i Oslo Iacob Mathiesen Inovio AS Forskningsveien 2a 0373 Oslo Det er sagt at intet annet helsefremmende tiltak har reddet flere menneskeliv enn innføringen av vaksiner for å forebygge sykdom. Helt siden Edward Jenner inokulerte James Phipps med kukopper i 1796, har vaksiner vært basert på bruken av svekkede eller inaktiverte mikrober eller ulike bestanddeler av disse. Tradisjonelle vaksiner har vært svært effektive mot en rekke sykdomsfremkallende bakterier og virus som poliomyelitt, kopper, kikhoste og stivkrampe, men har vært mindre vellykket i bekjempelse av infeksjonssykdommer der effektive cellulære immunresponser står sentralt, slik som hiv, tuberkulose og malaria, samt ved ulike kreftformer. Virkningsmekanismer for DNA-vaksiner Prinsippet for DNA-vaksiner ble oppdaget nærmest ved en tilfeldighet i slutten av 1980-årene da forskere med helt andre hensikter enn å ville utvikle vaksiner sprøytet inn bakterieplasmider i mus og fant at det ble utviklet sterke immunreaksjoner mot proteiner som ble produsert fra plasmidet (1, 2) (ordforklaringer er gitt i ramme 1). De første forsøkene med DNA-vaksiner i mus for 15 år siden viste at disse var særlig effektive til å stimulere nettopp den cellulære delen av immunsystemet. Dette førte til store forventninger om raskt å kunne utvikle effektiv terapeutisk eller profylaktisk behandling mot sykdommer der tradisjonelle vaksiner var kommet til kort. Ved genbasert vaksinering behandler man med små DNA-molekyler, bakterieplasmider, der det er satt inn sekvenser som koder for ett eller flere antigener (fig 1). Når plasmidet kommer inn i kroppens celler, anvendes cellens eget produksjonssystem, og det startes produksjon av det eller de kodede antigen(er). Ved at vaksinen produseres i kroppen, etterliknes en vanlig infeksjon der f.eks. virus trenger inn i celler og omprogrammerer disse til å lage virusproteiner. Fordi antigenet produseres inne i cellen, vil det effektivt kunne presenteres på MHC-klasse I-molekyler og dermed stimulere cellemedierte immunsvar (T-cellerespons). Dette er det ofte vanskelig å oppnå med tradisjonelle vaksiner (med unntak av svekkede eller attenuerte virus), der antigenene tas inn i cellen utenifra og presenteres på MHC-klasse IImolekyler, noe som først og fremst gir en humoral immunrespons (B-cellerespons) (fig 1). Siden antigenet ved DNA-vaksinering produseres inne i cellen, vil det dessuten være i sin native konfigurasjon. Dermed oppnår man også en immunrespons mot antigenet slik det virkelig forekommer in vivo. Dette kan være et problem ved en del tradisjonelle vaksiner der antigener kan denatureres under produksjonsprosessen, f.eks. som en følge av kjemisk inaktivering. Den bioteknologiske revolusjonen med muligheter til raskt og enkelt å modifisere DNA, har gjort genbaserte vaksiner til et uvurderlig forskningsverktøy i arbeidet med å «dissekere» ulike deler av immunsystemet og å øke vår kunnskap om molekylær immunologi generelt. Fra mus til menn fra suksess til fiasko De første vellykkede forsøkene med DNAvaksiner i mus ga støtet til en hektisk forskningsaktivitet. Utover i 1990-årene ble det demonstrert sterke immunresponser og beskyttelse mot en rekke patogener inkludert virus (f.eks. influensa, rabies og hepatitt B), bakterier (f.eks. Mycoplasma pulmonis, Mycobacterium tuberkulosis, Salmonella Typhi) og ulike parasitter (f.eks. Leishmania! Hovedbudskap Ved genbaserte vaksiner benyttes DNA som koder for antigener, som så produseres i kroppens egne celler og gir humorale og cellulære immunresponser DNA-vaksineteknologi kan gi rimelige og sikre vaksiner med kort utviklingsog produksjonstid DNA-vaksiner har så langt gitt skuffende resultater i kliniske tester 2964 Tidsskr Nor Lægeforen nr. 22, 2006; 126:
40 MEDISIN OG VITENSKAP og Schistosoma) (3). Også i en rekke kreftmodeller i mus viste DNA-vaksiner seg effektive, f.eks. ved kreft i bryst, pancreas, tykktarm og lunge (3). Da de første kliniske studiene med DNAvaksiner mot bl.a. hiv, influensa og multiple myelomer ble startet i slutten av 1990-årene, viste det seg imidlertid raskt at lovende resultater i mus ikke uten videre lot seg overføre til klinisk suksess i menneske. En rekke fase I-studier viste at vaksinene riktignok var meget sikre og ga få bivirkninger. Men dessverre ga de heller ingen effektiv beskyttelse. Selv når man etter hvert økte vaksinedosene til milligramnivå, så man kun moderate immunsvar hos pasienter (4). Det synes nå klart at årsaken til den manglende immunogenisitet i menneske særlig skyldes to faktorer. For det første gjør forskjeller i immunsystemet, og da særlig i repertoaret av ulike reseptorer på celleoverflaten, at DNA-vaksiner generelt er mindre potente i menneske enn f.eks. i mus (5). En like viktig årsak ligger i det nokså banale faktum at mennesket har en ganger større kroppsmasse enn en mus. I mus vil en 50 μl DNA-injeksjon i f.eks. m. quadriceps effektivt «fylle» hele muskelen og dessuten generere et betydelig vevstrykk, noe som letter opptaket av DNA inn i cellene. Det vil være vanskelig å oppskalere vaksinedoser tilvarende for å oppnå den samme effekten i mennesker, da dette ville innebære injeksjon av ml DNA-løsning. Siden DNA er store vannløselige molekyler som vanskelig krysser cellemembranen, vil en vanlig intramuskulær injeksjon av DNA føre til at bare ca. en av DNA-molekyler kommer inn i cellene (6). Resultatet er en utilstrekkelig produksjon av antigener. Strategier for å øke immunogenisiteten Nyere forskning har derfor særlig konsentrert seg om å gjøre DNA-vaksiner mer immunologisk potente, blant annet ved å utvikle metoder for mer effektiv levering inn i cellene. Mer effektiv levering En mulighet for effektiv levering av genbaserte vaksiner er å pakke disse i viruspartikler. Kombinasjonsvaksiner der man bruker DNA-vaksiner til å forberede (prime) immunsystemet for senere å styrke (boost) med virus, har vist seg å gi sterke immunsvar i en rekke dyremodeller (7). Virus er svært effektive i å komme inn cellen, og en rekke forsøk viser at bruk av virus gir svært potente immunresponser i primater. Viruspartikler kan også gi muligheten til å dirigere vaksinen til spesielle celler siden ulike virus har sitt eget utvalg av celletyper de infiserer. En svært interessant mulighet er f.eks. å benytte modifisert hiv til å uttrykke vaksineantigen direkte i ulike typer av immunceller. Hittil er imidlertid særlig adenovirus, som infiserer et svært bredt cellerepertoar, blitt benyttet, men også andre virus som f.eks. canarypoxvirus, vacciniavirus Ankara og vesikulær stomatitt-virus er blitt forsøkt. Imidlertid er produksjon av virusbaserte vektorer komplisert og kostbar. Størrelsen på viruspartiklene gjør dessuten at kun relativt små DNA-sekvenser kan pakkes, noe som legger begrensninger på vaksinedesign. Det største problemet er likevel at preimmunitet, dvs. utviklingen av immunitet mot kappeproteiner på selve viruspartikkelen, ofte gjør at viruset fjernes av immunsystemet før det får transfektert cellene og dermed levert vaksinen. Det pågår derfor en betydelig forskningsinnsats med det mål å lage virus som ikke ses av immunsystemet. De første eksemplene på slike skjulte (stealth) virus er nylig rapportert (8). Om denne strategien lykkes, har man ironisk nok også lagt grunnlaget for en teknologi som kan brukes til å produsere meget effektive biologiske våpen (9). En alternativ metode for å øke leveringseffektiviteten, er å blande DNA med ulike typer av polymerer eller mikropartikler som beskytter DNA fra degradering og/eller hjelper det inn i cellen. Særlig er forskjellige liposomformuleringer blitt forsøkt (10). Avhengig av hvilke formuleringer som brukes, oppnås også en viss adjuvant effekt ved at ulike toll-reseptorer aktiviseres (11). Mikropartikler fraktes dessuten til lokale lymfeknuter der de tas opp ved fagocytose i antigenpresenterende celler (12). Så langt har imidlertid liposomformuleringer og mikropartikler vist seg mindre potente enn bruk av viruspartikler i kliniske studier. Ved bruk av en genpistol (gene gun) skytes en «haglladning» med mikrometerstore gullpartikler dekket med DNA direkte mot huden. En fordel med bruk av genpistol er at man transefekterer antigenpresenterende langerhansceller i huden direkte. Det er også mulig å benytte metoden til å levere DNAvaksine til ulike slimhinner. Siden det er en ren fysisk metode, unngår man også en del problemer knyttet til biologiske leveringssystemer. Det er dessuten lettere å overføre resultater fra relevante dyremodeller til mennesker. Det britiske bioteknologiselskapet PowderMed har utviklet små håndholdte enheter som er velegnet til profylaktiske vaksiner, ikke minst fordi man også unngår sprøytestikksproblematikk. Bruk av genpistol har vist lovende resultater i enkelte kliniske studier, bl.a. i utprøving av genbaserte influensavaksiner (13, 14). Det er imidlertid bare mulig å levere mikrogrammengder med DNA ved hjelp av denne metoden, noe som kan vise seg å være utilstrekkelig for enkelte antigener. En annen lovende metode er elektroporering, der en bruker korte elektriske pulser for å «åpne» cellemembranen slik at DNA lettere kan komme inn i cellen. Derved oppnås ganger økning av antigenproduksjon (15). Metoden har også vist seg å ha en slags innebygd adjuvant effekt ved at det Ramme 1 Aktuelle ordforklaringer Adjuvantia er stoffer som forsterker immunresponsen mot et antigen. Mange adjuvantia virker ved å aktiver toll-reseptorer. Bakterieplasmid er små sirkulære DNA-molekyler som finnes naturlig i bakterier. Disse kan replikere seg selv uavhengig av bakteriens kromosomale DNA og finnes gjerne i mange kopier i hver bakteriecelle. Bioinformatikk refererer løselig til bruken av informatikk, statistikk, matematisk modulering m.m. for å løse komplekse biologiske problemer der store datamengder må behandles. F.eks. kan man utvikle algoritmer der man ut ifra en organismes DNA-sekvens med større eller mindre hell kan «gjette» ulike proteiners funksjon og plassering og hvilke andre proteiner de interagerer med. Av særlig interesse innen vaksineutvikling vil det være raskt å velge ut potensielle kandidatproteiner, modellere den tredimensjonale strukturen til disse og velge ut de deler av proteinet som trolig vil være mest immunogent. Cytokiner er små proteinbaserte signalstoffer som immunsystemet bruker til celle-celle- kommunikasjon. Disse kan f.eks. skilles ut lokalt for å tiltrekker immunceller til infisert vev eller som vekstsignaler som stimulerer immunceller til å vokse og dele seg. Lysosomer er organeller som fungerer som «cellens fordøyelsessystem» ved at de bryter ned proteiner, lipider og sukkerkjeder som cellene tar opp utenifra ved endocytose. Proteasomer er store proteinkomplekser lokalisert i cytosol. Proteasomets hovedfunksjon er å bryte ned cellens proteiner til mindre peptidfragmenter. Toll-reseptorer, ofte kalt toll-liknende reseptorer (toll like reseptor, TLR), er en klasse reseptorer som gjenkjenner konserverte deler av ulike patogener, som f.eks. LPS (toll-4-reseptor) og enkelt- eller dobbelttrådet RNA (toll-3-, toll-7- og toll-8-reseptorer). Ofte fører aktivering av toll-reseptorer til utskilling av ulike cytokiner, som alarmerer immunsystemet og utløser en inflammatorisk respons. oppstår en lokal inflammasjon i det behandlede området (16). Den første kliniske studien på mennesker med elektroporering for å levere en DNA-vaksine i pasienter med prostatakreft startet i 2005 et samarbeid mellom universitetet i Southampton, som Tidsskr Nor Lægeforen nr. 22, 2006;
41 Figur 1 Virkningsmekanismer for DNA-vaksine. En typisk DNA-vaksine består av et bakterieplasmid, der man har satt inn en ekstra bit DNA som koder for ett eller flere antigener, f.eks. for overflateproteiner fra et virus eller en bakterie. Foran genet er det også satt inn en promotor, vanligvis fra virus, som driver uttrykk av genene. Når DNA-vaksinen injiseres i f.eks. muskel, vil noen kopier av plasmidet tas opp i muskelceller. Her vil cellenes eget maskineri lese av den genetiske koden og produsere det tilsvarende proteinet (antigenet) intracellulært. Noe av antigenet kan brytes ned til peptidfragmenter av cellens proteasomer. Disse fragmentene presenteres på MHC- klasse I-molekyler på vertscellens celleoverflate og stimulerer CD8-positive T-celler til å igangsette en cytotoksisk (cellemediert) immunrespons. Antigenet kan også skilles ut av cellen og tas opp av antigenpresenterende celler, f.eks. makrofager og dendrittiske celler, ved endocytose eller fagocytose. Dette antigenet brytes så ned til peptidfragmenter i cellens lysosomer og resirkuleres til celleoverflaten på MHC- klasse II-molekyler, der de stimulerer CD4-positive T-celler, som i sin tur igangsetter en humoral immunrespons ved å aktivere B-celler (med antistoffer som gjenkjenner antigenet) til å dele seg og produsere antistoffer. ER = endoplasmatisk retikulum, APC = antigenpresenterende celle har utviklet selve vaksinen, og det norske biotekselskapet Inovio AS, som har utviklet metode og utstyr for levering (17). Til tross for en del bekymringer om ubehag og smerte viser foreløpige erfaringene fra denne og andre studier (18) at metoden kan benyttes uten bruk av anestesi. Det utvikles nå utstyr for å bruke elektroporering til profylaktiske vaksiner (19). Både levering til hud og til muskelsvev er mulig, og det kan leveres relativt store mengder DNA til forskjellige typer celler. Dette åpner opp for spennende muligheter siden flere ulike plasmider som koder for multiple antigener, kan leveres samtidig. I et nylig utført forsøk der vi testet en DNA-vaksine som kodet for seks forskjellige hivantigener (ca % av hivgenomet), sammen med et plasmid som kodet for interleukin-12 i primater, fant vi en gangers økning i vaksineeffektivitet, sammenliknet med konvensjonell intramuskulær injeksjon, og cellulære immunresponser tilsvarende det man tidligere har oppnådd med bruk av «virusboosting» (M. Egean og medarbeidere, personlig meddelelse). Elektroporing gjør det også mulig, som et alternativ til å benytte virus, å bruke DNA-plasmider som koder for et nesten komplett virus, slik at f.eks. muskelceller kan produsere tomme virusliknende partikler, såkalte VLP. Dette er en svært attraktiv strategi fordi DNA-vaksinens fordeler (enkel, billig, rask og sikker) kombineres med virusbaserte vaksiners svært gode immunogene egenskaper (20). Adjuvans og cytokiner DNA fra bakterier har en naturlig adjuvant effekt, fordi de inneholder umetylerte CpGsekvenser. Når immunsystemet gjenkjenner disse motivene ved hjelp av toll-9-reseptorer på dendrittiske celler, startes produksjon av blant annet interleukin-12, samt ulike interferoner som aktiviserer både det adaptive og det ikke-adaptive immunsystemet (21). Imidlertid har mennesker langt færre toll-9- reseptorer på celleoverflaten enn f.eks. mus. Dette er trolig en viktig årsak til DNA-vaksiners dårlige immunogenisitet i kliniske tester. Både tradisjonelle adjuvanter, som aluminiumfosfat (22) og genetiske varianter som å koble antigenet sammen med deler av svært immunogene toksinfragmenter, har vært prøvd med hell i ulike dyremodeller og er nå i klinisk testing. Antigenpresentasjonen kan også gjøres mer effektiv ved å koble på signalsekvenser for å dirigere antigenet til lysosomer (økt humoral respons) eller til degradering i proteasomer (økt cellulær respons). Antigenet kan også kobles til proteinsekvenser som målstyrer antigenet til antigenpresenterende celler (23, 24). Det har videre vist seg at antistoffer (25) og antistoffbaserte molekyler (vaksinemolekyler; vaccibodies) (26) kan utskilles av muskel først injisert med plasmider og deretter elektroporert. Vaksinemolekyler utskilt av muskel inneholder antigen 2966 Tidsskr Nor Lægeforen nr. 22, 2006; 126
42 MEDISIN OG VITENSKAP som målstyres mot antigenpresenterende celler. På den måten induseres kraftige immunresponser f.eks. mot tumorspesifikke antigener og proteksjon mot kreftceller (26). Identifikasjon av ulike immunmodulerende faktorer og økende forståelse av hvordan disse virker, har åpnet for muligheter til å manipulere immunresponsen. En lovende strategi for å øke effekten av DNA-vaksiner er å bruke genetisk kodede vekstfaktorer og cytokiner. Siden disse kodes på plasmider som leveres sammen med vaksinen, vil de samme cellene som uttrykker antigenet, også uttrykke vekstfaktorer og cytokiner, noe som kan øke immunresponser lokalt eller systemisk. Et eksempel på et lokalt virkende cytokin er granulocytt-makrofag-kolonistimulerende faktor (GM-CSF), som virker som en kjemoattraktant og fører til økt infiltrasjon av antigenpresenterende celler, slik som makrofager og dendrittiske celler, til det vaksinerte vevet (27). Dette har vist seg å øke humorale immunresponser (28). Flere terapeutiske DNA-baserte hivvaksiner i klinisk utprøvning omfatter nå granulocytt-makrofag-kolonistimulerende faktor. Plasmider som koder for interleukiner som f.eks. IL-2, IL-12 og IL-15, er også i klinisk testing som bestanddeler i DNA-vaksiner. Kostimulering med interleukin-12 forsterker både humoral og cellulære immunresponser i apeforsøk og øker varighet av cellulære immunsvar (29). Figur 2 Ulike trinn i utvikling og produksjon av en DNA-vaksine. Etter at et sykdomsfremkallende patogen er isolert, sekvenseres genomet, og sekvenser som koder for potensielle antigenepitoper, velges ut. Disse klones inn i en bakterivektor som deretter oppformeres i bakterier. Etter fermentering reisoleres vektoren og renses fra andre bakteriebestanddeler. Vaksinedoser kan formuleres og lagres i ulike løsninger eller som tørrstoff Sikkerhet ved bruk av DNA-vaksiner Som for annen ny teknologi har det vært reist spørsmål om sikkerheten av DNA-vaksiner. En særlig bekymring har vært muligheten for at plasmidet kan integreres i cellenes kromosomer eller overføres til arvestoff i kjønnsceller. Dyreforsøk har vist at dette neppe er et reelt problem. En viss integrasjon kan forekomme lokalt i vevet der vaksinen er blitt injisert, men i studier hvor dette har vært målbart, har integrasjonsfrekvensen vært mindre enn én tusendel av den naturlige mutasjonsraten cellene i en menneskekropp gjennomgår (6). Ved en vellykket vaksinering vil dessuten de celler som produserer antigenet, fjernes av immunsystemet på samme måten som ved en virusinfeksjon. Det har også vært bekymringer om autoimmune reaksjoner ved at det dannes antistoffer mot selve DNA-plasmidet. Dette er så langt bare blitt observert i enkelte dyreforsøk hvor man på ulike måter nettopp har forsøkt å fremtvinge en slik reaksjon. Generelt har DNA-vaksiner vist seg å ha få utilsiktede bivirkninger. I dag er Escherichia coli det vanligste produksjonssystemet for DNA-vaksiner. E coli inneholder betydelige mengder endotoksiner som f.eks. lipopolysakkarider. Et kritisk punkt i vaksineproduksjoner er derfor å rense plasmidet fra andre bakteriekomponenter. På lengre sikt vil overgang til sikrere produksjonssystemer bestående av grampositive bakterier, som f.eks. Lactobacillus lactis, gjøre at man helt unngår problemet med endotoksiner (30). Ironisk nok er lipopolysakkarider og liknende stoffer effektive adjuvantia for DNA-vaksiner dersom de gis i kontrollerte mengder. En ikke uvanlig, om enn udokumentert oppfatning, er da også at primitive produksjonsforhold, med mangelfull rensing av plasmid, faktisk var en medvirkende faktor til gode resultater med de første DNA-vaksinene. En bekymring ved bruk av plasmid-dna har vært at disse inneholder antibiotikaresistensgener som kan overføres til patogene bakterier og gjøre disse motstandsdyktige mot antibiotikabehandling. Ny vektorteknologi muliggjør produksjon av plasmider uten bruk av antibiotikaresistensgener. Denne typen plasmider vil trolig bli normen for fremtidige DNA-vaksiner (30). DNA-vaksiner rasjonelt, rimelig og raskt Foruten klare biologiske fortrinn har DNAbasert vaksineteknologi åpenbare tekniske og økonomiske fordeler. Konvensjonell vaksineutvikling er svært komplisert og kostbart, fordi produksjon, rensing og testing må tilpasses hvert enkelt produkt. Selv om også tradisjonell vaksineutvikling har dratt nytte av ny biologisk kunnskap, er slik virksomhet fortsatt i stor grad basert på empiri, prøving, feiling og ofte en god porsjon flaks. Dette reflekteres i høy grad i den lange tiden det tar å utvikle nye kommersielle vaksiner, i snitt mer enn ti år, og med en produksjonstid på 6 12 måneder. Selv for influensavaksiner løper utvikling og produksjon gjerne opp mot seks måneder. Genbaserte metoder åpner for en langt mer rasjonell tilnærming til utvikling og produksjon av vaksiner. I prinsippet kan alle DNA-vaksiner produseres på lik måte ved at samme type plasmid benyttes for forskjellige vaksiner; man bytter bare ut den biten som koder for antigenet. Dette forenkler produksjonen enormt og vil kunne gi langt rimeligere vaksiner. På lengre sikt vil det trolig også lette den regulatoriske prosessen med testing og godkjenning. Legemiddelfirmaet Merck kan nå produsere DNA-vaksiner for humant bruk til om lag 1 amerikansk dollar per dose. Det er ikke urimelig å tenke seg at kostnadene vil synke til en brøkdel av dette innen få år. DNA er dessuten svært stabilt, og en overlegen holdbarhet selv ved relativt høye temperaturer forenkler lagring og distribusjon, noe som vil kunne få særlig betydning ved bruk som profylaktiske vaksiner i den tredje verden. Den kanskje største fordelen er mulighetene for å utvikle og produsere nye vaksiner svært mye raskere. Som en slags biologisk parallell til Moors lov for doblingen av antall transistorer på databrikker, er tiden det tar for å sekvensere et bakteriegenom blitt halvert hver 23. måned de siste 15 årene. Illustrerende nok tok det flere år å knekke Tidsskr Nor Lægeforen nr. 22, 2006;
43 genkoden til hiv med dets beskjedne ni gener, mens sarsviruset ble identifisert og sekvensert i løpet av noen korte uker et tiår senere. Et typisk mikrobegenom på 2 4 kilobaser kan nå sekvenseres i løpet av en dag, og flere hundre patogengenomer er allerede tilgjengelige i ulike databaser (31). Sammen med en revolusjon innen molekylærbiologi og bioinformatikk muliggjør dette en DNA-basert vaksineplattform der man etter å ha identifisert et nytt patogen i prinsippet kan ha en vaksine klar i løpet av 3 4 uker (fig 2). Prosessen inkluderer sekvensering av patogenets genom (timer, dager), seleksjon av antigenepitoper ved hjelp av bioinformatikk (timer, dager), kloning og oppformering i bakterier (dager) og isolering, rensing, pakking og testing av DNA (dager, uker). At dette er mer enn science fiction ble demonstrert i praksis da man i et forsøk på å redde den utrydningstruede californiske kondoren ga det lille biotekselskapet Aldevron i Nord-Dakota oppdraget med å lage en DNA-basert vaksine mot Vest-Nilen-viruset. Vaksinen var klar i løpet av fire uker og ga glimrende immunresponser (32). Hiv, Legionella, Ebola og sars er alle påminnelser om at vi trolig vil oppleve flere nye infeksiøse sykdommer de nærmeste tiår (33, 34). I en stadig mer globalisert verden har også muligheten for pandemisk fugleinfluensa aktualisert behovet for en vaksineplattform som gjør det mulig å respondere svært raskt på nye utfordringer. Fremtidsutsikter fra fiasko til nøktern optimisme Vi må fremdeles vente i flere år før den første DNA-vaksinen kommer på markedet. Til tross for dette rår det nå en betydelig optimisme innen DNA-vaksinefeltet. Dette reflekteres i det faktum at det i dag pågår mer en 200 kliniske utprøvninger der DNAplasmider benyttes, omtrent en dobling fra år 2000 (35). Den økende optimismen skyldes flere faktorer. For det første synes det som om en rekke teknologiske begrensninger, som f.eks. problemer med effektiv levering av vaksiner, er i ferd med å bli løst. Videre har ny innsikt i molekylær immunologi ført til stadig forbedringer i vaksinedesign og ny forståelse av hvordan man kan modulere et mer effektivt immunsvar ved hjelp av genetiske adjuvantia. Bruk av bedre og mer uensartede dyremodeller har også «bygd bro» fra mus til menneske og muliggjort en større grad av forutsigbarhet i DNA-vaksineutvikling. Men den mest oppløftende nyhet er den første DNA-vaksinen for bruk i pattedyr: Wyeths vaksine mot Vest- Nilen-virus hos hest er nå godkjent i USA. Denne vaksinen er et overbevisende eksempel på at teknologien fungerer i større dyr og er en milepæl i DNA-vaksiners noe kronglete vei fra mus til menneske. Vi takker Trond Berg for kritisk gjennomlesning av manuskriptet. Oppgitte interessekonflikter: Rune Kjeken og Iacob Mathiesen er ansatt i og har eierinteresser i Inovio Biomedical Corporation, et privateid biotekselskap med DNA-vaksiner som et hovedsatsingsområde. De er medoppfinnere på flere patentsøknader vedrørende elektroporering og DNA-vaksiner. Bjarne Bogen solgte i 2003 opphavsrettighetene for et patent til Inovio og ble betalt med aksjer, som ble innløst i Han er en av tre oppfinnere bak en patentsøknad vedrørende målstyrte vaksinemolekyler (vaccibodies). Litteratur 1. Wolff JA, Malone RW, Williams P et al. Direct gene transfer into mouse muscle in vivo. Science 1990; 247: Tang DC, devit M, Johnston SA. Genetic immunization is a simple method for eliciting an immune response. Nature 1992; 356: Donnelly JJ, Ulmer JB, Shiver JW et al. DNA vaccines. Annu Rev Immunol 1997; 15: Liu MA, Ulmer JB. Human clinical trials of plasmid DNA vaccines. Adv Genet 2005; 55: Barouch DH. Rational design of gene-based vaccines. J Pathol 2006; 208: Ledwith BJ, Manam S, Troilo PJ et al. Plasmid DNA vaccines: investigation of integration into host cellular DNA following intramuscular injection in mice. Intervirology 2000; 43: Egan MA, Megati S, Roopchand V et al. Rational design of a plasmid DNA vaccine capable of eliciting cell-mediated immune responses to multiple HIV antigens in mice. Vaccine 2006; 24: E-publisert Roberts DM, Nanda A, Havenga MJ et al. Hexonchimaeric adenovirus serotype 5 vectors circumvent pre-existing anti-vector immunity. Nature 2006; 441: Aldhous P. The accidental terrorists. New Scientists , D Souza S, Rosseels V, Denis O et al. Improved tuberculosis DNA vaccines by formulation in cationic lipids. Infect Immun 2002; 70: O Hagan DT, Singh M, Ulmer JB. Microparticles for the delivery of DNA vaccines. Immunol Rev 2004; 199: Denis-Mize KS, Dupuis M, Singh M et al. Mechanisms of increased immunogenicity for DNAbased vaccines adsorbed onto cationic microparticles. Cell Immunol 2003; 225: PowderMed. ( ). 14. Drape RJ, Macklin MD, Barr LJ et al. Epidermal DNA vaccine for influenza is immunogenic in humans. Vaccine 2006; 24: Mathiesen I. Electropermeabilization of skeletal muscle enhances gene transfer in vivo. Gene Ther 1999; 6: Babiuk S, Baca-Estrada ME, Foldvari M et al. Electroporation improves the efficacy of DNA vaccines in large animals. Vaccine 2002; 20: Tjelle TE, Mathiesen I, Kjeken R. A novel electroporation device for gene delivery in large animals and humans. Vaccine 2006; 24: E-publisert Kjeken R, Mathiesen I, Kvale D et al. Clinical evaluation of pain and muscle damage induced by electroporation of skeletal muscle in humans. Mol Ther 2004; 9 (157 suppl): Li Z, Zhang H, Fan X et al. DNA electroporation prime and protein boost strategy enhances humoral immunity of tuberculosis DNA vaccines in mice and non-human primates. Vaccine 2006; 24: E-publisert Bellier B, Dalba C, Clerc B et al. DNA vaccines encoding retrovirus-based virus-like particles induce efficient immune responses without adjuvant. Vaccine 2006; 24: Tudor D, Dubuquoy C, Gaboriau V. TLR9 pathway is involved in adjuvant effects of plasmid DNAbased vaccines. Vaccine 2005; 23: Ulmer JB, DeWitt CM, Chastain M et al. Enhancement of DNA vaccine potency using conventional aluminum adjuvants. Vaccine 1999; 18: Lunde E, Western KH, Rasmussen IB et al. Efficient delivery of T cell epitopes to APC by use of MHC class II-specific Troybodies. J Immunol 2002; 168: Rasmussen IB, Lunde E, Michaelsen TE et al. The principle of delivery of T cell epitopes to antigen-presenting cells applied to peptides from influenza virus, ovalbumin, and hen egg lysozyme: implications for peptide vaccination. Proc Natl Acad Sci 2001; 98: Tjelle TE, Corthay A, Lunde E et al. Monoclonal antibodies produced by muscle after plasmid injection and electroporation. Mol Ther 2004; 9: Fredriksen AB, Sandlie I, Bogen B. DNA vaccines increase immunogenicity of idiotypic tumor antigen by targeting novel fusion proteins to antigenpresenting cells. Mol Ther 2006; 13: Haddad D, Ramprakash J, Sedegah M et al. Plasmid vaccine expressing granulocyte-macrophage colony-stimulating factor attracts infiltrates including immature dendritic cells into injected muscles. J Immunol 2000; 165: Barouch DH, Santra S, Tenner-Racz K et al. Potent CD4+ T cell responses elicited by a bicistronic HIV-1 DNA vaccine expressing gp120 and GM- CSF. J Immunol 2002; 168: Egan MA, Chong SY, Megati S et al. Priming with plasmid DNAs expressing interleukin-12 and simian immunodeficiency virus gag enhances the immunogenicity and efficacy of an experimental AIDS vaccine based on recombinant vesicular stomatitis virus. AIDS Res Hum Retroviruses 2005; 21: Glenting J, Wessels S. Ensuring safety of DNA vaccines. Microb Cell Fact 2005; 4: De Groot AS, Rappuoli R. Genome-derived vaccines. Expert Rev Vaccines 2004; 3: West Nile virus vaccine. ( ). 33. Rappuoli R. From Pasteur to genomics: progress and challenges in infectious diseases. Nat Med 2004; 10: Forde GM. Rapid-response vaccines does DNA offer a solution? Nat Biotechnol 2005; 23: Gene therapy clinical trials worldwide. co.uk/genetherapy/clinical/ ( ). Manuskriptet ble mottatt og godkjent Medisinsk redaktør Petter Gjersvik Tidsskr Nor Lægeforen nr. 22, 2006; 126
44 MEDISIN OG VITENSKAP Kreftvaksiner Sammendrag Immunterapi av kreft er prinsipielt attraktivt fordi behandlingsformen kan utnytte immunsystemets spesifisitet og systemiske rekkevidde. Tumorceller uttrykker en rekke muterte eller overuttrykte antigener, noe som gjør det mulig for immunsystemet å skille mellom tumorceller og normale celler. Ved kreftvaksiner benytter man tumorassosierte antigener til å stimulere pasientens immunceller. I klinisk sammenheng vil individuelle forskjeller være av sentral betydning. Det hevdes at majoriteten av tumorantigener er unike for den enkelte pasient. Genetiske forskjeller i pasientenes immunsystem medfører også at vaksineterapi i stor grad må individtilpasses. Denne artikkelen gir en kort innføring i sentrale prinsipper for tumorimmunologi og utvikling av kreftvaksiner. Videre omtales resultatene som per i dag er oppnådd i kliniske utprøvninger, med vekt på studier av peptidvaksiner og vaksiner med dendrittiske celler. Det diskuteres også aktuelle perspektiver for videre utvikling av kreftvaksiner. En rekke studier har vist at det er mulig å generere tumorspesifikke immunresponser, og bivirkningsprofilen er generelt lite problematisk. Imidlertid foreligger det begrenset dokumentasjon på klinisk effekt. Det er viktig å avklare hvorfor noen immunresponser synes å gi tumorregresjon, mens andre responser er uten klinisk betydning. Engelsk sammendrag finnes i artikkelen på Oppgitte interessekonflikter: Ingen Jon Amund Kyte [email protected] Seksjon for immunterapi Avdeling for immunologi Institutt for kreftforskning Rikshospitalet-Radiumhospitalet Montebello 0310 Oslo og Universitetet i Oslo De fleste kreftformer kan bare kureres i lokalt stadium, og det er derfor et sterkt behov for nye behandlingsformer med systemisk rekkevidde. Kirurgisk behandling og stråleterapi er av natur kun rettet mot lokalisert sykdom, mens cellegiftbehandling har begrenset spesifisitet. Immunterapi er prinsipielt attraktivt fordi behandlingsformen kan kombinere spesifisitet og systemisk rekkevidde. Det har i over 30 år vært antatt at immunsystemet beskytter mot utvikling av kreft (1). Ifølge teorien om immunovervåking blir tumorceller eliminert i tidlig fase, slik at mange krefttilløp aldri blir klinisk erkjennbare. Dette innebærer at immunsystemet er i stand til å skille tumorceller fra normale celler, hvilket er en forutsetning for spesifikk immunterapi. På den annen side vil tumorcellene i en erkjennbar svulst være immunologisk selektert (2). Ved klinisk immunterapi er man dermed stilt overfor en vanskelig utfordring: Hvordan kan man generere en effektiv immunrespons mot tumorceller som alt har unnsluppet angrepet fra immunsystemet? Svaret kan ligge i å utnytte basal immunologisk kunnskap for å oppnå optimal immunstimulering og motvirke tumorcellenes overlevelsesteknikker. Denne artikkelen gir en innføring i sentrale strategier for immunterapi av kreft. Ved infeksjonsprofylakse skilles det mellom passiv immunisering med injiserte antistoffer og aktiv immunisering (vaksinasjon) som stimulerer vertens immunforsvar. I kreftbehandling har man de senere år oppnådd lovende resultater med flere antistoffpreparater (3). Denne artikkelen omhandler vaksiner som skal stimulere vertens immunforsvar til spesifikk antitumorrespons. Forebyggende kreftvaksiner er i dag kun aktuelt ved et fåtall kreftformer, i hovedsak virusinduserte krefttyper som leverkreft (hepatitt B) og livmorhalskreft (humant papillomvirus type 16 og 18). Terapeutiske kreftvaksiner, som gis etter at kreft er diagnostisert, er derimot under utprøvning mot en rekke krefttyper. En del av de terapeutiske vaksinene kan også tenkes anvendt profylaktisk, spesielt hos pasienter med høy arvelig kreftdisposisjon. Hvordan kan immunsystemet gjenkjenne en kreftcelle? I utviklingen fra en normal celle til en tumorcelle vil det oppstå en rekke mutasjoner. Mutasjonene gir opphav til nye peptider som ikke finnes i normale celler. De tumorspesifikke peptidene blir vist frem på HLA-molekylene på tumorcellenes overflate, og T-cellene kan gjenkjenne tumorcellen ved at T- cellereseptor binder til komplekset av HLA og peptid (fig 1a). Dermed kan T-cellene skille mellom kreftceller og normale celler. Mutasjonene kan også føre til overuttrykk av normale proteiner. CD4-positive T-celler stimuleres av peptid bundet til HLA klasse II, mens CD8-positive T-celler stimuleres av peptid bundet til HLA klasse I. Kun et fåtall celletyper uttrykker HLA klasse II, og tumorceller uttrykker sjelden dette molekylet. Stimulering av CD4-positive T-celler er imidlertid sentralt for igangsetting og utvikling av immunresponser. Det er derfor avgjørende at tumorproteiner blir tatt av celler som uttrykker HLA klasse II, såkalte profesjonelle antigenpresenterende celler (dendrittiske celler, makrofager, B-celler). Den antigenpresenterende cellen kan da aktivere en tumorspesifikk CD4-positv T-celle, som i sin tur kan medvirke i aktivering av tumorspesifikke B- celler og CD8-positive T-celler. Figur 1b viser hvordan en dendrittisk celle kan ta opp tumorproteiner og stimulere tumorspesifikke CD4-positive og CD8-positive T-celler. Hvordan kan immunsystemet drepe en kreftcelle? CD8-positive T-celler kan drepe tumorceller, bl.a. ved utskilling av perforiner eller signalering gjennom binding til overflate-! Hovedbudskap Kreftvaksiner gir spesifikke immunresponser mot tumorantigener, men klinisk effekt er uavklart Kreftvaksiner har systemisk virkning, høy spesifisitet og lite bivirkninger Kreftvaksiner må tilpasses individuelle forskjeller i pasientenes tumorantigener og immunsystem Tidsskr Nor Lægeforen nr. 22, 2006; 126:
45 Figur 1 molekyler på målcellen (Fas-Fas-ligand). Spesifisiteten sikres ved at T-cellene bare binder til celler som presenterer det relevante tumorpeptidet på sine HLA-molekyler. B- cellene kan produsere antistoffer som binder til antigener på tumorcellenes overflatemembran. Antistoffbinding kan bl.a. stimulere komplimentsystemet eller fasilitere tumordrap via naturlige drepeceller som uttrykker antistoffreseptor (Fc-reseptor). Ved immunologisk aktivering vil både makrofager, dendrittiske celler, CD4-positive T-celler og CD8-positive T-celler produsere en rekke cytokiner som driver immunresponsen videre. Enkelte cytokiner, som TNF-α og interferon-γ, kan også ha direkte toksisk effekt på tumorcellene. Hvordan unnslipper kreftcellene immunsystemet? Tumorceller kan på ulike måter unnslippe immunforsvaret. For det første er tumorceller genetisk ustabile, og mutasjoner kan føre til at de slutter å uttrykke de tumorantigener som gjenkjennes av T-celle reseptor/-antistoff. Som nevnt uttrykker tumorceller vanligvis ikke HLA klasse II, og de gjenkjennes derfor ikke direkte av CD4-positive T-celler. Tumorceller kan dessuten slutte å uttrykke HLA klasse I og dermed bli «usynlige» også for CD8-positive T-celler. Selv om bare et fåtall tumorceller gjennomgår slike mutasjoner, vil disse cellene få en seleksjonsfordel. Videre kan tumorcellene aktivt undertrykke immunforsvaret ved produksjon av suppresjonscytokiner (f.eks. TGF-β) og aktivering av regulatoriske T-celler. Tumorcellene kan dessuten passivisere spesifikke T-celler ved at tumorpeptider (+HLA I) binder til T-cellereseptor på naive (tidligere ustimulerte) T-celler. Ved første binding til antigen trenger nemlig naive T-celler kostimulering for ikke å miste sin evne til senere å bli aktivert (fig 1b). a) Mutasjoner under utvikling av tumor fører til uttrykk av muterte proteiner. Både normale og muterte proteiner blir prosessert til peptider og presentert på tumorcellenes HLA-molekyler (klasse I). Pasientens repertoar av T-celler reagerer vanligvis ikke på kroppens egne peptider, men oppfatter de muterte peptider som fremmede. CD8-positive T-celler kan derfor gjenkjenne tumorceller ved interaksjon mellom T-cellereseptor (TCR) og peptid/hla-kompleks. b) Dendrittiske celler kan stimulere tumorspesifikke T-celler. Dendrittiske celler tar opp tumorproteiner. Prosesserte tumorpeptider blir presentert til CD4-positive T-celler på HLA klasse II (HLA II) og til CD8-positive T-celler på HLA klasse I (HLA I). T-cellene stimuleres gjennom binding av HLA/peptid til T-cellereseptor. Naive T-celler (tidligere ustimulerte) er også avhengig av to andre signaler for å bli fullverdig aktivert: 1) Signalering gjennom kostimulatoriske molekyler (bl.a. B7/CD28 som vist på figuren). 2) Interleukin-2 (IL-2)-stimulering. HLA II og kostimulatoriske molekyler uttrykkes i hovedsak kun av dendrittiske celler og andre profesjonelle antigenpresenterende celler. Disse cellene er derfor avgjørende for igangsetting av immunresponser. Ved stimulering begynner T-cellene selv å produsere store mengder IL-2. c) Peptidvaksiner er avhengig av individuelle forskjeller i HLA-ekspresjon og antigenekspresjon i tumor. I figur c) kan kun pasient I respondere på vaksinen med antitumorrespons. Pasient II har rett HLA-molekyl, slik at T-celler kan aktiveres, men vaksineantigenet er ikke uttrykt i tumor. Pasient III mangler et passende HLA-molekyl og får ingen T-celle aktivering. d) Individualisert kreftvaksine med dendrittiske celler. Dendrittiske celler lastes opp ex vivo med tumorantigener, f.eks. i form av tumorlysat eller tumor-mrna. Tumorpeptidene blir presentert til CD8-positive T-celler på HLA klasse I og til CD4 positive T-celler på HLA klasse II. Det benyttes autologe dendrittiske celler, og HLA-repertoaret er derfor individtilpasset. Hvis cellene lastes opp med lysat/mrna fra pasientens egen tumor, vil alle vaksineantigener være uttrykt i pasientens tumorvev. Vaksinen er da fullstendig individualisert Tumorantigener Det er identifisert en rekke tumorassosierte antigener (4). Tabell 1 viser et utvalg av antigener som er aktuelle i kliniske studier. Det ideelle vaksineantigen bør være immunstimulerende og bredt uttrykt i tumorceller, men ikke uttrykt i normale celler. Enkelte antigener er tilnærmet tumorspesifikke. Andre antigener er svakt uttrykt i normalt vev, men betydelig overuttrykt i tumorvev. De såkalte cancer-germline-antigener er høyt uttrykt i mange kreftformer, men ikke i normalvev, med unntak av placenta og testikkel. Videre kan ulike differensieringsantigener være gode vaksinekandidater, ettersom de er vevsspesifikke. Dette gjelder i første rekke kreftformer der sykdom i det aktuelle organ ikke vil ha alvorlig klinisk betydning. Eksempelvis kan prostatitt og vitiligo være akseptable bivirkninger for pasienter med henholdsvis prostatakreft og malignt melanom. Tumor kan som nevnt unnslippe immun Tidsskr Nor Lægeforen nr. 22, 2006; 126
46 MEDISIN OG VITENSKAP responsen ved at enkelte tumorceller slutter å uttrykke vaksineantigenet. Dette er ikke mulig hvis vaksineproteinet er nødvendig for videre vekst av tumor. Telomeraseproteinet antas å være uttrykt i over 85 % av solide svulster og er nødvendig for kreftcellenes evne til stadig nye celledelinger (5). Dette proteinet er således en interessant kandidat for en universell kreftvaksine, selv om proteinet også i noen grad er uttrykt i normale stamceller. Individtilpassede vaksiner Valg av kreftvaksine kan ikke kun foretas ut fra diagnosen, men må tilpasses individuelle forskjeller. For det første må vaksineantigenet være uttrykt i pasientens tumor (fig 1c). De kjente tumorantigener er kun uttrykt hos en viss andel av pasientene. Videre er T-cellenes spesifisitet ikke kun knyttet til antigenet, men også til HLA-molekylet. Det er stor variasjon i HLA-molekylene fra menneske til menneske, og et vaksinepeptid kan bare stimulere T-celler hos de pasientene som har matchende HLA-type (fig 1c). Pasienter med samme kreftform kan altså ha behov for forskjellige vaksinepeptider på bakgrunn av individuell ekspresjon av tumorantigener og HLA-molekyler. På den annen side er mange tumorantigener uttrykt i flere kreftformer, slik at samme vaksinepeptid kan anvendes på pasienter med ulike diagnoser. Ved kreftvaksiner blir betydningen av individuelle forskjeller lett å se fordi virkningsmekanismene er godt klarlagt. Situasjonen er oftest annerledes ved behandling med cytostatika. I mange tilfeller kjenner man da kun effekten i diagnosegruppen som helhet og har små muligheter til å forutsi hvilke enkeltindivider som vil ha nytte av behandlingen. Tabell 1 Et utvalg av tumorantigener som anvendes i kreftvaksiner. Vanligvis benyttes ikke hele proteinet, men peptider som inneholder aminosyresekvenser som lett gjenkjennes av T-cellereseptor. Cancer-germline-antigener er uttrykt i en rekke kreftformer samt i normalt testikkel- og placentavev MAGE-1 MAGE-3 NY-ESO-1 Cancer-germline Cancer-germline Cancer-germline Kliniske studier med peptidvaksiner Den første studien med peptidvaksinasjon av kreftpasienter ble utført på Rikshospitalet i 1995 (6), og det er nå rapportert flere hundre kliniske studier. Peptidene injiseres oftest intradermalt. For å imøtegå HLA-variasjon i pasientpopulasjonen, søker man å finne frem til peptider som kan presenteres effektivt på flere ulike HLA-molekyler. Generelt observeres lite bivirkninger, og mange studier påviser spesifikke immunresponser hos en stor andel av pasientene (7 9). De kliniske responser er ofte mindre overbevisende. Det er også vanskelig å trekke konklusjoner mht. klinisk effekt fordi det i hovedsak er utført mindre og ikke-randomiserte utprøvninger (fase I og II). Likevel observeres i flere studier en assosiasjon mellom immunrespons og tumorrespons og/eller overlevelse (8 10). Dette innebærer at pasientene som får immunrespons, synes å ha en mer fordelaktig klinisk utvikling. En slik assosiasjon er oppløftende, men beviser ingen årsakssammenheng. Det er ikke mulig å utelukke at pasientene som utviklet immunrespons, ville ha fått et gunstigere klinisk forløp også uten vaksinasjon. Generelt indikerer resultatene at det er langt lettere å utløse en immunologisk respons enn å oppnå betydelige kliniske effekter (11). Dette kan delvis skyldes at de fleste studier er utført på pasienter med svært avansert sykdom. Muligheten for klinisk effekt vil trolig være bedre hvis vaksiner gis til pasienter med liten tumormasse, for eksempel som adjuvant terapi etter stråling eller kirurgiske inngrep. I denne sammenheng viser en fersk studie fra Radiumhospitalet og Ullevål universitetssykehus interessante resultater. Her ble 20 pasienter med bukspyttkjertelkreft operert og samtidig behandlet med en peptidvaksine (mutert ras). Ved langtidsoppfølging har man nå funnet at fem av 20 pasienter er i live etter 8 10 år. Videre er det påvist at to av pasientene fortsatt har spesifikke immunresponser mot vaksinepeptidet (upubliserte data; Gustav Gaudernack, personlig meddelelse). Det arbeides med ulike strategier for å oppnå forsterket vaksinerespons. Tumorpeptider kan bl.a. lastes opp på dendrittiske celler ex vivo, som beskrevet nedenfor, eller kombineres med cytokiner eller andre adjuvantia (12). Av særlig interesse er substanser som kan stimulere dendrittiske celler in vivo, til økt peptidopptak, migrasjon til lymfeknuter og forsterket T-celleaktivering. Dendrittiske celler kan bl.a. stimuleres via membranbundne og intracellulære toll-liknende reseptorer (TLR). Speiser og medarbeidere rapporterte i 2005 lovende vaksineresponser ved bruk av en TLR-9-agonist (CpG) (13). Ved Radiumhospitalet evalueres nå i pågående studier effekten av en TLR-7-agonist (imiquimod). Vaksiner med dendrittiske celler Dendrittiske celler regnes som de mest potente antigenpresenterende cellene og har en Kreftform K-ras (mutert) Tumorspesifikt Pancreas, colon MUC-1 (endret glykosylering) Tumorspesifikt Adenokarsinomer Melanom, sarkom, lunge, prostata, mamma p53 Mutert/overuttrykt Alle krefttyper HER 2/neu Overuttrykt Ovarie, mamma htert Overuttrykt Alle krefttyper Survivin Overuttrykt Alle krefttyper PSMA Overuttrykt Prostata CEA Overuttrykt Colon, mamma, pancreas, lunge Melan A/MART-1 Vevsspesifikt Melanom Tyrosinase Vevsspesifikt Melanom gp100 Vevsspesifikt Melanom PSA Vevsspesifikt Prostata avgjørende rolle ved igangsetting av immunresponser (14, 15). De senere år er det utviklet teknikker for å generere store mengder autologe dendrittiske celler ex vivo, fra pasientens monocytter (16) eller CD34-positive beinmargsceller (10). Videre er det etablert effektive metoder for å laste opp dendrittiske celler med antigen. Dermed kan man i laboratoriet produsere dendrittiske celler som effektivt presenterer tumorantigener (fig 1d). Tanken er at vaksinasjon med slike celler vil gi en kraftigere immunstimulering enn bruk av vaksinepeptider alene. De første vaksinestudiene med dendrittiske celler viste interessante resultater (16, 17). Nestle og medarbeidere behandlet melanompasienter med dendrittiske celler lastet opp med tumorlysat eller en cocktail av flere peptider. Studien påviste spesifikke immunresponser mot vaksineantigener i 11 av 16 pasienter og objektiv tumorregresjon hos fem pasienter. Senere er det påvist immunologiske responser i en lang rekke kliniske studier (11), og bivirkningsprofilen er generelt lite problematisk. Flere undersøkelser indikerer dessuten en assosiasjon mellom immunrespons og klinisk respons (10, 18, 19). Slike assosiasjoner er som nevnt ikke ensbetydende med årsakssammenheng, og det er behov for større randomiserte studier for å bedømme de kliniske effekter. Dendrittiske celler for vaksine må produseres individuelt for hver pasient, ettersom HLA-variasjonene medfører at kun pasientens egne celler vil fungere in vivo. Produksjonsprosessen blir dermed mer omstendelig. På den annen side kan man benytte vaksineantigener som blir naturlig prosessert i cellene (f.eks. proteiner eller mrna). Da kan hele pasientens HLA-repertoar utnyttes til rekruttering av T-celler, og det vil ikke være behov for HLA-screening (fig 1d). Tumorantigenene kan bli presentert på både HLA klasse I og HLA klasse II (20), og så Tidsskr Nor Lægeforen nr. 22, 2006;
47 vel CD4-positive som CD8-positive T-celler kan bli stimulert (19, 21). Dette antas å være av stor betydning for en effektiv immunrespons (15). Det arbeides med å optimalisere fenotypen av dendrittiske celler for vaksineformål. Mens de første kreftstudiene brukte såkalt umodne dendrittiske celler (16), benyttes nå ulike stimulatoriske agenser for å «modne» cellene slik at de får større uttrykk av HLA og kostimulatoriske molekyler (14). Modne dendrittiske celler gir en kraftigere T-cellestimulering og bidrar til gunstigere differensiering av de stimulerte T-cellene. Ved tumorresponser er det ønskelig at differensieringen styres i retning av en cytotoksisk T-cellerespons, og at man unngår utvikling av regulatoriske T-celler. Dendrittiske celler kan imidlertid også tenkes anvendt i vaksiner mot autoimmune sykdommer. Til dette formål utvikler man dendrittiske celler som er egnet til å dempe de aktuelle immunresponser. De fleste studier har benyttet dendrittiske celler lastet opp med peptider, proteiner eller tumorlysater. Et annet interessant alternativ er fusjon av dendrittiske celler med tumorceller (22). Dendrittiske celler kan også lastes opp med antigen i form av DNA, men dette er foreløpig mindre aktuelt i pasientbehandling, bl.a. fordi DNA-integrasjon i vertens genom kan forårsake varige genetiske forandringer. RNA blir raskt nedbrutt og anses som tryggere for klinisk bruk. De senere år har forbedrede transfeksjonsmetoder aktualisert bruk av RNA (23). Ved Radiumhospitalet anvendte vi nylig dendrittiske celler transfektert med tumor-mrna i to kliniske studier, utført på pasienter med prostatakreft eller malignt melanom (19, 24). Totalt er det nå rapportert ni vaksinestudier med RNA-transfekterte dendrittiske celler (25). Det utvikles også metoder for å laste opp dendrittiske celler med tumorantigener in vivo (26). Dette kan eksempelvis gjøres med målstyrte antistoffer som inneholder T-celleepitoper og spesifikt binder til overflatemolekyler på antigenpresenterende celler (27). Alternativt kan tenkes elektropermeabilisering in vivo etter injeksjon av antigen (28). Aktuelle perspektiver Valg av vaksineantigen Som nevnt har man identifisert en rekke tumorassosierte antigener, og disse kan benyttes både i form av peptider, proteiner og RNA. En kreftsvulst er imidlertid ofte genetisk ustabil og derfor heterogen mht. antigenekspresjon. Ved vaksiner mot definerte tumorantigener risikerer man at tumor unnslipper fordi enkelte kreftceller ikke uttrykker det anvendte vaksineantigen. Spekteret av vaksineantigener kan økes ved kombinasjon av flere peptider (10) eller utvides kraftig ved bruk av totalt tumormateriale fra allogene kreftcellelinjer (19, 29) eller autolog tumor (24, 30). Pasientens egen tumor synes å representere en særlig attraktiv antigenkilde. Det hevdes at majoriteten av tumorantigener er unike for hver enkelt pasient (31 33). De individuelle antigener antas å oppstå som følge av tilfeldige mutasjoner under utvikling av tumor. Siden flertallet av mutasjoner ikke har avgjørende betydning for kreftutviklingen, er det rimelig å anta at mange muterte antigener ikke vil gjenfinnes hos andre pasienter. Hvis man transfekterer pasientens egne dendrittiske celler med pasientens eget tumormateriale, vil vaksinen være fullstendig individualisert (fig 1d). Det er da verken behov for å undersøke antigenekspresjon i tumor eller HLA-ekspresjon. I prinsippet er en slik vaksine både unik for hver pasient og anvendbar for enhver kreftform. På Radiumhospitalet benyttet vi autolog tumor som antigenkilde i den nevnte vaksinestudien på melanompasienter (24). Autologt tumorvev av god kvalitet kan imidlertid være vanskelig tilgjengelig, og det er også andre ulemper knyttet til bruk av totalt tumormateriale i vaksiner. De fleste inkluderte antigener vil være ukjente, til forskjell fra vaksiner som baseres på definerte tumorantigener. Den immunologiske responsen kan derfor ikke karakteriseres like inngående. Dessuten inkluderes er stort antall autoantigener, noe som kan medføre økt risiko for autoimmun sykdom. Erfaring fra en rekke kliniske studier indikerer likevel at bivirkninger i liten grad forekommer (25). Mottrekk mot tumortoleranse Et velfungerende immunsystem er avhengig av balanse mellom aktiverende og dempende mekanismer, og immunologisk toleranse er avgjørende for beskyttelse mot autoimmunitet. Ved de fleste kreftvaksiner er imidlertid bivirkningsprofilen uproblematisk. Utfordringen ligger i å forsterke responsene slik at det oppnås klinisk effekt. I kreftforskningen er det derfor stor interesse for metoder som kan motvirke tumortoleranse. Regulatoriske CD25-positive CD4positive T-celler (Treg) antas å undertrykke den immunologiske respons mot tumor (34, 35). Det kan derfor være gunstig å bruke spesifikke agenser for å fjerne Treg forut for vaksinasjon. I en nylig publisert vaksinestudie ble det anvendt et immuntoksin som binder til Treg (IL-2-toksinkonjugat). Behandlingen resulterte både i effektiv eliminasjon av regulatoriske T-celler og forsterkede T-celleresponser mot vaksinen (30). Konvensjonell cellegiftbehandling kan også tenkes å motvirke effekten av Treg. Ved Radiumhospitalet undersøker vi nå dette spørsmålet i pågående studier hvor kreftvaksiner kombineres med cytostatika. Videre kan dendrittiske celler med en «tolerogen» cytokinprofil (økt IL-10-nivå, økt TGF-β-nivå og redusert IL-12-nivå) rekruttere cytokinproduserende Treg. Ved vaksiner basert på dendrittiske celler søker man å forhindre dette ved å optimalisere vaksinecellenes fenotype, bl.a. ved å stimulere cellene med ulike cytokiner og TLR-agonister (14). Balansen mellom immunaktivering og immunsuppresjon er ikke bare avhengig av regulatoriske T-celler. I en fysiologisk immunrespons vil aktiverte T-celler oppregulere sitt uttrykk av membranmolekylet CTLA- 4, og signalering via CTLA-4 bidrar vesentlig til at immunresponsen blir terminert. Data fra musestudier indikerer at antistoffer mot CTLA-4 kan forlenge og forsterke T- celleresponser. I klinisk sammenheng ble det nylig påvist tumorregresjon hos melanompasienter etter monoterapi med et antistoff mot CTLA-4 (36). Trolig kan anti- CTLA-4-terapi være særlig effektivt i kombinasjon med kreftvaksiner (37, 38). Uavklarte spørsmål Det er i dag en lang rekke uavklarte spørsmål med hensyn til optimalisering av kreftvaksiner. Det er behov for å bestemme hvordan vaksinene bør injiseres (intradermalt, intravenøst, intranodalt), samt dosering, frekvens og varighet av behandling. Ved vaksiner med dendrittiske celler arbeider man også med å definere ideell cellulær fenotype, antigenform og transfeksjonsmetode. Det kan synes overraskende at slike grunnleggende spørsmål ikke er avklart, til tross for at flere hundre kliniske studier er utført. Faktorer som cellulær fenotype, antigenform og transfeksjonsmetode kan undersøkes hver for seg i elegante musemodeller, men resultater fra innavlede modellmus er ikke direkte overførbare til pasienter. Translasjon til klinisk medisin viser seg å være meget komplisert. Pasientpopulasjonen er svært heterogen, og det er sjelden mulig å begrense variasjonen til en enkelt faktor. Poenget kan illustreres med et eksempel fra våre vaksinestudier med RNA-transfekterte dendrittiske celler ved Radiumhospitalet (19, 24). Vi inkluderte der en sammenlikning av to former for vaksineinjeksjon, intradermal og intranodal (ultralydveiledet i ingvinal lymfeknute). Resultatene viste en signifikant høyere responsrate i pasientgruppen som ble vaksinert intradermalt (p = 0,01). Denne gruppen viste seg imidlertid også å ha en gunstigere fenotype av de dendrittiske celler (høyere uttrykk av CD83), noe som kunne tenkes å forklare responsforskjellen. Selv om slike forstyrrende faktorer ikke observeres, er det i mindre studier alltid en fare for at ukjente faktorer spiller inn. De ulike spørsmål kan derfor bare avklares gjennom store randomiserte studier. Slike studier er svært kostnadskrevende og vanskelige å gjennomføre. Dessuten må det først dokumenteres gjennom mindre undersøkelser at behandlingen ikke er forbundet med alvorlige bivirkninger. Dette gjør det nyttig å sammenholde data fra mange mindre studier. For å muliggjøre gode sammenlikninger er det viktig at «forstyrrende» individuelle variasjoner, bl.a. i forhold til 2972 Tidsskr Nor Lægeforen nr. 22, 2006; 126
48 MEDISIN OG VITENSKAP cellulær fenotype, rapporteres detaljert når studiene publiseres. Det er også behov for å standardisere kriteriene for positiv immunrespons (39). Hva skiller respondere fra ikke-respondere? Noen pasienter synes å få en immunrespons med klinisk effekt, andre pasienter får ineffektive immunresponser og atter andre reagerer ikke immunologisk overhodet. Hvis vi kan forklare hvordan diversiteten i respons oppstår, vil det ha betydning både for hvordan kreftvaksiner bør designes og for hvilke pasienter som bør få hvilke vaksiner. For det første kan det antas at sykdomsgrad og allmenntilstand påvirker pasientens immunstatus og evne til vaksinerespons. Dessuten vil den individuelle ekspresjon av tumorantigener og HLA-molekyler være av betydning. Trolig spiller også mindre karakteriserte genetiske variasjoner en sentral rolle. Det er stor interesse for polymorfismer innen immunologiske nøkkelgener, f.eks. med hensyn til CTLA-4, toll-liknende reseptorer og diverse cytokiner. Immunsystemets kompleksitet tilsier likevel at det kan bli vanskelig å påvise sikre årsakssammenhenger mellom en genetisk variant og en immunologisk respons. I vaksinestudiene er det videre behov for å forbedre metodene for evaluering av immunrespons. Trolig vil en nærmere karakterisering av de responderende T-cellers cytokinprofil og vandringsmønster in vivo kunne belyse hvorfor noen immunresponser leder til tumorregresjon, mens andre responser synes klinisk irrelevante. Konklusjoner En rekke vaksinestudier viser at det er mulig å stimulere immunsystemet til spesifikk respons mot tumorceller. Bivirkningsprofilen er generelt lite problematisk, men det foreligger så langt begrenset dokumentasjon på klinisk effekt. De fleste studier er utført på pasienter med svært avansert sykdom. Trolig vil pasienter med mindre avansert sykdom ha bedre forutsetninger for å respondere klinisk på immunterapi, på bakgrunn av et mer intakt immunsystem og mindre tumormasse. Kreftvaksiner kan være særlig aktuelt som adjuvant terapi etter kirurgisk behandling og/eller stråling. Vaksinene har systemisk virkning og kan derfor ramme påvisbare og skjulte fjernmetastaser. Det arbeides med en rekke strategier for å forbedre kreftvaksinene. Ny viten innen basal tumorimmunologi frembringer stadig nye muligheter, men translasjon til klinisk medisin er meget komplisert. Individuelle forskjeller i pasientpopulasjonen representerer en særlig utfordring og vil trolig medføre at terapien i økende grad blir bestemt ut fra individuelle faktorer. Samlet sett gir kreftvaksineforskningen grunnlag for optimisme, men viser også at det er behov for tålmodighet og langsiktighet når klinisk terapi skal utvikles fra basal biologisk kunnskap. Litteratur 1. Burnet FM. The concept of immunological surveillance. Prog Exp Tumor Res 1970; 13: Dunn GP, Bruce AT, Ikeda H et al. Cancer immunoediting: from immunosurveillance to tumor escape. Nat Immunol 2002; 3: Ross JS, Gray K, Gray GS et al. Anticancer antibodies. Am J Clin Pathol 2003; 119: Renkvist N, Castelli C, Robbins PF et al. A listing of human tumor antigens recognized by T cells. Cancer Immunol Immunother 2001; 50: Shay JW, Bacchetti S. A survey of telomerase activity in human cancer. Eur J Cancer 1997; 33: Gjertsen MK, Bakka A, Breivik J et al. Vaccination with mutant ras peptides and induction of T-cell responsiveness in pancreatic carcinoma patients carrying the corresponding RAS mutation. Lancet 1995; 346: Rosenberg SA, Yang JC, Schwartzentruber DJ et al. Immunologic and therapeutic evaluation of a synthetic peptide vaccine for the treatment of patients with metastatic melanoma. Nat Med 1998; 4: Gjertsen MK, Buanes T, Rosseland AR et al. Intradermal ras peptide vaccination with granulocytemacrophage colony-stimulating factor as adjuvant: clinical and immunological responses in patients with pancreatic adenocarcinoma. Int J Cancer 2001; 92: Carbone DP, Ciernik IF, Kelley MJ et al. Immunization with mutant p53- and K-ras-derived peptides in cancer patients: immune response and clinical outcome. J Clin Oncol 2005; 23: Banchereau J, Palucka AK, Dhodapkar M et al. Immune and clinical responses in patients with metastatic melanoma to CD34(+) progenitor-derived dendritic cell vaccine. Cancer Res 2001; 61: Berzofsky JA, Terabe M, Oh S et al. Progress on new vaccine strategies for the immunotherapy and prevention of cancer. J Clin Invest 2004; 113: Schaed SG, Klimek VM, Panageas KS et al. T-cell responses against tyrosinase (370D) peptide in HLA*A0201+ melanoma patients: randomized trial comparing incomplete Freund s adjuvant, granulocyte macrophage colony-stimulating factor, and QS-21 as immunological adjuvants. Clin Cancer Res 2002; 8: Speiser DE, Liénard D, Rufer N et al. Rapid and strong human CD8+ T cell responses to vaccination with peptide, IFA, and CpG oligodeoxynucleotide J Clin Invest 2005; 115: O Neill DW, Adams S, Bhardwaj N. Manipulating dendritic cell biology for the active immunotherapy of cancer. Blood 2004; 104: Banchereau J, Palucka AK. Dendritic cells as therapeutic vaccines against cancer. Nat Rev Cancer 2005; 5: Nestle FO, Alijagic S, Gilliet M et al. Vaccination of melanoma patients with peptide- or tumor lysate-pulsed dendritic cells. Nat Med 1998; 4: Hsu FJ, Benike C, Fagnoni F et al. Vaccination of patients with B-cell lymphoma using autologous antigen-pulsed dendritic cells. Nat Med 1996; 2: Heiser A, Coleman D, Dannull J et al. Autologous dendritic cells transfected with prostate-specific antigen RNA stimulate CTL responses against metastatic prostate tumors. J Clin Invest 2002; Mu LJ, Kyte JA, Kvalheim G et al. Immunotherapy with allotumor mrna-transfected dendritic cells in androgen-resistant prostate cancer patients. Br J Cancer 2005; 93: Dengjel J, Schoor O, Fischer R et al. Autophagy promotes MHC class II presentation of peptides from intracellular source proteins. PNAS 2005; 102: Kyte JA, Kvalheim G, Aamdal S et al. Preclinical full-scale evaluation of dendritic cells transfected with autologous tumor-mrna for melanoma vaccination. Cancer Gene Ther 2005; 12: Gong J, Nikrui N, Chen D et al. Fusions of human ovarian carcinoma cells with autologous or allogeneic dendritic cells induce antitumor immunity. J Immunol 2000; 165: Saebøe-Larssen S, Fossberg E, Gaudernack G. mrna-based electrotransfection of human dendritic cells and induction of cytotoxic T lymphocyte responses against the telomerase catalytic subunit (htert). J Immunol Methods 2002; 259: Kyte JA, Mu LJ, Aamdal S et al. Phase I/II trial of melanoma therapy with dendritic cells transfected with autologous tumor-mrna. Cancer Gene Ther 2006; 13: E-publisert Kyte JA and Gaudernack G. Immuno-gene therapy of cancer with tumour-mrna transfected dendritic cells. Cancer Immunol Immunother 2006; 55: E-publisert Boscardin SB, Hafalla JC, Masilamani RF et al. Antigen targeting to dendritic cells elicits longlived T cell help for antibody responses. J Exp Med 2006; 203: Lunde E, Munthe LA, Vabø A et al. Antibodies engineered with IgD specificity efficiently deliver integrated T-cell epitopes for antigen presentation by B cells. Nat Biotechnol 1999; 17: Larkin J, Soden D, Collins C et al. Combined electric field and ultrasound therapy as a novel antitumour treatment. Eur J Cancer 2005; 41: Hirschowitz EA, Foody T, Kryscio R et al. Autologous dendritic cell vaccines for non-small-cell lung cancer. J Clin Oncol 2004; 22: Dannull J, Su Z, Rizzieri D et al. Enhancement of vaccine-mediated antitumor immunity in cancer patients after depletion of regulatory T cells. J Clin Invest. 2005; 115: Boczkowski D, Nair SK, Nam JH et al. Induction of tumor immunity and cytotoxic T lymphocyte responses using dendritic cells transfected with messenger RNA amplified from tumor cells. Cancer Res 2000; 60: Slingluff CL. Targeting unique tumor antigens and modulating the cytokine environment may improve immunotherapy for tumors with immune escape mechanisms. Cancer Immunol Immunother 1999; 48: Srivastava PK. Do human cancers express shared protective antigens? or the necessity of remembrance of things past. Semin Immunol 1996; 8: Curiel TJ, Coukos G, Zou L et al. Specific recruitment of regulatory T cells in ovarian carcinoma fosters immune privilege and predicts reduced survival. Nat Med 2004; 10: Sakaguchi S, Sakaguchi N, Shimizu J et al. Immunologic tolerance maintained by CD25+ CD4+ regulatory T cells: their common role in controlling autoimmunity, tumor immunity, and transplantation tolerance. Immunological Reviews 2001; 182: Ribas A, Camacho LH, Lopez-Berestein G et al. Antitumor activity in melanoma and anti-self responses in a phase I trial with the anti-cytotoxic T lymphocyte-associated antigen 4 monoclonal antibody CP-675,206. J Clin Oncol 2005; 23: Ribas A, Glaspy JA, Lee Y et al. Role of dendritic cell phenotype, determinant spreading, and negative costimulatory blockade in dendritic cell-based melanoma immunotherapy. J Immunotherapy 2004; 27: Hodi FS, Mihm MC, Soiffer RJ et al. Biologic activity of cytotoxic T lymphocyte-associated antigen 4 antibody blockade in previously vaccinated metastatic melanoma and ovarian carcinoma patients. PNAS 2003; 100: Figdor CG, De Vries IJ, Lesterhuis WJ et al. Dendritic cell immunotherapy: mapping the way. Nat Med 2004; 10: Manuskriptet ble mottatt og godkjent Medisinsk redaktør Petter Gjersvik. Tidsskr Nor Lægeforen nr. 22, 2006;
49 Vaksiner mot rusmidler Sammendrag Enkelte rusmidler, inkludert nikotin, kan bli immunogene dersom de kobles kovalent til et bærerprotein og danner et kompleks. Injeksjon av slike komplekser kan føre til forhøyede konsentrasjoner av antistoffer rettet mot rusmidlet. Dersom rusmidlet deretter inntas, vil antistoffene binde en større eller mindre del av den inntatte dose og redusere samt forsinke overgangen til hjernen. Det er særlig hos tidligere avhengige som har et sensitisert belønningssystem i hjernen, og som er avvendt fra rusmidler, at man forventer å se nytte av slik vaksinering. Ny stofftilførsel kan vekke til live latent sensitisering for bruk av stoffene, med ledsagende opplevelse av en sterk trang til stoffbruk. Dersom dette skjer hos en vaksinert, vil stoffene kunne bli bundet av sirkulerende antistoffer med redusert og forsinket overgang til hjernen. Dette vil kunne redusere trangen og forhindre ytterligere rusmiddelbruk. For nikotin og kokain har man eksperimentelle resultater som i noen grad underbygger denne hypotese. De fleste slike undersøkelser er gjort på dyr, men det foreligger også lovende funn fra forsøk med avvendte røykere og kokainbrukere når det gjelder å hindre tilbakefall til stoffbruk. Den eventuelle praktiske nytten er imidlertid ikke utredet, og bruken av vaksiner for avvenning fra stoffbruk, inkludert røyking, er i forsøksstadiet. Oppgitte interessekonflikter: Ingen Jørg Mørland [email protected] Divisjon for rettstoksikologi og rusmiddelforskning Nasjonalt folkehelseinstitutt Postboks 4404 Nydalen 0403 Oslo og Det medisinske fakultet Universitetet i Oslo Carrera og medarbeidere viste i 1995 at det var mulig å få forsøksdyr til å danne antistoffer mot kokain ved å gi kokainvaksine (1). De fant videre at slike immuniserte dyr hadde mindre uttalte sentralnervøse virkninger sammenliknet med kontrolldyr, når de ble tilført kokain. Deres studier var starten på en periode der man med økende interesse studerer hva vaksiner kan bety innen rusmiddelfeltet. Det er nå vist at injeksjon av en rekke rusmidler, inkludert nikotin, som gir tilnærmet de samme akutte og kroniske effektene i hjernens mesolimbiske-striokortikale system som andre rusmidler, koblet til større fremmedproteinmolekyler, kan gi opphav til produksjon av spesifikke antistoffer rettet mot selve det aktuelle rusmidlet. Antistoffresponsen kan foregå helt og holdent in vivo som ved vanlig aktiv immunisering ved vaksinasjon. Det er imidlertid også utviklet teknikker der antistoffproduksjonen skjer in vitro med danning av monoklonale antistoffer. Disse kan igjen brukes til passiv immunisering mot rusmidler. Slike undersøkelser har så langt bare vært gjort i dyremodeller. Bruk av monoklonale antistoffer mot rusmidler og nikotin vil derfor ikke bli nærmere gjennomgått her. Det antas imidlertid at for flere av de anvendelsesområdene for rusmiddelvaksiner som omtales, vil også bruken av monoklonale antistoffer kunne være aktuell i fremtiden. Dette vil særlig gjelde de tilfeller hvor man ønsker rask tilstedeværelse av antistoffer mot rusmidler (2, 3). Hvorfor vaksinere mot rusmidler? Når det ved vaksinasjon er dannet antistoffer mot rusmidler, vil sirkulerende rusmiddelmolekyler kunne bindes til de respektive antistoffer i større eller mindre grad. Slike rusmiddel-antistoff-komplekser med en molekylvekt på rundt Da vil ha en størrelse ( ganger det aktive stoff) som gjør at de vanskelig kan penetrere blodhjerne-barrieren og andre tilsvarende biologiske barrierer, for eksempel placenta. Derfor vil rusmiddeleffekten bli svekket i organer som på denne måten blir tilført mindre rusmiddel enn ellers (2, 3). Aktiv immunisering (vaksinasjon) har først og fremst vært forsøkt for kokain, metamfetamin, heroin og nikotin. I praksis har man tenkt seg nytte av aktiv immuniseringen for fire områder: Hindre overdoseeffekter Hindre fosterskader Hindre tilbakefall til ny storbruk hos abstinente rusmiddelavhengige eller nikotinavhengige (terapeutiske vaksiner) Hindre avhengighetsutvikling i populasjoner der faren for slik utvikling er relativt høy (profylaktisk vaksine) For det første området vil det være slik at en person som har antistoffer som binder store deler av en sirkulerende rusmiddelmengde, har større mulighet for å unngå toksiske effekter i hjernen enn en annen som ikke har denne beskyttelsen. Tilsvarende kan man også tenke seg forholdene for et foster hos en rusmiddelbrukende eller røykende gravid, med eller uten sirkulerende antistoffer. I løpet av de senere år er det vist at gjentatt bruk av de aller fleste rusmidler og nikotin fører til langvarige funksjonelle og strukturelle forandringer i det mesolimbiske-strikortikale system. Disse forandringene synes å kunne foreligge i flere år etter siste stoffbruk (4, 5). Man mener videre at disse forandringene er knyttet til en latent sensitisering av behov og motivasjon for å bruke rusmiddel. Denne latente trangen, som synes knyttet til visse morfologiske endringer i de mesolimbiske systemene, kan gjøres bevisst i form av sterk følt trang (craving) overfor stoff av minst tre forhold: generelt stress, påminnere (cues) overfor rusrelaterte personer eller situasjoner og (små) inntak av rusmid-! Hovedbudskap Rusmidler som nikotin og kokain kan bli immunogene gjennom kovalent kobling til et bærerprotein Antistoffdanning mot slike komplekser kan tenkes å hindre rusmidlets overgang til hjernen Eksperimentelle studier på dyr og mennesker gir håp om at vaksinering kan være til hjelp for å hindre tilbakefall hos avvendte røykere og kokainbrukere 2974 Tidsskr Nor Lægeforen nr. 22, 2006; 126:
50 MEDISIN OG VITENSKAP I et folkehelseperspektiv er nikotin, ved siden av alkohol, det viktigste stoffet hva gjelder avhengighet og helseskader. Foto MAY, BSIP/ GV-Press Mye forskning og utprøvning gjenstår før man kan evaluere den praktiske nytten av kokain- og heroinvaksiner. Foto Science Photo Library/ GV-Press AG del. I praksis er det oftest stress eller påminnere som medfører en «sprekk», dvs. stoffbruk. Denne bruken forsterker ytterligere trangen til gjentatt bruk ved den siste mekanismen. Vaksinering som følges av antistoffdanning vil kunne kupere denne veien til eskalert rusmiddelbruk ved at effekten av den første «sprekken» med rusmiddel reduseres eller elimineres, ettersom det inntatte stoffet ikke kommer frem til hjernen i tilstrekkelig mengde til å gi ytterligere motivasjon for rusmiddelbruk. Denne vaksineringen må foregå i god tid før en «sprekk». Avhengige vil således kunne vaksineres for å hindre ev. fremtidige tilbakefall. Bruk av profylaktisk vaksine mot rusmidler og nikotin til barn og unge kunne synes som en besnærende og effektiv forebyggingsstrategi mot rusmiddelproblemer og røyking. De vaksiner som foreligger i dag, har imidlertid flere svakheter som foreløpig ikke gjør en slik strategi aktuell. I forhold til flere stoffer er det et problem at de antistoffkonsentrasjoner som oppnås, er utilstrekkelige til å blokkere virkningen av (høye) rusdoser. Videre vil antistoffkonsentrasjonene synke raskt, slik at stadig gjentatte vaksinasjoner, kanskje 2 3 per år, måtte til. Man står da overfor en vurdering av risikoen knyttet til gjentatte vaksinasjoner i relasjon til risikoen for å utvikle fremtidig rusmiddelavhengighet. Vaksinasjon vil heller ikke motvirke unge menneskers lyst til å eksperimentere med stoff, og det finnes per i dag en rekke rusmidler der det ikke er påvist immuniseringsmuligheter. Dette er noe av grunnen til at oppmerksomheten i dag er rettet mot rusmiddelvaksiner i terapeutisk hensikt for å hindre tilbakefall hos avvendte, tidligere avhengige personer. Rusmiddelvaksinering Rusmidler har for liten molekylstørrelse (molekylvekt under Da) til å generere en immunrespons. Dersom slike stoffer kobles kovalent til et fremmed bærerprotein, som bovint serumal-bumin eller inaktivert koleratoksin, kan kroppen respondere med antistoffproduksjon. Den optimale antistoffproduksjonen vil avhenge av hvordan det lavmolekylære stoffet er orientert på overflaten av bærerproteinet. Når dette er kartlagt, må den samme koblingstypen også brukes ved revaksinasjon for å få en god boosterrespons, etter alt å dømme fordi den immunologiske hukommelsen er knyttet til strukturen av hapten-adjuvans-koblingen. Inntak av rusmidler hos et dyr eller menneske som tidligere er rusmiddelvaksinert, vil derfor ikke føre til noen ny antistoffproduksjon. Erfaringen så langt tyder videre på at revaksinering må skje med noen få måneders mellomrom for å opprettholde en oppnådd antistoffkonsentrasjon. Det er også vist at denne timingen og doseringen av ny vaksine er meget kritisk, og at man faktisk kan risikere å redusere den sirkulerende antistoffmengden ved uheldige valg av dose og vaksineringsintervall. Dette vil variere fra vaksinetype til vaksinetype og synes også å avhenge av genetiske faktorer hos den vaksinerte. Slike faktorer er antakelig også årsaken til de meget uttalte individuelle variasjoner som er registrert mht. grad av antistoffrespons av rusmiddelvaksinering. Det gjenstår betydelig forskning og utviklingsarbeid for å optimalisere og effektivisere de vaksiner som foreligger. I forsøk har de oppnådde antistoffnivåene ved vaksinering og gjentatt vaksinering vært relativt lave, slik at vanlige brukerdoser av stoff som når sirkulasjonen, ikke vil bli fullstendig bundet. Deler av dosen kan således nå sentralnervesystemet. Det er også et problem at det kreves en periode på minst 2 6 måneder med vaksinering og revaksinering før tilstrekkelig høye antistoffkonsentrasjoner oppnås. Her vil ev. monoklonale antistoffer kunne benyttes i startfasen. Terapeutisk vaksinering av rusmiddelavhengige for å hindre «sprekk» vil antakelig kreve flere års opprettholdelse av tilstrekkelige høye antistoffnivåer, ettersom både nevrobiologisk og klinisk forskning indikerer at det mesolimbiske striokortikale systemet vil være sensitisert i perioder på flere år etter siste inntak av rusmiddel. På den annen side vil én revaksinering gi antistoffnivåer av måneders varighet og ikke kreve daglig motivasjon fra pasientens side, mens bruken av andre medikamenter hos slike pasienter vil være avhengig av daglig pasientmedvirkning. Hva er oppnådd med vaksinering så langt? Dyreforsøk For nikotin er det vist at 2 4 vaksineringer over en periode på 4 8 uker gir antistoffnivåer som påvirker farmakokinetikken til nikotin som gis til vaksinerte dyr (6, 7). Ved å teste med nikotindoser som gir blodkonsentrasjoner som hos røykere, kunne man vise at vaksineringen reduserte nikotindistribusjonen til hjernen med % (6, 7). Tilsvarende reduksjon ble også funnet hos dyr som ble utsatt for gjentatt nikotineksponering (6, 7). I forsøk der det ble gitt ekstreme nikotinbelastninger som overskred bindingskapasiteten til antistoffene med nærmere 70 ganger, fikk man også en liten, men signifikant reduksjon av fordelingen av nikotin til hjernen (8). Nikotinvaksinering ble også funnet å forsinke nikotinovergangen til hjernen (2, 9). Det siste kan være av stor betydning, fordi utviklingen av de nevrobiologiske endringene i hjernen knyttet til avhengighet skjer raskere jo raskere stoffet går inn i hjernen (10). Nikotinvaksinerte dyr viser mindre dopaminfrigjøring i mesolimbiske strukturer og mindre grad av utvikling av nikotin selvadministrering enn ikke-vaksinerte dyr (2, 11). I såkalte tilbakefallsmodeller var tidligere nikotinavhengige dyr som ble vaksinert, bedre beskyttet mot tilbakefall enn de ikke vaksinerte (12). Det samme ble funnet for graden av abstinenssymptomer (13). Betydningen av nikotinvaksine mht. nikotinnivå hos rottefoster fra nikotinbehandlede mødre, er noe uklart. Reduksjon av nikotin- Tidsskr Nor Lægeforen nr. 22, 2006;
51 nivået i fosteret etter enkelttilførsel er funnet (14), mens kronisk akkumulering av nikotin i fosteret og visse nevrobiologiske virkninger ikke ble reduser (Pentel og medarbeidere, personlig meddelelse). For kokain er det vist at tre vaksineringer i løpet av fem uker medførte betydelige antistoffnivåer (1). Disse nivåene var tilstrekkelige til å redusere overgangen av kokain til hjernen med % (1, 15). Samtidig ble kokainets nevrobiologiske effekter redusert (1, 15). Kokainvaksinering er vist å ha en gunstig effekt i tilbakefallsmodeller hos vaksinerte, tidligere kokainavhengige dyr (16). Vaksinering har også vært forsøkt overfor metamfetamin i dyremodeller. Tre vaksineringer i løpet av 7 8 uker ga målbare antistoffmengder. Hos slike dyr ble metamfetaminets effekter i hjernen imidlertid ikke svekket (17). Også heroinvaksinering har vært forsøkt i dyrestudier (18, 19). Disse undersøkelsene, som ble publisert for ca. 30 år siden, har i liten grad vært fulgt opp. Problemer med å få frem en tilstrekkelig og varig antistoffrespons har vært et problem. Studier hos mennesker Nikotinvaksine fra flere produsenter er for tiden til utprøving på mennesker. Tre vaksiner har vist seg sikre med hensyn til registrerte bivirkninger så langt. Alle vaksinene har gitt antistoffrespons, men med meget store individuelle variasjoner (opptil 20 ganger). Det synes å være en viss sammenheng mellom vaksinedose og størrelsen på antistoffresponsen. Det synes også å være forskjeller mellom vaksinene mht. i hvilken grad de(t) produserte antistoff(er) binder nikotin. En av vaksinene har gitt signifikant antistoffrespons som vedvarte fire måneder etter siste vaksinering. I et placebokontrollert, dobbelblindt forsøk, der endepunktet var vedvarende røykestopp, fant man at 57 % av personene med høye antistoffkonsentrasjoner tilfredsstilte dette endepunktet i løpet av observasjonsperioden. Til sammenlikning oppnådde ca. 30 % av personene i gruppen med moderat eller lavt antistoffnivå og i placebogruppen røykestopp. Disse resultatene foreligger foreløpig bare som møtereferat (3). For kokain foreligger det en undersøkelse som viser at en vaksine kan føre til produksjon av antistoffer med høy affinitet (20). Kokainvaksinerte med kraftig antistoffrespons opplevde mindre kokainpåvirkning når de røykte standardiserte doser kokain enn vaksinerte med dårlig antistoffrespons (Haney og medarbeidere, personlig meddelelse). En helt ny undersøkelse viste at et vaksineregime med fem høye doser gitt i løpet av 12 uker resulterte i høyere antistoffnivåer enn et regime med fire lave doser over åtte uker (21). Martell og medarbeidere fant at polikliniske kokainavhengige pasienter med høye antistoffnivåer brukte mindre kokain enn pasienter med lav antistoffrespons (21). Videre utvikling Det foregår for tiden flere forsøk med både nikotin og kokainvaksiner på menneske, der sammenhengen mellom vaksinedoser, vaksineregimer og antistoffrespons studeres og med flere kliniske mål. Man er i denne sammenheng særlig opptatt av placeboeffekten. Det kan synes som om en nikotinvaksine så langt har større potensial enn kokainvaksine, fordi antistoffresponsen for nikotinvaksinene i langt større grad vil være i stand til å blokkere effektene av relevante nikotindoser enn tilsvarende for kokain. Mye forskning og utprøving gjenstår før man kan evaluere den praktiske nytten av nikotin- og kokainvaksiner. Selv med fullstendig blokade av sirkulerende nikotin og kokain mht. transport inn i hjernen, kan det tenkes at andre mekanismer, slik som stress og påminnere, kan føre til sterkt ønske om å innta stoffene, som da kanskje vil bli brukt i så høye doser at antistoffene ikke lenger vil kunne blokkere tilstrekkelig. Denne innvendingen, som kan rettes mot alle rusmiddelvaksiner, vil først kunne imøtegås når omfattende kliniske utprøvninger er gjennomført. Et annet problem ved vaksinering er at aktivt stoff som er bundet til antistoff, metaboliserer langsommere og således vil være lenger i kroppen. Dette synes å være tilfellet for nikotin. Utvikling av katalytiske antistoffer har vært forsøkt, blant annet for kokain. Binding til disse vil økte nedbrytningshastigheten for kokain. Foreløpig har ikke utviklingen av vaksiner overfor andre rusmidler enn kokain og nikotin kommet særlig langt hos mennesker. Dersom nikotin- og kokainvaksinene viser seg å ha praktisk nyttige virkninger, kan man forvente en betydelig opptrapping. Det er dessuten et tankekors at den vestlige verdens rusmiddel nr. 1, alkohol, neppe kan gjøres gjenstand for vaksineforsøk det er vanskelig å tenke seg antistoffproduksjon rettet mot en etyldel av et tenkt hapten-protein-kompleks. I et folkehelseperspektiv er nikotin og alkohol de aller viktigste stoffene hva gjelder avhengighet og helseskader, og det er altså bare for nikotin at vaksinasjon, et klassisk redskap i folkehelsearbeidet, kan tenkes å få betydning. Litteratur 1. Carrera MRA, Ashley JA, Parsons LH et al. Suppression of psychoactive effects of cocaine by active immunization. Nature 1995; 378: Pentel PR, Keyler DE. Vaccines to treat drug addiction. I: Levine MM, Kaper JB, Rappuoli R et al, red. New generation vaccines. 3. utg. New York: Marcel Dekker, Kosten T, Owens SM. Immunotherapy for the treatment of drug abuse. Pharmacol Ther 2005; 108: Volkow ND, Fowler JS, Wang G-J et al. Dopamine in drug abuse and addiction results from imaging studies and treatment implications. Mol Psychiatry 2004; 9: Spanagel R, Heilig M. Addiction and its brain science. Addiction 2005; 100: Hieda Y, Keyler DE, Ennifar S et al. Vaccination against nicotine during continued nicotine administration in rats: immunogenicity of the vaccine and effects on nicotine distribution to brain. Int J Immunopharmacol 2000; 22: Pentel PR, Malin DH, Ennifar S et al. A nicotine conjugate vaccine reduces nicotine distribution to brain and attenuates its behavioral and cardiovascular effects in rats. Pharmacol Biochem Behav 2000; 65: Tuncok Y, Hieda Y, Keyler DE et al. Inhibition of nicotine-induced seizures in rats by combining vaccination against nicotine with chronic nicotine infusion. Exp Clin Psychopharmacol 2001; 9: Satoskar SD, Keyler DE, LeSage MG et al. Tissuedependent effects of immunization with a nicotine conjugate vaccine on the distribution of nicotine in rats. Int J Immunopharmacol 2003; 3: Samaha A-N, Robinson TE. Why does the rapid delivery of drugs to the brain promote addiction? Trends Pharmacol Sci 2005; 26: Villiers SHL, Lindblom N, Kalayanov G et al. Active immunization against nicotine suppresses nicotine-induced dopamine release in the rat nucleus accumbens shell. Respiration 2002; 69: Lindblom N, de Villiers SHL, Kalayanov G et al. Active immunization against nicotine prevents reinstatement of nicotine-seeking behavior in rats. Respiration 2002; 69: Malin DH, Lake JR, Lin A et al. Passive immunization against nicotine prevents nicotine alleviation of nicotine abstinence syndrome. Pharmacol Biochem Behav 2001; 68: Keyler DE, Shoeman MG, Lesage MG et al. Maternal vaccination against nicotine reduces nicotine distribution to fetal brain in rats. J Pharmacol Exp Ther 2003; 305: Fox BS, Kantak KM, Edwards MA et al. Efficacy of a therapeutic cocaine vaccine in rodent models. Nat Med 1996; 2: Carrera MRA, Ashley JA, Zhou B et al. Cocaine vaccines; antibody protection against relapse in a rat model. Proc Natl Acad Sci 2000; 97: Byrnes-Blake KA, Carroll FI, Abraham P et al. Generation of anti-(+)methamphetamine antibodies is not empeded by (+)methamphetamine administration during active immunization of rats. Int J Immunopharmacol 2001; 1: Bonese KF, Wainer BH, Ftich FW et al. Changes in heroin self-administration by a rhesus monkey after morphine immunization. Nature 1974; 252: Killian A, Bonese K, Rothberg RM et al. Effects of passive immunization against morphine on heroin self-administration. Pharmacol Biochem Behav 1978; 9: Kosten TR, Rosen M, Bond J et al. Human therapeutic cocaine vaccine: safety and immunogenicity. Vaccine 2002; 20: Martell BA, Mitchell E, Poling J et al. Vaccine pharmacotherapy for the treatment of cocaine dependence. Biol Psychiatry 2005; 58: Manuskriptet ble mottatt og godkjent Medisinsk redaktør Petter Gjersvik Tidsskr Nor Lægeforen nr. 22, 2006; 126
NITO Bioingeniørfaglig Institutt kurs i Immunologi The Edge, Tromsø, 11. februar 2015. Generell Immunologi
 NITO Bioingeniørfaglig Institutt kurs i Immunologi The Edge, Tromsø, 11. februar 2015 Generell Immunologi Tor B Stuge Immunologisk forskningsgruppe, IMB Universitetet i Tromsø Innhold: 1. Immunsystemets
NITO Bioingeniørfaglig Institutt kurs i Immunologi The Edge, Tromsø, 11. februar 2015 Generell Immunologi Tor B Stuge Immunologisk forskningsgruppe, IMB Universitetet i Tromsø Innhold: 1. Immunsystemets
Forløp av ikke-adaptiv og adaptiv immunrespons. Mononukleære celler, metylfiolett farging
 Forløp av ikke-adaptiv og adaptiv immunrespons Mononukleære celler, metylfiolett farging 1 Nøytrofile granulocytter Gjenkjennelsesprinsipper medfødt vs. adaptiv immunitet Toll Like Receptors Mikroorganismer
Forløp av ikke-adaptiv og adaptiv immunrespons Mononukleære celler, metylfiolett farging 1 Nøytrofile granulocytter Gjenkjennelsesprinsipper medfødt vs. adaptiv immunitet Toll Like Receptors Mikroorganismer
1. Medfødt og ervervet immunitet. Karl Schenck, V2015
 1. Medfødt og ervervet immunitet Karl Schenck, V2015 Medfødt og ervervet immunforsvar Antimicrobial peptides «Alltid beredt!» Relativt uspesifikt Må aktiveres Spesifikt Komponenter av medfødt immunitet
1. Medfødt og ervervet immunitet Karl Schenck, V2015 Medfødt og ervervet immunforsvar Antimicrobial peptides «Alltid beredt!» Relativt uspesifikt Må aktiveres Spesifikt Komponenter av medfødt immunitet
Oppgave: MED1100-3_OPPGAVE2_V18_ORD
 Side 15 av 46 Oppgave: MED1100-3_OPPGAVE2_V18_ORD Del 1: Hvilke av de følgende celler uttrykker normalt (i hvilende tilstand) HLA klasse II molekyler hos mennesket? Angi de tre riktigste svarene. Fibroblaster
Side 15 av 46 Oppgave: MED1100-3_OPPGAVE2_V18_ORD Del 1: Hvilke av de følgende celler uttrykker normalt (i hvilende tilstand) HLA klasse II molekyler hos mennesket? Angi de tre riktigste svarene. Fibroblaster
Generell immunologi og immunforsvaret på 45 minutt
 Generell immunologi og immunforsvaret på 45 minutt NITO BIOINGENIØRFAGLIG INSTITUTT, Immunologi og immunologiske metoder, etterutdanningskurs 27. 28.november 2018 Kirsti Hokland bioingeniør og universitetslektor
Generell immunologi og immunforsvaret på 45 minutt NITO BIOINGENIØRFAGLIG INSTITUTT, Immunologi og immunologiske metoder, etterutdanningskurs 27. 28.november 2018 Kirsti Hokland bioingeniør og universitetslektor
Selv. Trygg Ignorere. Farlig. Fremmed. Immunsystemet: Generelt, og om allergi spesielt. Immunsystemets utfordring. Medfødte og ervervete immunsystemet
 U N I V E R S I T E T E T I B E R G E N Immunsystemet: Generelt, og om allergi spesielt Silke Appel Broegelmanns Forskningslaboratorium Klinisk Institutt 2 Universitetet i Bergen silke.appel@ Immunsystemets
U N I V E R S I T E T E T I B E R G E N Immunsystemet: Generelt, og om allergi spesielt Silke Appel Broegelmanns Forskningslaboratorium Klinisk Institutt 2 Universitetet i Bergen silke.appel@ Immunsystemets
Oppgave: MED1100-3_OPPGAVE2_H16_KONT
 Side 10 av 35 Oppgave: MED1100-3_OPPGAVE2_H16_KONT Del 1: Ola har en arvelig betinget kombinert immundefekt med mangel på både T-celler og B-celler. Ola får derfor gjentatte Hvorfor er Ola beskyttet mot
Side 10 av 35 Oppgave: MED1100-3_OPPGAVE2_H16_KONT Del 1: Ola har en arvelig betinget kombinert immundefekt med mangel på både T-celler og B-celler. Ola får derfor gjentatte Hvorfor er Ola beskyttet mot
Hva er en vaksine? Hanne Nøkleby, Nasjonalt folkehelseinstitutt
 Hva er en vaksine? Hanne Nøkleby, Nasjonalt folkehelseinstitutt Utgangspunktet Mange infeksjonssykdommer gir langvarig / livslang immunitet Vaksinering har som mål å få kroppen til å utvikle samme immunitet
Hva er en vaksine? Hanne Nøkleby, Nasjonalt folkehelseinstitutt Utgangspunktet Mange infeksjonssykdommer gir langvarig / livslang immunitet Vaksinering har som mål å få kroppen til å utvikle samme immunitet
BIOS 1 Biologi
 . Figurer kapittel 10: Menneskets immunsystem Figur s. 281 En oversikt over immunsystemet og viktige celletyper.> Immunsystemet Uspesifikt immunforsvar Spesifikt immunforsvar Ytre forsvar: hindrer mikroorganismer
. Figurer kapittel 10: Menneskets immunsystem Figur s. 281 En oversikt over immunsystemet og viktige celletyper.> Immunsystemet Uspesifikt immunforsvar Spesifikt immunforsvar Ytre forsvar: hindrer mikroorganismer
5. T cellers effektorfunksjoner
 Immunologi 3. semester, V2015 5. T cellers effektorfunksjoner Karl Schenck Institutt for oral biologi Noen typer effektor T celler 3 3 IFNg IL-4 IL-17 IL-10 TGFb TGFb IL-4 Secretory IgA Enhance mast cell
Immunologi 3. semester, V2015 5. T cellers effektorfunksjoner Karl Schenck Institutt for oral biologi Noen typer effektor T celler 3 3 IFNg IL-4 IL-17 IL-10 TGFb TGFb IL-4 Secretory IgA Enhance mast cell
Flervalgsoppgaver: Immunsystemet
 Flervalgsoppgaver - immunsystemet Hver oppgave har ett riktig svaralternativ. Immunsystemet 1 Vaksinasjon der det tilføres drepte, sykdomsfremkallende virus gir A) passiv, kunstig immunitet B) aktiv kunstig,
Flervalgsoppgaver - immunsystemet Hver oppgave har ett riktig svaralternativ. Immunsystemet 1 Vaksinasjon der det tilføres drepte, sykdomsfremkallende virus gir A) passiv, kunstig immunitet B) aktiv kunstig,
Grunnkurs C. Janne Dahle-Melhus Kommuneoverlege Sola kommune Smittevernoverlege Stavanger kommune
 Grunnkurs C Janne Dahle-Melhus Kommuneoverlege Sola kommune Smittevernoverlege Stavanger kommune 1 Hvorfor vaksinere? Muligheten til å forebygge alvorlig sykdom med stor utbredelse har vært forutsetningen
Grunnkurs C Janne Dahle-Melhus Kommuneoverlege Sola kommune Smittevernoverlege Stavanger kommune 1 Hvorfor vaksinere? Muligheten til å forebygge alvorlig sykdom med stor utbredelse har vært forutsetningen
Kua, gutten og lymfeknuten immunologiske prinsipper for vaksinasjon
 MEDISIN OG VITENSKAP Tema Vaksinasjon Medisin og vitenskap tema Vaksinasjon Kua, gutten og lymfeknuten immunologiske prinsipper for vaksinasjon 2532 7 Sammendrag Vaksiner stimulerer immunsystemet ved å
MEDISIN OG VITENSKAP Tema Vaksinasjon Medisin og vitenskap tema Vaksinasjon Kua, gutten og lymfeknuten immunologiske prinsipper for vaksinasjon 2532 7 Sammendrag Vaksiner stimulerer immunsystemet ved å
4. Antigenpresentasjon til T celler. MHC molekyler.
 Immunologi 3. semester, V2015 4. Antigenpresentasjon til T celler. MHC molekyler. Karl Schenck Institutt for oral biologi TcR og MHC molekyler Noen hovedgrupper T celler som forlater thymus T celler med
Immunologi 3. semester, V2015 4. Antigenpresentasjon til T celler. MHC molekyler. Karl Schenck Institutt for oral biologi TcR og MHC molekyler Noen hovedgrupper T celler som forlater thymus T celler med
Immunitet hos eldre. Lisbeth Meyer Næss Divisjon for smittevern. Vaksinedagene 2010
 Immunitet hos eldre Lisbeth Meyer Næss Divisjon for smittevern Vaksinedagene 2010 Andelen eldre i befolkningen øker 14 % av befolkning 12 10 8 6 4 2 2010 2020 2060 0 67-79 80- Alder Antall > 65 år 2010:
Immunitet hos eldre Lisbeth Meyer Næss Divisjon for smittevern Vaksinedagene 2010 Andelen eldre i befolkningen øker 14 % av befolkning 12 10 8 6 4 2 2010 2020 2060 0 67-79 80- Alder Antall > 65 år 2010:
Hensikten med et vaksinasjonsprogram
 Hensikten med et vaksinasjonsprogram Individuell vaksinasjon versus samfunnsrettet vaksinasjonsprogram Hanne Nøkleby Nasjonalt folkehelseinstitutt Hva skiller vaksinasjonsprogram fra annen vaksinering?
Hensikten med et vaksinasjonsprogram Individuell vaksinasjon versus samfunnsrettet vaksinasjonsprogram Hanne Nøkleby Nasjonalt folkehelseinstitutt Hva skiller vaksinasjonsprogram fra annen vaksinering?
Vaksineprinsipper og immunrespons
 Vaksineprinsipper og immunrespons - Hvordan virker vaksiner på immunforsvaret vårt? Lisbeth Meyer Næss Seniorforsker Divisjon for Smittevern Folkehelseinstituttet Nordisk naturmedisinsk fagkongress 2015
Vaksineprinsipper og immunrespons - Hvordan virker vaksiner på immunforsvaret vårt? Lisbeth Meyer Næss Seniorforsker Divisjon for Smittevern Folkehelseinstituttet Nordisk naturmedisinsk fagkongress 2015
Hvorfor er det viktig med høy vaksinasjonsdekning, og hvordan oppnå det? Hanne Nøkleby Folkehelseinstituttet Agderkonferansen 2016
 Hvorfor er det viktig med høy vaksinasjonsdekning, og hvordan oppnå det? Hanne Nøkleby Folkehelseinstituttet Agderkonferansen 2016 Hvorfor fokus på vaksinasjonsprogrammet? All vaksinasjon tar sikte på
Hvorfor er det viktig med høy vaksinasjonsdekning, og hvordan oppnå det? Hanne Nøkleby Folkehelseinstituttet Agderkonferansen 2016 Hvorfor fokus på vaksinasjonsprogrammet? All vaksinasjon tar sikte på
Immunologi 5 Effektormekanismer Trond S. Halstensen
 Immunologi 5 Effektormekanismer Trond S. Halstensen Aktivering av naive/memory T celler Th1 / Th2 konseptet Regulatoriske mekanismer T-cytotoxiske celler T-celler gjenkjenner lineære peptider presentert
Immunologi 5 Effektormekanismer Trond S. Halstensen Aktivering av naive/memory T celler Th1 / Th2 konseptet Regulatoriske mekanismer T-cytotoxiske celler T-celler gjenkjenner lineære peptider presentert
Cellebiologiske prosesser som respons på virusinfeksjon
 Cellebiologiske prosesser som respons på virusinfeksjon PBM 336 2005 Siri Mjaaland Infeksjoner - immunresponser 1 Figure 2-49 Interferoner Uspesifikk immunitet viral infeksjon stimulerer direkte produksjon
Cellebiologiske prosesser som respons på virusinfeksjon PBM 336 2005 Siri Mjaaland Infeksjoner - immunresponser 1 Figure 2-49 Interferoner Uspesifikk immunitet viral infeksjon stimulerer direkte produksjon
T celle aktivering og HLA Trond S. S. Halstensen
 T celle aktivering og HLA Trond S. S. Halstensen T-celler og Thymus T cellens identifisering av antigener Human Leukocyt Antigen (HLA) restriksjon, CD4 og CD8 Antigen prosessering: cytosol- og endocytisk
T celle aktivering og HLA Trond S. S. Halstensen T-celler og Thymus T cellens identifisering av antigener Human Leukocyt Antigen (HLA) restriksjon, CD4 og CD8 Antigen prosessering: cytosol- og endocytisk
B celler og antistoffer
 Immunologi 3. semester, V2015 Forelesning 3: B celler og antistoffer Karl Schenck Institutt for oral biologi I dag Innledning Struktur lymfeknuter og milt Migrasjon av leukocytter Primær og sekundær respons
Immunologi 3. semester, V2015 Forelesning 3: B celler og antistoffer Karl Schenck Institutt for oral biologi I dag Innledning Struktur lymfeknuter og milt Migrasjon av leukocytter Primær og sekundær respons
Institutt for biologi Faglig kontaktperson(er) under eksamen: Diem Hong Tran, mobil tlf. nr
 Side 1 av 6 Norges teknisknaturvitenskapelige universitet Fakultet for naturvitenskap og teknologi Institutt for biologi Faglig kontaktperson(er) under eksamen: Diem Hong Tran, mobil tlf. nr. 906 30 861
Side 1 av 6 Norges teknisknaturvitenskapelige universitet Fakultet for naturvitenskap og teknologi Institutt for biologi Faglig kontaktperson(er) under eksamen: Diem Hong Tran, mobil tlf. nr. 906 30 861
Vaksiner en liten historikk. Hanne Nøkleby
 Vaksiner en liten historikk Hanne Nøkleby Det begynte i Asia: Kina 3000 år f.kr: inhalasjon av pulver fra koppeskorper! Variolisiering: inokuloasjon av pustelmateriale fra lett tilfelle av kopper Kanskje
Vaksiner en liten historikk Hanne Nøkleby Det begynte i Asia: Kina 3000 år f.kr: inhalasjon av pulver fra koppeskorper! Variolisiering: inokuloasjon av pustelmateriale fra lett tilfelle av kopper Kanskje
6. Antistoffklasser og deres funksjon Komplementsystemet. Immunisering. Hypersensitivitet. Toleranse.
 Immunologi 3. semester, V2015 6. Antistoffklasser og deres funksjon Komplementsystemet. Immunisering. Hypersensitivitet. Toleranse. Karl Schenck Institutt for oral biologi Antistoffklasser og deres funksjon
Immunologi 3. semester, V2015 6. Antistoffklasser og deres funksjon Komplementsystemet. Immunisering. Hypersensitivitet. Toleranse. Karl Schenck Institutt for oral biologi Antistoffklasser og deres funksjon
'1$YDNVLQHUÃHQÃQ\ÃYDNVLQDVMRQVVWUDWHJLÃ
 '1$YDNVLQHUÃHQÃQ\ÃYDNVLQDVMRQVVWUDWHJLÃ $XGXQÃ1HUODQGÃ 'HWÃHUÃLQJHQÃWYLOÃRPÃDWÃYDNVLQHULQJÃHUÃHQÃDYÃKRYHGJUXQQHQHÃWLOÃDWÃILVNHRSSGUHWWÃ KDUÃYRNVWÃWLOÃHQÃDYÃ1RUJHVÃVW UVWHÃQ ULQJHUÃLÃO SHWÃDYÃGHÃVLVWHÃÃnUHQHÃ7UDVVÃLÃ
'1$YDNVLQHUÃHQÃQ\ÃYDNVLQDVMRQVVWUDWHJLÃ $XGXQÃ1HUODQGÃ 'HWÃHUÃLQJHQÃWYLOÃRPÃDWÃYDNVLQHULQJÃHUÃHQÃDYÃKRYHGJUXQQHQHÃWLOÃDWÃILVNHRSSGUHWWÃ KDUÃYRNVWÃWLOÃHQÃDYÃ1RUJHVÃVW UVWHÃQ ULQJHUÃLÃO SHWÃDYÃGHÃVLVWHÃÃnUHQHÃ7UDVVÃLÃ
GMO og samfunnsnytte. GMO-vurderingskriterier PGD og ukjent bærerstatus Norsk vaksineoppfinnelse
 Tidsskrift fra Bioteknologinemnda Nr. 4/2009 18. årgang GMO og samfunnsnytte GMO-vurderingskriterier PGD og ukjent bærerstatus Norsk vaksineoppfinnelse Genmodifisert sukkerbete Vi er alle «bønder» Syntetisk
Tidsskrift fra Bioteknologinemnda Nr. 4/2009 18. årgang GMO og samfunnsnytte GMO-vurderingskriterier PGD og ukjent bærerstatus Norsk vaksineoppfinnelse Genmodifisert sukkerbete Vi er alle «bønder» Syntetisk
An#bio#karesistens: Er vaksiner løsningen? Hanne Nøkleby Folkehelseins#tu;et 6. November 2015
 An#bio#karesistens: Er vaksiner løsningen? Hanne Nøkleby Folkehelseins#tu;et 6. November 2015 Mulig vaksineeffekt mot an#bio#karesistens Redusere mengden infeksjoner som krever an#bio#kabehandling Redusere
An#bio#karesistens: Er vaksiner løsningen? Hanne Nøkleby Folkehelseins#tu;et 6. November 2015 Mulig vaksineeffekt mot an#bio#karesistens Redusere mengden infeksjoner som krever an#bio#kabehandling Redusere
INNHOLD 13. SEKSJON I Introduksjon
 INNHOLD 13 SEKSJON I Introduksjon 14 SEKSJON I, INTRODUKSJON KAPITTEL 1 Innledningen til immunologien. En oversikt TEMA Medfødt og ervervet infeksjonsforsvar danner kroppens forsvar mot mikrorganismer.
INNHOLD 13 SEKSJON I Introduksjon 14 SEKSJON I, INTRODUKSJON KAPITTEL 1 Innledningen til immunologien. En oversikt TEMA Medfødt og ervervet infeksjonsforsvar danner kroppens forsvar mot mikrorganismer.
Har vi et barnevaksinasjonsprogram som virker? Marianne A. Riise Bergsaker Avdeling for vaksine Divisjon for smittevern Folkehelseinstituttet
 Har vi et barnevaksinasjonsprogram som virker? Marianne A. Riise Bergsaker Avdeling for vaksine Divisjon for smittevern Folkehelseinstituttet Vaksiner redder liv Lørdagsseminar UiO 26. april 2014 Hva er
Har vi et barnevaksinasjonsprogram som virker? Marianne A. Riise Bergsaker Avdeling for vaksine Divisjon for smittevern Folkehelseinstituttet Vaksiner redder liv Lørdagsseminar UiO 26. april 2014 Hva er
Barnevaksinasjonsprogrammet sett med folkehelsebriller
 Barnevaksinasjonsprogrammet sett med folkehelsebriller Hanne Nøkleby, Folkehelseinstituttet 27.09.2018 Hva er forskjellen på vaksinasjonsprogram og annen vaksinasjon? All vaksinasjon tar sikte på å beskytte
Barnevaksinasjonsprogrammet sett med folkehelsebriller Hanne Nøkleby, Folkehelseinstituttet 27.09.2018 Hva er forskjellen på vaksinasjonsprogram og annen vaksinasjon? All vaksinasjon tar sikte på å beskytte
Immunitet mot rubella. Hanne Nøkleby Folkehelseinstituttet Vaksinedagene 2015
 Immunitet mot rubella Hanne Nøkleby Folkehelseinstituttet Vaksinedagene 2015 Utgangspunktet: Forespørsel fra en mikrobiologisk avdeling: Hvordan skal vi tolke prøvesvar der vi finner antistoff mot rubella,
Immunitet mot rubella Hanne Nøkleby Folkehelseinstituttet Vaksinedagene 2015 Utgangspunktet: Forespørsel fra en mikrobiologisk avdeling: Hvordan skal vi tolke prøvesvar der vi finner antistoff mot rubella,
KROPPENS FORSVARSMEKANISMER
 KROPPENS FORSVARSMEKANISMER Immunitet = fri for, uberørt av Immunologi Immunsystemet Uspesifikke forsvarsmekanismer Ytre- og indre forsvarslinje Spesifikke forsvarsmekanismer Cellulære forsvar (T-celler)
KROPPENS FORSVARSMEKANISMER Immunitet = fri for, uberørt av Immunologi Immunsystemet Uspesifikke forsvarsmekanismer Ytre- og indre forsvarslinje Spesifikke forsvarsmekanismer Cellulære forsvar (T-celler)
Grunnleggende immunologi
 Grunnleggende immunologi Anne Storset [email protected] Institutt for Mattrygghet og infeksjonsbiologi Norges miljø- og biovitenskapelige universitet 1 Sykdom Ervervet immunitet Medfødt immunitet Fysiske
Grunnleggende immunologi Anne Storset [email protected] Institutt for Mattrygghet og infeksjonsbiologi Norges miljø- og biovitenskapelige universitet 1 Sykdom Ervervet immunitet Medfødt immunitet Fysiske
1 FYS3710 Immunologi
 1 2 Immunsystemet Dette kan best sammenlignes med et allestedsnærværende geriljaforsvar mot fremmede molekyler 3 Definisjoner av begreper. Infeksjon: Invasjon i kroppen av infeksiøse agens. Disse omfatter
1 2 Immunsystemet Dette kan best sammenlignes med et allestedsnærværende geriljaforsvar mot fremmede molekyler 3 Definisjoner av begreper. Infeksjon: Invasjon i kroppen av infeksiøse agens. Disse omfatter
Vaksiner før og nå (med litt om herpes zoster og ebola)
 Vaksiner før og nå (med litt om herpes zoster og ebola) Hanne Nøkleby, Nasjonalt folkehelseinstitutt Hva er vaksiner og hvordan ble de til? Litt historikk Litt om det som skjer på vaksinefeltet Litt om
Vaksiner før og nå (med litt om herpes zoster og ebola) Hanne Nøkleby, Nasjonalt folkehelseinstitutt Hva er vaksiner og hvordan ble de til? Litt historikk Litt om det som skjer på vaksinefeltet Litt om
Barnevaksinasjonsprogrammet i Norge. Marianne A. Riise Bergsaker Avdeling for vaksine Divisjon for smittevern Nasjonalt folkehelseinstitutt
 Barnevaksinasjonsprogrammet i Norge Marianne A. Riise Bergsaker Avdeling for vaksine Divisjon for smittevern Nasjonalt folkehelseinstitutt Dagsseminar om vaksinasjon av barn, Bristol 2013 Hva er forskjellen
Barnevaksinasjonsprogrammet i Norge Marianne A. Riise Bergsaker Avdeling for vaksine Divisjon for smittevern Nasjonalt folkehelseinstitutt Dagsseminar om vaksinasjon av barn, Bristol 2013 Hva er forskjellen
«Immunterapi» Kreftutvikling. Myelomatose. Immunterapi. Anders'Sundan Senter'for'myelomforskning Institutt'for'klinisk'og'molekylær'medisin,'NTNU
 «Immunterapi» Kreftutvikling Myelomatose Immunterapi Anders'Sundan Senter'for'myelomforskning Institutt'for'klinisk'og'molekylær'medisin,'NTNU 1 Kreft er genetiske sykdommer i den forstand at det alltid
«Immunterapi» Kreftutvikling Myelomatose Immunterapi Anders'Sundan Senter'for'myelomforskning Institutt'for'klinisk'og'molekylær'medisin,'NTNU 1 Kreft er genetiske sykdommer i den forstand at det alltid
Utvikling av nye vaksiner. Hanne Nøkleby, Nasjonalt folkehelseinstitutt
 Utvikling av nye vaksiner Hanne Nøkleby, Nasjonalt folkehelseinstitutt Utfordringer De vaksinene som er «lette å lage» har vi allerede De vaksinene det nå arbeides med, er vanskelige: Gjennomgått sykdom
Utvikling av nye vaksiner Hanne Nøkleby, Nasjonalt folkehelseinstitutt Utfordringer De vaksinene som er «lette å lage» har vi allerede De vaksinene det nå arbeides med, er vanskelige: Gjennomgått sykdom
Vaksinering av personer med nedsatt immunforsvar
 Vaksinering av personer med nedsatt immunforsvar FIRM konferanse Bodø 25.08.13 Eigil Gulliksen Forsvaret Stamina Bryggeklinikken Disposisjon Kort om immunsvikt Immunsvikt og vaksinering generelt Immunsvikt
Vaksinering av personer med nedsatt immunforsvar FIRM konferanse Bodø 25.08.13 Eigil Gulliksen Forsvaret Stamina Bryggeklinikken Disposisjon Kort om immunsvikt Immunsvikt og vaksinering generelt Immunsvikt
Barn påp. reise. 8. sept. 2006 Harald Hauge overlege
 Barn påp reise 8. sept. 2006 Harald Hauge overlege Risiko for alvorlig infeksjoner hos de minste barnna NORMENN PÅ REISE ÅR 2006 Ca. 1,2 mill. nordmenn dro ut av Norge juli med fly!! 1 av 3 blir syke på
Barn påp reise 8. sept. 2006 Harald Hauge overlege Risiko for alvorlig infeksjoner hos de minste barnna NORMENN PÅ REISE ÅR 2006 Ca. 1,2 mill. nordmenn dro ut av Norge juli med fly!! 1 av 3 blir syke på
Alkoholens effekter på immunsystemet
 Alkoholens effekter på immunsystemet NFRAM Jubileumskonferanse i Bodø 12.10.16. Asle Enger, klinikkoverlege Trasoppklinikken Om alkohol og økt infeksjonsrisiko «I praksis hver eneste celle i kroppen kan
Alkoholens effekter på immunsystemet NFRAM Jubileumskonferanse i Bodø 12.10.16. Asle Enger, klinikkoverlege Trasoppklinikken Om alkohol og økt infeksjonsrisiko «I praksis hver eneste celle i kroppen kan
Grunnleggende kunnskap for vaksineutvikling
 Strategisamling FHF Trondheim 1. juni 2001 Grunnleggende kunnskap for vaksineutvikling Siri Mjaaland Veterinærinstituttet / FHI Bakgrunn Virussykdommer stort problem for oppdrettsnæringen Dagens vaksiner
Strategisamling FHF Trondheim 1. juni 2001 Grunnleggende kunnskap for vaksineutvikling Siri Mjaaland Veterinærinstituttet / FHI Bakgrunn Virussykdommer stort problem for oppdrettsnæringen Dagens vaksiner
Hva er Immunterapi? Anders Sundan Senter for myelomforskning, NTNU
 Hva er Immunterapi? Anders Sundan Senter for myelomforskning, NTNU 1 3 typer immunterapi; Antistoffer som aktiverer immunforsvaret mot kreftcellene. (Anti-CTLA4, -PD1/PD1L) Antistoffer som binder kreftceller
Hva er Immunterapi? Anders Sundan Senter for myelomforskning, NTNU 1 3 typer immunterapi; Antistoffer som aktiverer immunforsvaret mot kreftcellene. (Anti-CTLA4, -PD1/PD1L) Antistoffer som binder kreftceller
Vaksinering av immunsupprimerte. Hanne Nøkleby Nasjonalt folkehelseinstitutt
 Vaksinering av immunsupprimerte Hanne Nøkleby Nasjonalt folkehelseinstitutt Tre spørsmål før vaksinering av immunsupprimerte pasienter: Kan det være farlig å vaksinere? Har vaksinen effekt? Er det behov
Vaksinering av immunsupprimerte Hanne Nøkleby Nasjonalt folkehelseinstitutt Tre spørsmål før vaksinering av immunsupprimerte pasienter: Kan det være farlig å vaksinere? Har vaksinen effekt? Er det behov
Vaksinering og vaksineskepsis i Nesodden Kommune. Liv Bertheussen Tangløkken Hagen kommuneoverlege og fastlege i Nesodden kommune
 Vaksinering og vaksineskepsis i Nesodden Kommune Liv Bertheussen Tangløkken Hagen kommuneoverlege og fastlege i Nesodden kommune Barnevaksinasjonsprogrammet *Barnevaksinasjonsprogrammet startet i 1952
Vaksinering og vaksineskepsis i Nesodden Kommune Liv Bertheussen Tangløkken Hagen kommuneoverlege og fastlege i Nesodden kommune Barnevaksinasjonsprogrammet *Barnevaksinasjonsprogrammet startet i 1952
Første Tann. Bakterie kolonisering Immunreaksjon? Streptokoccus Mut. Toleranse? IgA mot Str. Mut? IgG beskytter. Ekslusjon og toleranse?
 Første Tann Bakterie kolonisering Immunreaksjon? Streptokoccus Mut. Toleranse? IgA mot Str. Mut? IgG beskytter Ekslusjon og toleranse? Naturlig Immunitet Barrierer Hud: Fysisk sterk, Normal bakterie flora,
Første Tann Bakterie kolonisering Immunreaksjon? Streptokoccus Mut. Toleranse? IgA mot Str. Mut? IgG beskytter Ekslusjon og toleranse? Naturlig Immunitet Barrierer Hud: Fysisk sterk, Normal bakterie flora,
Innhold. Kikhoste 05.11.2015. Barnevaksinasjonsprogrammet - går det mot amerikanske tilstander?
 Barnevaksinasjonsprogrammet - går det mot amerikanske tilstander? Øystein Riise, barnelege Avd. for vaksine Divisjon for smittevern Innhold Hvorfor har vi et barnevaksinasjonsprogram? Utviklingen av programmet
Barnevaksinasjonsprogrammet - går det mot amerikanske tilstander? Øystein Riise, barnelege Avd. for vaksine Divisjon for smittevern Innhold Hvorfor har vi et barnevaksinasjonsprogram? Utviklingen av programmet
Pnemokokkvaksine i barnevaksinasjonsprogrammet
 Pnemokokkvaksine i barnevaksinasjonsprogrammet Marianne A. Riise Bergsaker, overlege Avdeling for vaksine Divisjon for smittevern Nasjonalt folkehelseinstitutt 1 Vaksinedagene 2006 Pressemelding Nr.: 5
Pnemokokkvaksine i barnevaksinasjonsprogrammet Marianne A. Riise Bergsaker, overlege Avdeling for vaksine Divisjon for smittevern Nasjonalt folkehelseinstitutt 1 Vaksinedagene 2006 Pressemelding Nr.: 5
Influensa og immunsystemet Kristin G-I Mohn HUS, Influensasenteret i Bergen 13.06.13
 Influensa og immunsystemet Kristin G-I Mohn HUS, Influensasenteret i Bergen 13.06.13 Vakkert og virulent Virus - virulens - virkning Virus replikerer i luftveiene Aerosoler smitter Hemaggluttinin (HA)
Influensa og immunsystemet Kristin G-I Mohn HUS, Influensasenteret i Bergen 13.06.13 Vakkert og virulent Virus - virulens - virkning Virus replikerer i luftveiene Aerosoler smitter Hemaggluttinin (HA)
Vaksinasjon av helsepersonell i sykehjem Hva og hvorfor?
 Vaksinasjon av helsepersonell i sykehjem Hva og hvorfor? Overlege Ragnhild Raastad Avd. for smittevern, OUS Vaksiner en forbannet velsignelse Fram til 1940 var det ikke våpen, men infeksjoner som tok
Vaksinasjon av helsepersonell i sykehjem Hva og hvorfor? Overlege Ragnhild Raastad Avd. for smittevern, OUS Vaksiner en forbannet velsignelse Fram til 1940 var det ikke våpen, men infeksjoner som tok
for overlevelse, men med risiko for kreft Fagdagene 10. juni 2010, Bodil Kavli
 Ervervet immunitetnødvendig for overlevelse, men med risiko for kreft Fagdagene 10. juni 2010, Bodil Kavli 1 Ervervet (spesifikk) immunitet Celle-mediert immunrespons Løselig immunrespons jenkjenner/ responderer
Ervervet immunitetnødvendig for overlevelse, men med risiko for kreft Fagdagene 10. juni 2010, Bodil Kavli 1 Ervervet (spesifikk) immunitet Celle-mediert immunrespons Løselig immunrespons jenkjenner/ responderer
AKTUELLE VAKSINER FOR HELSEARBEIDERE OG HVILKET TILBUD FINNES?
 AKTUELLE VAKSINER FOR HELSEARBEIDERE OG HVILKET TILBUD FINNES? Regionmøte i smittevern Solstrand 30. mai 2018 Trude Duelien Skorge Bedriftslege Bedriftshelsetjenesten i Helse Bergen Agenda 1. Bakgrunn
AKTUELLE VAKSINER FOR HELSEARBEIDERE OG HVILKET TILBUD FINNES? Regionmøte i smittevern Solstrand 30. mai 2018 Trude Duelien Skorge Bedriftslege Bedriftshelsetjenesten i Helse Bergen Agenda 1. Bakgrunn
Immunologi 6 Hypersensitivitetsmekanismer Trond S. Halstensen
 Immunologi 6 Hypersensitivitetsmekanismer Trond S. Halstensen Repetisjon av antigenpresentasjon og effektormekanismer Type I-V immunreaksjoner T-celler gjenkjenner lineære peptider presentert i HLA (Human
Immunologi 6 Hypersensitivitetsmekanismer Trond S. Halstensen Repetisjon av antigenpresentasjon og effektormekanismer Type I-V immunreaksjoner T-celler gjenkjenner lineære peptider presentert i HLA (Human
Figurer og tabeller kapittel 13 Immunforsvar, smittespredning og hygiene
 Side 262 Øre med ørevoks Øye med tårer Munn med spytt og slimhinner Slimhinner med normalflora Flimmerhår og slim i luftveier Hud med normalflora Magesyre Slimhinner med normalflora i urinveier og skjede
Side 262 Øre med ørevoks Øye med tårer Munn med spytt og slimhinner Slimhinner med normalflora Flimmerhår og slim i luftveier Hud med normalflora Magesyre Slimhinner med normalflora i urinveier og skjede
TNF/BiO og dermatologiske utfordringer. Øystein Sandanger, MD, PhD Seksjon for hudsykdommer, OUS Institutt for indremedisinsk forskning, OUS
 TNF/BiO og dermatologiske utfordringer Øystein Sandanger, MD, PhD Seksjon for hudsykdommer, OUS Institutt for indremedisinsk forskning, OUS Viktige dermatologiske lidelser som behandles med monoklonale
TNF/BiO og dermatologiske utfordringer Øystein Sandanger, MD, PhD Seksjon for hudsykdommer, OUS Institutt for indremedisinsk forskning, OUS Viktige dermatologiske lidelser som behandles med monoklonale
Vaksineskepsis. Hanne Nøkleby Folkehelseinstituttet 14. November 2017
 Vaksineskepsis Hanne Nøkleby Folkehelseinstituttet 14. November 2017 Er vaksineskepsis et problem i Norge? Difteri Stivkrampe Kikhoste Polio Hib Pneumokokk Meslinger Kusma Rødehunder Landsbasis, 2016 95,739
Vaksineskepsis Hanne Nøkleby Folkehelseinstituttet 14. November 2017 Er vaksineskepsis et problem i Norge? Difteri Stivkrampe Kikhoste Polio Hib Pneumokokk Meslinger Kusma Rødehunder Landsbasis, 2016 95,739
VAKSINERE NÅ? Aktuelt om vaksinasjon og sykdommer hos hest
 VAKSINERE NÅ? Aktuelt om vaksinasjon og sykdommer hos hest PASS PÅ HESTEN DIN Luftveisinfeksjoner og andre smittsomme sykdommer kan idag spres raskt fordi hester transporteres i større grad i forbindelse
VAKSINERE NÅ? Aktuelt om vaksinasjon og sykdommer hos hest PASS PÅ HESTEN DIN Luftveisinfeksjoner og andre smittsomme sykdommer kan idag spres raskt fordi hester transporteres i større grad i forbindelse
Medikamentell Behandling
 www.printo.it/pediatric-rheumatology/no/intro Medikamentell Behandling Versjon av 2016 13. Biologiske legemidler Gjennom bruk av biologiske legemidler har nye behandlingsprinsipper mot revmatisk sykdom
www.printo.it/pediatric-rheumatology/no/intro Medikamentell Behandling Versjon av 2016 13. Biologiske legemidler Gjennom bruk av biologiske legemidler har nye behandlingsprinsipper mot revmatisk sykdom
FORSKRIFT OM KOMMUNENS VAKSINASJONSTILBUD I HENHOLD TIL DET NASJONALE VAKSINASJONSPROGRAMMET
 FORSKRIFT OM KOMMUNENS VAKSINASJONSTILBUD I HENHOLD TIL DET NASJONALE VAKSINASJONSPROGRAMMET Fastsatt av Helse- og omsorgsdepartementet (dato) med hjemmel i lov 19. november 1982 nr. 66 om helsetjenesten
FORSKRIFT OM KOMMUNENS VAKSINASJONSTILBUD I HENHOLD TIL DET NASJONALE VAKSINASJONSPROGRAMMET Fastsatt av Helse- og omsorgsdepartementet (dato) med hjemmel i lov 19. november 1982 nr. 66 om helsetjenesten
Hva er myelomatose? Hva er immunterapi?
 Hva er myelomatose? Hva er immunterapi? Anders Sundan Senter for myelomforskning KREFTFORENINGEN 1 Kreft er genetiske sykdommer i den forstand at det alltid er genetiske forandringer (mutasjoner) i kreftcellene
Hva er myelomatose? Hva er immunterapi? Anders Sundan Senter for myelomforskning KREFTFORENINGEN 1 Kreft er genetiske sykdommer i den forstand at det alltid er genetiske forandringer (mutasjoner) i kreftcellene
Ny kreftvaksine: Viktigheten av å kommersialisere medisinsk forskning
 Ny kreftvaksine: Viktigheten av å kommersialisere medisinsk forskning Gustav Gaudernack Immunologisk avdeling Institutt for Kreftforskning Oslo Universitetsykehus-Radiumhospitalet Helse- og omsorgskonferansen
Ny kreftvaksine: Viktigheten av å kommersialisere medisinsk forskning Gustav Gaudernack Immunologisk avdeling Institutt for Kreftforskning Oslo Universitetsykehus-Radiumhospitalet Helse- og omsorgskonferansen
Immunsystemets dobbeltrolle i kreftutvikling
 MED-3950 5.-årsoppgaven Profesjonsstudiet i medisin ved Universitetet i Tromsø Immunsystemets dobbeltrolle i kreftutvikling Nora Ness MK-09 97533239, [email protected] Veileder: Elin Richardsen IMB,
MED-3950 5.-årsoppgaven Profesjonsstudiet i medisin ved Universitetet i Tromsø Immunsystemets dobbeltrolle i kreftutvikling Nora Ness MK-09 97533239, [email protected] Veileder: Elin Richardsen IMB,
KARAKTERISERING AV IgG1 OG IgG3 ANTISTOFFER DANNET ETTER VAKSINERING MED MenBvac
 Hovedoppgave i farmakognosi for graden cand. pharm. KARAKTERISERING AV IgG1 OG IgG3 ANTISTOFFER DANNET ETTER VAKSINERING MED MenBvac av Marit Øfsdahl Avdeling for farmasøytisk kjemi Farmasøytisk institutt
Hovedoppgave i farmakognosi for graden cand. pharm. KARAKTERISERING AV IgG1 OG IgG3 ANTISTOFFER DANNET ETTER VAKSINERING MED MenBvac av Marit Øfsdahl Avdeling for farmasøytisk kjemi Farmasøytisk institutt
Høringsnotat - forslag til endringer i blåreseptforskriften
 Høringsnotat - forslag til endringer i blåreseptforskriften Helse- og omsorgsdepartementet sender med dette forslag til endringer i Forskrift om stønad til dekning av utgifter til viktige legemidler mv.
Høringsnotat - forslag til endringer i blåreseptforskriften Helse- og omsorgsdepartementet sender med dette forslag til endringer i Forskrift om stønad til dekning av utgifter til viktige legemidler mv.
Colostrum FAQ. Hyppig stilte spørsmål om LRs Colostrum-produkter
 Colostrum FAQ Hyppig stilte spørsmål om LRs Colostrum-produkter Innholdsfortegnelse I. Hva er colostrum? S 3 II. Hvilket dyr kommer colostrum fra? S 3 III. Hva skjer med kalvene? S 3 IV. Hvorfor er colostrum
Colostrum FAQ Hyppig stilte spørsmål om LRs Colostrum-produkter Innholdsfortegnelse I. Hva er colostrum? S 3 II. Hvilket dyr kommer colostrum fra? S 3 III. Hva skjer med kalvene? S 3 IV. Hvorfor er colostrum
Figurer kap 6: Menneskets immunforsvar Figur s. 156
 Figurer kap 6: Menneskets immunforsvar Figur s. 156 kjemiske forbindelser bakterie røde blodceller fagocytt kapillæråre Huden blir skadet, og mikroorganismer kommer inn i kroppen. Mange fagocytter beveger
Figurer kap 6: Menneskets immunforsvar Figur s. 156 kjemiske forbindelser bakterie røde blodceller fagocytt kapillæråre Huden blir skadet, og mikroorganismer kommer inn i kroppen. Mange fagocytter beveger
Læringsutbyttebeskrivelse
 Inngår i emne: MED-1501 Medisin og odontologi 1. studieår Oppdatert dato: 10. november 2018 Godkjent av Studieplanutvalget medisin: 04.12.18 Omfang: 5 uker Faglig innhold Delemnet introduserer studenten
Inngår i emne: MED-1501 Medisin og odontologi 1. studieår Oppdatert dato: 10. november 2018 Godkjent av Studieplanutvalget medisin: 04.12.18 Omfang: 5 uker Faglig innhold Delemnet introduserer studenten
Immunsystemet Immunterapien og dens ulike former Kreftsykdommer som behandles Bivirkninger av immunterapi Laboratorieanalyser nå og i fremtiden
 AGENDA Immunsystemet Immunterapien og dens ulike former Kreftsykdommer som behandles Bivirkninger av immunterapi Laboratorieanalyser nå og i fremtiden 1 IMMUNSYSTEMET Immunsystemet vårt er designet for
AGENDA Immunsystemet Immunterapien og dens ulike former Kreftsykdommer som behandles Bivirkninger av immunterapi Laboratorieanalyser nå og i fremtiden 1 IMMUNSYSTEMET Immunsystemet vårt er designet for
HIV / AIDS -infeksjon - behandling
 HIV / AIDS -infeksjon - behandling HIV / AIDS 1981 første gang anerkjent som distinkt sykdom Opprinnelig overført fra sjimpanse Viruset kan ha sirkulert fra 1915-1941 Trolig sirkulert blant populasjoner
HIV / AIDS -infeksjon - behandling HIV / AIDS 1981 første gang anerkjent som distinkt sykdom Opprinnelig overført fra sjimpanse Viruset kan ha sirkulert fra 1915-1941 Trolig sirkulert blant populasjoner
BCG - flytting av spedbarnsvaksinasjon - vaksinasjon av helsefagstudenter
 BCG - flytting av spedbarnsvaksinasjon - vaksinasjon av helsefagstudenter Synne Sandbu, overlege Avd. for vaksine Divisjon for smittevern Nasjonalt folkehelseinstitutt Vaksinedagene 2014 2 Følger av at
BCG - flytting av spedbarnsvaksinasjon - vaksinasjon av helsefagstudenter Synne Sandbu, overlege Avd. for vaksine Divisjon for smittevern Nasjonalt folkehelseinstitutt Vaksinedagene 2014 2 Følger av at
Utvikling av kreftvaksiner
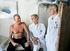 Utvikling av kreftvaksiner Gustav Gaudernack Dagens Medisin Arena Kreft og prioritering 10.04.13 Section for Immunology Dept. of Cancer Research Oslo University Hospital- Norwegian Radium Hospital Status
Utvikling av kreftvaksiner Gustav Gaudernack Dagens Medisin Arena Kreft og prioritering 10.04.13 Section for Immunology Dept. of Cancer Research Oslo University Hospital- Norwegian Radium Hospital Status
Får vi et vaksinasjonsprogram for voksne? Hanne Nøkleby Folkehelseinstituttet
 Får vi et vaksinasjonsprogram for voksne? Hanne Nøkleby Folkehelseinstituttet Oppdrag fra Helse- og omsorgsdepartementet: Utrede opprettelsen av et vaksinasjonsprogram for voksne tilsvarende barnevaksinasjonsprogrammet
Får vi et vaksinasjonsprogram for voksne? Hanne Nøkleby Folkehelseinstituttet Oppdrag fra Helse- og omsorgsdepartementet: Utrede opprettelsen av et vaksinasjonsprogram for voksne tilsvarende barnevaksinasjonsprogrammet
Myelomatose. Aymen Bushra0Ahmed.0MD.0PhD Seksjonsoverlege: Hematologisk0seksjon Haukeland0Universitetssykehus. Onsdag
 Myelomatose Aymen Bushra0Ahmed.0MD.0PhD Seksjonsoverlege: Hematologisk0seksjon Haukeland0Universitetssykehus Onsdag005.11.18 Hva er kreft og hvorfor/hvordan oppstår kreft? Hva er benmargen Hva er myelomatose
Myelomatose Aymen Bushra0Ahmed.0MD.0PhD Seksjonsoverlege: Hematologisk0seksjon Haukeland0Universitetssykehus Onsdag005.11.18 Hva er kreft og hvorfor/hvordan oppstår kreft? Hva er benmargen Hva er myelomatose
Vaksinasjon av utsatte grupper: - Flyktninger og asylsøkere - Personer med (medfødt) immunsvikt. Hanne Nøkleby Folkehelseinstituttet
 Vaksinasjon av utsatte grupper: - Flyktninger og asylsøkere - Personer med (medfødt) immunsvikt Hanne Nøkleby Folkehelseinstituttet Hensikt med å vaksinere flyktninger og asylsøkere Hindre utbrudd i mottak
Vaksinasjon av utsatte grupper: - Flyktninger og asylsøkere - Personer med (medfødt) immunsvikt Hanne Nøkleby Folkehelseinstituttet Hensikt med å vaksinere flyktninger og asylsøkere Hindre utbrudd i mottak
Diagnostikk og oppfølging av cøliakipasienter klinikers og patologs perspektiv
 Diagnostikk og oppfølging av cøliakipasienter klinikers og patologs perspektiv Knut E. A. Lundin, Medisinsk klinikk Inger Nina Farstad, Patologiklinikken Hva er cøliaki? Normal proksimal tynntarm (Marsh
Diagnostikk og oppfølging av cøliakipasienter klinikers og patologs perspektiv Knut E. A. Lundin, Medisinsk klinikk Inger Nina Farstad, Patologiklinikken Hva er cøliaki? Normal proksimal tynntarm (Marsh
Vaksinasjon noen oppdateringer. Hanne Nøkleby Folkehelseinstituttet 15. September 2015
 Vaksinasjon noen oppdateringer Hanne Nøkleby Folkehelseinstituttet 15. September 2015 Utvalgte temaer Influensa Meningokokker Rotavirus Meslinger Hepatitt B Influensavaksine en barnevaksine? Sykeligheten
Vaksinasjon noen oppdateringer Hanne Nøkleby Folkehelseinstituttet 15. September 2015 Utvalgte temaer Influensa Meningokokker Rotavirus Meslinger Hepatitt B Influensavaksine en barnevaksine? Sykeligheten
Om HPV-vaksinen i barnevaksinasjonsprogrammet
 Bokmål 2016 Vaksine for forebygging av livmorhalskreft tilbud til jenter i 7. klasse Informasjon til barn og foreldre Om HPV-vaksinen i barnevaksinasjonsprogrammet 1 Vaksine mot humant papillomavirus (HPV)
Bokmål 2016 Vaksine for forebygging av livmorhalskreft tilbud til jenter i 7. klasse Informasjon til barn og foreldre Om HPV-vaksinen i barnevaksinasjonsprogrammet 1 Vaksine mot humant papillomavirus (HPV)
Nytt om influensavaksiner. Hanne Nøkleby, Nasjonalt folkehelseinstitutt
 Nytt om influensavaksiner Hanne Nøkleby, Nasjonalt folkehelseinstitutt Nytt på influensavaksinefronten Erfaring med levende, nasal vaksine Influensavaksiner med adjuvans Helt nye influensavaksiner Levende,
Nytt om influensavaksiner Hanne Nøkleby, Nasjonalt folkehelseinstitutt Nytt på influensavaksinefronten Erfaring med levende, nasal vaksine Influensavaksiner med adjuvans Helt nye influensavaksiner Levende,
Innføring av hepatitt B-vaksine i barnevaksinasjonsprogrammet. Forslag til endringer i forskrift om nasjonalt vaksinasjonsprogram
 Helse- og omsorgsdepartementet Innføring av hepatitt B-vaksine i barnevaksinasjonsprogrammet Forslag til endringer i forskrift om nasjonalt vaksinasjonsprogram Høringsfrist: 17. april 2015 Innhold 1. Innledning...
Helse- og omsorgsdepartementet Innføring av hepatitt B-vaksine i barnevaksinasjonsprogrammet Forslag til endringer i forskrift om nasjonalt vaksinasjonsprogram Høringsfrist: 17. april 2015 Innhold 1. Innledning...
Juridiske rammer for Vaksinasjonsprogram i Norge
 Juridiske rammer for Vaksinasjonsprogram i Norge Møte i Faglig referansegruppe for nasjonale vaksinasjonsprogram 21.05.2019 Ellen Furuseth, overlege ved avdeling for vaksineforebyggbare sykdommer, FHI
Juridiske rammer for Vaksinasjonsprogram i Norge Møte i Faglig referansegruppe for nasjonale vaksinasjonsprogram 21.05.2019 Ellen Furuseth, overlege ved avdeling for vaksineforebyggbare sykdommer, FHI
HPV-vaksine - hvordan går det? Berit Feiring Avdeling for vaksine Nasjonalt folkehelseinstitutt
 HPV-vaksine - hvordan går det? Berit Feiring Avdeling for vaksine Nasjonalt folkehelseinstitutt HPV-vaksine i vaksinasjonsprogrammet HPV-vaksine ble inkludert i barnevaksinasjonsprogrammet fra høsten 2009
HPV-vaksine - hvordan går det? Berit Feiring Avdeling for vaksine Nasjonalt folkehelseinstitutt HPV-vaksine i vaksinasjonsprogrammet HPV-vaksine ble inkludert i barnevaksinasjonsprogrammet fra høsten 2009
Bioteknologi i dag muligheter for fremtiden
 Bioteknologi i dag muligheter for fremtiden Arvestoff Genetisk materiale, DNA. Baser En del av et nukleotid som betegnes med bokstavene A, C, G og T. Med disse fire bokstavene skriver DNAtrådene sine beskjeder
Bioteknologi i dag muligheter for fremtiden Arvestoff Genetisk materiale, DNA. Baser En del av et nukleotid som betegnes med bokstavene A, C, G og T. Med disse fire bokstavene skriver DNAtrådene sine beskjeder
Forekomst og forebygging av kikhoste hos barn under 1 år
 Forekomst og forebygging av kikhoste hos barn under 1 år Margrethe Greve-Isdahl Overlege, Avdeling for Vaksine Divisjon for Smittevern Nasjonalt Folkehelseinstitutt Bakgrunn Flere industrialiserte land
Forekomst og forebygging av kikhoste hos barn under 1 år Margrethe Greve-Isdahl Overlege, Avdeling for Vaksine Divisjon for Smittevern Nasjonalt Folkehelseinstitutt Bakgrunn Flere industrialiserte land
Urinsyrekrystaller som adjuvans i fiskevaksiner
 Norges fiskerihøgskole Urinsyrekrystaller som adjuvans i fiskevaksiner Bjarte Langhelle Masteroppgave i fiskehelse (60 stp) Desember 2013 Forord Forord Denne oppgaven ble utført ved Norges fiskerihøgskole,
Norges fiskerihøgskole Urinsyrekrystaller som adjuvans i fiskevaksiner Bjarte Langhelle Masteroppgave i fiskehelse (60 stp) Desember 2013 Forord Forord Denne oppgaven ble utført ved Norges fiskerihøgskole,
Om HPV-vaksinen i barnevaksinasjonsprogrammet
 Bokmål Vaksine for forebygging av livmorhalskreft tilbud til jenter i 7. klasse Informasjon til barn og foreldre Om HPV-vaksinen i barnevaksinasjonsprogrammet 1 Fra høsten 2009 får alle jenter i 7. klasse
Bokmål Vaksine for forebygging av livmorhalskreft tilbud til jenter i 7. klasse Informasjon til barn og foreldre Om HPV-vaksinen i barnevaksinasjonsprogrammet 1 Fra høsten 2009 får alle jenter i 7. klasse
TUBERKULOSE OG FORHÅNDSREGLER FOREBYGGING VED VAKSINASJON. Marianne Breunig Fornes Smitteverndag 2019, Haugesund Kommune
 TUBERKULOSE OG FORHÅNDSREGLER FOREBYGGING VED VAKSINASJON Marianne Breunig Fornes Smitteverndag 2019, Haugesund Kommune Gyiiiiiii AGENDA Tuberkulose - Forekomst og kontroll VAKSINASJON - Generelt - Yrkesvaksinasjon
TUBERKULOSE OG FORHÅNDSREGLER FOREBYGGING VED VAKSINASJON Marianne Breunig Fornes Smitteverndag 2019, Haugesund Kommune Gyiiiiiii AGENDA Tuberkulose - Forekomst og kontroll VAKSINASJON - Generelt - Yrkesvaksinasjon
Vaksine mot kre/ Thea Eline Hetland, lege, PhD student, Avd. For Gynekologisk kre/, Radiumhospitalet
 Vaksine mot kre/ Thea Eline Hetland, lege, PhD student, Avd. For Gynekologisk kre/, Radiumhospitalet ca 200 ulike krebsykdommer Hva er kre/? Mange likehetstrekk Mye som skiller dem fra hverandre Ca 27
Vaksine mot kre/ Thea Eline Hetland, lege, PhD student, Avd. For Gynekologisk kre/, Radiumhospitalet ca 200 ulike krebsykdommer Hva er kre/? Mange likehetstrekk Mye som skiller dem fra hverandre Ca 27
HPV-vaksine: Endringer i barnevaksinasjonsprogrammet. Margrethe Greve-Isdahl Overlege Avdeling for vaksineforebyggbare sykdommer
 HPV-vaksine: Endringer i barnevaksinasjonsprogrammet Margrethe Greve-Isdahl Overlege Avdeling for vaksineforebyggbare sykdommer Endringer i barnevaksinasjonsprogrammet 1. Vaksinetype endres fra Gardasil
HPV-vaksine: Endringer i barnevaksinasjonsprogrammet Margrethe Greve-Isdahl Overlege Avdeling for vaksineforebyggbare sykdommer Endringer i barnevaksinasjonsprogrammet 1. Vaksinetype endres fra Gardasil
Influensavaksiner - fra produksjon til injeksjon
 Influensavaksiner - fra produksjon til injeksjon Kine Willbergh og Hilde Bakke Avdeling for vaksine Vaksinedagene 7.-8. september 2006 1 Disposisjon Influensavaksiner, ulike typer» Levende, svekket vaksine
Influensavaksiner - fra produksjon til injeksjon Kine Willbergh og Hilde Bakke Avdeling for vaksine Vaksinedagene 7.-8. september 2006 1 Disposisjon Influensavaksiner, ulike typer» Levende, svekket vaksine
Essayoppgaver termin 1C-1D 2010 Utsatt eksamen. Oppgave 1 (10 poeng) Morfologi Jostein Halgunset
 Essayoppgaver termin 1C-1D 2010 Utsatt eksamen Morfologi Jostein Halgunset Oppgave 1 (10 poeng) En 52 år gammel kvinne, som to år tidligere var operert for brystkreft med påfølgende cellegiftbehandling,
Essayoppgaver termin 1C-1D 2010 Utsatt eksamen Morfologi Jostein Halgunset Oppgave 1 (10 poeng) En 52 år gammel kvinne, som to år tidligere var operert for brystkreft med påfølgende cellegiftbehandling,
Hvor farlig er det å puste inn bioaerosoler?
 Hvor farlig er det å puste inn bioaerosoler? Symptomer og sykdom ved eksponering for bioaerosoler Helse effekter Infeksjon Patogener Toksiske effekter Mykotoksiner Inflammasjon Uspesifikt medfødt immunforsvar
Hvor farlig er det å puste inn bioaerosoler? Symptomer og sykdom ved eksponering for bioaerosoler Helse effekter Infeksjon Patogener Toksiske effekter Mykotoksiner Inflammasjon Uspesifikt medfødt immunforsvar
Tone Fredsvik Gregers. Alt du må vite om vaksiner
 Tone Fredsvik Gregers Alt du må vite om vaksiner HUMANIST FORLAG 2016 Humanist forlag 2016 Omslag: Lilo design Tilrettelagt for ebok av eboknorden as ISBN: 978-82-8282-128-5 (epub) ISBN: 978-82-8282-127-8
Tone Fredsvik Gregers Alt du må vite om vaksiner HUMANIST FORLAG 2016 Humanist forlag 2016 Omslag: Lilo design Tilrettelagt for ebok av eboknorden as ISBN: 978-82-8282-128-5 (epub) ISBN: 978-82-8282-127-8
