OPPFINNELSESOMRÅDE. Proteinet NY-ESO-1 er 180 aminosyrer langt og kan beskrives som sammensatt av tre
|
|
|
- Adrian Severin Sletten
- 6 år siden
- Visninger:
Transkript
1 1 OPPFINNELSESOMRÅDE Foreliggende oppfinnelse vedrører generelt polypeptider og konstruksjoner som omfatter et antigen avledet fra det ene eller begge av tumorrejeksjons-antigenene NY5 ESO-1 og LAGE-1. BAKGRUNN FOR OPPFINNELSEN CT- (cancer testis) antigener er en klasse av tumorassosierte antigener med ekspresjon som normalt er begrenset til kimceller i testiklene, ovariene eller 10 trofoblastceller. Disse antigenene uttrykkes ikke vanligvis i voksnes somatiske vev. Se Simpson, et al., Nat. Rev. Cancer, 5(8): (2005); Scanlan, et al., Immunol. Reviews, 188:22-32 (2002); Scanlan, et al., Canc. Immun., 4:1-15 (2004). Genreguleringen av CT-antigener er forstyrret hos cancerpasienter, hvilket fører til 15 aberrant ekspresjon av disse antigenene i et bredt utvalg av tumorer. Det første CTantigen som ble identifisert, MAGE-1, ble identifisert tidlig på 1990-tallet ved T-celle epitopkloning (van der Bruggen et al, 1991, Science 13:254(5038):1643-7; van der Bruggen et al, 1999, Science 254: ; Traversari, et al, 1992, Immunogenetics, 35(3): ; og U.S. Patent ). Siden den gang har SEREX- 20 teknikk (serological expression cloning) (Sahin et al., Proc. Natl. Acad. Sci. USA, 92(25): (1995) og U.S. Patent ), rekombinant antigenekspresjon på gjær-overflate (RAYS) (Mischo, et al., Canc. Immun., 3:5-16 (2003) og differensiell mrna-ekspresjonsanalyse (Gure, et al., Int. J. Canc., 85(5): (2000)) ført til identifikasjonen av nærmere 90 CT-antigener, og antallet forventes å 25 tilta fremover. Immunogeniteten av enkelte CT-antigener i cancerpasienter gjør dem til et ideelt mål for utviklingen av tumorvaksiner. NY-ESO-1. Et CT-antigen som for tiden er av interesse for bruk innen cancerimmunterapi er NY-ESO-1. Dette antigen ble først identifisert av SEREX i et øsofagealt 30 skvamøst cellekarsinom på slutten av 90-tallet ved New-York avdelingen av Ludwig Institute for Cancer Research (Chen, et al., PNAS USA, 94(5): (1997) og U.S. Patent Proteinet NY-ESO-1 er 180 aminosyrer langt og kan beskrives som sammensatt av tre 35 regioner: En N-terminal region ca. eller tilnærmet aminosyrer 1 til 70, En sentralregion ca. eller tilnærmet aminosyrer 71 til 134 og
2 2 En C-terminal regionca. eller tilnærmet aminosyrer 135 til 180. En kollagenlignende region omfatter ca. eller tilnærmet ca. aminosyrer 15 til 73 av den N-terminale region (se Figur 1) Proteinet NY-ESO-1 har vært funnet i et bredt utvalg av tumorer, inklusivt, men ikke begrenset til, ovarialcancer, lungekreft, brystkreft, prostata, øsofaguscancer, blærecancer og i melanomer. (Nicholaou, T. et al, Immunol. Cell Biol Jun; 84(3): og Jungbluth, et al. 2001, Int. J. Canc., 92(6): ). Spontane humorale og cellulære immunresponser mot dette antigen har vært beskrevet hos pasienter med NY-ESO-1-positive tumorer, og en rekke HLA (Human Leukocyte Antigen) klasse I- og II-restringerte peptider har vært identifisert (Jager, et al., 1998, J. Exp. Med., 187(2): ; Yamaguchi, et al., 2004, Clin. Canc. Res., 10(3): og Davis, et al., 2004, Proc. Natl. Acad. Sci. USA, 101(29): ). Eksempler fra patentlitteraturen er U.S. Patent ; ; ; ; ; ; ; ; ; ; og I et klinisk forsøk har tre partielt overlappende NY-ESO-1-avledede peptider med bindingsmotiver til HLA-A2 ( , og ) vært benyttet i en vaksine for å behandle tolv pasienter med metastatiske NY-ESO-1-uttrykkende tumorer. Studien viser at syntetiske NY-ESO-1-peptider trygt kan administreres og er i stand til å generere potensielt fordelaktige T-celleresponser (Jager, et al., 2000, PNAS USA, 97(22): ) En rekke MHC (major histocompatibility complex) klasse I- og II-epitoper i proteinet er blitt identifisert av forskjellige grupper, se for eksempel Figur 1. Disse epitopene er kun representative for epitoper rapportert for proteinet, og listen i Figur 1 er ikke uttømmende. Dessuten er minst en eller flere av de epitoper som er rapportert og/eller angitt i Figur 1, ikke blitt bekreftet eksperimentelt. Den kollagenlignende region i N-terminalen inneholder minst en MHC-klasse I-epitop, her omtalt som A31. Den sentrale region omfatter flere MHC-klasse 2-epitoper her referert til som DR1, DR2, DR4, DR7 og DP4. Denne regionen inneholder også flere MI-IC-klasse I-epitoper her referert til som B35, B51, Cw3 og Cw6. C-terminalen antas å inneholde minst to klasse II-epitoper (DR4 og DP4) og en klasse I-epitop (A2). 35 LAGE-1. Et ytterligere cancer testis-antigen, LAGE-1, er også blitt identifisert. To LAGE-1 transkripter er blitt beskrevet, LAGE-1a og LAGE1b. LAGE-1b er ufullstendig
3 3 spleiset og koder for et antatt protein på tilnærmet 210 aminosyrerester, mens LAGE1a-genproduktet inneholder 180 aminosyrerester (Sun et al. Cancer Immunol. Immunother. 2006:55: ) De N-terminale regionene av LAGE-1- og NY-ESO-1-proteinene er høyt konserverte og antas å ha mer enn 97% identitet. LAGE-1 adskiller seg imidlertid fra NY-ESO-1 i de sentrale regioner som bare er 62% identiske. C-terminalen av NY-ESO-1 og LAGE-1a er høyt konserverte (mer enn 97% identitet). C-terminalen av LAGE-1b er imidlertid lenger og ikke konservert og antas å ha mindre enn 50% identitet med den samme region i LAGE-1a/NY-ESO-1. Generell informasjon angående disse proteinene er tilgjengelig fra LICR-nettstedet (se SAMMENFATNING AV OPPFINNELSEN Foreliggende oppfinnelse tilveiebringer et immunogent fusjonsprotein som omfatter: (i) NY-EWA eller et fragment derav, koblet til (ii) LAGE-1 eller et fragment derav, hvor minst ett av NY-ESO-1 og/eller LAGE-1 er trunkert eller delvis trunkert, eller er et fragment som inkluderer en eller flere epitoper av NY-ESO-1 eller LAGE-1, hvor fusjonsproteinet omfatter en aminosyresekvens valgt fra gruppen bestående av SEKV.ID.NR:73, SEKV.ID.NR:75, SEKV.ID.NR:79, SEKV.ID.NR:81, SEKV.ID.NR:83, SEKV.ID.NR:85, SEKV.ID.NR:89, SEKV.ID.NR:93 og SEKV.ID.NR: Blandinger som involverer fusjonsproteiner og polypeptider tilveiebringes også. KORT BESKRIVELSE AV FIGURENE 30 Figur 1 viser en rekke MHC (major histocompatibility complex) klasse I- og IIepitoper på NY-ESO-1-proteinet som er blitt identifisert av forskjellige grupper. Disse epitopene er bare representative for epitoper som er rapportert for proteinet, og listen i Figur 1 er således ikke uttømmende. En eller flere av epitopene rapportert og/eller angitt i Figur 1, er dessuten ikke blitt eksperimentelt bekreftet. Den rapporterte aminosyresekvens for NY-ESO-1 finnes her i SEKV.ID.NR: Figur 2 viser konstruksjon A, et fusjonsprotein som omfatter fullengdes NY-ESO-1 og trunkert LAGE-1, så som LAGE-1a. I denne utførelsesform er C-terminalen av NY-ESO-
4 4 1 fusjonert til N-terminalen av trunkert LAGE-1, sammen med en histidin affinitets-tag for å gi et fusjonsprotein av 288 aminosyrers lengde. Ytterligere detaljer angående konstruksjon A er angitt i Tabell 1 (SEKV.ID.NR:1, SEKV.ID.NR:3) Figur 3 viser konstruksjon B, et fusjonsprotein som omfatter den første tredjedel av protein D uten dens sekresjonssignal (for eksempel aminosyrene 20 til 127), fullengdes NY-ESO-1 og trunkert LAGE-1, så som LAGE-1a. I denne utførelsesform er aminosyre 127 av protein D fusjonert til N-terminalen av NY-ESO-1, C-terminalen av denne fusjonert til N-terminalen av trunkert LAGE-1, for å gi et fusjonsprotein på 398 aminosyrers lengde. Ytterlige detaljer angående konstruksjon B er angitt i Tabell 1 i seksjon 1.6 (SEKV.ID.NR:2; SEKV.ID.NR:4). 15 Figur 4 viser konstruksjon C, et fusjonsprotein som omfatter partielt trunkert NY-ESO- 1 og trunkert LAGE-1, så som LAGE-1a. I denne utførelsesform er C-terminalen av partielt trunkert NY-ESO-1 fusjonert til N-terminalen av trunkert LAGE-1 for å gi et fusjonsprotein på 242 aminosyrers lengde. Ytterligere detaljer angående konstruksjon C er angitt i Tabell 1. (SEKV.ID.NR:5; SEKV.ID.NR:7) Figur 5 viser konstruksjon D, et fusjonsprotein som omfatter den første tredjedel av protein D uten dens sekresjonssignal (for eksempel aminosyrene 20 til cirka eller tilnærmet 127), partielt trunkert NY-ESO-1 og trunkert LAGE-1 så som LAGE-1a. I denne utførelsesform er aminosyre 127 av protein D fusjonert til N-terminalen av partielt trunkert NY-ESO-1, C-terminalen av denne fusjonert til N-terminalen av det trunkerte LAGE-1 for å gi et fusjonsprotein på 352 aminosyrers lengde. Ytterligere detaljer angående denne utførelsesform er angitt i Tabell 1 (SEKV.ID.NR:6; SEKV.ID.NR:8). 30 Figur 6 viser konstruksjon E, et fusjonsprotein som omfatter trunkert NY-ESO-1 og trunkert LAGE-1, så som LAGE-1a. I denne utførelsesform er C-terminalen av trunkert NY-ESO-1 fusjonert til N-terminalen av trunkert LAGE-1 for å gi et fusjonsprotein på 211 aminosyrers lengde. Ytterligere detaljer angående konstruksjon E er gitt i Tabell 1 (SEKV.ID.NR:9; SEKV.ID.NR:11). 35 Figur 7 viser konstruksjon F, et fusjonsprotein som omfatter den første tredjedel av protein D uten dets sekresjonssignal (for eksempel aminosyrene 20 til cirka eller tilnærmet 127), trunkert NY-ESO-1 og trunkert LAGE-1, så som LAGE-1a. I denne utførelsesform er aminosyre 127 av protein D fusjonert til N-terminalen av trunkert
5 5 NY-ESO-1, C-terminalen av denne fusjonert til N-terminalen av trunkert LAGE 1 for å gi et fusjonsprotein på 321 aminosyrers lengde. Ytterligere detaljer angående konstruksjon F er gitt i Tabell 1 (SEKV.ID.NR:10; SEKV.ID.NR:12). 5 Figur 8 viser en alternativ utførelsesform av konstruksjon E, nemlig E, hvor C- terminalen av trunkert LAGE-1 er fusjonert til N-terminalen av trunkert NY-ESO-1 for å gi et fusjonsprotein på 212 aminosyrers lengde. Ytterligere detaljer angående denne utførelsesform, konstruksjon E, er angitt i Tabell 1 (SEKV.ID.NR:21; SEKV.ID.NR:23) Figur 9 viser konstruksjon G, et fusjonsprotein som omfatter trunkert NY-ESO-1, trunkert LAGE-1, så som LAGE-1a og den kollagenlignende region, så som kollagenregionen fra NY-ESO-1. I denne utførelsesform er C-terminalen av den kollagenlignende region, for eksempel fusjonert til N-terminalen av trunkert LAGE-1. I sin tur er C-terminalen av den trunkerte LAGE-1 fusjonert til N-terminalen av trunkert NY- ESO-1 for å gi et fusjonsprotein på 289 aminosyrers lengde. Ytterligere detaljer angående konstruksjon G er angitt i Tabell 1 (SEKV.ID.NR:13; SEKV.ID.NR:15). 20 Figur 10 viser skjematisk et eksempel på et rekombinant polypeptid som omfatter NY- ESO-1 med et partielt trunkert kollagenlignende domene. Epitopene vist i Figurene er bare representative for epitoper rapportert for proteinet og har ikke vært eksperimentelt bekreftet. 25 Figur 11 viser skjematisk et eksempel på et fusjonsprotein som omfatter den første tredjedel av protein D uten dets sekresjonssignal (for eksempel aminosyrene 20 til cirka eller tilnærmet 127) og NY-ESO-1 med et partielt trunkert kollagenlignende domene. Figur 12 viser skjematisk et eksempel på et rekombinant polypeptid som omfatter NY- ESO-1 med et partielt trunkert kollagenlignende domene. 30 Figur 13 viser skjematisk et eksempel på et fusjonsprotein som omfatter den første tredjedel av protein D uten dets sekresjonssignal (for eksempel aminosyrene 20 til cirka eller tilnærmet 127) og NY-ESO-1 med et trunkert kollagenlignende domene. 35 Figur 14 er et skjema som viser et antall epitoper identifisert innenfor det trunkerte LAGE-1a-protein. Disse epitopene er bare representative for epitoper rapportert for proteinet og listen er således ikke uttømmende. For å unngå tvil kan de epitoper som
6 6 5 er rapportert og/eller angitt i figurene være bekreftet, eller ikke, eksperimentelt (dvs. de kan ha vært predikert, etc.) om intet annet her er angitt. Den fullstendige LAGE- 1a-aminosyresekvens er angitt i sekvenslisten som SEKV.ID.NR:58. Den fullstendige LAGE-1b-aminosyresekvens (LAGE-1b ikke vist i denne figur) er angitt i sekvenslisten som SEKV.ID.NR: Figur 15 viser skjematisk både NY-ESO-1 og LAGE-1, så vel som en rekke MHC (major histocompatibility complex) klasse I- og II-epitoper. Disse epitopene er bare representative for epitoper rapportert for proteinet og listen er således ikke uttømmende. En eller flere av de epitoper som er rapportert og/eller angitt har ikke vært eksperimentelt bekreftet. Figur 16 viser skjematisk NY-ESO-1/LAGE-1-fusjonsdesign Figur 17 sammenfatter på skjematisk måte femten konstruksjoner og deres produksjonsnivåer. P=protein D; C (grå boks) =NY-ESO-1-kollagenlignende domene; C (hvit boks) =trunkert kollagenlignende domene; L= LAGE-1 uten det kollagenlignende domene; N= NY-ESO-1 uten det kollagenlignende domene; sort pil=polyhistidin-tag (-) =lav produksjon; (+)=noe produksjon; (++)=høy produksjon; (+++)=best produksjon. Aminosyresekvensene for åtte av konstruksjonene og de nukleotidsekvenser som koder for disse, er sammenfattet i Tabell 4 og sekvenslisten. 25 Figur 18 sammenfatter screening nr.1, et 76-dagers forsøk ved bruk av CB6F1-mus for å vurdere hver av LVL076, LVL079, LVL78, LVL68, LVL020, LVL26, LVL024, LVL30 for å bestemme hvorvidt intramuskulær immunisering med fusjonsproteinet pluss adjuvans ga beskyttelse mot subkutant irritament med transplanterte tumorer (B16/NY-ES0-1). 30 Figur 19 sammenfatter B-16-NY-ESO-1 tumorvekst i kontrollmus benyttet i 76-dagers forsøket. Figur 20 viser overlevelsen til mus immunisert med fullengdes NY-ESO-1, LVL030, LVL068, LVL079 eller LVL Figur 21 sammenfatter de NY-ESO-1 spesifikke immunresponser målt ved ELISA, FACS og western blotting og LAGE-1a (uten det kollagenlignende domenet) spesifikke immunresponser som målt ved ELISA og FACS.
7 7 5 Figur 22 sammenfatter den eksperimentelle design av screening nr. 2, et 105-dagers forsøk for å bestemme hvorvidt intramuskulær immunisering med utvalgte fusjonsproteiner pluss adjuvans gir beskyttelse mot B16/NY-ESO-1-irritament og B16/LAGE- 1a-irritament. B16/NY-ESO-1-irritament er vist. Figur 23 sammenfatter screening nr.2 og viser B16/LAGE-1a-irritamentet. 10 Figur 24 viser overlevelse av mus immunisert med LVL078, LVL068, fullengdes NY- ESO-1, LVL024 og LVL076 etter B-16/NY-ESO-1 irritament. Se Figur 24. Figur 25 viser overlevelse av mus immunisert med LVL076, LAGE-1a uten den kollagenlignende region, LVL024, fullengdes NY-ESO-1, LVL078 eller LVL068 etter B16/LAGE-1a irritament Figur 26. Kolonnene 1-8, fra venstre mot høyre, viser resultatene av ELISA foretatt for å påvise mulige humane kollagenspesifikke immunresponser hos mus immunisert med ett av følgende: (1) buffere (kontroll); (2) fullengde NY-ESO-1; (3) LAGE-1a uten det kollagenlignende domene;( 4) LVL068; (5) LVL078; (6) LVL024; (7) LVL076. Positiv kontroll (kolonne 8) inneholder et antihumant kollagent 1-monoklonalt antistoff (mab) antihumant kollagen I). DETALJERT BESKRIVELSE AV OPPFINNELSEN Fusjonsproteiner. Fusjonsproteinene ifølge oppfinnelsen er egnet til behandling av cancere, og mer spesifikt behandling av melanom; brystkreft; prostatacancer; blærecancer inklusivt transisjonelt cellecarsinom; lungekreft, inklusivt ikke-småcellet lungecarsinom (NSCLC); hode- og hals-kreft inklusivt øsofagus-carsinom; skvamøst cellecarsinom; carsinom av gastrointestinaltrakten; leverkreft; hjernetumorer; leukemi og diverse sarkomer. 35 På basis av ekspresjonsprofilene av LAGE-1 og NY-ESO-1 har fusjonsproteinet i henhold til oppfinnelsen evne til å virke effektivt anslagsvis i 37% av brystkrefttilfeller. Behandlingen i henhold til foreliggende oppfinnelse kan også være særlig hensiktsmessig til behandlingen av pasienter som ikke kan få Her2/neu målrettet terapi. Fusjonsproteinet ifølge oppfinnelsen forventes også å være effektivt i tilnærmet 35% hos prostatacancerpasienter, 35% av blærecancerpasienter, 40% av melanom-
8 8 5 pasienter og 35% av pasienter med NSCLC (ikke-småcellet lungecarsinom). I én utførelsesform kan fusjonsproteinet ifølge oppfinnelsen gjøre det mulig å behandle en større populasjon av pasienter, fordi pasienter som har tumorer som uttrykker både NY-ESO-1 og/eller LAGE-1 (inklusivt LAGE-1a og LAGE-1b) kan gis et fusjonsprotein ifølge foreliggende oppfinnelse Fusjonsproteinet i henhold til oppfinnelsen kan også være mer immunogent enn dets individuelle komponentproteiner av følgende grunner: fjerning av ett eller flere av de kollagenlignende domener kan redusere potensiell immuntoleranse av forbindelsen forårsaket av dens homologi med naturlig endogen kollagenstruktur, eller den eventuelle addisjon av en heterolog fusjonspartner kan ytterligere stimulere CD4 T-celleresponser. Fusjonsproteinene er således egnet til indusering av en immunogen respons i et cancerantigen så som NY-ESO-1 eller LAGE-1, eller begge NY-ESO-1 som her er beskrevet kan være i full lengde, partielt trunkert eller trunkert NY-ESO-1 eller ethvert fragment derav som inkluderer én eller flere epitoper som kan fremme en immunrespons for NY-ESO-1-. Fullengdes NY-ESO-1-protein er i denne sammenheng ment å bety et protein med cirka eller tilnærmet 1 til 180 aminosyrer og minst 95, 96, 97, 98, 99% eller 100% identisk med det naturlig forekommende protein (SEKV.ID.NR:49). I denne sammenheng refererer betegnelsen «LAGE-1» seg til ett eller flere av medlemmene innen LAGE-1 familien, så som LAGE-1a og LAGE-1b, som beskrevet i linjene nedenfor. «Fullengdes LAGE-1a» protein er ment å bety et protein som er 95, 96, 97, 98, 99% eller 100% identisk med SEKV.ID.NR:58. Tilsvarende er det «fullengde LAGE-1b» protein ment å bety et protein 95, 96, 97, 98, 99% eller 100% identisk med det naturlig forekommende protein (SEKV.ID.NR:71) I ett eksempel er identiteten over sekvensens fulle lengde. Fusjonsproteiner med konservative substitusjoner er således også beskrevet. Konservative substitusjoner er velkjente og inngår i alminnelighet som forhåndsdefinerte skåre-matriser i dataprogrammer for sekvensjustering. Disse programmene innbefatter PAM25O (Dayhoft M.O. et. Al., (1978), «A model of evolutionary changes in proteins», «Atlas of Protein sequence and structure» 5(3) M.O. Dayhoft (red.), ), National Biomedical Research Foundation, Washington, og Blosum 62 (Steven Henikoft & Jorja G. Henikoft (1992), og «Amino acid substitution matricies from protein blocks»), Proc. Natl. Acad. Sci. USA 89 (Biochemistry):
9 9 5 Generelt er substitusjoner innen følgende grupper konservative substitusjoner, men substitusjoner mellom grupper anses som ikke-konserverte. Gruppene er: i) Aspartat/asparagin/glutamat/glutamin ii) Serin/treonin iii) Lysin/arginin iv) Fenylalanin/tyrosin/trypofan v) Leucin/isoleucin/valin/metionin vi) Glycin/alanin. 10 «Partielt trunkert» er i sammenheng med denne beskrivelse ment å bety NY-ESO-1- eller LAGE-1-protein (alt etter forholdene) hvor majoriteten av den kollagenlignende region er fjernet, men fremdeles omfatter eller består av den epitop A31 som er funnet i denne region I ett eksempel omfatter eller består partielt trunkert NY-ESO-1 og/eller LAGE-1 av et utvalg aminosyrer fra aminosyre 44, 45, 46, 47, 48, 49, 50, 51 eller 52 til aminosyre 175, 176, 177, 178, 179 eller 180 eller en hvilken som helst kombinasjon av disse aminosyrene, for eksempel fra aminosyre 48 til aminosyre 180 eller fra aminosyre 46 til 178. I én utførelsesform omfatter eller består partielt trunkert NY-ESO-1 eller LAGE-1 av cirka eller eksakt, aminosyrene 48 til 180 (eller cirka eller eksakt, aminosyrene når det gjelder LAGE-1b). I én utførelsesform er betegnelsen «cirka» i denne sammenheng ment å bety at aminosyrer opp til +/- 10% av det totale antall aminosyrer av sekvensen, eventuelt er addert eller deletert fra sekvensen. I én utførelsesform omfatter eller består partielt trunkert NY-ESO-1 av aminosyrene 48 til 180 av NY-ESO I ett eksempel omfatter eller består partielt trunkert LAGE-1b av et utvalg av aminosyrer fra aminosyre 44, 45, 46, 47, 48, 49, 50, 51 eller 52 til aminosyre 205, 206, 207, 208, 209 eller 210, eller enhver kombinasjon av disse aminosyrene, for eksempel fra aminosyre 48 til aminosyre 210 eller fra aminosyre 46 til 208. I ett eksempel omfatter eller består partielt trunkert LAGE-1b av cirka eller eksakt, aminosyrene 48 til 210. Betegnelsen «cirka» kan i denne sammenheng oppfattes å bety at aminosyrer opptil +/- 10% av det totale antall aminosyrer i sekvensen, eventuelt er addert eller deletert fra sekvensen. I ett eksempel omfatter eller består partielt trunkert LAGE-1b av aminosyrene 48 til 210 av LAGE-1b.
10 10 5 «Trunkert» er i denne sammenheng ment å bety NY-ESO-1- eller LAGE-1-protein (som relevant) hvor den kollagenlignende region er blitt fjernet (inklusivt fjerningen av A31 epitopen). Trunkert NY-ESO-1 og/eller LAGE-1 omfatter eller består av cirka eller eksakt, aminosyrene (eller cirka eller eksakt, aminosyre når det gjelder LAGE-1b). 10 I ett eksempel omfatter eller består trunkert NY-ESO-1 eller LAGE-1 av et utvalg aminosyrer fra aminosyre 67, 68, 69, 70, 71, 72, 73, 74 eller 75 til aminosyre 175, 176, 177, 178, 179 eller 180 eller enhver kombinasjon av disse aminosyrene, for eksempel fra aminosyre 71 til aminosyre 180 eller fra aminosyre 69 til 178. I ett eksempel omfatter eller består trunkert NY-ESO-1 eller LAGE-1 av cirka eller eksakt, aminosyrene 71 til 180 (eller cirka eller eksakt, aminosyrene når det gjelder LAGE-1b). 15 Betegnelsen «cirka» kan i denne sammenheng oppfattes å bety at aminosyrer opp til +/-10% av det totale antall aminosyrer av sekvensen eventuelt er addert eller deletert fra sekvensen. I ett eksempel omfatter eller består trunkert NY-ESO-1 eller LAGE-1 av aminosyrene 71 til 180 av NY-ESO-1 eller LAGE I ett eksempel omfatter eller består trunkert LAGE-1b av et utvalg av aminosyrer fra aminosyre 67, 68, 69, 70, 71, 72, 73, 74 eller 75 til aminosyre 205, 206, 207, 208, 209 eller 210 eller enhver kombinasjon av disse aminosyrene, for eksempel fra aminosyre 71 til aminosyre 210 eller fra aminosyre 69 til 208. I ett eksempel omfatter eller består trunkert LAGE-1b av cirka eller eksakt, aminosyrene 71 til 210. Betegnelsen «cirka» kan i den sammenheng oppfattes å bety at aminosyrer opptil +/- 10% av det totale antall aminosyrer i sekvensen eventuelt er addert eller deletert fra sekvensen. I ett eksempel omfatter eller består trunkert LAGE-1b av aminosyrene 71 til 210 av LAGE-1b. 30 Med «andre fragmenter» menes de som, ved inkorporering i fusjonsproteinet ifølge oppfinnelsen, resulterer i et sluttprotein med de ønskede egenskaper og fordeler til fusjonsproteinene ifølge oppfinnelsen. 35 NY-ESO-1. I overensstemmelse med det foran nevnte tilveiebringes modifiserte antigener som omfatter et antigen avledet fra tumorrejeksjons-antigenet NY-ESO-1, hvor kollagenregionen er partielt trunkert eller fullstendig trunkert. I enkelte eksempler er mer enn kollagenregionen fjernet. I enkelte eksempler er det modifiserte antigen genetisk modifisert. I enkelte eksempler er det modifiserte antigen
11 11 5 rekombinant. I enkelte eksempler tilveiebringes polypeptider som omfatter et antigen som beskrevet i setningene foran. I enkelte eksempler omfatter polypeptideksempler et heterologt protein, så som protein D fra haemophilus influenzae type B eller et fragment derav. I enkelte eksempler tilveiebringes konstruksjoner som omfatter en nukleotidsekvens som koder for de ovennevnte polypeptider. Proteinene for inkludering i en fusjonspartner ifølge foreliggende oppfinnelse, kan være kjemisk konjugert eller uttrykt som rekombinante fusjonsproteiner. I én utførelsesform uttrykkes fusjonsproteinet som et rekombinant fusjonsprotein. 10 Den ytterligere heterologe fusjonspartner kan bidra til å gi T-hjelperepitoper (immunologisk fusjonspartner) eller bidra til å uttrykke proteinet i høyere utbytter (ekspresjonsforsterket). I én utførelsesform kan den ytterligere heterologe fusjonspartner både være en immunologisk fusjonspartner og en ekspresjonsforsterkende partner I én utførelsesform omfatter protein D eller et derivat derav, cirka eller eksakt, den første 1/3 av proteinet, for eksempel cirka eller eksakt, aminosyrene 1 til 109 av protein D. I denne utførelsesform kan aminosyrene 2-Lys og/eller 3-Thr av den native protein D-sekvens være erstattet med aminosyrene 2-Asp og/eller 3-Pro. I en ytterligere utførelsesform omfatter eller består protein D eller derivat derav, av cirka eller eksakt, aminosyrene 20 til 127 av protein D. I én utførelsesform inkluderer ikke proteinet D for bruk i henhold til foreliggende oppfinnelse, sekresjonssekvensen til proteinet. I fusjonsproteiner ifølge foreliggende oppfinnelse er protein D-derivatet i alminnelighet ikke lipidert. 25 I én utførelsesform omfatter protein D ytterligere aminosyrene Met, Asp og Pro for eksempel fusjonert til N-terminalen av protein D-fragmentet (dvs. konstruksjonen kan omfatte eller bestå av «MDP protein D»). Det antas at disse tre ytterligere aminosyrene kan bidra til stabiliteten av proteinet og/eller øke graden av dets proteinekspresjon. 30 I henhold til ett aspekt tilveiebringer oppfinnelsen et fusjonsprotein hvor det N- terminale fragment (dvs. den første tredjedel) av protein D (som beskrevet ovenfor) er fusjonert til N-terminalen av et fusjonsprotein ifølge oppfinnelsen eller et immunogent fragment derav. Nærmere bestemt kan en fusjon av protein D og N- terminalen av fusjonsproteinet ifølge oppfinnelsen skje slik at sistnevnte erstatter det C-terminale fragment av protein D som er blitt fjernet. N-terminalen av protein D blir derved N-terminalen av fusjonsproteinet.
12 12 Andre heterologe fusjonspartnere eller fragmenter derav kan inngå i fusjonsproteinet ifølge oppfinnelsen i stedet for eller i tillegg til protein D, for eksempel: 5 10 det ikke-strukturelle protein fra influensavirus, NS1 (hemagglutinin). Typisk kan de N-terminale 81 aminosyrene benyttes, selv om forskjellige fragmenter kan benyttes forutsatt at de inkluderer T-hjelperepitoper; LytA avledet fra streptococcus pneumoniae, som syntetiserer en N-acetyl-Lalaninamidase LytA kodet av LytA-genet (Gene, 43 (1986) side ) slik som repetisjonsdelen av det LytA-molekyl som finnes i C-terminalen, for eksempel med start i rest 178, så som restene I én utførelsesform er den heterologe fusjonspartner ClytA. I en ytterligere utførelsesform er den heterologe fusjonspartner CPC, et fusjonsprotein som omfatter ClytA-P2-ClytA, som beskrevet i WO03/ Rensing av hybridproteiner som inneholder ClytA-fragmentet i dets aminoterminal har vært beskrevet i Biotechnology:10, (1992) side Fusjonsproteiner ifølge oppfinnelsen kan dessuten innbefatte en affinitets-tag, for eksempel en histidinhale (også kjent som en His-tag) som omfatter mellom 1 og 10, for eksempel 6 eller 10 histidinrester. Disse restene kan for eksempel være i den terminale del, så som den N-terminale og/eller den C-terminale del av proteinet. Denne affinitets-tag kan være inkorporert for ytterligere å forbedre rensingen av proteinet. 25 Enkelte spesifikke fusjonsproteiner ifølge oppfinnelsen kan for eksempel konstrueres som beskrevet i figurene. Hver av de utførelsesformer som er angitt i figurene representerer uavhengige aspekter ved oppfinnelsen. Ytterligere eksempler på konstruksjoner av fusjonsproteinet i henhold til foreliggende oppfinnelse er angitt i Tabell 1-4 og i sekvenslisten. 30 Nukleinsyrer. Foreliggende oppfinnelse omfatter også de nukleinsyrer og polynukleinsyrer, så som DNA, som koder for fusjonsproteiner ifølge oppfinnelsen. Fremgangsmåtene ifølge oppfinnelsen kan gjennomføres ved hjelp av konvensjonell rekombinant teknikk, som beskrevet i Maniatis et al., Molecular Cloning A Laboratory Manual; Cold Spring Harbor, Spesielt kan en prosess omfatte trinnene: i) fremstilling av en replikerbar eller integrerende ekspresjonsvektor som i en vertscelle er i stand til å uttrykke en DNA-polymer som omfatter en
13 13 5 nukleotidsekvens som koder for fusjonsproteinet eller et immunogent derivat derav; ii) transformering av en vertscelle med nevnte vektor; iii) dyrking av nevnte transformerte vertscelle under betingelser som tillater ekspresjon av nevnte DNA-polymer for å fremstille nevnte protein; og iv) gjenvinning av proteinet Betegnelsen «transformering» benyttes her i betydningen innføring av fremmed DNA i en vertscelle. Dett kan oppnås for eksempel ved transformasjon, transfeksjon eller infeksjon med et passende plasmid eller en viral vektor ved å benytte konvensjonelle teknikker som beskrevet i Genetic Engineering; Red. S.M. Kingsman & A.J. Kingsman; Blackwell Scientific Publications; Oxford, England Betegnelsen «transformert» eller «transformant» vil heretter gjelde den resulterende vertscelle som inneholder og uttrykker det fremmede gen av interesse. Ekspresjonsvektorer som omfatter nukleotidsekvenser som koder for fusjonsproteiner ifølge foreliggende oppfinnelse er nye og utgjør også del av oppfinnelsen. 20 De replikerbare ekspresjonsvektorene kan fremstilles i henhold til oppfinnelsen ved å spalte en vektor som er forlikelig med vertscellen, for å gi et lineært DNA-segment som har et intakt replikon, og kombinere nevnte lineære segment med ett eller flere DNA-molekyler, som sammen med nevnte lineære segment koder for det ønskede produkt, så som den DNA-polymer som koder for proteinet ifølge oppfinnelsen eller et derivat derav, under ligeringsbetingelser. DNA-polymeren kan således formes på forhånd eller under konstruksjonen av vektoren, etter ønske Vektorvalget vil til dels bestemmes av vertscellen, som kan være prokaryot eller eukaryot, men er i alminnelighet E.coli eller CHO-celler. Egnede vektorer innbefatter plasmider for eksempel TMCP14 eller pet21 eller pet26, pcdna3, bakteriofager, kosmider og rekombinante virus. I én utførelsesform hvor ekspresjonen skjer i baculovirus, gjær eller CHO-vertsceller, vil én av følgende vektorer kunne benyttes: pee14, ppicza, ppiczb, ppiczc, pdmt-dest48 og pacsg2. Fremstillingen av den replikerbare ekspresjonsvektor kan foretas konvensjonelt med passende enzymer for restriksjon, polymerisasjon og ligering av DNA, ved fremgangsmåter beskrevet for eksempel i Maniatis et al. Sitert ovenfor. 35 Den rekombinante vertscelle fremstilles, i henhold til oppfinnelsen, ved å transformere en vertscelle med en replikerbar ekspresjonsvektor ifølge oppfinnelsen under transformasjonsbetingelser. Egnede transformasjonsbetingelser er de konvensjonelle og er beskrevet for eksempel i Maniatis et al. Sitert ovenfor, eller «DNA Cloning»
14 14 5 Bd.II, D.M. Glover red., IRL Press Ltd Valget av transformasjonsbetingelser bestemmes ut fra vertscellen. En bakteriell vert så som E.coli, kan behandles med en løsning av CaCl2 (Cohen et al., Proc. Nat. Acad. Sci., 1973, 69, 2110) eller med en løsning som inneholder en blanding av RbCl, MnCl2, kaliumacetat og glycerol, og deretter med 3-[N-morfolino]-propan-sulfonsyre, RbCl og glycerol. I kultur kan pattedyrceller transformeres ved kalsium kopresipitasjon av vektor-dna på cellene. Oppfinnelsen omfatter også en vertscelle transformert med en replikerbar ekspresjonsvektor ifølge oppfinnelsen. 10 DNA kan være kodon-optimalisert ved hjelp av standardteknikker for ytterligere å lette ekspresjon av den relevante vert. 15 Dyrkning av den transformerte vertscelle under betingelser som tillater ekspresjon av DNA-polymeren foretas konvensjonelt som beskrevet i for eksempel Maniatis et al. og i «DNA Cloning» sitert ovenfor. Cellen tilføres således fortrinnsvis næringsløsning og dyrkes ved en temperatur lavere enn 50 C. Proteinene ifølge foreliggende oppfinnelse kan uttrykkes i prokaryoter eller eukaryoter, så som gjær, men uttrykkes ofte i E.coli. Spesielle stammer av E.coli så som: 20 AR58: et kryptisk λ-lysogen avledet fra N99 som er gal E::Tn 10,Δ-8(chlD-pgi), Δ-H1(cro-chlA),N + og cl857 (ref: Proc. Natl. Acad. Sci. USA Bd. 82, s , januar 1985 Biochemistry) BLR (DE3) Novagen, WI, USA (katalognummer ): BLR er et reca - derivat av BL21 kan benyttes. I alminnelighet inkorporeres en seleksjonsmarkør, for eksempel kanamycinresistens eller ampicillinresistens for å lette påvisning av vellykket inkorporering av det rekombinante gen/konstruksjon i ekspresjonssystemet Produktet gjenvinnes etter konvensjonelle metoder alt etter vertscellen og i henhold til lokaliseringen av ekspresjonsproduktet (intracellulært eller utskilt i dyrkningsmediet eller i celleperiplasma). Når vertscellen er bakteriell, så som E. coli, kan den således for eksempel lyseres fysisk, kjemisk eller enzymatisk og proteinproduktet isoleres fra det resulterende lysat. Når vertscellen er fra pattedyr kan produktet i alminnelighet isoleres fra næringsmediet eller fra cellefrie ekstrakter. Konvensjonelle proteinisoleringsteknikker innbefatter selektiv utfelling, adsorpsjonskromatografi og affinitetskromatografi inklusivt en monoklonal antistoff-affinitetskolonne. Proteinene ifølge foreliggende oppfinnelse oppnås enten løselige i en flytende form, eller i en lyofilisert form. Foreliggende oppfinnelse tilveiebringer også farmasøytiske
15 15 blandinger, så som en vaksine som omfatter et fusjonsprotein ifølge foreliggende oppfinnelse og et farmasøytisk akseptabelt hjelpestoff. 5 Ved administrering kan den terapeutiske blandingen ifølge foreliggende oppfinnelse administreres i farmasøytisk akseptable tilberedninger. Slike tilberedninger kan vanligvis inneholde farmasøytisk akseptable konsentrasjoner av salt, buffermidler, konserveringsmidler, forlikelige bærere, supplerende immunpotensierende midler så som adjuvanser og cytokiner og eventuelt andre terapeutiske midler Mengdene vil selvsagt avhenge av den bestemte tilstand som skal behandles, tilstandens alvor, de individuelle pasientparametere, herunder alder, fysisk tilstand, størrelse og vekt, behandlingens varighet, (eventuell) samtidig behandling, den bestemte administrasjonsmåte og lignende faktorer innenfor helsepersonalets kunnskap og ekspertise. Disse faktorene er velkjente for fagmannen og kan håndteres uten mer enn rutinemessig eksperimentering. I alminnelighet foretrekkes det at det benyttes en maksimal dose av de enkelte komponenter eller kombinasjoner av disse, som ut fra rimelig medisinsk vurdering er den høyeste dose som trygt kan benyttes. Fagmannen vil imidlertid innse at en pasient kan insistere på en lavere dose eller en tolererbar dose, av medisinske grunner, psykologiske grunner eller faktisk enhver annen grunn. Det vil i alminnelighet forventes at hver human dose vil omfatte µg av proteinet og fortrinnsvis µg. 20 I henhold til ett aspekt vil den farmasøytiske blanding benyttet til administrering av fusjonsproteinene ifølge oppfinnelsen, være en vaksine. Vaksinen kan eventuelt inneholde ett eller flere andre tumorassosierte antigener, polypeptider og/eller peptider, eksempelvis medlemmer av MAGE-, LAGE- og GAGE-familiene. 25 Fusjonsproteinene ifølge foreliggende oppfinnelse kan dessuten eventuelt omfatte én eller flere aminosyrer som «linkere» mellom sekvensene til antigenet og fusjonspartnerne eller fusjonspartner-proteinene eller mellom antigenet og en His-hale, om den forefinnes. Aminosyrene kan være uten relasjon til sekvensene for antigenet og/eller fusjonspartneren. 30 Fusjonsproteiner ifølge foreliggende oppfinnelse, som her beskrevet, kan dessuten omfatte aminosyrene Met-Asp-Pro i den N-terminale ende av fusjonsproteinsekvensen. Met-aminosyren kan være fra den opprinnelige protein-d-sekvens eller fra en urelatert sekvens.
16 16 Foreliggende oppfinnelse innbefatter også fremgangsmåter for fremstilling av nevnte vaksiner/blandinger og fusjonsproteiner og vaksiner/blandinger oppnådd ved eller kan oppnås ved hjelp av de beskrevne fremgangsmåter. 5 Vaksinetilberedninger er generelt beskrevet i Vaccine Design («The subunit and adjuvant approach» (red. Powell, M.F. & Newman, M.J. (1995) Plenum Press New York). Innkapsling i liposomer er beskrevet av Fullerton, US. Patent Fusjonsproteinene ifølge foreliggende oppfinnelse kan inngå som adjuvans i en vaksineformulering ifølge oppfinnelsen. Egnede adjuvanser er et aluminiumsalt så som aluminiumhydroksydgel (alum) eller aluminiumfosfat, men kan også være et salt av kalsium, jern eller zink, eller være en uløselig suspensjon av acylert tyrosin eller acylerte sukkere, kationisk eller anionisk derivatiserte polysakkarider eller polyfosfatzener. Andre kjente adjuvanser innbefatter CpG-holdige oligonukleotider. Oligonukleotidene karakteriseres ved at CpG-dinukleotidet er umetylert. Slike oligonukleotider er velkjente og er beskrevet for eksempel i WO 96/ I formuleringen ifølge oppfinnelsen kan det være ønskelig at adjuvansblandingen induserer en immunrespons som fortrinnsvis er av TH1 typen. I henhold til én utførelsesform tilveiebringes et adjuvanssystem som for eksempel inkluderer en kombinasjon av monofosforyl-lipid A, fortrinnsvis 3-de-O-acylert monofosforyl-lipid A (3D-MPL) sammen med et aluminiumsalt. CpG-oligonukleotider kan også indusere en TH1-respons og kan også inngå I én utførelsesform tilveiebringes en blanding som omfatter et fusjonsprotein som her beskrevet, og en adjuvansblanding som omfatter kombinasjonen av et monofosforyllipid A og et saponinderivat, særlig kombinasjonen av QS21 og 3D-MPL som angitt i WO94/00153, eller en mindre reaktogen blanding hvor QS21 er dempet med kolesterol som angitt i WO 96/ En formulering som kan benyttes omfatter QS21, 3D-MPL & tokoferol for eksempel i en olje-i-vann emulsjon som beskrevet i WO 95/ En annen adjuvansformulering for bruk i henhold til foreliggende oppfinnelse kan omfatte QS21, 3-D-MPL & CpG eller deres tilsvarende, for eksempel i en olje-i-vann emulsjon eller som en liposomal formulering. I én utførelsesform av foreliggende oppfinnelse tilveiebringes følgelig en vaksine som omfatter et fusjonsprotein ifølge oppfinnelsen og en adjuvans, for eksempel som beskrevet ovenfor. Foreliggende oppfinnelse omfatter også fremgangsmåter for fremstilling av vaksiner og blandinger som inneholder fusjonsproteiner som her beskrevet.
17 I henhold til foreliggende oppfinnelse er det også tenkt på avlevering av de her beskrevne nukleinsyrer, polypeptider eller peptider for vaksinasjon. Avlevering av polypeptider og peptider kan skje i henhold til vanlige vaksinasjonsprotokoller som er velkjent på området. I henhold til en annen utførelsesform kan avleveringen av nukleinsyre skje ved ex vivo metoder, dvs. ved å ta ut en celle fra et individ, manipulere cellen genetisk for å innføre et cancer-assosiert antigen og føre den manipulerte celle inn igjen i vedkommende individ. Generelt kan dette involvere innføring in vitro av en funksjonell kopi av et gen inn i et individs celle og returnere de genetisk manipulerte cellene til individet. Den funksjonelle kopi av genet er under operativ kontroll av regulatorelementer som muliggjør ekspresjon av genet i de genetisk manipulerte cellene. Mange transfeksjons- og transduksjons-teknikker så vel som passende ekspresjonsvektorer er velkjent for fagmannen, og enkelte av disse er beskrevet i PCT-søknad WO95/ In vivo nukleinsyre-avlevering ved bruk av vektorer så som virus og målrettede liposomer kan i henhold til oppfinnelsen også tenkes. Forkortelser: CO W/O koll PD1/3 kollagenlignende region uten kollagenlignende region (kollagenlignende domene) protein D, første tredjedel 20 Eksempler på utførelsesformer av fusjonsproteiner og den nukleotidsekvens som koder for disse, er angitt i Tabell Tabell 1. Eksempler på utførelsesformer av fusjonsproteiner og de nukleotidsekvenser som koder for disse er angitt. Hver nukleotidsekvens er beskrevet ved foreliggende stoff, identifisert ved unik nukleotidsekvens-identifikator (SEKV.ID.NR, og angitt i sekvenslisten. Hvert fusjonsprotein er beskrevet ved foreliggende stoff, indentifisert ved unik aminosyresekvens-identifikator (SEKV.ID.NR, og angitt i sekvenslisten. 30
18 18 SEKV. ID.NR: TABELL 1 BESKRIVELSE AV KONSTRUKSJON SEKVENS- KOMPONENTER Hybrid kollagen NY-ESO-1/LAGE1a uten kollagen Utførelsesform A nukleotidsekvens Hybrid koll NY-ESO- 1 1/LAGE1a uten koll (kodonoptimalisert) Kollagen-lignende domene 1-210bp NY-ESO bp Linker bp LAGE1a bp His-tag bp Stopp bp 2 Utførelsesform B-nukleotidsekvens 1/3 protein D/Hybrid koll NY-ESO-1/LAGE1a uten koll (kodonoptimalisert) MDP initieringssekvens 1-9bp 1/3 protein D bp Kollagen-lignende domene bp NY-ESO bp Linker bp LAGE1a bp His-tag bp Stopp bp 3 Utførelsesform A-aminosyresekvens Hybrid koll NY-ESO-1/LAGE1a uten koll med His-tag Kollagen-lignende domene 1-70aa NY-ESO aa Linker aa LAGE1a aa His-tag aa 4 Utførelsesform B-aminosyresekvens 1/3 protein D/Hybrid koll NY-ESO-1/LAGE1a uten koll med His-tag MDP initieringssekvens 1-3aa 1/3 protein D 4-111aa Kollagen-lignende domene aa NY-ESO aa Linker aa LAGE1a aa His-tag aa Hybrid kollagen trunkert NY-ESO-1/LAGE1a uten kollagen 5 Utførelsesform C hybrid koll trunkert NY-ESO-1/LAGE1a uten koll (kodonoptimalisert) Kollagen-lignende domene 1-72bp NY-ESO bp Linker bp LAGE1a bp His-tag bp Stopp bp
19 19 SEKV. ID.NR: TABELL 1 BESKRIVELSE AV KONSTRUKSJON SEKVENS- KOMPONENTER 6 Utførelsesform D-nukleotidsekvens 1/3 protein D/Hybrid koll trunk NY-ESO-1/LAGE1a uten koll (kodonoptimalisert) MDP initieringssekvens 1-9bp 1/3 protein D bp Kollagen-lignende domene bp NY-ESO bp Linker bp LAGE1a bp His-tag bp Stopp bp 7 Utførelsesform C-Hybrid koll trunk NY-ESO-1/LAGE1a uten koll med His-tag Kollagen-lignende domene 1-24aa NY-ESO aa Linker aa LAGE1a aa His-tag aa 8 Utførelsesform D-aminosyresekvens 1/3 protein D/Hybrid koll trunk NY-ESO-1/LAGE1a uten koll med His-tag MDP initieringssekvens 1-3aa 1/3 protein D 4-111aa Kollagen-lignende domene aa NY-ESO aa Linker aa LAGE1a aa His-tag aa Hybrid NY-ESO-1/LAGE1a uten kollagen-lignende domene og sammenhengende cysteinrik region (8aa) 9 Utførelsesform E-nukleotidsekvens Hybrid NY-ESO-1/LAGE1a uten koll (kodonoptimalisert) NY-ESO bp Linker bp LAGE1a bp His-tag bp Stopp bp 10 Utførelsesform F-nukleotidsekvens 1/3 protein D/Hybrid NY-ESO-1/LAGE1a uten koll (kodonoptimalisert) MDP initiseringssekvens 1-9bp 1/3 protein D bp NY-ESO bp Linker bp LAGE1a bp His-tag bp Stopp bp
20 20 SEKV. ID.NR: TABELL 1 BESKRIVELSE AV KONSTRUKSJON SEKVENS- KOMPONENTER 11 Utførelsesform E aminosyresekvens Hybrid NY-ESO-1/LAGE1a uten koll med His-tag NY-ESO aa Linker aa LAGE1a aa His-tag aa 12 Utførelsesform F aminosyresekvens 1/3 protein D/hybrid NY-ESO-1/LAGE1a uten koll med His-tag MDP initieringssekvens 1-3aa 1/3 protein D 4-111aa NY-ESO aa Linker aa LAGE1a aa His-tag aa Hybrid kollagen LAGE1a/NY-ESO-1 uten kollagen 13 Utførelsesform G- nukleotidsekvens Hybrid koll LAGE1a/NY-ESO-1 uten koll (kodonoptimalisert) Kollagen-lignende domene av NY-ESO bp LAGE1a bp Linker bp NY-ESO bp His-tag bp Stopp bp 14 1/3 protein D/Hybrid koll LAGE1a/NY-ESO-1 uten koll (kodonoptimalisert) MDP initieringssekvens 1-9bp 1/3 protein D bp Kollagen-lignende domene av NY-ESO bp LAGE1a bp Linker bp NY-ESO bp His-tag bp Stopp bp 15 Utførelsesform G-aminosyresekvens Hybrid koll LAGE1a/NY-ESO-1 uten koll med His-tag Kollagen-lignende domene av NY-ESO aa LAGE1a aa Linker aa NY-ESO aa His-tag aa 16 1/3 protein D/Hybrid koll LAGE1a/NY-ESO-1 uten Koll med His-tag (kodet av SEKV.ID.NR:14) MDP initieringssekvens 1-3aa 1/3 protein D 4-111aa Kollagen-lignende domene av NY-ESO aa LAGE1a aa Linker aa NY-ESO aa His-tag aa
21 21 SEKV. ID.NR: TABELL 1 BESKRIVELSE AV KONSTRUKSJON SEKVENS- KOMPONENTER Hybrid kollagen trunkert LAGE1a/NY-ESO-1 uten kollagen 17 Hybrid koll trunk LAGE1a/NY-ESO-1 uten koll (kodonoptimalisert) Kollagen-lignende domene av NY-ESO bp LAGE1a bp Linker bp NY-ESO bp His-tag bp Stopp bp 18 1/3 protein D/Hybrid koll trunk LAGE1a/NY-ESO-1 uten koll (kodonoptimalisert) MDP initieringssekvens 1-9bp 1/3 protein D bp Kollagen-lignende domene av NY-ESO bp LAGE1a bp Linker bp NY-ESO bp His-tag bp Stopp bp 19 Hybrid koll trunk LAGE1a/NY-ESO-1 uten koll med His-tag (kodet av SEKV.ID.NR:17) Kollagen-lignende domene av NY-ESO aa LAGE1a aa Linker aa NY-ESO aa His-tag aa 20 1/3 protein D/Hybrid koll trunk LAGE1a/NY-ESO-1 uten Koll med His-tag (kodet av SEKV.ID.NR:18 MDP initieringssekvens 1-3aa 1/3 protein D 4-111aa Kollagen-lignende domene av NY-ESO aa LAGE1a aa Linker aa NY-ESO aa His-tag aa Hybrid LAGE1a/NY-ESO-1 uten kollagen-lignende domene og sammenhengende cysteinrik region (8aa) 21 Utførelsesform E -nukleotidsekvens Hybrid LAGE1a/NY-ESO-1 uten koll. (kodonoptimalisert) LAGE1a 1-309bp Linker bp NY-ESO bp His-tag bp Stopp bp
22 22 SEKV. ID.NR: TABELL 1 BESKRIVELSE AV KONSTRUKSJON SEKVENS- KOMPONENTER 22 1/3 protein D/Hybrid LAGE1a/NY-ESO-1 uten koll (kodonoptimalisert) MDP initieringssekvens 1-9bp 1/3 protein D bp LAGE1a bp Linker bp NY-ESO bp His-tag bp Stopp bp SEKV. ID.NR: TABELL 1 BESKRIVELSE AV KONSTRUKSJON SEKVENS- KOMPONENTER 23 Utførelsesform E -aminosyresekvens Hybrid LAGE1a/NY-ESO-1 uten koll med His-tag LAGE1a 1-103aa Linker aa NY-ESO aa His-tag aa 24 1/3 protein D/hydrid LAGE1a/NY-ESO-1 uten koll med His-tag (kodet av SEKV.ID.NR:22) MDP initieringssekvens 1-3aa 1/3 protein D 4-111aa LAGE1a aa Linker aa NY-ESO aa His-tag aa His-N-terminal Hybrid NY-ESO-1/LAGE1a uten kollagen og sammenhengende cysteinrik region (8aa) 25 His-enterokinase-sete-NY-ESO-1/LAGE1a (kodonoptimalisert) His-tag sekvens 1-36bp Enterokinase-sete 37-72bp NY-ESO bp Linker bp LAGE1a bp Stopp bp 26 His-enterokinase-sete-NY-ESO-1/LAGE1a (kodet av SEKV.ID.NR:25) His-tag (10His) 1-12aa Enterokinase-sete 13-24aa NY-ESO aa Linker aa LAGE1a aa 27 His-NY-ESO-1/LAGE1a (kodonoptimalisert) His-tag sekvens 1-21bp NY-ESO bp Linker bp LAGE1a bp Stopp bp
23 23 28 His-NY-ESO-1/LAGE1a (kodet av SEKV.ID.NR:26) His-tag (6His) 1-7aa NY-ESO aa Linker aa LAGE1a aa SEKV. ID.NR: TABELL 1 BESKRIVELSE AV KONSTRUKSJON SEKVENS- KOMPONENTER His-N-terminal Hybrid kollagen trunkert NY-ESO-1/LAGE1a uten kollagen 29 His-enterokinase-sete-koll trunk-ny-eso-1/lage1a (kodonoptimalisert) His-tag sekvens 1-36bp Enterokinase-sete 37-72bp Kollagen-lignende domene bp NY-ESO bp Linker bp LAGE1a bp Stopp bp 30 His-enterokinase-sete-koll trunk-ny-eso-1/lage1a (kodet av SEKV.ID.NR:29) His-tag (10His) 1-12aa Enterokinase-sete 13-24aa Kollagen-lignende domene 25-47aa NY-ESO aa Linker aa LAGE1a aa 31 His-koll trunk-ny-eso-1/lage1a (kodonoptimalisert) His-tag sekvens 1-21bp Kollagen-lignende domene 22-90bp NY-ESO bp Linker bp LAGE1a bp Stopp bp 32 His-koll trunk-ny-eso-1/lage1a (kodet av SEKV.ID.NR:31) His-tag (6His) 1-7aa Kollagen-lignende domene 8-30aa NY-ESO aa Linker aa LAGE1a aa His N-terminal Hybrid kollagen NY-ESO-1/LAGE1a uten kollagen-lignende domene 33 His-enterokinase-sete-koll-NY-ESO-1/LAGE1a (kodonoptimalisert) His-tag sekvens 1-36bp Enterokinase-sete 37-72bp Kollagen-lignende domene bp NY-ESO bp Linker bp LAGE1a bp Stopp bp
24 24 SEKV. ID.NR: TABELL 1 BESKRIVELSE AV KONSTRUKSJON SEKVENS- KOMPONENTER 34 His-enterokinase-sete-koll-NY-ESO-1/LAGE1a (kodet av SEKV.ID.NR:33) His-tag (10His) 1-12aa Enterokinase-sete 13-24aa Kollagen-lignende domene 25-93aa NY-ESO aa Linker aa LAGE1a aa 35 His-koll-NY-ESO-1/LAGE1a(kodonoptimalisert) His-tag sekvens 1-21bp Kollagen-lignende domene bp NY-ESO bp Linker bp LAGE1a bp Stopp bp 36 His-koll-NY-ESO-1/LAGE1a (kodet av SEKV.ID.NR:35) His-tag (6His) 1-7aa Kollagen-lignende domene 8-76aa NY-ESO aa Linker aa LAGE1a aa His-N-terminal Hybrid LAGE1a/NY-ESO-1 uten kollagen og sammenhengende cysteinrik region (8aa) 37 His-enterokinase-sete-LAGE1a/NY-ESO-1 (kodonoptimalisert) His-tag sekvens 1-36bp Enterokinase-sete 37-72bp LAGE1a bp Linker bp NY-ESO bp Stopp bp 38 His-enterokinase-sete-LAGE1a/NY-ESO-1 (kodet av SEKV.ID. NR:37) His-tag (10His) 1-12aa Enterokinase-sete 13-24aa LAGE1a aa Linker aa NY-ESO aa
25 25 SEKV. ID.NR: TABELL 1 BESKRIVELSE AV KONSTRUKSJON SEKVENS- KOMPONENTER 39 His-LAGE1a/NY-ESO-1 (kodonoptimalisert) His-tag sekvens 1-21bp LAGE1a bp Linker bp NY-ESO bp Stopp bp 40 His-LAGE1a/NY-ESO-1 (kodet av SEKV.ID.NR:39) His-tag (6His) 1-7aa LAGE1a 8-109aa Linker aa NY-ESO aa His-N-terminal Hybrid kollagen trunkert LAGE1a/NY-ESO-1 uten kollagen 41 His-enterokinase-sete-koll trunk-lage1a/ny-eso-1 (kodonoptimalisert) His-tag sekvens 1-36bp Enterokinase-sete 37-72bp Kollagen-lignende domene av NY-ESO bp LAGE1a bp Linker bp NY-ESO bp Stopp bp 42 His-enterokinase-sete-koll trunk-lage1a/ NY-ESO-1 (kodet av SEKV.ID.NR:41) His-tag (10His) 1-12aa Enterokinase-sete 13-24aa Kollagen-lignende domene av NY-ESO aa LAGE1a aa Linker aa NY-ESO aa 43 His-koll trunk-lage1a/ny-eso-1 (kodonoptimalisert) His-tag sekvens 1-21bp Kollagen-lignende domene av NY-ESO bp LAGE1a bp Linker bp NY-ESO bp Stopp bp 44 His-koll trunk-lage1a/ny-eso-1 (kodet av SEKV.ID.NR:43) His-tag (6His) 1-7aa Kollagen-lignende domene av NY-ESO aa LAGE1a aa Linker aa NY-ESO aa
26 26 SEKV. ID.NR: TABELL 1 BESKRIVELSE AV KONSTRUKSJON SEKVENS- KOMPONENTER His N-terminal Hybrid kollagen LAGE1a/NY-ESO-1 uten kollagen-lignende domene 45 His-enterokinase-sete-koll-LAGE1a/NY-ESO-1 (kodonoptimalisert) His-tag sekvens 1-36bp Enterokinase-sete 37-72bp Kollagen-lignende domene av NY-ESO bp LAGE1a bp Linker bp NY-ESO bp Stopp bp 46 His-enterokinase-sete-koll-LAGE1a/NY-ESO-1 (kodet av SEKV.ID.NR:45) His-tag (10His) 1-12aa Enterokinase-sete 13-24aa Kollagen-lignende domene av NY-ESO aa LAGE1a aa Linker aa NY-ESO aa 47 His-koll-LAGE1a/NY-ESO-1 (kodonoptimalisert) His-tag sekvens 1-21bp Kollagen-lignende domene av NY-ESO bp LAGE1a bp Linker bp NY-ESO bp Stopp bp 48 His-koll-LAGE1a/NY-ESO-1 (kodet av SEKV.ID. NR:47) His-tag (6His) 1-7aa Kollagen-lignende domene av NY-ESO aa LAGE1a aa Linker aa NY-ESO aa 5 Tabell 2 Ytterligere eksempler på utførelsesformer av fusjonsproteiner og de nukleotidsekvenser som koder for disse er angitt. Hver nukleotidsekvens er beskrevet ved foreliggende stoff, identifisert ved unik nukleotidsekvens-identifikator (SEKV.ID. NR, og angitt i sekvenslisten. Hvert fusjonsprotein er beskrevet ved foreliggende stoff, identifisert ved unik aminosyresekvens-identifikator (SEKV.ID.NR, og angitt i sekvenslisten. 10
27 27 SEKV. ID.NR: TABELL 2 BESKRIVELSE AV KONSTRUKSJON SEKVENS- KOMPONENTER Delvis trunkert kollagen NY-ESO-1 50 Koll trunk NY-ESO-1 (kodonoptimalisert) Kollagen-lignende domene 1-72bp NY-ESO bp His-tag bp Stopp bp 51 Koll trunk NY-ESO-1 med His-tag (kodet av SEKV.ID.NR:50) Kollagen-lignende domene 1-24aa NY-ESO aa His-tag aa 52 1/3 protein D/koll trunk NY-ESO-1 (kodonoptimalisert) MDP initieringssekvens 1-9bp 1/3 protein D bp Kollagen-lignende domene bp NY-ESO bp His-tag bp Stopp bp 53 1/3 protein D/koll trunk NY-ESO-1 med His-tag (kodet av SEKV.ID.NR:52) MDP initieringssekvens 1-3aa 1/3 protein D 4-111aa Kollagen-lignende domene aa NY-ESO aa His-tag aa NY-ESO-1 uten koll 54 NY-ESO-1 uten koll (kodonoptimalisert) NY-ESO bp His-tag bp Stopp bp 55 NY-ESO-1 uten koll med His-tag (kodet av SEKV.ID.NR:54) NY-ESO aa His-tag aa 56 1/3 protein D/NY-ESO-1 uten koll (kodonoptimalisert) MDP initieringssekvens 1-9bp 1/3 protein D bp NY-ESO bp His-tag bp Stopp bp 57 1/3 protein D/NY-ESO-1 uten koll med His-tag (kodet av SEKV.ID.NR:56) MDP initieringssekvens 1-3aa 1/3 protein D 4-111aa NY-ESO aa His-tag aa
28 28 5 Tabell 3 Ytterligere eksempler på utførelsesformer av fusjonsproteiner og de nukleotidsekvenser som koder for disse er angitt. Hver nukleotidsekvens er beskrevet ved foreliggende stoff, identifisert ved unik nukleotidsekvens-identifikator (SEKV.ID.NR, og angitt i sekvenslisten. Hvert fusjonsprotein er beskrevet ved foreliggende stoff, identifisert ved unik aminosyresekvens-identifikator (SEKV.ID.NR, og angitt i sekvenslisten. SEKV. ID.NR: TABELL 3 BESKRIVELSE SEKVENS- KOMPONENTER Hybrid kollagen LAGE-1a uten LAGE-1a kollagen-lignende domene 59 Hybrid koll LAGE-1a uten koll (kodonoptimalisert) Kollagen-lignende domene av NY-ESO bp LAGE-1a bp His-tag bp Stopp bp 60 Hybrid koll LAGE-1a uten koll med His-tag (kodet av SEKV.ID.NR:59) Kollagen-lignende domene av NY-ESO aa LAGE-1a aa His-tag aa 61 1/3 protein D/Hybrid koll LAGE-1a uten koll med His-tag (kodonoptimalisert) MDP initieringssekvens 1-9bp 1/3 protein D bp Kollagen-lignende domene av NY-ESO bp LAGE-1a bp His-tag bp Stopp bp 62 1/3 protein D/Hybrid koll LAGE-1a uten koll med His-tag (kodet av SEKV.ID.NR:61) MDP initieringssekvens 1-3aa 1/3 protein D 4-111aa Kollagen-lignende domene av NY-ESO aa LAGE-1a aa His-tag aa
29 29 SEKV. ID.NR: TABELL 3 BESKRIVELSE SEKVENS- KOMPONENTER Hybrid kollagen trunkert LAGE-1a uten kollagen-lignende domene 63 Hybrid kollagen trunkert Lage-1a uten kollagen-lignende domene Kollagen-lignende domene av NY-ESO bp LAGE-1a bp His-tag bp Stopp bp 64 Hybrid koll trunk LAGE-1a uten koll med His-tag (kodet av SEKV.ID.NR:63) Kollagen-lignende domene av NY-ESO aa LAGE-1a aa His-tag aa SEKV. ID.NR: TABELL 3 BESKRIVELSE SEKVENS- KOMPONENTER 65 1/3 protein D/Hybrid koll trunk LAGE-1a uten koll med His-tag (kodonoptimalisert) MDP initieringssekvens 1-9bp 1/3 protein D bp Kollagen-lignende domene av NY-ESO bp LAGE-1a bp His-tag bp Stopp bp 66 1/3 protein D/Hybrid koll trunk LAGE-1a uten koll med His-tag (kodet av SEKV.ID.NR:65) MDP initieringssekvens 1-3aa 1/3 protein D 4-111aa Kollagen-lignende domene av NY-ESO aa LAGE-1a aa His-tag aa LAGE-1a uten kollagen-lignende domene og sammenhengende cysteinrik region(8aa) 67 LAGE-1a uten koll (kodonoptimalisert) LAGE-1a 1-309bp His-tag bp Stopp bp 68 LAGE-1a uten koll med His-tag (kodet av SEKV.ID.NR:67) LAGE-1a 1-103aa His-tag aa 69 1/3 protein D/LAGE-1a uten koll (kodonoptimalisert) MDP initieringssekvens 1-9bp 1/3 protein D bp LAGE-1a bp His-tag bp Stopp bp 70 1/3 protein D/LAGE-1a uten koll med His-tag (kodet av SEKV.ID.NR:69) MDP initieringsekvens 1-3aa 1/3 protein D 4-111aa LAGE-1a aa His-tag aa
30 30 5 Tabell 4 Fusjonsproteinene omtalt i eksemplene og de nukleotidsekvenser som koder for disse angis her. Hver nukleotidsekvens er beskrevet ved foreliggende stoff, identifisert ved unik nukleotidsekvens-identifikator (SEKV.ID.NR, og angitt i sekvenslisten. Hvert fusjonsprotein er beskrevet ved foreliggende stoff, identifisert ved unik aminosyresekvens-identifikator (SEKV.ID.NR, og angitt i sekvenslisten. Tabell 4 Konstruksjonsnavn Nukleotidsekvens Aminosyresekvens LVL020 SEKV.ID.NR:72 SEKV.ID.NR:73 LVL024 SEKV.ID.NR:74 SEKV.ID.NR:75 LVL026 SEKV.ID.NR:76 SEKV.ID.NR:77 LVL030 SEKV.ID.NR:78 SEKV.ID.NR:79 LVL068 SEKV.ID.NR:80 SEKV.ID.NR:81 LVL076 SEKV.ID.NR:82 SEKV.ID.NR:83 LVL078 SEKV.ID.NR:84 SEKV.ID.NR:85 LVL079 SEKV.ID.NR:86 SEKV.ID.NR:87 LVL106 SEKV.ID.NR:88 SEKV.ID.NR:89 LVL151 SEKV.ID.NR:90 SEKV.ID.NR:91 LVL155 SEKV.ID.NR:92 SEKV.ID.NR:93 LVL156 SEKV.ID.NR:94 SEKV.ID.NR:95 LVL157 SEKV.ID.NR:96 SEKV.ID.NR: Det fremgår klart fra sekvenslisten at mange at konstruksjonene i Tabell 4 har lignende design som én eller flere utførelsesformer angitt i de foregående tabeller. For eksempel har LVL068 samme design som utførelsesformen angitt som SEKV.ID.NR:45, Tabell 1. LVL076 har den samme design som utførelsesformen angitt som SEKV.ID.NR:25, Tabell 1. LVL078 har den samme design som utførelsesformen angitt som SEKV.ID.NR:33, Tabell 1. LVL079 har den samme design som utførelsesformen angitt som SEKV.ID.NR:37, Tabell Dessuten ble flere av fusjonsproteinkonstruksjonene angitt i Tabell 4, nemlig LVL155, LVL106, LVL156, LVL157, LVL151 frembragt ved rutinemodifikasjoner av andre fusjonsproteinsekvenser angitt i Tabell 4, nemlig henholdsvis LVL068, LVL030,
31 31 5 Tabell 5. Samsvar mellom LVL068, LVL030, LVL076, LVL078, LVL024 og modifisert LVL155, LVL106, LVL156, LVL157, LVL Tabell 5 KORRESPONDERER MED LVL076, LVL078, LVL024. Slike modifikasjoner inkluderer fjerningen av aminosyrerestene mellom protein D og begynnelsen av kimærene (dvs. den del som er avledet fra en av NY-ESO-1 og LAGE-1) og fjerningen av aminosyrene mellom His-tag og begynnelsen av kimæren. Enkelte av fusjonsproteinene i Tabell 4 samsvarer således nært med andre fusjonsproteiner i Tabell 4. Samsvaret mellom disse fusjonsproteinene er angitt i Tabell 5 og mer detaljert beskrevet i Eksempel 4. FUSJONSPROTEIN- KONSTRUKSJON LVL068 LVL030 LVL076 LVL078 LVL024 FUSJONSPROTEIN- KONSTRUKSJON LVL155 LVL106 LVL156 LVL157 LVL151 EKSEMPLER Eksempel 1. NY-LA1 kimærprotein-design og fremstilling Diverse NY-ESO-1/LAGE-1 fusjonsproteiner ble konstruert med og uten det kollagenlignende domene og med og uten terminalen av protein D slik som sammenfattet i Figur 17. Konstruksjonene ble kodonoptimalisert for ekspresjon Escherichia coli. Det syntetiske gen ble satt sammen fra oligonukleotider og/eller PCR-produkter. Fragmentet ble klonet inn i pga4-ryggraden (AmpR) ved å benytte KpnI- og SacIrestriksjonsseter med addisjonen av NdeI- og XhoI-seter henholdsvis i 5 -enden og 3 -enden av det optimaliserte gen. 25 Plasmidet DNA ble renset fra transformerte bakterier og konsentrasjonen bestemt ved UV-spektrometri. Den endelige konstruksjon ble verifisert ved sekvensering. Den optimaliserte kodende sekvens for de forskjellige NY/LAGE kimære konstruksjoner ble subklonet direkte inn i pet19 (AmpR) multippelt kloningssete ved bruk av NdeI- og XhoI-restriksjonsseter for å oppnå de NY/LAGE kimære ekspresjonsplasmidene. For
32 kloning inn i pet26, ble det konstruert PCR-primere for å addere N-terminal histidinhale. Denne amplifiseringen resulterte i addisjon av 6 histidin-halen i fase med den kodende region av de forskjellige konstruksjonene. Dette amplifiserte fragment ble oppsluttet enzymatisk med NdeI/XhoI-restriksjonsenzymer, og de forskjellige NY/LAGE kimære konstruksjonene ble deretter klonet inn i pet26 (KanR) multippelt kloningssete for å oppnå ekspresjonsplasmidet. De endelige konstruksjonene ble verifisert ved sekvensering. Rysteflaske-produksjon. Vekst og induksjon av bakteriell vertsstamme. Kultur Bakterier ble dyrket på 800mL Luria-Bertani (LB) buljong (BD) + 1% (vekt/vol) glukose (Laboratoire MAT, katalognummer: GR-0101) + antibiotikum (carbenicillin 100µg/mL for pet19, kanamycin 40µg/mL for pet26) i 2,5L rysteflaske. Kulturene ble inkubert ved 37 C for BLR (DE3) celler inntil en O.D. 600nm på cirka 0, Induksjon Ved O.D. 600nm på cirka 0,8 ble kulturene BLR (DE3) indusert med 1mM isopropyl-β-d- 1-tiogalaktopyranosid (IPTG; EMD Chemicals Inc., katalognummer: 5815) og inkubert i timer ved 16 C. 5 til 15mg spesifikt protein/800ml er blitt oppnådd med konstruksjon LVL106, 151, 155 og 157. Proteinproduksjonen for hver konstruksjon er sammenfattet Figur Eksempel 2. Sammenfatning av preliminær rensing og stabilitet Ekstraksjon og rensing av proteinet Celler ble høstet ved sentrifugering og deretter sprengt ved hjelp av fysikalske eller kjemiske midler, og det resulterende råekstrakt benyttet for å isolere polypeptidet av interesse. 30 Rensing De uttrykte rekombinante proteinene ble solubilisert med guanidinhydroklorid-løsning og avsatt på en immobilisert metallaffinitets-kromatografiharpiks (IMAC). Proteiner ble deretter vasket på kolonnen med 8M og 4M urealøsninger før eluering med økende imidazol-konsentrasjon. Proteiner ble deretter avsaltet i den endelige 4M urea-buffer, ph7,0 for videre bruk. Rensingen ble evaluert ved SDS PAGE og Western blotting, for å verifisere renheten og identiteten av proteinene. 35 Stabilitetstest av renset fusjonsprotein
33 33 Stabilitetsbestemmelser ble foretatt ved 37 C, og proteiner ble evaluert vedsds- PAGE. Preliminær stabilitetsbestemmelse avdekket ikke major issue. 5 Preliminær solubiliseringstest Løseligheten av proteinene ble vurdert som sammenfattet i det følgende diagram. KONSTRUKSJON BUFFER LVL 076 LVL 079 LVL 78 LVL 68 LVL 020 LVL 26 LVL 024 LVL 30 PBS 1X; 1mM TCEP; 1mM EDTA, ph 7,03 p S S P P P NT P 20mM bicine;138mm NaCl; 1mM TCEP; p S P P P P NT P 1mM EDTA, phh 8,68 20mM imidazol; 138mM NaCl;1mM TCEP; p S P P P P NT P 1mM EDTA, ph 5,99 10mM natriumacetat; 5mM NaCl; 1mM TCEP S S S S S S NT S 1mM EDTA, ph 4,99 10mM sitronsyre; 5mM NaCl; 1mM TCEP; 1mM EDTA, ph 3,7 NT NT S S NT NT NT S Diagram 1. Fusjonsprotein-solubilitet Nøkkel: P-presipitat; S intet presipitat; NT ikke testet Eksempel 3: IM-immunisering med fusjonsproteiner Fusjonsproteinene ble evaluert preklinisk i en musemodell som involvert en rekke intramuskulære immunisasjons-screeninger, som beskrevet nedenfor. Musemodellen som ble valgt var CB6F1, en første generasjon som skrev seg fra kryssningen av C57BL6 mus og Balb/c mus. Slike mus er kommersielt tilgjengelige fra Charles River Laboratories, Inc., 251 Ballardvale Street, Wilmington, MA Den valgte tumorcellelinje var B16 (musemelanom-cellelinje), et transplanterbart murint melanom som er kommersielt tilgjengelig for studium av cancerterapier.
34 34 5 Screening Nr. 1 Forsøksopplegg. I et 76-dagers forsøk ble CB6F1 mus benyttet til å vurdere hver av LVL076, LVL079, LVL078, LVL068, LVL020, LVL026, LVL024, LVL030 for å bestemme hvorvidt intramuskulær immunisering med fusjonsprotein pluss adjuvans ga beskyttelse mot subkutant irritament med transplanterte tumorceller (B16/NYESO1). Nærmere bestemt ble mus immunisert intramuskulært med 50µL injeksjoner inneholdende 15µg protein og en adjuvans. Adjuvansen som ble valgt var AS15. AS15 er en liposomal adjuvansformulering som inneholder QS21, 3D-MPL og CpG Forsøk ble foretatt med fusjonsproteiner angitt nedenfor i 1A og 1B. Mus ble delt i grupper på 15 mus/gruppe. Mus ble immunisert på dag 0 og igjen på dag 14 som følger: Forsøk 1A LVL079 LVL026 LVL068 LVL030 Forsøk 1B LVL076 LVL020 LVL078 LVL024 Kontroller Antigenbuffer/AS15-buffer Fullengdes NY-ESO-1 LAGE-1a uten det kollagenlignende domene (CLD) MAGE A Seks mus/gruppe ble utsatt for irritament med subkutant transplantert B16/NY-ESO- 1-tumorer på dag 28. Antistoffrespons på NY-ESO-1 fullengde, LAGE-1a uten kollagenlignende domene og humant kollagen ble bestemt på dag 0, 14, 28 og 76 ved ELISA (IgG1 og IgG2a). Cellemediert respons ble bestemt ved FACS på dag 28 ved å benytte høstede splenocytter (restimulering 3 forråd på 3 med NY-ESO-1 og LAGE-1a peptidforråd). Forsøksopplegget for screening Nr. 1 er sammenfattet i Figur 18.
35 35 5 Resultater. Av de fire kontrollene ga bare fullengdes NY-ESO-1 en viss beskyttelse sammenlignet med buffer. Se Figur 19. Av de grupper av mus som fikk enten fullengdes NY-ESO-1 eller LVL030 var to fra hver gruppe tumorfri ved slutten av forsøket. Av musene som fikk LVL068 var fire tumorfri ved slutten av studiet. LVL068 og LVL078 ga lenger overlevelse sammenlignet med mus som fikk buffere. Se Figur 20. NY-ESO-1-spesifikke immunresponser ble bestemt ved ELISA, FACS og Western blotting. LAGE-1a (uten det kollagenlignende domene) spesifikke immunresponser ble bestemt ved ELISA og FACS. Se Figur 21. Disse resultatene er sammenfattet i det følgende diagram. 10 Immunogen B16/NY-ESO-1 Beskyttelse NY-ESO-1 Spesifikk immunitet LAGE1a Spesifikk immunitet LVL LVL LVL LVL LVL LVL LVL LVL Diagram 2. Spesifikk immunitet sammenfatning Nøkkel: (-) lavest respons; (+) middels respons; (++) høyest respons Screening Nr. 2 Forsøksopplegg. I et 105-dagers forsøk ble CB6F1 mus benyttet til å vurdere hver av LVL076, LVL078, LVL068 og LVL024 for å bestemme hvorvidt intramuskulær immunisering med fusjonsprotein pluss adjuvans ga beskyttelse mot subkutant irritament med B16/NYESO1-transplanterte tumorceller (etter to immuniseringer) eller med B16/LAGE-1a-tumorceller (etter fire immuniseringer). Nærmere bestemt ble mus immunisert intramuskulært med 50µL injeksjoner inneholdende 15µg protein og 25µL AS15 adjuvans. 25 Mus ble delt i grupper på 29 mus/gruppe. Mus ble immunisert på dag 0, 14, 28 og 42 som følger:
36 Forsøk LVL076 LVL068 LVL078 LVL024 Kontroller Antigenbuffer/AS15-buffer Full lengde NY-ESO-1 LAGE-1a uten det kollagenlignende domene (CLD) MAGE A3 15 Ti mus/gruppe ble utsatt for irritament med subkutant transplantert B16/NY-ESO-1 tumorceller på dag 28. Ni mus/gruppe ble gitt irritament med subkutant transplanterte B16/LAGE-1a tumorceller på dag 56. Serum ble uttatt og antistoffrespons på (i) NY- ESO-1 full lengde, (ii) LAGE-1a uten kollagenlignende domene og (ii) humant kollagen ble bestemt på dag 0, 14, 28, 42, 56, 84 og 105 ved ELISA (IgG1 og IgG2a). Forsøksopplegget for screening Nr. 2 er sammenfattet i Figurene 22 og 23. Resultater B16/NYESO1 Tumor-irritament Av de mus som fikk LVL078 var to tumorfrie i over 50 dager etter B16-NY-ESO-1- irritament. Av de mus som enten fikk fullengde NY-ESO-1 eller LVL024 var to fra hver gruppe tumorfrie i over 50 dager, tre var i live. Av de mus som fikk LVL068 var tre tumorfrie og fire i live. Av de mus som fikk LVL076 var tre tumorfrie og fem i live. Se Figur B16-LAGE1a Tumor-irritament Alle mus som fikk LVL076 eller LAGE-1a uten den kollagenlignende region var døde tidligere enn dag 40 etter irritament. Av de mus som kun fikk buffer overlevde én tumorfri til avsluttet studium. Av de mus som fikk LVL024 var én tumorfri ved slutten av studiet. Av de mus som fikk fullengdes NY-ESO-1 var ingen tumorfrie, men én var fremdeles levende ved slutten av studiet. Av de som fikk LVL078 var én mus tumorfri. Av som fikk LVL068 var tre mus tumorfrie. Av de mus som fikk LVL076 var tre tumorfrie ved slutten av studien. Se Figur 25. Disse resultatene er sammenfattet i det følgende diagram.
37 37 NY-ESO-1 LAGE-1a Immunogen Beskyttelse Spesifikk immunitet Beskyttelse Spesifikk immunitet LVL LVL LVL024 ± LVL Diagram 3. Beskyttelse versus B16-LAGE1a tumor-irritament. Nøkkel: Nøkkel: (-) lavest; (±) nest lavest respons; (+) middels respons; (++) høyest respons Human kollagenspesifikke immunresponser For å undersøke hvorvidt det kollagenlignende domene av NY-ESO-1 stimulerte human kollagenspesifikke immunresponser ble sera uttatt og sammenslått 14 dager etter inokulering fra mus immunisert med ett av følgende: (1) buffere (kontroll); (2) fullengdes NY-ESO-1; (3) LAGE-1a uten det kollagenlignende domene; (4) LVL068; (5) LVL078; (6) LVL024; (7) LVL076. ELISA ble foretatt for hver av disse syv serumforråd så vel som for en positiv kontroll inneholdende mab antihumant kollagen I. Det kollagenlignende domene stimulerte ikke mus-antihumant kollagen I antistoffproduksjon. Se Figur 26. Lignende studier (resultater ikke vist) ble foretatt for kollagen III og kollagen VI. Verken mus anti-humant kollagen III eller musantihumant kollagen VI antistoff-produksjon ble påvist Eksempel 4: Forbedrede konstruksjoner Modifikasjoner ble foretatt ved å benytte rutinemessige kloningsteknikker for enkelte av konstruksjonene angitt i Tabell 4. Nærmere bestemt ble LVL068, LVL030, LVL076, LVL078, LVL024 modifisert for å gi LVL155, LVL106, LVL156, LVL157, LVL151. Det ble foretatt to slags modifikasjoner, først fjerningen av 5 aminosyrerester mellom protein D og starten av kimærene. Denne modifikasjon ble for eksempel foretatt med LVL024 (SEKV.ID.NR:74; SEKV.ID.NR:75) for å gi LVL151 (SEKV.ID.NR:90; SEKV.ID.NR:91). LVL024 tilsvarer således LVL151. Den andre type modifikasjon var fjerningen av aminosyrene mellom His-tag og begynnelsen av kimæren. Denne modifikasjon ble foretatt med LVL068 (SEKV.ID.NR:80; SEKV.ID.NR:81) for å gi LVL155 (SEKV.ID.NR:92; SEKV.ID.NR:93). LVL068 tilsvarer således LVL151. Hver fusjonsproteinkonstruksjon som var modifisert og fusjonsproteinkonstruksjonen som den tilsvarer er angitt i Tabell 5 i beskrivelsen. 30
38 38 5 Det vil være klart at modifikasjonene beskrevet ovenfor ikke forventes å resultere i funksjonelle forskjeller mellom et fusjonsprotein og dets tilsvarende modifiserte fusjonsprotein. Det forventes således at man kan benytte hvert modifiserte fusjonsprotein angitt på høyre side av Tabell 5 om hverandre med dets tilsvarende fusjonsprotein angitt på den venstre siden i diagrammet. 10 Eksempel 5 Forsøksopplegg. I et 105 dagers forsøk ble CB6F1 mus benyttet til å vurdere hver av LVL068, LVL030, LVL076, LVL078, LVL024 og det modifiserte LVL155, LVL106, LVL156, LVL157, LVL151 for å studere intramuskulær immunisering med fusjonsproteinet pluss adjuvans, mot subkutant irritament med B16/NYESO1-transplanterte tumorceller (etter to immuniseringer) eller med B16/LAGE-1a tumorceller (etter fire immuniseringer). Nærmere bestemt ble mus immunisert intramuskulært med 50µL injeksjoner inneholdende 15µg protein og 25µL av AS15 adjuvans Mus ble inndelt i grupper på 29 mus/gruppe. Mus ble immunisert på dag 0, 14, 28 og 42 som følger: Forsøk LVL068 LVL030 LVL076 LVL078 LVL024 LVL155 LVL106 LVL156 LVL157 LVL151 Kontroller Antigenbuffer/AS15 buffer Full lengde NY-ESO-1 LAGE-1a uten det kollagenlignende domene MAGE A3 35 Ti mus/gruppe ble utsatt for irritament med subkutant transplanterte B16/NY-ESO-1 tumorceller på dag 28. Ni mus/gruppe ble utsatt for irritament med subkutant transplanterte B16/LAGE-1a tumorceller på dag 56. For å overvåke spesifikk immun-
39 39 respons kan det uttas sera og antistoffrespons måles til (i) NY-ESO-1 full lengde, (ii) LAGE-1a uten kollagenlignende domene og (ii) human-kollagen på dag 0, 14, 28, 42, 56, 84 og 105 ved ELISA (IgG1 og IgG2a). 5 De foregående eksempler er tatt med som illustrasjon, ikke som begrensning. 10 I den foreliggende beskrivelse er artikkelen «en» og «et» her benyttet for å angi én eller flere enn én (dvs. minst én) av artikkelens grammatiske objekt. Som eksempel betyr «et element» ett eller flere elementer. Betegnelsen «tilnærmet» og «cirka» er her ment eventuelt å kunne utelates eller erstattes med betegnelsen «eksakt» dersom søkeren krever det Enheter, prefikser og symboler kan være angitt i deres SI-aksepterte form. Om intet annet er angitt er nukleinsyre skrevet fra venstre mot høyre i 5 til 3 orientering; aminosyresekvenser skrevet fra venstre mot høyre i amino-karboksy-orientering. Numeriske områder inkluderer de tall som definerer området. Aminosyrer kan her være omtalt enten ved deres vanlig kjente tre-bokstavs symboler eller ved enbokstavs symbolene anbefalt av IUPAC-IUB Biochemical Nomenclature Commission. Nukleotider kan likeledes være omtalt med deres vanlig aksepterte en-bokstavs kode. De ovenfor definerte betegnelser defineres mer fullstendig ved henvisning til beskrivelsen i sin helhet.
40 5 40
41 41
42 42
43 43
44 44
45 45
46 46
47 5 47
48 48
49 49
50 50
51 51
52 5 52
53 5 53
54 54
55 55
56 56
57 57
58 58
59 59
60 60
61 5 61
62 62
63 63
64 64
65 65
66 66
67 67
68 68
69 5 69
70 70
71 71
72 72
73 73
74 5 74
75 75
76 76
77 77
78 78
79 5 79
80 80
81 81
82 82
83 83
84 84
85 85
86 86
87 5 87
88 5 88
89 89
90 90
91 91
92 92
93 93
94 5 94
95 95
96 96
97 97
98 98
99 5 99
100 5 100
101 5 101
102 102
103 103
104 104
105 105 5 PATENTKRAV 1. Fusjonsprotein omfattende: (a) NY-ESO-1 eller et fragment derav, koblet til (b) LAGE-1 eller et fragment derav, hvor minst ett av NY-ESO-1 og/eller LAGE-1 er trunkert eller delvis trunkert, eller er et fragment som inkluderer en eller flere epitoper av NY-ESO-1 eller LAGE-1, hvor fusjonsproteinet omfatter en aminosyresekvens valgt fra gruppen bestående av SEKV.ID.NR:73, SEKV.ID.NR:75, SEKV.ID.NR:79, SEKV.ID.NR:81, SEKV.ID.NR:83, SEKV.ID.NR:85, SEKV.ID.NR:89, SEKV.ID.NR:93 og SEKV.ID.NR: Nukleinsyremolekyl som koder for fusjonsproteinet ifølge krav Vektor som inneholder nukleinsyremolekylet ifølge krav Vertscelle transformert med en vektor ifølge krav Immunogen blanding eller vaksine som inneholder et fusjonsprotein i henhold til krav 1, et nukleinsyremolekyl som angitt i krav 2 eller en vektor som angitt i krav 3, som i tillegg inneholder en adjuvans og/eller et immunstimulerende cytokin eller kjemokin. 6. Immunogen blanding eller vaksine som angitt i krav 5, for medisinsk anvendelse.
106 106 1/26
107 107 2/26
108 108 3/26
109 109 4/26
110 110 5/26
111 111 6/26
112 112 7/26
113 113 8/26
114 114 9/26
115 115 10/26
116 116 11/26 Figur 11 Kollagen-lignende
117 117 12/26 Figur 12 Trunkert
118 118 13/26 Figur 13 Trunkert
119 119 14/26 Figur 14 Trunkert
120 120 15/26 Figur 15 Mest immunogen (T-celle), MEN divergent region Kollagen-lignende domene Sentral region Kollagen-lignende domene Sentral region
121 (Kollagen-lignende) Sentral sentral Mest immunogen (T-celle), Men divergent region /26 Figur 16
122 Kol-lig.. Dom (CLD) Trunk. Kol. lig. dom /26 Figur 17
123 2. immunisering 9 Mus/gruppe CMI (Splenocytter).restimulering (blandinger av 3) med NYESO1, LAGE1a peptide blandinger Tumor eksponering B16/NYESO1 tumorvekst oppfølging (6 mus/gruppe) Figur 18. Humant kollagen 1. Immunisering Mus/gruppe Koll.lig.dom (CLD) /26
124 Tumorstørrelse (mm2) Tumorstørrelse (mm2) Dager etter eksmponering Dager etter eksponering Gjennomsnittlig tid for Tumorvekst (100 mm2) 0/6 tumorfri Antigen/adjuvant buffer Dager etter eksponering Dager etter eksponering /26 Figur 19 Tumorstørrelse (mm2) Tumorstørrelse (mm2)
125 125 20/26 Figur 20 Prosent overlevelse 4 tumorfri 2 tumorfri 2 tumorfri Prosent overlevelse Dager etter eksponering 2 tumorfri Dager etter eksponering
126 126 21/26 Figur 21 Screening#1: NYESO1 spesifikke immunresponser Immunogener Screening #1: LAGE 1a w/o CLD spesifikke immunresponser Immunogener
127 Dager B16-NY eksponering Mus/gruppe ELISA (sera): 1gG1, 1gG2a. NYESO1-FL. LAGE1a w/o CLD (LVL75). Humant kollagen B16/NYES01 tumorvekst oppfølging (10 mus/gruppe) B16/Lage 1a tumorvekst oppfølging (9 mus/gruppe) /26 Figur 22
128 1. Immunis. 2. Immunis. Mus/gruppe B16-LA1 eksponering Immunis. Immunis. Humant kollagen B16/NYESO1 tumorvekst oppfølging ( 10 mus/gruppe) B16/Lage 1 a tumorvekst oppfølging (9 mus/gruppe) /26 Figur 23
129 129 24/26 Prosent overlevelse Figur 24 3 tumorfri/4 levende 2 tumorfri/3 levende Buffere 2 tumorfri Prosent overlevelse Dager etter eksponering 3 tumorfri/5 levende 2 tumorfri/3 levende Buffere 2 tumorfri/3 levende Dager etter eksponering
130 130 25/26 Prosent overlevelse (mus med tumorer under 200 mm2) Figur 25 Buffere 3/9 (3 tumorfri for LVL068) 1/9 (1 tumorfri for LVL078) 1/9 (0 tumorfri for LVL078) 1/8 (1 tumorfri for buffere) Dager etter B16F10/LAGE-1a eksponering Prosent overlevelse (mus med tumorer under 200mm2) Buffere 1/9 (1 tumorfri for LVL024) 1/9 (0 tumorfri for NYESO-1) 1/8 (1 tumorfri for buffere 0/9 (0 tumorfri for LVL076) og LAGE1a w/o CLD Dager etter B16F10/LAGE-1a eksponering
131 131 26/26 Figur 26 Sammenslåtte sera 14 dager etter 4:1/500 Buffere
1. En ikke-naturlig forekommende eller konstruert sammensetning omfattende:
 1 Patentkrav EP2931898 1. En ikke-naturlig forekommende eller konstruert sammensetning omfattende: et leveringssystem som er operativt konfigurert for å levere CRISPR-Caskomplekskomponenter eller polynukleotidsekvenser
1 Patentkrav EP2931898 1. En ikke-naturlig forekommende eller konstruert sammensetning omfattende: et leveringssystem som er operativt konfigurert for å levere CRISPR-Caskomplekskomponenter eller polynukleotidsekvenser
PATENTKRAV. og en første lett kjede og en andre lett kjede, hvor første og andre lette kjeder er forskjellige.
 1 PATENTKRAV 1. Isolert monoklonalt antistoff som bærer en forskjellig spesifisitet i hvert kombinasjonssete og som består av to kopier av et enkelt tung kjede polypeptid og en første lett kjede og en
1 PATENTKRAV 1. Isolert monoklonalt antistoff som bærer en forskjellig spesifisitet i hvert kombinasjonssete og som består av to kopier av et enkelt tung kjede polypeptid og en første lett kjede og en
EP Patentkrav. 1. En sammensetning som omfatter:
 1 Patentkrav EP2129 1 2 3 1. En sammensetning som omfatter: et fusjonsprotein som omfatter første og andre peptid-deler, karakterisert ved at nevnte første peptid-del består av en aminosyresekvens valgt
1 Patentkrav EP2129 1 2 3 1. En sammensetning som omfatter: et fusjonsprotein som omfatter første og andre peptid-deler, karakterisert ved at nevnte første peptid-del består av en aminosyresekvens valgt
2. Polypeptid ifølge krav 1, hvor polypeptidet utløser en beskyttende immunrespons hos en pattedyrvert mot stammer av C.difficile.
 1 Patentkrav 1 1. Polypeptid som omfatter et første fragment og et andre fragment, hvor (i) det første fragmentet er et toksin A repeterende domenefragment; (ii) det andre fragmentet er et toksin B repeterende
1 Patentkrav 1 1. Polypeptid som omfatter et første fragment og et andre fragment, hvor (i) det første fragmentet er et toksin A repeterende domenefragment; (ii) det andre fragmentet er et toksin B repeterende
2. Fremgangsmåten ifølge krav 1, hvori dsrna-duplekset har en lengde fra 8 basepar (bp) ti 30 bp.
 1 Patentkrav 1. Fremgangsmåte for å endre et mål-dna, der fremgangsmåten omfatter å bringe mål-dna-et i kontakt med et kompleks omfattende: (a) et Cas9-polypeptid og (b) et enkeltmolekyl-rna som er målrettet
1 Patentkrav 1. Fremgangsmåte for å endre et mål-dna, der fremgangsmåten omfatter å bringe mål-dna-et i kontakt med et kompleks omfattende: (a) et Cas9-polypeptid og (b) et enkeltmolekyl-rna som er målrettet
Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten
 1 Patentkrav 1. Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten omfatter: innsetting inn i et gnagercellegenom;
1 Patentkrav 1. Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten omfatter: innsetting inn i et gnagercellegenom;
EP Patentkrav
 1 EP26727 Patentkrav 1. Monoklonalt antistoff, eller et funksjonelt fragment derav som spesifikt gjenkjenner ett eller flere Siglec- polypeptider bestående av en aminosyresekvens som beskrevet i hvilket
1 EP26727 Patentkrav 1. Monoklonalt antistoff, eller et funksjonelt fragment derav som spesifikt gjenkjenner ett eller flere Siglec- polypeptider bestående av en aminosyresekvens som beskrevet i hvilket
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2131860 B1 (19) NO NORGE (51) Int Cl. A61K 39/395 (2006.01) Patentstyret (21) Oversettelse publisert 2014.03.24 (80) Dato for Den Europeiske Patentmyndighets
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2131860 B1 (19) NO NORGE (51) Int Cl. A61K 39/395 (2006.01) Patentstyret (21) Oversettelse publisert 2014.03.24 (80) Dato for Den Europeiske Patentmyndighets
'1$YDNVLQHUÃHQÃQ\ÃYDNVLQDVMRQVVWUDWHJLÃ
 '1$YDNVLQHUÃHQÃQ\ÃYDNVLQDVMRQVVWUDWHJLÃ $XGXQÃ1HUODQGÃ 'HWÃHUÃLQJHQÃWYLOÃRPÃDWÃYDNVLQHULQJÃHUÃHQÃDYÃKRYHGJUXQQHQHÃWLOÃDWÃILVNHRSSGUHWWÃ KDUÃYRNVWÃWLOÃHQÃDYÃ1RUJHVÃVW UVWHÃQ ULQJHUÃLÃO SHWÃDYÃGHÃVLVWHÃÃnUHQHÃ7UDVVÃLÃ
'1$YDNVLQHUÃHQÃQ\ÃYDNVLQDVMRQVVWUDWHJLÃ $XGXQÃ1HUODQGÃ 'HWÃHUÃLQJHQÃWYLOÃRPÃDWÃYDNVLQHULQJÃHUÃHQÃDYÃKRYHGJUXQQHQHÃWLOÃDWÃILVNHRSSGUHWWÃ KDUÃYRNVWÃWLOÃHQÃDYÃ1RUJHVÃVW UVWHÃQ ULQJHUÃLÃO SHWÃDYÃGHÃVLVWHÃÃnUHQHÃ7UDVVÃLÃ
Det vedlegges et nytt kravsett som ønskes lagt til grunn for søknadens videre behandling.
 Patentstyret Postboks 8160 Dept 0033 Oslo Patentavdelingen Dato 26. mars 2014 Deres ref. 200031183 Vår ref. E29031 TFU/MJU Norsk patentsøknad nr. 20031183 Vaksine - SmithKline Beecham Biologicals SA Det
Patentstyret Postboks 8160 Dept 0033 Oslo Patentavdelingen Dato 26. mars 2014 Deres ref. 200031183 Vår ref. E29031 TFU/MJU Norsk patentsøknad nr. 20031183 Vaksine - SmithKline Beecham Biologicals SA Det
1. Isolert protein omfattende et stabilisert aktivin IIB reseptor polypeptid, hvori polypeptidet er valgt fra gruppen bestående av:
 1 Patentkrav. 1. Isolert protein omfattende et stabilisert aktivin IIB reseptor polypeptid, hvori polypeptidet er valgt fra gruppen bestående av: (a) et polypeptid bestående av sekvensen representert ved
1 Patentkrav. 1. Isolert protein omfattende et stabilisert aktivin IIB reseptor polypeptid, hvori polypeptidet er valgt fra gruppen bestående av: (a) et polypeptid bestående av sekvensen representert ved
Bioteknologi i dag muligheter for fremtiden
 Bioteknologi i dag muligheter for fremtiden Arvestoff Genetisk materiale, DNA. Baser En del av et nukleotid som betegnes med bokstavene A, C, G og T. Med disse fire bokstavene skriver DNAtrådene sine beskjeder
Bioteknologi i dag muligheter for fremtiden Arvestoff Genetisk materiale, DNA. Baser En del av et nukleotid som betegnes med bokstavene A, C, G og T. Med disse fire bokstavene skriver DNAtrådene sine beskjeder
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2140006 B1 (19) NO NORWAY (51) Int Cl. C12N 15/53 (2006.01) C12N 9/02 (2006.01) C12P 7/64 (2006.01) Norwegian Industrial Property Office (21)
(12) Translation of european patent specification (11) NO/EP 2140006 B1 (19) NO NORWAY (51) Int Cl. C12N 15/53 (2006.01) C12N 9/02 (2006.01) C12P 7/64 (2006.01) Norwegian Industrial Property Office (21)
NORGE. Patentstyret (12) SØKNAD (19) NO (21) (13) A1
 (12) SØKNAD (19) NO (21) 20093386 (13) A1 NORGE (51) Int Cl. C07K 16/18 (2006.01) C07K 16/12 (2006.01) C07K 16/08 (2006.01) A61K 39/395 (2006.01) C12P 21/08 (2006.01) C12N 15/13 (2006.01) A61P 35/00 (2006.01)
(12) SØKNAD (19) NO (21) 20093386 (13) A1 NORGE (51) Int Cl. C07K 16/18 (2006.01) C07K 16/12 (2006.01) C07K 16/08 (2006.01) A61K 39/395 (2006.01) C12P 21/08 (2006.01) C12N 15/13 (2006.01) A61P 35/00 (2006.01)
4260 Mikrobiologi. Midtprøveoppgaver. 02. oktober 2013
 1 Høgskolen i Telemark Fakultet for allmennvitenskapelige fag 4260 Mikrobiologi Midtprøveoppgaver 02. oktober 2013 Tid: 2 timer Sidetall: 7 (40 spørsmål) Hjelpemidler: Ingen Velg kun ett svaralternativ
1 Høgskolen i Telemark Fakultet for allmennvitenskapelige fag 4260 Mikrobiologi Midtprøveoppgaver 02. oktober 2013 Tid: 2 timer Sidetall: 7 (40 spørsmål) Hjelpemidler: Ingen Velg kun ett svaralternativ
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2150617 B1 (19) NO NORGE (51) Int Cl. C12N 15/85 (2006.01) C12N 15/86 (2006.01) Patentstyret (21) Oversettelse publisert 2015.03.02 (80) Dato for
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2150617 B1 (19) NO NORGE (51) Int Cl. C12N 15/85 (2006.01) C12N 15/86 (2006.01) Patentstyret (21) Oversettelse publisert 2015.03.02 (80) Dato for
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2606064 B1 (19) NO NORWAY (1) Int Cl. C07K 16/00 (06.01) C07K 16/24 (06.01) C07K 16/28 (06.01) C07K 16/46 (06.01) C12N 1/ (06.01) Norwegian
(12) Translation of european patent specification (11) NO/EP 2606064 B1 (19) NO NORWAY (1) Int Cl. C07K 16/00 (06.01) C07K 16/24 (06.01) C07K 16/28 (06.01) C07K 16/46 (06.01) C12N 1/ (06.01) Norwegian
FYS3710 Molekylærbiologi
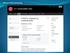 1 2 I en eukaryot celle er kromosomene festet i en indre membran som omgir en kjerne. Proteinene produseres i cellens cytoplasma. 3 I en prokaryot celle (for eksempel en bakteriecelle) er det ett kromosom.
1 2 I en eukaryot celle er kromosomene festet i en indre membran som omgir en kjerne. Proteinene produseres i cellens cytoplasma. 3 I en prokaryot celle (for eksempel en bakteriecelle) er det ett kromosom.
Nytt om influensavaksiner. Hanne Nøkleby, Nasjonalt folkehelseinstitutt
 Nytt om influensavaksiner Hanne Nøkleby, Nasjonalt folkehelseinstitutt Nytt på influensavaksinefronten Erfaring med levende, nasal vaksine Influensavaksiner med adjuvans Helt nye influensavaksiner Levende,
Nytt om influensavaksiner Hanne Nøkleby, Nasjonalt folkehelseinstitutt Nytt på influensavaksinefronten Erfaring med levende, nasal vaksine Influensavaksiner med adjuvans Helt nye influensavaksiner Levende,
Anvendelse av en sensibiliseringssammensetning for et eksplosiv
 1 Anvendelse av en sensibiliseringssammensetning for et eksplosiv BAKGRUNN FOR OPPFINNELSEN [0001] Denne oppfinnelsen vedrører generelt en sensibiliseringssammensetning for anvendelse med slurry- og emulsjonssprengstoff
1 Anvendelse av en sensibiliseringssammensetning for et eksplosiv BAKGRUNN FOR OPPFINNELSEN [0001] Denne oppfinnelsen vedrører generelt en sensibiliseringssammensetning for anvendelse med slurry- og emulsjonssprengstoff
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2121731 B1 (19) NO NORGE (51) Int Cl. A61K 39/00 (2006.01) C07K 14/47 (2006.01) C07K 14/745 (2006.01) Patentstyret (21) Oversettelse publisert 2013.12.23
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2121731 B1 (19) NO NORGE (51) Int Cl. A61K 39/00 (2006.01) C07K 14/47 (2006.01) C07K 14/745 (2006.01) Patentstyret (21) Oversettelse publisert 2013.12.23
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2193803 B1 (19) NO NORGE (51) Int Cl. A61K 39/00 (2006.01) C12N 15/13 (2006.01) Patentstyret (21) Oversettelse publisert 2012.02.13 (80) Dato for
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2193803 B1 (19) NO NORGE (51) Int Cl. A61K 39/00 (2006.01) C12N 15/13 (2006.01) Patentstyret (21) Oversettelse publisert 2012.02.13 (80) Dato for
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2328616 B1 (19) NO NORWAY (1) Int Cl. A61K 39/39 (2006.01) C07K 16/18 (2006.01) Norwegian Industrial Property Office (21) Translation Published
(12) Translation of european patent specification (11) NO/EP 2328616 B1 (19) NO NORWAY (1) Int Cl. A61K 39/39 (2006.01) C07K 16/18 (2006.01) Norwegian Industrial Property Office (21) Translation Published
(12) PATENT (19) NO (11) 330271 (13) B1 NORGE. (51) Int Cl. Patentstyret
 (12) PATENT (19) NO (11) 3271 (13) B1 NORGE (1) Int Cl. G06Q /00 (06.01) Patentstyret (21) Søknadsnr 08 (86) Int.inng.dag og søknadsnr (22) Inng.dag.03.04 (8) Videreføringsdag (24) Løpedag.03.04 () Prioritet
(12) PATENT (19) NO (11) 3271 (13) B1 NORGE (1) Int Cl. G06Q /00 (06.01) Patentstyret (21) Søknadsnr 08 (86) Int.inng.dag og søknadsnr (22) Inng.dag.03.04 (8) Videreføringsdag (24) Løpedag.03.04 () Prioritet
Forløp av ikke-adaptiv og adaptiv immunrespons. Mononukleære celler, metylfiolett farging
 Forløp av ikke-adaptiv og adaptiv immunrespons Mononukleære celler, metylfiolett farging 1 Nøytrofile granulocytter Gjenkjennelsesprinsipper medfødt vs. adaptiv immunitet Toll Like Receptors Mikroorganismer
Forløp av ikke-adaptiv og adaptiv immunrespons Mononukleære celler, metylfiolett farging 1 Nøytrofile granulocytter Gjenkjennelsesprinsipper medfødt vs. adaptiv immunitet Toll Like Receptors Mikroorganismer
NORGE. Patentstyret (12) SØKNAD (19) NO (21) 20101728 (13) A1. (51) Int Cl. G06Q 20/00 (2006.01)
 (12) SØKNAD (19) NO (21) 1728 (13) A1 NORGE (1) Int Cl. G06Q /00 (06.01) Patentstyret (21) Søknadsnr 1728 (86) Int.inng.dag og søknadsnr (22) Inng.dag.12. (8) Videreføringsdag (24) Løpedag.12. () Prioritet.03.04,
(12) SØKNAD (19) NO (21) 1728 (13) A1 NORGE (1) Int Cl. G06Q /00 (06.01) Patentstyret (21) Søknadsnr 1728 (86) Int.inng.dag og søknadsnr (22) Inng.dag.12. (8) Videreføringsdag (24) Løpedag.12. () Prioritet.03.04,
Forelesninger i BI Cellebiologi Proteinrensing - Væskekromatografi. Figure 3-43 b
 Proteinrensing - Væskekromatografi Figure 3-43 b Proteinrensing - Væskekromatografi Ved affinitets-kromatografi brukes en søyle med kuler som er dekket med ligander (f.eks. et enzym-substrat eller et annet
Proteinrensing - Væskekromatografi Figure 3-43 b Proteinrensing - Væskekromatografi Ved affinitets-kromatografi brukes en søyle med kuler som er dekket med ligander (f.eks. et enzym-substrat eller et annet
T celle aktivering og HLA Trond S. S. Halstensen
 T celle aktivering og HLA Trond S. S. Halstensen T-celler og Thymus T cellens identifisering av antigener Human Leukocyt Antigen (HLA) restriksjon, CD4 og CD8 Antigen prosessering: cytosol- og endocytisk
T celle aktivering og HLA Trond S. S. Halstensen T-celler og Thymus T cellens identifisering av antigener Human Leukocyt Antigen (HLA) restriksjon, CD4 og CD8 Antigen prosessering: cytosol- og endocytisk
Søker: University of Massachusetts og E. R. Squibb & Sons L.L.C.
 O.nr. 113075/ EH/KN/KN Patentsøknad nr. 20063767 Søker: University of Massachusetts og E. R. Squibb & Sons L.L.C. Tittel: Isolert monoklonalt antistoff eller antigen bindende del derav, samt anvendelse
O.nr. 113075/ EH/KN/KN Patentsøknad nr. 20063767 Søker: University of Massachusetts og E. R. Squibb & Sons L.L.C. Tittel: Isolert monoklonalt antistoff eller antigen bindende del derav, samt anvendelse
Hva er en vaksine? Hanne Nøkleby, Nasjonalt folkehelseinstitutt
 Hva er en vaksine? Hanne Nøkleby, Nasjonalt folkehelseinstitutt Utgangspunktet Mange infeksjonssykdommer gir langvarig / livslang immunitet Vaksinering har som mål å få kroppen til å utvikle samme immunitet
Hva er en vaksine? Hanne Nøkleby, Nasjonalt folkehelseinstitutt Utgangspunktet Mange infeksjonssykdommer gir langvarig / livslang immunitet Vaksinering har som mål å få kroppen til å utvikle samme immunitet
Polynukleotid som omfatter en nukleinsyre valgt fra gruppen som består av: a) en nukleinsyre med en nukleinsyresekvens som vist i SEKV. ID nr.
 168 PATENTKRAV 1. Polynukleotid som omfatter en nukleinsyre valgt fra gruppen som består av: a) en nukleinsyre med en nukleinsyresekvens som vist i SEKV. ID nr. 1; 5 b) en nukleinsyre som koder for et
168 PATENTKRAV 1. Polynukleotid som omfatter en nukleinsyre valgt fra gruppen som består av: a) en nukleinsyre med en nukleinsyresekvens som vist i SEKV. ID nr. 1; 5 b) en nukleinsyre som koder for et
1. Medfødt og ervervet immunitet. Karl Schenck, V2015
 1. Medfødt og ervervet immunitet Karl Schenck, V2015 Medfødt og ervervet immunforsvar Antimicrobial peptides «Alltid beredt!» Relativt uspesifikt Må aktiveres Spesifikt Komponenter av medfødt immunitet
1. Medfødt og ervervet immunitet Karl Schenck, V2015 Medfødt og ervervet immunforsvar Antimicrobial peptides «Alltid beredt!» Relativt uspesifikt Må aktiveres Spesifikt Komponenter av medfødt immunitet
Det vises til Patentstyrets skriv av 6. juni 2014 i ovenfor nevnte patentsøknad.
 Patentstyret Postboks 8160 Dept 0033 Oslo Patentavdelingen Dato 3. september 2014 Deres ref. 20031183 Vår ref. E29031 KOH/HBA Norsk patentsøknad nr. 20031183 Vaksine - SmithKline Beecham Biologicals SA
Patentstyret Postboks 8160 Dept 0033 Oslo Patentavdelingen Dato 3. september 2014 Deres ref. 20031183 Vår ref. E29031 KOH/HBA Norsk patentsøknad nr. 20031183 Vaksine - SmithKline Beecham Biologicals SA
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2222697 B1 (19) NO NORGE (1) Int Cl. C07K 14/70 (06.01) Patentstyret (21) Oversettelse publisert 13.04.29 (80) Dato for Den Europeiske Patentmyndighets
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2222697 B1 (19) NO NORGE (1) Int Cl. C07K 14/70 (06.01) Patentstyret (21) Oversettelse publisert 13.04.29 (80) Dato for Den Europeiske Patentmyndighets
4. Antigenpresentasjon til T celler. MHC molekyler.
 Immunologi 3. semester, V2015 4. Antigenpresentasjon til T celler. MHC molekyler. Karl Schenck Institutt for oral biologi TcR og MHC molekyler Noen hovedgrupper T celler som forlater thymus T celler med
Immunologi 3. semester, V2015 4. Antigenpresentasjon til T celler. MHC molekyler. Karl Schenck Institutt for oral biologi TcR og MHC molekyler Noen hovedgrupper T celler som forlater thymus T celler med
(12) PATENT (19) NO (11) 332854 (13) B1 NORGE. (51) Int Cl. Patentstyret
 (12) PATENT (19) NO (11) 33284 (13) B1 NORGE (1) Int Cl. B01D 1/00 (2006.01) B01D 3/10 (2006.01) Patentstyret (21) Søknadsnr 2009011 (86) Int.inng.dag og søknadsnr (22) Inng.dag 2009.01.08 (8) Videreføringsdag
(12) PATENT (19) NO (11) 33284 (13) B1 NORGE (1) Int Cl. B01D 1/00 (2006.01) B01D 3/10 (2006.01) Patentstyret (21) Søknadsnr 2009011 (86) Int.inng.dag og søknadsnr (22) Inng.dag 2009.01.08 (8) Videreføringsdag
Denne beskrivelsen dreier seg om alternative fremgangsmåter og emulsjoner til de som er beskrevet i WO2005/
 1 SPISELIG EMULSJON 5 Denne beskrivelsen vedrører spiselige emulsjoner. Beskrivelsen vedrører også fremgangsmåter for å fremstille spiselige emulsjoner, og/eller fremgangsmåter for å fremstille majonessammensetninger.
1 SPISELIG EMULSJON 5 Denne beskrivelsen vedrører spiselige emulsjoner. Beskrivelsen vedrører også fremgangsmåter for å fremstille spiselige emulsjoner, og/eller fremgangsmåter for å fremstille majonessammensetninger.
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2176 B1 (19) NO NORWAY (1) Int Cl. A01K 67/027 (06.01) C07K 16/00 (06.01) C07K 16/46 (06.01) C12N 1/8 (06.01) Norwegian Industrial Property
(12) Translation of european patent specification (11) NO/EP 2176 B1 (19) NO NORWAY (1) Int Cl. A01K 67/027 (06.01) C07K 16/00 (06.01) C07K 16/46 (06.01) C12N 1/8 (06.01) Norwegian Industrial Property
idet, en eller flere innskuddshendelser anvender den setespesifikke rekombinasjonen,
 1 Patentkrav 1. Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten omfatter: innsetting inn i et gnagercellegenom;
1 Patentkrav 1. Fremgangsmåte for å produsere en gnager med evne til å produsere et repertoar av kimære antistoffer eller tunge antistoffkjeder, idet fremgangsmåten omfatter: innsetting inn i et gnagercellegenom;
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 26098 B1 (19) NO NORWAY (1) Int Cl. C07K 14/08 (06.01) C12Q 1/70 (06.01) Norwegian Industrial Property Office (21) Translation Published 16..24
(12) Translation of european patent specification (11) NO/EP 26098 B1 (19) NO NORWAY (1) Int Cl. C07K 14/08 (06.01) C12Q 1/70 (06.01) Norwegian Industrial Property Office (21) Translation Published 16..24
Flervalgsoppgaver: proteinsyntese
 Flervalgsoppgaver - proteinsyntese Hver oppgave har ett riktig svaralternativ. Proteinsyntese 1 Hva blir transkribert fra denne DNA sekvensen: 3'-C-C-G-A-A-T-G-T-C-5'? A) 3'-G-G-C-U-U-A-C-A-G-5' B) 3'-G-G-C-T-T-A-C-A-G-5'
Flervalgsoppgaver - proteinsyntese Hver oppgave har ett riktig svaralternativ. Proteinsyntese 1 Hva blir transkribert fra denne DNA sekvensen: 3'-C-C-G-A-A-T-G-T-C-5'? A) 3'-G-G-C-U-U-A-C-A-G-5' B) 3'-G-G-C-T-T-A-C-A-G-5'
Sammenligningen mellom Arabidopsis thaliana genomet og de kjente genomene fra cyanobakterier, gjær, bananflue og nematode, viser bl. a.
 Sammenligningen mellom Arabidopsis thaliana genomet og de kjente genomene fra cyanobakterier, gjær, bananflue og nematode, viser bl. a. Antall gener som er involvert i cellulær kommunikasjon og signaloverføring
Sammenligningen mellom Arabidopsis thaliana genomet og de kjente genomene fra cyanobakterier, gjær, bananflue og nematode, viser bl. a. Antall gener som er involvert i cellulær kommunikasjon og signaloverføring
Hvordan standardisere en metode for isolering av plasmid til syntese av diabetes antigener?
 Hvordan standardisere en metode for isolering av plasmid til syntese av diabetes antigener? Ranveig Østrem, Bioingeniør Hormonlaboratoriet, Aker Oslo Universitetssykehus Bakgrunn for analysen Pasienter
Hvordan standardisere en metode for isolering av plasmid til syntese av diabetes antigener? Ranveig Østrem, Bioingeniør Hormonlaboratoriet, Aker Oslo Universitetssykehus Bakgrunn for analysen Pasienter
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2465864 B1 (19) NO NORGE (51) Int Cl. C07K 14/47 (2006.01) A61K 39/00 (2006.01) A61P 35/00 (2006.01) C07K 14/745 (2006.01) C12N 5/10 (2006.01) G01N
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2465864 B1 (19) NO NORGE (51) Int Cl. C07K 14/47 (2006.01) A61K 39/00 (2006.01) A61P 35/00 (2006.01) C07K 14/745 (2006.01) C12N 5/10 (2006.01) G01N
europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 217099 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61K 39/39 (06.01) A61P 3/00 (06.01) Patentstyret (21) Oversettelse publisert 14.02.17 (80)
(12) Oversettelse av europeisk patentskrift (11) NO/EP 217099 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61K 39/39 (06.01) A61P 3/00 (06.01) Patentstyret (21) Oversettelse publisert 14.02.17 (80)
GENETISKE MEKANISMER INVOLVERT I SPREDING AV RESISTENS
 GENETISKE MEKANISMER INVOLVERT I SPREDING AV RESISTENS KRISTIN HEGSTAD OUTLINE Hvordan erverves nye egenskaper? Mekanismer for horisontal genoverføring (HGT) Genetiske elementer involvert i spredning Definisjoner
GENETISKE MEKANISMER INVOLVERT I SPREDING AV RESISTENS KRISTIN HEGSTAD OUTLINE Hvordan erverves nye egenskaper? Mekanismer for horisontal genoverføring (HGT) Genetiske elementer involvert i spredning Definisjoner
Tittel: Fremgangsmåte for dannelse av disulfidbindinger
 V1483NO00 EP 2190987 B1 Tittel: Fremgangsmåte for dannelse av disulfidbindinger 1 1 2 3 Beskrivelse Oppfinnelsens bakgrunn [0001] I 190 viste Smith for første gang at filamentøs bakteriofag tolererer innsetning
V1483NO00 EP 2190987 B1 Tittel: Fremgangsmåte for dannelse av disulfidbindinger 1 1 2 3 Beskrivelse Oppfinnelsens bakgrunn [0001] I 190 viste Smith for første gang at filamentøs bakteriofag tolererer innsetning
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 240726 B1 (19) NO NORGE (1) Int Cl. H0K 3/36 (2006.01) H0K 3/42 (2006.01) H0K 3/46 (2006.01) Patentstyret (21) Oversettelse publisert 2014.03.17 (80)
(12) Oversettelse av europeisk patentskrift (11) NO/EP 240726 B1 (19) NO NORGE (1) Int Cl. H0K 3/36 (2006.01) H0K 3/42 (2006.01) H0K 3/46 (2006.01) Patentstyret (21) Oversettelse publisert 2014.03.17 (80)
Leketøysbyggesett. Med det er det mulig f.eks. for et barn å bygge konstruksjoner, så som leketøysfigurer med leddede kroppsdeler.
 1 Leketøysbyggesett Foreliggende oppfinnelse vedrører et leketøysbyggesett omfattende en gruppe av byggeelementer, som hvert har minst én kule anordnet på byggeelementet, og hvor kulen er koblet til andre
1 Leketøysbyggesett Foreliggende oppfinnelse vedrører et leketøysbyggesett omfattende en gruppe av byggeelementer, som hvert har minst én kule anordnet på byggeelementet, og hvor kulen er koblet til andre
FR tilveiebringer et kimært antistoff med variabelt område som kan gjenkjenne interleukin-2-reseptor.
 1 1 2 3 Den foreliggende søknaden har prioritet i forhold til US foreløpig søknad nr. 60/469,600 innsendt 6. mai 03, US foreløpige søknad nr. 60/487,964 innsendt 17. juli 03 og US foreløpigs søknad nr.
1 1 2 3 Den foreliggende søknaden har prioritet i forhold til US foreløpig søknad nr. 60/469,600 innsendt 6. mai 03, US foreløpige søknad nr. 60/487,964 innsendt 17. juli 03 og US foreløpigs søknad nr.
Vaksineprinsipper og immunrespons
 Vaksineprinsipper og immunrespons - Hvordan virker vaksiner på immunforsvaret vårt? Lisbeth Meyer Næss Seniorforsker Divisjon for Smittevern Folkehelseinstituttet Nordisk naturmedisinsk fagkongress 2015
Vaksineprinsipper og immunrespons - Hvordan virker vaksiner på immunforsvaret vårt? Lisbeth Meyer Næss Seniorforsker Divisjon for Smittevern Folkehelseinstituttet Nordisk naturmedisinsk fagkongress 2015
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2242771 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61P 3/00 (06.01) Patentstyret (21) Oversettelse publisert 13.09. (80) Dato for Den Europeiske
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2242771 B1 (19) NO NORGE (1) Int Cl. C07K 16/28 (06.01) A61P 3/00 (06.01) Patentstyret (21) Oversettelse publisert 13.09. (80) Dato for Den Europeiske
MENVEO vaksine mot meningokokkinfeksjon gruppe A, C, W135 og Y (konjugert)
 MENVEO vaksine mot meningokokkinfeksjon gruppe A, C, W135 og Y (konjugert) Christian Syvertsen, Seksjon for biologiske legemidler og vaksiner September 2010. Menveo godkjent i sentral prosedyre (EU) European
MENVEO vaksine mot meningokokkinfeksjon gruppe A, C, W135 og Y (konjugert) Christian Syvertsen, Seksjon for biologiske legemidler og vaksiner September 2010. Menveo godkjent i sentral prosedyre (EU) European
ML-208, generell informasjon
 ML-208, generell informasjon Emnekode: ML-208 Emnenavn: Molekylærbiologi Dato:20.12.2017 Varighet:4 timer Tillatte hjelpemidler: Ingen Merknader:Lag gjerne tegninger og figurer for å illustrere og forklare
ML-208, generell informasjon Emnekode: ML-208 Emnenavn: Molekylærbiologi Dato:20.12.2017 Varighet:4 timer Tillatte hjelpemidler: Ingen Merknader:Lag gjerne tegninger og figurer for å illustrere og forklare
LEKSJON 4: BIOTEKNOLOGI HVORDAN VI BRUKER NATURENS EGNE MEKANISMER TIL VÅR FORDEL, OG UTFORDRINGENE SOM FØLGER MED
 LEKSJON 4: BIOTEKNOLOGI HVORDAN VI BRUKER NATURENS EGNE MEKANISMER TIL VÅR FORDEL, OG UTFORDRINGENE SOM FØLGER MED KOMPETANSEMÅL Forklarebegrepene krysning og genmodifisering, og hvordan bioteknologi brukes
LEKSJON 4: BIOTEKNOLOGI HVORDAN VI BRUKER NATURENS EGNE MEKANISMER TIL VÅR FORDEL, OG UTFORDRINGENE SOM FØLGER MED KOMPETANSEMÅL Forklarebegrepene krysning og genmodifisering, og hvordan bioteknologi brukes
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 2252329 B1 (19) NO NORWAY (51) Int Cl. A61K 48/00 (2006.01) A61K 39/12 (2006.01) A61K 39/39 (2006.01) C07K 14/075 (2006.01) C12N 9/02 (2006.01)
(12) Translation of european patent specification (11) NO/EP 2252329 B1 (19) NO NORWAY (51) Int Cl. A61K 48/00 (2006.01) A61K 39/12 (2006.01) A61K 39/39 (2006.01) C07K 14/075 (2006.01) C12N 9/02 (2006.01)
ANTI-HEPCIDINANTISTOFFER OG ANVENDELSER DERAV. Beskrivelse
 1 ANTI-HEPCIDINANTISTOFFER OG ANVENDELSER DERAV Beskrivelse 5 10 Den foreliggende oppfinnelse er innen det medisinske felt, særlig innen feltet for antistoffer mot humant modent hepcidin. Oppfinnelsen
1 ANTI-HEPCIDINANTISTOFFER OG ANVENDELSER DERAV Beskrivelse 5 10 Den foreliggende oppfinnelse er innen det medisinske felt, særlig innen feltet for antistoffer mot humant modent hepcidin. Oppfinnelsen
VEDLEGG I PREPARATOMTALE
 VEDLEGG I PREPARATOMTALE 1 1. VETERINÆRPREPARATETS NAVN Porcilis APP vet. injeksjonsvæske, suspensjon 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver dose på 2 ml inneholder: Virkestoffer: 600 mg Actinobacillus
VEDLEGG I PREPARATOMTALE 1 1. VETERINÆRPREPARATETS NAVN Porcilis APP vet. injeksjonsvæske, suspensjon 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver dose på 2 ml inneholder: Virkestoffer: 600 mg Actinobacillus
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 26727 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (06.01) A61K 31/122 (06.01) A61K 31/32 (06.01) A61K 31/93 (06.01) A61K 31/663 (06.01) A61K 39/39
(12) Translation of european patent specification (11) NO/EP 26727 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (06.01) A61K 31/122 (06.01) A61K 31/32 (06.01) A61K 31/93 (06.01) A61K 31/663 (06.01) A61K 39/39
Cellebiologiske prosesser som respons på virusinfeksjon
 Cellebiologiske prosesser som respons på virusinfeksjon PBM 336 2005 Siri Mjaaland Infeksjoner - immunresponser 1 Figure 2-49 Interferoner Uspesifikk immunitet viral infeksjon stimulerer direkte produksjon
Cellebiologiske prosesser som respons på virusinfeksjon PBM 336 2005 Siri Mjaaland Infeksjoner - immunresponser 1 Figure 2-49 Interferoner Uspesifikk immunitet viral infeksjon stimulerer direkte produksjon
Mikroalger til medisin; krefthemmere
 Mikroalger til medisin; krefthemmere Kari Skjånes og Hanne Skomedal Bioforsk Jord og Miljø og Plantehelse Agenda Hvorfor mikroalger som krefthemmere Kreftutvikling Potensiale Hva kan utvikles Hvordan utvikle
Mikroalger til medisin; krefthemmere Kari Skjånes og Hanne Skomedal Bioforsk Jord og Miljø og Plantehelse Agenda Hvorfor mikroalger som krefthemmere Kreftutvikling Potensiale Hva kan utvikles Hvordan utvikle
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 230129 B1 (19) NO NORWAY (1) Int Cl. C07K 14/47 (06.01) C07K 14/2 (06.01) C07K 14/70 (06.01) C07K 14/71 (06.01) C12N 1/62 (06.01) Norwegian
(12) Translation of european patent specification (11) NO/EP 230129 B1 (19) NO NORWAY (1) Int Cl. C07K 14/47 (06.01) C07K 14/2 (06.01) C07K 14/70 (06.01) C07K 14/71 (06.01) C12N 1/62 (06.01) Norwegian
Vellykket immunrespons og sikker bruk er dokumentert i studie med nasal vaksinering (nesedråper) av HIV vaksinen Vacc-4x sammen med Endocine
 MeldingsID: 304913 Innsendt dato: 10.05.2012 08:31 UtstederID: Utsteder: Instrument: - Marked: Kategori: Informasjonspliktig: Lagringspliktig: Vedlegg: Tittel: Meldingstekst: BIONOR Bionor Pharma ASA XOSL
MeldingsID: 304913 Innsendt dato: 10.05.2012 08:31 UtstederID: Utsteder: Instrument: - Marked: Kategori: Informasjonspliktig: Lagringspliktig: Vedlegg: Tittel: Meldingstekst: BIONOR Bionor Pharma ASA XOSL
(12) PATENT (19) NO (11) (13) B1 NORGE. (51) Int Cl. Patentstyret
 (12) PATENT (19) NO (11) 331387 (13) B1 NORGE (1) Int Cl. B6D 90/08 (2006.01) B6D 88/10 (2006.01) F17C 1/02 (2006.01) Patentstyret (21) Søknadsnr 20100968 (86) Int.inng.dag og søknadsnr (22) Inng.dag 2010.07.02
(12) PATENT (19) NO (11) 331387 (13) B1 NORGE (1) Int Cl. B6D 90/08 (2006.01) B6D 88/10 (2006.01) F17C 1/02 (2006.01) Patentstyret (21) Søknadsnr 20100968 (86) Int.inng.dag og søknadsnr (22) Inng.dag 2010.07.02
Fremgangsmåte for fremstilling av et eksplosiv
 Fremgangsmåte for fremstilling av et eksplosiv 1 Foreliggende oppfinnelse vedrører i store trekk ammoniumnitrat/brenseloljeeksplosiver, også kjent som ANFO- eller ANFEX-eksplosiver, og heretter også vist
Fremgangsmåte for fremstilling av et eksplosiv 1 Foreliggende oppfinnelse vedrører i store trekk ammoniumnitrat/brenseloljeeksplosiver, også kjent som ANFO- eller ANFEX-eksplosiver, og heretter også vist
Grunnkurs C. Janne Dahle-Melhus Kommuneoverlege Sola kommune Smittevernoverlege Stavanger kommune
 Grunnkurs C Janne Dahle-Melhus Kommuneoverlege Sola kommune Smittevernoverlege Stavanger kommune 1 Hvorfor vaksinere? Muligheten til å forebygge alvorlig sykdom med stor utbredelse har vært forutsetningen
Grunnkurs C Janne Dahle-Melhus Kommuneoverlege Sola kommune Smittevernoverlege Stavanger kommune 1 Hvorfor vaksinere? Muligheten til å forebygge alvorlig sykdom med stor utbredelse har vært forutsetningen
(12) PATENT (19) NO (11) (13) B1. (51) Int Cl. NORGE. Patentstyret
 (12) PATENT (19) NO (11) 33249 (13) B1 NORGE (1) Int Cl. A61K 39/02 (06.01) A61K 39/09 (06.01) A61K 39/2 (06.01) A61K 39/116 (06.01) A61K 39/08 (06.01) A61K 39/08 (06.01) A61K 39/09 (06.01) A61K 39/ (06.01)
(12) PATENT (19) NO (11) 33249 (13) B1 NORGE (1) Int Cl. A61K 39/02 (06.01) A61K 39/09 (06.01) A61K 39/2 (06.01) A61K 39/116 (06.01) A61K 39/08 (06.01) A61K 39/08 (06.01) A61K 39/09 (06.01) A61K 39/ (06.01)
(12) Oversettelse av europeisk patentskrift. Avviker fra Patent B1 etter innsigelse
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 217368 B2 (19) NO NORGE (1) Int Cl. B42D / (06.01) Patentstyret Avviker fra Patent B1 etter innsigelse (21) Oversettelse publisert.04. (80) Dato for
(12) Oversettelse av europeisk patentskrift (11) NO/EP 217368 B2 (19) NO NORGE (1) Int Cl. B42D / (06.01) Patentstyret Avviker fra Patent B1 etter innsigelse (21) Oversettelse publisert.04. (80) Dato for
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2096 B1 (19) NO NORGE (1) Int Cl. C12N 1/ (2006.01) Patentstyret (21) Oversettelse publisert 201.04.13 (80) Dato for Den Europeiske Patentmyndighets
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2096 B1 (19) NO NORGE (1) Int Cl. C12N 1/ (2006.01) Patentstyret (21) Oversettelse publisert 201.04.13 (80) Dato for Den Europeiske Patentmyndighets
NORGE. Patentstyret (12) SØKNAD (19) NO (21) (13) A1. (51) Int Cl.
 (12) SØKNAD (19) NO (21) 171288 (13) A1 NORGE (1) Int Cl. C07K 16/18 (06.01) C07K 16/28 (06.01) A61K 39/39 (06.01) Patentstyret (21) Søknadsnr 171288 (86) Int.inng.dag og søknadsnr 0.09.02 PCT/US0/031401
(12) SØKNAD (19) NO (21) 171288 (13) A1 NORGE (1) Int Cl. C07K 16/18 (06.01) C07K 16/28 (06.01) A61K 39/39 (06.01) Patentstyret (21) Søknadsnr 171288 (86) Int.inng.dag og søknadsnr 0.09.02 PCT/US0/031401
Oppfinnelsen angår generelt fleksible rør og især en ny utforming for et fleksibelt rør med et tett båndlag og en fremgangsmåte for å fremstille et
 1 1 2 3 Oppfinnelsen angår generelt fleksible rør og især en ny utforming for et fleksibelt rør med et tett båndlag og en fremgangsmåte for å fremstille et rør. Fleksible rør er vanlig og blir vanligvis
1 1 2 3 Oppfinnelsen angår generelt fleksible rør og især en ny utforming for et fleksibelt rør med et tett båndlag og en fremgangsmåte for å fremstille et rør. Fleksible rør er vanlig og blir vanligvis
PATENTKRAV. 2. Analog av glukagon (SEQ ID nr. 1) som har GIP-agonistaktivitet, med de. følgende modifiseringene:
 1 PATENTKRAV 1 2 1. Analog av glukagon (SEQ ID nr. 1) som har GIP-agonistaktivitet, med de følgende modifiseringene: (a) en aminosyremodifisering på posisjon 1 som overfører GIPagonistaktivitet, eventuelt
1 PATENTKRAV 1 2 1. Analog av glukagon (SEQ ID nr. 1) som har GIP-agonistaktivitet, med de følgende modifiseringene: (a) en aminosyremodifisering på posisjon 1 som overfører GIPagonistaktivitet, eventuelt
Ny kreftvaksine: Viktigheten av å kommersialisere medisinsk forskning
 Ny kreftvaksine: Viktigheten av å kommersialisere medisinsk forskning Gustav Gaudernack Immunologisk avdeling Institutt for Kreftforskning Oslo Universitetsykehus-Radiumhospitalet Helse- og omsorgskonferansen
Ny kreftvaksine: Viktigheten av å kommersialisere medisinsk forskning Gustav Gaudernack Immunologisk avdeling Institutt for Kreftforskning Oslo Universitetsykehus-Radiumhospitalet Helse- og omsorgskonferansen
(12) Translation of european patent specification
 (12) Translation of european patent specification (11) NO/EP 222267 B1 (19) NO NORWAY (1) Int Cl. A01N 1/02 (06.01) A23G 9/38 (06.01) C07K 14/43 (06.01) Norwegian Industrial Property Office (21) Translation
(12) Translation of european patent specification (11) NO/EP 222267 B1 (19) NO NORWAY (1) Int Cl. A01N 1/02 (06.01) A23G 9/38 (06.01) C07K 14/43 (06.01) Norwegian Industrial Property Office (21) Translation
(12) PATENT (19) NO (11) (13) B1 NORGE. (51) Int Cl. Patentstyret
 (12) PATENT (19) NO (11) 332 (13) B1 NORGE (1) Int Cl. A61K 39/09 (06.01) A61K 3/74 (06.01) A61K 39/02 (06.01) A61K 39/09 (06.01) A61K 39/116 (06.01) A61K 39/39 (06.01) C07K 14/31 (06.01) A61P 11/00 (06.01)
(12) PATENT (19) NO (11) 332 (13) B1 NORGE (1) Int Cl. A61K 39/09 (06.01) A61K 3/74 (06.01) A61K 39/02 (06.01) A61K 39/09 (06.01) A61K 39/116 (06.01) A61K 39/39 (06.01) C07K 14/31 (06.01) A61P 11/00 (06.01)
P28416NO05. Fagfelt Oppfinnelsen angår generelt fleksible rør og især en ny utforming for et fleksibelt rør med et tett båndlag.
 P28416NO05 1 5 30 35 Fagfelt Oppfinnelsen angår generelt fleksible rør og især en ny utforming for et fleksibelt rør med et tett båndlag. Bakgrunn Fleksible rør er vanlig og blir vanligvis fremstilt av
P28416NO05 1 5 30 35 Fagfelt Oppfinnelsen angår generelt fleksible rør og især en ny utforming for et fleksibelt rør med et tett båndlag. Bakgrunn Fleksible rør er vanlig og blir vanligvis fremstilt av
Cellesignalisering II: Reseptor tyrosin kinaser, cytosoliske kinaser
 Cellesignalisering II: Reseptor tyrosin kinaser, cytosoliske kinaser! Introduksjon! Definisjon og klassifisering! Kinasefamilier: Receptor/cytosol! Receptor Tyrosin kinase-mediert signalisering! MAP kinase
Cellesignalisering II: Reseptor tyrosin kinaser, cytosoliske kinaser! Introduksjon! Definisjon og klassifisering! Kinasefamilier: Receptor/cytosol! Receptor Tyrosin kinase-mediert signalisering! MAP kinase
NORGE. Patentstyret (12) SØKNAD (19) NO (21) (13) A1. (51) Int Cl.
 (12) SØKNAD (19) NO (21) 1409 (13) A1 NORGE (1) Int Cl. A47J 43/28 (06.01) A47J 36/00 (06.01) A47J 47/16 (06.01) Patentstyret (21) Søknadsnr 1409 (86) Int.inng.dag og søknadsnr (22) Inng.dag 14.08.01 (8)
(12) SØKNAD (19) NO (21) 1409 (13) A1 NORGE (1) Int Cl. A47J 43/28 (06.01) A47J 36/00 (06.01) A47J 47/16 (06.01) Patentstyret (21) Søknadsnr 1409 (86) Int.inng.dag og søknadsnr (22) Inng.dag 14.08.01 (8)
«Immunterapi» Kreftutvikling. Myelomatose. Immunterapi. Anders'Sundan Senter'for'myelomforskning Institutt'for'klinisk'og'molekylær'medisin,'NTNU
 «Immunterapi» Kreftutvikling Myelomatose Immunterapi Anders'Sundan Senter'for'myelomforskning Institutt'for'klinisk'og'molekylær'medisin,'NTNU 1 Kreft er genetiske sykdommer i den forstand at det alltid
«Immunterapi» Kreftutvikling Myelomatose Immunterapi Anders'Sundan Senter'for'myelomforskning Institutt'for'klinisk'og'molekylær'medisin,'NTNU 1 Kreft er genetiske sykdommer i den forstand at det alltid
Forelesninger i BI Cellebiologi. Denaturering og renaturering. Figure 3-13
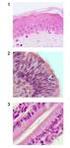 Figure 3.9 Denaturering og renaturering Figure 3-13 Denaturering og renaturering Figure 3-14 Viser tre trinn i refolding av et protein som har vært denaturert. Molten globule -formen er en intermediær
Figure 3.9 Denaturering og renaturering Figure 3-13 Denaturering og renaturering Figure 3-14 Viser tre trinn i refolding av et protein som har vært denaturert. Molten globule -formen er en intermediær
Utvikling av kreftvaksiner
 Utvikling av kreftvaksiner Gustav Gaudernack Dagens Medisin Arena Kreft og prioritering 10.04.13 Section for Immunology Dept. of Cancer Research Oslo University Hospital- Norwegian Radium Hospital Status
Utvikling av kreftvaksiner Gustav Gaudernack Dagens Medisin Arena Kreft og prioritering 10.04.13 Section for Immunology Dept. of Cancer Research Oslo University Hospital- Norwegian Radium Hospital Status
EP Patentkrav. 1. Forbindelse med generell formel (I): R 1 representerer. hvor * indikerer festepunktet for gruppen til resten av molekylet;
 1 Patentkrav EP2791136 1. Forbindelse med generell formel (I): hvor: R 1 representerer hvor * indikerer festepunktet for gruppen til resten av molekylet; R 2 representerer 1 hvor * indikerer festepunktet
1 Patentkrav EP2791136 1. Forbindelse med generell formel (I): hvor: R 1 representerer hvor * indikerer festepunktet for gruppen til resten av molekylet; R 2 representerer 1 hvor * indikerer festepunktet
Selv. Trygg Ignorere. Farlig. Fremmed. Immunsystemet: Generelt, og om allergi spesielt. Immunsystemets utfordring. Medfødte og ervervete immunsystemet
 U N I V E R S I T E T E T I B E R G E N Immunsystemet: Generelt, og om allergi spesielt Silke Appel Broegelmanns Forskningslaboratorium Klinisk Institutt 2 Universitetet i Bergen silke.appel@ Immunsystemets
U N I V E R S I T E T E T I B E R G E N Immunsystemet: Generelt, og om allergi spesielt Silke Appel Broegelmanns Forskningslaboratorium Klinisk Institutt 2 Universitetet i Bergen silke.appel@ Immunsystemets
AVGJØRELSE 1. april 2016 Sak PAT 13/014. Klagenemnda for industrielle rettigheter sammensatt av følgende utvalg:
 AVGJØRELSE 1. april 2016 Sak PAT 13/014 Klager: Merck Sharp & Dohme Corp Representert ved: Tandbergs Patentkontor AS Klagenemnda for industrielle rettigheter sammensatt av følgende utvalg: Elisabeth Ohm,
AVGJØRELSE 1. april 2016 Sak PAT 13/014 Klager: Merck Sharp & Dohme Corp Representert ved: Tandbergs Patentkontor AS Klagenemnda for industrielle rettigheter sammensatt av følgende utvalg: Elisabeth Ohm,
(12) Translation of european patent specification
 NO/EP20 (12) Translation of european patent specification (11) NO/EP 20 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (2006.01) A61P 3/00 (2006.01) A61P 37/00 (2006.01) Norwegian Industrial Property Office
NO/EP20 (12) Translation of european patent specification (11) NO/EP 20 B1 (19) NO NORWAY (1) Int Cl. C07K 16/28 (2006.01) A61P 3/00 (2006.01) A61P 37/00 (2006.01) Norwegian Industrial Property Office
ML-208, generell informasjon
 ML-208, generell informasjon Emnekode: ML-208 Emnenavn: Molekylærbiologi Dato:20.12.2017 Varighet:4 timer Tillatte hjelpemidler: Ingen Merknader:Lag gjerne tegninger og figurer for å illustrere og forklare
ML-208, generell informasjon Emnekode: ML-208 Emnenavn: Molekylærbiologi Dato:20.12.2017 Varighet:4 timer Tillatte hjelpemidler: Ingen Merknader:Lag gjerne tegninger og figurer for å illustrere og forklare
(12) Translation of European patent specification
 (12) Translation of European patent specification (11) NO/EP 2370463 B1 (19) NO NORWAY (1) Int Cl. C07K 14/49 (06.01) C07K 14/71 (06.01) Norwegian Industrial Property Office (21) Translation Published
(12) Translation of European patent specification (11) NO/EP 2370463 B1 (19) NO NORWAY (1) Int Cl. C07K 14/49 (06.01) C07K 14/71 (06.01) Norwegian Industrial Property Office (21) Translation Published
(12) PATENT (19) NO (11) (13) B1. (51) Int Cl. NORGE. Patentstyret
 (12) PATENT (19) NO (11) (13) B1 NORGE (1) Int Cl. A47J 43/28 (06.01) A47J 36/00 (06.01) A47J 47/16 (06.01) Patentstyret (21) Søknadsnr 1409 (86) Int.inng.dag og søknadsnr (22) Inng.dag 14.08.01 (8) Videreføringsdag
(12) PATENT (19) NO (11) (13) B1 NORGE (1) Int Cl. A47J 43/28 (06.01) A47J 36/00 (06.01) A47J 47/16 (06.01) Patentstyret (21) Søknadsnr 1409 (86) Int.inng.dag og søknadsnr (22) Inng.dag 14.08.01 (8) Videreføringsdag
Så, hvordan lager man nye nerveceller?
 Forskningsnyheter om Huntingtons sykdom. I et lettfattelig språk. Skrevet av forskere. Til det globale HS-fellesskapet. Å omdanne hudceller til hjerneceller: et gjennombrudd innen forskning på Huntingtons
Forskningsnyheter om Huntingtons sykdom. I et lettfattelig språk. Skrevet av forskere. Til det globale HS-fellesskapet. Å omdanne hudceller til hjerneceller: et gjennombrudd innen forskning på Huntingtons
individ som lider av dette eller til å forhindre forekomst hos et risikoindivid.
 1 OPPFINNELSESOMRÅDE Foreliggende beskrivelse vedrører fremgangsmåter for behandling og/eller forebyggelse av reumatoid artritt. Slike fremgangsmåter kan benyttes til å behandle et individ som lider av
1 OPPFINNELSESOMRÅDE Foreliggende beskrivelse vedrører fremgangsmåter for behandling og/eller forebyggelse av reumatoid artritt. Slike fremgangsmåter kan benyttes til å behandle et individ som lider av
PatXML 1/ HT. Teknikkens område
 PatXML 1/11 122704HT Teknikkens område [0001] Den foreliggende oppfinnelse relaterer seg til elektrisk utladning av rør/slanger, mer spesielt relaterer den foreliggende oppfinnelse seg til elektrisk utladning
PatXML 1/11 122704HT Teknikkens område [0001] Den foreliggende oppfinnelse relaterer seg til elektrisk utladning av rør/slanger, mer spesielt relaterer den foreliggende oppfinnelse seg til elektrisk utladning
Oppfinnelsen vedrører en sykkel som har en ramme, et sykkelstyre og en kopling som er utformet for festing og låsing på en fast holder anbrakt i
 1 Oppfinnelsen vedrører en sykkel som har en ramme, et sykkelstyre og en kopling som er utformet for festing og låsing på en fast holder anbrakt i overensstemmelse med innledningen til krav 1. 3 Sykler
1 Oppfinnelsen vedrører en sykkel som har en ramme, et sykkelstyre og en kopling som er utformet for festing og låsing på en fast holder anbrakt i overensstemmelse med innledningen til krav 1. 3 Sykler
Den foreliggende oppfinnelsen vedrører generelt en propell for anvendelse i en båt, og mer spesifikt en propell som kan øke båtens fremdriftskraft.
 1 PROPELL FOR BÅT BAKGRUNN FOR OPPFINNELSEN 1. Oppfinnelsens område Den foreliggende oppfinnelsen vedrører generelt en propell for anvendelse i en båt, og mer spesifikt en propell som kan øke båtens fremdriftskraft.
1 PROPELL FOR BÅT BAKGRUNN FOR OPPFINNELSEN 1. Oppfinnelsens område Den foreliggende oppfinnelsen vedrører generelt en propell for anvendelse i en båt, og mer spesifikt en propell som kan øke båtens fremdriftskraft.
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2310034 B1 (19) NO NORGE (51) Int Cl. A61K 38/08 (2006.01) A61P 25/28 (2006.01) A61P 27/16 (2006.01) C07K 16/18 (2006.01) Patentstyret (21) Oversettelse
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2310034 B1 (19) NO NORGE (51) Int Cl. A61K 38/08 (2006.01) A61P 25/28 (2006.01) A61P 27/16 (2006.01) C07K 16/18 (2006.01) Patentstyret (21) Oversettelse
Hfr-stammer Kartlegging ved avbrutt konjugasjon (time of entry)
 BAKTERIE OG FAG GENETIKK Man studerer ofte E. coli fordi den inneholder få gener (4700 kb)sammenlihgnet med menneskets ca 6 mill kb, har kort generasjonstid (20 min) og er hele livssyklusen i haploid tilstand.
BAKTERIE OG FAG GENETIKK Man studerer ofte E. coli fordi den inneholder få gener (4700 kb)sammenlihgnet med menneskets ca 6 mill kb, har kort generasjonstid (20 min) og er hele livssyklusen i haploid tilstand.
(12) PATENT (19) NO (11) (13) B1 NORGE. (51) Int Cl. Patentstyret
 (12) PATENT (19) NO (11) 334496 (13) B1 NORGE (1) Int Cl. C07K 7/06 (06.01) C07K 16/18 (06.01) A61K 38/08 (06.01) A61K 38/17 (06.01) A61P 3/00 (06.01) Patentstyret (21) Søknadsnr 121261 (86) Int.inng.dag
(12) PATENT (19) NO (11) 334496 (13) B1 NORGE (1) Int Cl. C07K 7/06 (06.01) C07K 16/18 (06.01) A61K 38/08 (06.01) A61K 38/17 (06.01) A61P 3/00 (06.01) Patentstyret (21) Søknadsnr 121261 (86) Int.inng.dag
(12) PATENT (19) NO (11) (13) B1 NORGE. (51) Int Cl. A61K 39/385 ( ) A61K 39/00 ( ) Patentstyret
 (12) PATENT (19) NO (11) 340432 (13) B1 NORGE (51) Int Cl. A61K 39/385 (2006.01) A61K 39/00 (2006.01) Patentstyret (21) Søknadsnr 20062687 (86) Int.inng.dag og søknadsnr 2004.12.17 PCT/US2004/42701 (22)
(12) PATENT (19) NO (11) 340432 (13) B1 NORGE (51) Int Cl. A61K 39/385 (2006.01) A61K 39/00 (2006.01) Patentstyret (21) Søknadsnr 20062687 (86) Int.inng.dag og søknadsnr 2004.12.17 PCT/US2004/42701 (22)
NITO Bioingeniørfaglig Institutt kurs i Immunologi The Edge, Tromsø, 11. februar 2015. Generell Immunologi
 NITO Bioingeniørfaglig Institutt kurs i Immunologi The Edge, Tromsø, 11. februar 2015 Generell Immunologi Tor B Stuge Immunologisk forskningsgruppe, IMB Universitetet i Tromsø Innhold: 1. Immunsystemets
NITO Bioingeniørfaglig Institutt kurs i Immunologi The Edge, Tromsø, 11. februar 2015 Generell Immunologi Tor B Stuge Immunologisk forskningsgruppe, IMB Universitetet i Tromsø Innhold: 1. Immunsystemets
(12) Oversettelse av europeisk patentskrift
 (12) Oversettelse av europeisk patentskrift (11) NO/EP 2391650 B1 (19) NO NORGE (51) Int Cl. C07K 16/24 (2006.01) A61K 39/00 (2006.01) A61K 39/395 (2006.01) Patentstyret (21) Oversettelse publisert 2015.03.09
(12) Oversettelse av europeisk patentskrift (11) NO/EP 2391650 B1 (19) NO NORGE (51) Int Cl. C07K 16/24 (2006.01) A61K 39/00 (2006.01) A61K 39/395 (2006.01) Patentstyret (21) Oversettelse publisert 2015.03.09
INNRETNING FOR FREMSTILLING AV EN DRIKKE EKSTRAHERT FRA EN KAPSEL. Beskrivelse
 1 INNRETNING FOR FREMSTILLING AV EN DRIKKE EKSTRAHERT FRA EN KAPSEL Beskrivelse 5 Oppfinnelsens område [0001] 10 Den foreliggende oppfinnelsen angår området fremstilling av drikker, f.eks. basert på kaffe,
1 INNRETNING FOR FREMSTILLING AV EN DRIKKE EKSTRAHERT FRA EN KAPSEL Beskrivelse 5 Oppfinnelsens område [0001] 10 Den foreliggende oppfinnelsen angår området fremstilling av drikker, f.eks. basert på kaffe,
