Pakningsvedlegg: Informasjon til brukeren
|
|
|
- Frøydis Klausen
- 8 år siden
- Visninger:
Transkript
1 Pakningsvedlegg: Informasjon til brukeren IntronA 18 millioner IE, 30 millioner IE og 60 millioner IE injeksjonsvæske, oppløsning i flerdosepenn Interferon alfa-2b Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. Det inneholder informasjon som er viktig for deg. - Ta vare på dette pakningsvedlegget. Du kan få behov for å lese det igjen. - Hvis du har ytterligere spørsmål, kontakt lege, apotek eller sykepleier. - Dette legemidlet er skrevet ut kun til deg. Ikke gi det videre til andre. Det kan skade dem, selv om de har symptomer på sykdom som ligner dine. - Kontakt lege eller apotek dersom du opplever bivirkninger, inkludert mulige bivirkninger som ikke er nevnt i dette pakningsvedlegget. Se avsnitt 4. I dette pakningsvedlegget finner du informasjon om: 1. Hva IntronA er, og hva det brukes mot 2. Hva du må vite før du bruker IntronA 3. Hvordan du bruker IntronA 4. Mulige bivirkninger 5. Hvordan du oppbevarer IntronA 6. Innholdet i pakningen og ytterligere informasjon 1. Hva IntronA er, og hva brukes det mot IntronA (interferon alfa-2b) påvirker kroppens immunforsvar og bistår dette i kampen mot infeksjoner og alvorlige sykdommer. IntronA anvendes hos voksne pasienter i behandlingen av visse sykdommer som påvirker blodet, benmargen, lymfekjertlene eller huden og som kan spre seg til kroppen. Dette omfatter hårcelleleukemi, kronisk myelogen leukemi, multippelt myelom, follikulære lymfomer, karsinoider og malignt melanom. IntronA anvendes også hos voksne pasienter i behandlingen av kronisk hepatitt B eller C, som er virusinfeksjoner i leveren. IntronA brukes i kombinasjon med ribavirin hos barn fra og med 3 år og ungdom som ikke tidligere er behandlet for kronisk hepatitt C. 2. Hva du må vite før du bruker IntronA Bruk ikke IntronA - hvis du er allergisk overfor interferon eller noen av de andre innholdsstoffene i dette legemidlet (listet opp i avsnitt 6). - dersom du har en alvorlig hjertesykdom. - dersom du har nedsatt nyre- eller leverfunksjon. - dersom du har avansert dekompensert (ukontrollert) leversykdom. - dersom du har hepatitt og nylig har vært behandlet med legemidler som nedsetter immunforsvaret (med unntak av korttidsbehandling med legemidler av typen kortisoner). - dersom du har hatt kramper (konvulsjoner). - dersom du har hatt en autoimmun sykdom eller har gjennomgått organtransplantasjon og tar legemidler som nedsetter ditt immunforsvar (immunsystemet ditt beskytter deg mot infeksjoner). 1
2 - dersom du har en sykdom i skjoldbruskkjertelen som ikke er tilfredsstillende behandlet med legemidler. - hvis du behandles med legemidlet telbivudin (se "Andre legemidler og med IntronA"). Barn og ungdom: - dersom du har hatt alvorlig nervøse eller mentale problemer, slik som alvorlig depresjon eller selvmordstanker. Advarsler og forsiktighetsregler Rådfør deg med lege, apotek eller sykepleier før du bruker IntronA - dersom du er gravid eller planlegger å bli gravid (se avsnitt Graviditet og amming ). - dersom du blir behandlet for en sinnslidelse eller tidligere har blitt behandlet for noen annen nervesykdom eller mental lidelse, inkludert depresjon (f.eks. følelse av tristhet, motløshet) eller selvmords- eller drapsatferd (se avsnitt 4 Mulige bivirkninger ). Bruk av interferon alfa-2b hos barn og ungdom som har eller har hatt en alvorlig psykiatrisk tilstand er kontraindisert (se avsnitt Bruk ikke IntronA ). - dersom du har skrumplever eller andre leverproblemer (andre enn hepatitt B eller C). - dersom du har psoriasis, kan denne bli verre under behandling med IntronA. - når du bruker IntronA kan du av og til ha en høyere risiko for å utvikle en infeksjon. Fortell legen din dersom du tror du holder på å få en infeksjon. - dersom du utvikler symptomer som kan forbindes med en forkjølelse eller andre luftveisinfeksjoner, slik som feber, hoste eller pustebesvær, fortell dette til legen din. - dersom du merker en unormal tendens til blødning eller blåmerker, fortell dette umiddelbart til legen din. - dersom du utvikler symptomer på en alvorlig allergisk reaksjon (som pustebesvær, pipende pust eller elveblest) i det du tar dette legemidlet, søk umiddelbart medisinsk hjelp. - dersom du også blir behandlet for HIV (se avsnitt Andre legemidler og IntronA ). - dersom du har gjennomgått organtransplantasjon av enten nyre eller lever kan interferonbehandling øke risikoen for avstøtning. Dette må du diskutere med legen din. Tann- og tannkjøttlidelser som kan føre til tap av tenner er blitt rapportert hos pasienter som fikk IntronA og ribavirin i kombinasjonsbehandling. I tillegg kan munntørrhet ha en ødeleggende effekt på tenner og slimhinne i munnen under langtidsbehandling med kombinasjonen av IntronA og ribavirin. Du bør børste tennene grundig to ganger daglig og ha regelmessige tannundersøkelser. I tillegg kan noen pasienter få oppkast. Dersom dette skjer, må du passe på å skylle munnen din etterpå. Fortell legen din dersom du noen gang har hatt hjerteinfarkt eller hjerteproblemer, hvis du har hatt uregelmessig pust eller lungebetennelse, problemer med blodkoagulasjon, leverpåvirkning, problemer med skjoldbruskkjertelen, sukkersyke eller høyt eller lavt blodtrykk. Fortell legen din om du noen gang har vært behandlet for depresjon eller noen annen psykiatrisk sykdom, forvirring eller bevisstløshet, selvmordstanker eller selvmordsforsøk, eller tidligere har misbrukt stoff (f.eks., alkohol eller narkotika). Fortell legen din dersom du tar den kinesiske urtemedisinen Shosaikoto. Andre legemidler og IntronA IntronA forsterker effekten av substanser som nedsetter din reaksjonshastighet og kan forårsake døsighet. Sjekk derfor med legen din eller apoteket angående inntak av alkoholholdige drikker, søvntabletter, beroligende midler eller sterke smertestillende midler. Fortell legen din dersom du tar teofyllin eller aminofyllin mot astma og om alle andre legemidler du tar eller nylig har tatt, også reseptfrie, da dosen av visse legemidler kan behøve tilpasning under behandlingen med IntronA. Pasienter som også har HIV-infeksjon: Laktoacidose og forverring av leverfunksjonen er bivirkninger som har sammenheng med høyaktiv antiretroviral behandling (HAART), en behandling for HIV. 2
3 Dersom du får HAART i tillegg til IntronA og ribavirin, kan din risiko for å få laktoacidose og leversvikt øke. Legen din vil følge deg nøye opp for tegn og symptomer på disse tilstandene (Vennligst også les pakningsvedlegget for ribavirin). Dessuten kan pasienter som får zidovudin i tillegg til kombinasjonsbehandling med IntronA og ribavirin ha en økt risiko for å utvikle anemi (lavt antall røde blodceller). Hvis du tar telbivudin sammen med et pegylert interferon alfa-2a- eller en annen type injiserbart interferon-produkt, er risikoen for å utvikle perifer nevropati (nummenhet, stikkende og/eller brennende følelse i armer og/eller ben) høyere. Disse hendelsene kan være alvorlige. Derfor skal ikke telbivudin brukes sammen med IntronA. Rådfør deg med lege eller apotek dersom du bruker eller nylig har brukt andre legemidler, dette gjelder også reseptfrie legemidler. Inntak av IntronA sammen med mat og drikke og alkohol Under behandling med IntronA, kan det hende at legen din ber deg drikke ekstra mye væske for å motvirke lavt blodtrykk. Graviditet, amming og fertilitet Rådfør deg med lege eller apotek før du tar dette legemidlet dersom du er gravid eller ammer, tror at du kan være gravid eller planlegger å bli gravid. I studier på drektige dyr har interferoner i enkelte tilfeller ført til spontanabort. Effekten på graviditet hos mennesker er ukjent. Ved kombinasjonsbehandling med IntronA og ribavirin kan ribavirin være meget skadelig for fosteret. Både kvinnelige og mannlige pasienter må ta spesielle forholdsregler ved seksuell aktivitet hvis det er mulighet for at graviditet kan oppstå: - dersom du er jente eller kvinne i fruktbar alder, må du ha en negativ graviditetstest før behandling, hver måned under behandling og i 4 måneder etter at behandlingen er avsluttet. Du må bruke effektiv prevensjon i løpet av tiden du tar ribavirin og 4 måneder etter avsluttet behandling. Dette kan diskuteres med legen din. - dersom du er mann som tar ribavirin, må du ikke ha sex med en gravid kvinne hvis du ikke bruker kondom. Dette vil minske sjansen for at kvinnen får ribavirin i kroppen. Hvis din kvinnelige partner ikke er gravid nå, men er i fruktbar alder, må hun ta en graviditetstest hver måned under behandling og i 7 måneder etter at behandlingen er avsluttet. Dette kan diskuteres med legen din. Hvis du er mannlig pasient, må du eller din partner bruke et effektivt prevensjonsmiddel i løpet av hele behandlingen med ribavirin og i 7 måneder etter avsluttet behandling. Dette kan diskuteres med legen din. Det er ikke kjent om dette legemidlet utskilles i morsmelk og derfor skal du ikke amme hvis du tar IntronA. Ved kombinasjonsbehandling med ribavirin, gjør deg kjent med de respektive informasjonstekstene for produkter som inneholder ribavirin. Kjøring og bruk av maskiner Dersom du blir trøtt, søvnig eller føler deg forvirret under behandlingen med IntronA, bør du ikke kjøre bil eller bruke maskiner. IntronA inneholder mindre enn 1 mmol natrium (23 mg) per 1,2 ml, dvs. praktisk talt natriumfritt. 3. Hvordan du bruker IntronA Bruk alltid dette legemidlet nøyaktig slik legen din eller apoteket har fortalt deg. Kontakt lege eller apotek hvis du er usikker. Legen din har forskrevet IntronA spesielt til deg og for din nåværende tilstand. Del ikke dette legemidlet med noen annen. Nøyaktig dose bestemmes av legen din. Dosen vil variere avhengig av hvilken sykdom du behandles for. 3
4 Pennen er laget for å levere sitt innhold på 18 millioner IE i doser fra 1,5 til 6 millioner IE. Pennen vil levere maksimalt 12 doser med 1,5 millioner IE over en periode som ikke overstiger 4 uker. Pennen er laget for å levere sitt innhold på 30 millioner IE i doser fra 2,5 til 10 millioner IE. Pennen vil levere maksimalt 12 doser med 2,5 millioner IE over en periode som ikke overstiger 4 uker. Pennen er laget for å levere sitt innhold på 60 millioner IE i doser fra 5 til 20 millioner IE. Pennen vil levere maksimalt 12 doser med 5 millioner IE over en periode som ikke overstiger 4 uker. Dersom du injiserer IntronA selv, vær nøye med at dosen som du har fått forskrevet tydelig fremgår av legemiddelpakningen du har mottatt. Doser som skal gis 3 ganger per uke er best å ta annenhver dag. Den normale startdosen for hver tilstand følger, individuelle doser kan imidlertid variere og legen din kan endre dosen din basert på dine spesifikke behov: Kronisk hepatitt B: 5 til 10 millioner IE 3 ganger per uke (annenhver dag) injisert subkutant (under huden). Kronisk hepatitt C: Voksne - 3 millioner IE 3 ganger per uke (annenhver dag) injisert subkutant (under huden) i kombinasjon med ribavirin eller alene. Barn fra og med 3 år og ungdom 3 millioner IE/m 2 3 ganger per uke (annenhver dag) injisert subkutant (under huden) i kombinasjon med ribavirin (Se også pakningsvedlegg for ribavirin). Hårcelleleukemi: 2 millioner IE/m 2 3 ganger per uke (annenhver dag) injisert subkutant (under huden). Kronisk myelogen leukemi: 4-5 millioner IE/m 2 daglig injisert subkutant (under huden). Multippelt myelom: 3 millioner IE/m 2 3 ganger per uke (annenhver dag) injisert subkutant (under huden). Folikkulære lymfomer: Som tillegg til kjemoterapi 5 millioner IE 3 ganger per uke (annenhver dag) injisert subkutant (under huden). Karsinoider: 5 millioner IE 3 ganger per uke (annenhver dag) injisert subkutant (under huden). Malignt melanom: Innledende behandling: 20 millioner IE/m 2 gis intravenøst daglig 5 dager i uken i en 4-ukers periode. Vedlikeholdsbehandling: 10 millioner IE/m 2, 3 ganger i uken (annenhver dag) injisert subkutant (under huden). Legen din kan forskrive en annen dose med IntronA alene eller i kombinasjon med andre legemidler (f. eks. cytarabin, ribavirin). Om du har fått forskrevet IntronA i kombinasjon med et annet legemiddel, les pakningsvedlegget for legemidlet du bruker i kombinasjon for mer informasjon. Legen din vil bestemme den eksakte doseringen ut i fra dine behov. Hvis du mener at virkningen av IntronA er for kraftig eller for svak, bør du rådføre deg med legen eller apoteket om dette. Subkutan bruk: IntronA er vanligvis beregnet til subkutan bruk. Dette betyr at IntronA injiseres med en kort kanyle i fettvevet like under huden. Dersom du injiserer dette legemidlet selv, vil du få instruksjoner om hvordan du skal tilberede og gi injeksjonen. Detaljerte instruksjoner for subkutan injeksjon finnes i dette pakningsvedlegget (se avsnitt HVORDAN MAN SELV INJISERER INTRONA på slutten av pakningsvedlegget). En dose med IntronA gis på en bestemt dag. IntronA gis enten daglig (5 eller 7 dager per uke) eller tre ganger per uke, annenhver dag, for eksempel på mandag, onsdag og fredag. Interferoner kan forårsake uvanlig trøtthet. Dersom du injiserer selv eller gir det til et barn, gjør dette ved sengetid. Bruk IntronA nøyaktig som legen din har forskrevet. Overskrid ikke den anbefalte dosen og bruk IntronA så lenge som forskrevet. 4
5 Dersom du tar for mye av IntronA Kontakt legen din eller en sykepleier så snart som mulig. Dersom du har glemt å ta IntronA Dersom du selv administrerer IntronA eller har omsorg for et barn som tar IntronA i kombinasjon med ribavirin, injiser den anbefalte dosen så snart du husker og fortsett behandlingen som vanlig. Du må ikke ta en dobbelt dose som erstatning for en glemt dose. Dersom det er forskrevet at du skal injisere dette legemidlet hver dag og du glemmer en hel dagsdose, fortsett behandlingen med den vanlige dosen neste dag. Kontakt legen din eller apoteket dersom nødvendig. 4. Mulige bivirkninger Som alle legemidler kan dette legemidlet forårsake bivirkninger, men ikke alle får det. Selv om ikke alle disse bivirkningene oppstår, kan de kreve medisinsk hjelp dersom de inntreffer. Psykiatri og sentralnervesystemet: Noen personer blir deprimerte når de bruker IntronA alene eller i kombinasjonsbehandling med ribavirin, og i noen tilfeller har pasienter hatt tanker om å true andre på livet, selvmordstanker eller aggressiv oppførsel (noen ganger rettet mot andre). Noen pasienter har faktisk begått selvmord. Søk øyeblikkelig hjelp dersom du oppdager at du blir deprimert eller har selvmordstanker eller endret oppførsel. Du bør vurdere å spørre et familiemedlem eller en nær venn om å hjelpe deg å være oppmerksom overfor tegn på depresjon eller endringer i oppførselen din. Barn og ungdom er spesielt utsatt for å utvikle depresjon når de behandles med IntronA og ribavirin. Kontakt legen umiddelbart eller søk behandling øyeblikkelig dersom de viser noen unormale adferdssymptomer, føler seg deprimerte eller har ønsker om å skade seg selv eller andre. Vekst og utvikling (barn og ungdom): I løpet av det året behandlingen med IntronA i kombinasjon med ribavirin varte, var det noen barn og ungdommer som ikke vokste eller la på seg så mye som forventet. Noen barn nådde ikke sin forventete høyde innen år etter fullført behandling. Dersom noen av de følgende bivirkningene inntreffer, avslutt behandlingen med IntronA og fortell dette umiddelbart til legen din eller kom deg til akuttmottaket på ditt nærmeste sykehus: opphovning av hendene, føttene, anklene, ansiktet, leppene, munnen eller i halsen som kan føre til vanskeligheter med å svelge eller puste, elveblest, besvimelse. Disse er alle svært alvorlige bivirkninger. Dersom du får dem kan du ha fått en alvorlig allergisk reaksjon på IntronA. Du kan trenge akutt medisinsk hjelp eller sykehusinnleggelse. Disse svært alvorlige bivirkningene opptrer svært sjelden. Fortell legen din umiddelbart dersom noen av de følgende bivirkningene oppstår: brystsmerte eller vedvarende og alvorlig hoste, uregelmessig eller rask hjerterytme, kortpustethet, forvirring, vankeligheter med å holde seg årvåken, nummenhet eller stikkende følelse eller smerte i hender eller føtter, krampeanfall, problemer med søvn, tankeevne eller konsentrasjon, forandret sinnstilstand, selvmordstanker, selvmordsforsøk, endret oppførsel eller aggressiv oppførsel (noen ganger rettet mot andre), hallusinasjoner, alvorlige magesmerter, svart eller tjærelignende avføring, blod i avføring eller urin, alvorlig neseblødning, vokslignende blekhet av huden, høyt blodsukker, feber eller frysninger som oppstår etter noen få ukers behandling, smerte i nedre del av ryggen eller i siden, vanskelig urinering, problemer med øynene eller syns- eller hørselsproblemer, tap av hørsel, alvorlig eller smertefull rødme eller ømhet på huden din eller slimhinnene. Dette kan signalisere alvorlige bivirkninger som kan trenge akutt medisinsk hjelp. Legen din vil teste blodet ditt for å kontrollere at antallet hvite blodceller (celler som bekjemper infeksjon), røde blodceller (celler som transporterer jern og oksygen), blodplater (blodlevringsceller) og andre 5
6 laboratorieverdier er på akseptable nivåer. Moderat og vanligvis reversibel reduksjon er blitt rapportert for alle tre blodelementene hvite blodceller, røde blodceller og blodplater. I oppstarten av IntronA-behandlingen kan du oppleve en influensalignende reaksjon med feber, tretthet/utmattelse, hodepine, muskelverk, leddsmerte og frysninger/stivhet. Legen din kan anbefale deg at du tar paracetamol dersom du utvikler disse symptomene. Mulige bivirkninger oppført under er gruppert etter frekvensen de oppstår med: Svært vanlige (berører flere enn 1 av 10 brukere) Vanlige (berører 1 til 10 av 100 brukere) Mindre vanlige (berører 1 til 10 av 1000 brukere) Sjeldne (berører 1 til 10 av brukere) Svært sjeldne (berører færre enn 1 av brukere) Ikke kjent (kan ikke anslås utifra tilgjengelige data) Følgende bivirkninger er blitt rapportert: Svært vanlig rapporterte bivirkninger: smerte, opphovning og rødhet eller hudskader på injeksjonsstedet, hårtap, svimmelhet, appetittforandringer, mage- eller buksmerter, diaré, kvalme (sykdomsfølelse), virusinfeksjon, depresjon, emosjonell labilitet, søvnløshet, angst, sår hals og smerte ved svelging, tretthet, frysninger/stivhet, feber, influensalignende reaksjon, generell følelse av ubehag, hodepine, vekttap, oppkast, irritabilitet, svakhet, humørsvingninger, hoste (noen ganger alvorlig), kortpustethet, kløe, tørr hud, utslett, plutselig og alvorlig muskelsmerte, leddsmerte, smerte i muskel/skjelett, endring i blodverdier, inklusive en reduksjon i antall hvite blodceller. Noen barn har hatt en reduksjon i veksthastigheten sin (høyde og vekt). Vanlig rapporterte bivirkninger: tørste, dehydrering, høyt blodtrykk, migrene, hovne kjertler, rødme, menstruelle problemer, redusert seksuell drift, vaginalforstyrrelse, brystsmerte, testikkelsmerte, problemer med skjoldbruskkjertelen, røde gommer, munntørrhet, rødhet eller sår i munnen eller på tungen, tannsmerte eller tannsykdom, herpes simplex (forkjølelsessår), smaksforandringer, urolig mage, dyspepsi (sure oppstøt), forstoppelse, forstørret lever (leverproblemer, i blant alvorlige), løs avføring, sengevæting hos barn, bihulebetennelse, bronkitt, øyesmerte, problemer med tårekanalene, konjunktivitt ( røde øyne ), agitasjon, søvnighet, søvngjengeri, adferdsproblemer, nervøsitet, tett eller rennende nese, nysing, rask pust, blek eller rød hud, blåmerker, problem med hud eller negler, psoriasis (ny eller forverret), økt svetting, økt trang til vannlating, lett skjelving, redusert sensitivitet for berøring, artritt. Mindre vanlig rapporterte bivirkninger: bakterieinfeksjon og stikkende og prikkende følelse. Sjelden rapporterte bivirkninger: lungebetennelse. Svært sjelden rapporterte bivirkninger: lavt blodtrykk, hovent ansikt, diabetes, leggkramper, smerte i ryggen, nyreproblemer, nerveskade, blødende gommer, aplastisk anemi (en type blodmangel). Ren erytroaplasi, en tilstand hvor kroppen har ingen eller redusert produksjon av røde blodceller, er blitt rapportert. Dette forårsaker alvorlig anemi, symptomer som inkluderer unormal tretthet og mangel på energi. Sarkoidose (en sykdom karakterisert av vedvarende feber, vekttap, leddsmerte- og hevelse, hudskader og hovne kjertler) har i svært sjeldne tilfeller blitt rapportert. Tap av bevissthet har forekommet i svært sjeldne tilfeller men først og fremst hos eldre pasienter som ble behandlet med høye doser. Tilfeller av slag (cerebrovaskulære tilfeller) har blitt rapportert. Ta umiddelbart kontakt med legen dersom du har noen av disse symptomene. Bivirkninger rapportert med ikke kjent frekvens: 6
7 Periodentale (påvirker tannkjøttet) og dentale sykdommer, endret mental status, tap av bevissthet, akutte hypersensitivitetsreaksjoner, inklusive urtikaria (elveblest), angioødem (hovne hender, føtter, ankler, ansikt, lepper, munn eller hals som kan føre til vanskeligheter med å svelge eller puste), bronkokonstriksjon og anafylaksi (en alvorlig allergisk reaksjon i hele kroppen) er blitt rapportert, men frekvensen er ikke kjent. I tillegg er det blitt rapportert tilfeller av Vogt-Koyanagi-Harada syndrom (en autoimmun inflammatorisk sykdom som påvirker øynene, huden og membranene i øret, hjernen og ryggmargen), tanker om å true andre på livet, mani (overdreven eller irrasjonell entusiasme), bipolare sykdommer (forstyrret sinnsstemning karakterisert ved vekslende episoder av tristhet og entusiasme), hjertesvikt, perikardvæske (en væskeansamling som oppstår mellom perikardet (hjertesekkhinnen) og hjertet) og lungefibrose (arrdannelse i lungene) ved bruk av IntronA. Pulmonal arteriell hypertensjon en sykdom med betydelig innsnevring av blodårene i lungene, noe som fører til høyt blodtrykk i blodårene som frakter blod fra hjertet til lungene. Dette kan spesielt oppstå hos pasienter med risikofaktorer som HIV infeksjon eller alvorlige leverproblemer (cirrhose). Bivirkningen kan oppstå ved ulike tidspunkt under behandlingen, typisk flere måneder etter oppstart av behandlingen med IntronA. Melding av bivirkninger Kontakt lege, apotek eller sykepleier dersom du opplever bivirkninger, inkludert mulige bivirkninger som ikke er nevnt i dette pakningsvedlegget. Du kan også melde fra om bivirkninger direkte via meldeskjema som finnes på nettsiden til Statens legemiddelverk: Ved å melde fra om bivirkninger bidrar du med informasjon om sikkerheten ved bruk av dette legemidlet. 5. Hvordan du oppbevarer IntronA Oppbevares utilgjengelig for barn. Bruk ikke dette legemidlet etter utløpsdatoen som er angitt på pakningen. Utløpsdatoen henviser til den siste dagen i den måneden. Oppbevares i kjøleskap (2 ºC 8 ºC). Skal ikke fryses. Hver penn er beregnet for brukstid på maksimalt fire uker og må deretter kasseres. Maksimalt tillates 48 timer (to døgn) ved høyst 25 ºC i løpet av 4-ukers perioden for å dekke uforutsette forsinkelser i å sette pennen tilbake i kjøleskapet. Bruk ikke dette legemidlet, hvis du oppdager at IntronA endrer utseende. Det kan være ekstra kanyler og renseservietter igjen i pakningen, dette avhenger av din dose. Disse skal kastes på et passende og sikkert sted. Legemidler skal ikke kastes i avløpsvann eller sammen med husholdningsavfall. Spør på apoteket hvordan du skal kaste legemidler som du ikke lenger bruker. Disse tiltakene bidrar til å beskytte miljøet. 6. Innholdet i pakningen og ytterligere informasjon Sammensetning av IntronA - Virkestoff er rekombinant interferon alfa-2b. Hver penn inneholder 18 millioner IE, 30 millioner IE eller 60 millioner IE. 7
8 - Andre innholdsstoffer er dinatriumfosfat vannfritt, natriumdihydrogenfosfatmonohydrat, natriumedetat, natriumklorid, m-kresol, polysorbat 80 og vann til injeksjonsvæsker. Hvordan IntronA ser ut og innholdet i pakningen IntronA finnes som injeksjonsvæske, oppløsning i en flerdosepenn. Den klare og fargeløse oppløsningen er pakket i en sylinderampulle i glass. IntronA er tilgjengelig i tre forskjellige pakningsstørrelser: - Pakning med 1 penn, 12 kanyler og 12 renseservietter - Pakning med 2 penner, 24 kanyler og 24 renseservietter - Pakning med 8 penner, 96 kanyler og 96 renseservietter Ikke alle pakningsstørrelser vil nødvendigvis bli markedsført. Innehaver av markedsføringstillatelsen Tilvirker Merck Sharp & Dohme Limited SP Labo N.V. Hertford Road, Hoddesdon Industriepark 30 Hertfordshire EN11 9BUl B-2220 Heist-op-den-Berg Storbritannia Belgia For ytterligere informasjon om dette legemidlet bes henvendelser rettet til den lokale representant for innehaveren av markedsføringstillatelsen: België/Belgique/Belgien MSD Belgium BVBA/SPRL Tél/Tel: (+32(0) ) dpoc_belux@merck.com България Мерк Шарп и Доум България ЕООД Тел.: info-msdbg@merck.com Česká republika Merck Sharp & Dohme s.r.o. Tel: dpoc_czechslovak@merck.com Danmark MSD Danmark ApS Tlf: dkmail@merck.com Deutschland MSD SHARP & DOHME GMBH Tel: (+49 (0) ) @msd.de Eesti Merck Sharp & Dohme OÜ Tel.: msdeesti@merck.com Lietuva UAB Merck Sharp & Dohme Tel msd_lietuva@merck.com Luxembourg/Luxemburg MSD Belgium BVBA/SPRL Tél/Tel: +32(0) dpoc_belux@merck.com Magyarország MSD Pharma Hungary Kft. Tel.: hungary_msd@merck.com Malta Merck Sharp & Dohme Cyprus Limited Tel: ( ) malta_info@merck.com Nederland Merck Sharp & Dohme BV Tel: ( ) medicalinfo.nl@merck.com Norge MSD (Norge) AS Tlf: msdnorge@msd.no 8
9 Ελλάδα MSD Α.Φ.Β.Ε.Ε. Τηλ: España Merck Sharp & Dohme de España, S.A. Tel: France MSD France Tél: + 33-(0) Hrvatska Merck Sharp & Dohme d.o.o. Tel: croatia_info@merck.com Ireland Merck Sharp & Dohme Ireland (Human Health) Limited Tel: +353 (0) medinfo_ireland@merck.com Ísland Vistor hf. Sími: Italia MSD Italia S.r.l. Tel: medicalinformation.it@merck.com Κύπρος Merck Sharp & Dohme Cyprus Limited Τηλ.: ( ) cyprus_info@merck.com Latvija SIA Merck Sharp & Dohme Latvija Tel: msd_lv@merck.com Österreich Merck Sharp & Dohme Ges.m.b.H. Tel: +43 (0) msd-medizin@merck.com Polska MSD Polska Sp. z o.o. Tel: msdpolska@merck.com Portugal Merck Sharp & Dohme, Lda Tel: clic@merck.com România Merck Sharp & Dohme Romania S.R.L. Tel: msdromania@merck.com Slovenija Merck Sharp & Dohme, inovativna zdravila d.o.o. Tel: msd.slovenia@merck.com Slovenská republika Merck Sharp & Dohme, s. r. o. Tel: dpoc_czechslovak@merck.com Suomi/Finland MSD Finland Oy Puh/Tel: +358 (0) info@msd.fi Sverige Merck Sharp & Dohme (Sweden) AB Tel: medicinskinfo@merck.com United Kingdom Merck Sharp & Dohme Limited Tel: +44 (0) medicalinformationuk@merck.com Dette pakningsvedlegget ble sist oppdatert 25. juni Andre informasjonskilder Detaljert informasjon om dette legemiddel er tilgjengelig på nettstedet til Det europeiske legemiddelkontoret Dette pakningsvedlegget er tilgjengelig på alle EU/EØS-språk på nettstedet til Det europeiske legemiddelkontoret (The European Medicines Agency). 9
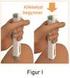
10 HVORDAN MAN SELV INJISERER INTRONA Følgende instruksjoner forklarer hvordan du injiserer IntronA selv. Les instruksjonene nøye og følg dem steg for steg. Legen din eller hans/hennes sykepleier vil instruere deg. Ikke forsøk å injisere selv hvis du ikke er sikker på om du forstår hvordan man gjør det. Forberedelse Legg frem følgende ting før du begynner: - flerdosepenn med IntronA - en kanyle for subkutan injeksjon (vedlagt i pakningen) - en renseserviett (vedlagt i pakningen). Vask hendene grundig. Bruk de kanylene som finnes i pakningen kun til IntronA. Bruk en ny kanyle for hver dose. Forsikre deg om at væsken er romtemperert (opptil 25 C) når den skal injiseres. Figur A og B viser de ulike delene av pennen og kanylen. De viktigste delene er som følger: - Trykknappsskalaen viser hvilken dose som er stilt inn. - Streken med den brune, blå eller rosa fargekoden og trykknappen finnes nederst på pennen når beskyttelseshetten holdes oppover. - Pennen er kun beskyttet når trekanten på hylstermarkeringene er i linje med doseindikatoren på penneskaftet. Beskyttelseshette Hylstermarkering Kanyle Gummimembran Sylinderampull Doseindikator Penneskaft Fargekode Trykknapp Trykknappskala Figur A Figur B 10
11 Beregning av dosen IntronA Ta ut pennen fra kjøleskapet ca. 30 minutter før bruk, slik at injeksjonsvæsken romtempereres. Når du er klar til å injisere forbered pennen som følgende: Før bruk, kontroller alltid at IntronA injeksjonsvæsken er klar og fargeløs. Hvis væsken er misfarget eller inneholder partikler må den ikke brukes. Dra av beskyttelseshetten fra pennen og desinfiser gummimembranen med en renseserviett (figur C). Penneskaft Trykknapp Gummimembran Figur C Dra bort beskyttelsespapiret fra kanylen. Husk på at den bakre delen av kanylen kommer frem når papiret fjernes (figur D). Figur D Sett forsiktig kanylen på pennen (figur E). (Den bakre delen av kanylen kommer til å punktere gummimembranen som du desinfiserte tidligere.) Skru kanylen fast på pennen ved å skru mot høyre (med sola) (figur F). Figur E Figur F 11
12 Dra først av den ytre kanylebeskytteren (figur G). Dra deretter forsiktig av den indre kanylebeskytteren og husk at kanylen nå eksponeres (figur H). Behold den ytre beskytteren for senere bruk. Figur G Figur H Pennen er nå klar til bruk. Ettersom litt luft kan samle seg i kanylen og sylinderampullen under oppbevaring, er neste steg og prøve å få bort eventuelle luftbobler. Dette steget kalles for Air-shot. Hold pennen slik at kanylen peker oppover. Knips forsiktig på sylinderampullen slik at eventuelle luftbobler stiger opp til toppen av sylinderampullen, til like under kanylen (figur I). Sylinderampull Figur I Hold pennen i skaftet og vri sylinderampullen i den retning som pilen viser på figur J (mot høyre) til du kjenner et klikk. Figur J Mens du ennå har pennen pekende oppover, trykk så trykknappen helt opp og kontroller at en dråpe injeksjonsvæske kommer til syne på kanylespissen (Legg merke til dråpen ved kanylens spiss i figur K). 12
13 Figur K Hvis det ikke kommer noen dråpe, bruk en annen penn og returner den defekte pennen til den som ga den til deg. OBS! Det kan fremdeles finnes luft igjen i pennen, men det er ikke viktig ettersom du har fjernet luften fra kanylen og dosen blir korrekt. Sett beskyttelseshetten tilbake på pennen med trekanten i linje med doseindikatoren som vist i figur L. Figur L Pennen er nå klar til å stille inn dosen. I neste steg, hold pennen på midten av skaftet. Dette gjør at trykknappen kan røre seg fritt og medfører at rett dosering stilles inn. Hold skaftet på pennen horisontalt, med en hånd. Med den andre hånden vrir du beskyttelseshetten mot høyre som vises i figur M. Du ser da at trykknappen går ut og indikerer den innstilte dosen. For å stille inn rett dose, vri hylsteret antall ganger som beskrevet nedenfor: 13
14 Antall med vri og klikk 1 hel vridning (5 klikk) 6 klikk 7 klikk 8 klikk 9 klikk 2 hele vridninger (10 klikk) 11 klikk 12 klikk 13 klikk 14 klikk 3 hele vridninger (15 klikk) 16 klikk 17 klikk 18 klikk 19 klikk Korresponderende doser (millioner IE) med IntronA, injeksjonsvæske, oppløsning, flerdosepenn 18 millioner IE/penn 1,5 1,8 2,1 2,4 2,7 3 3,3 3,6 3,9 4,2 4,5 4,8 5,1 5,4 5,7 Figur M 4 hele vridninger (20 klikk)* *4 hele vridninger korresponderer med den maksimale dosen som skal gis i en injeksjon. Pennen er laget for å levere sitt innhold på 18 millioner IE i doser fra 1,5 til 6 millioner IE. Pennen vil levere maksimalt 12 doser med 1,5 millioner IE over en periode som ikke overstiger 4 uker. Trykknappskalaen viser hvilken dose som er innstilt (figur N). For doser som korresponderer med hele vridninger vil skalaen tangere det korrekte dosemerket. For doser som korresponderer med antall klikk mellom hele vridninger vil skalaen plassere seg mellom to dosemerker. Kontroller nå at du har riktig dose. 6 14
15 Figur N Antall med vri og klikk 1 hel vridning (5 klikk) 6 klikk 7 klikk 8 klikk 9 klikk 2 hele vridninger (10 klikk) 11 klikk 12 klikk 13 klikk 14 klikk 3 hele vridninger (15 klikk) 16 klikk 17 klikk 18 klikk 19 klikk Korresponderende doser (millioner IE) med IntronA, injeksjonsvæske, oppløsning, flerdosepenn 30 millioner IE/penn 2,5 3 3,5 4 4,5 5 5,5 6 6,5 7 7,5 8 8,5 9 9,5 Figur M 4 hele vridninger (20 klikk)* *4 hele vridninger korresponderer med den maksimale dosen som skal gis i en injeksjon. Pennen er laget for å levere sitt innhold på 30 millioner IE i doser fra 2,5 til 10 millioner IE. Pennen vil levere maksimalt 12 doser med 2,5 millioner IE over en periode som ikke overstiger 4 uker. Trykknappskalaen viser hvilken dose som er innstilt (figur N). For doser som korresponderer med hele vridninger vil skalaen tangere det korrekte dosemerket. For doser som korresponderer med antall klikk 10 15
16 mellom hele vridninger vil skalaen plassere seg mellom to dosemerker. Kontroller nå at du har riktig dose. Figur N Antall med vri og klikk 1 hel vridning (5 klikk) 6 klikk 7 klikk 8 klikk 9 klikk 2 hele vridninger (10 klikk) 11 klikk 12 klikk 13 klikk 14 klikk 3 hele vridninger (15 klikk) 16 klikk 17 klikk 18 klikk 19 klikk Korresponderende doser (millioner IE) med IntronA, injeksjonsvæske, oppløsning, flerdosepenn 60 millioner IE/penn Figur M 4 hele vridninger (20 klikk)* *4 hele vridninger korresponderer med den maksimale dosen som skal gis i en injeksjon. Pennen er laget for å levere sitt innhold på 60 millioner IE i doser fra 5 til 20 millioner IE. Pennen vil levere maksimalt 12 doser med 5 millioner IE over en periode som ikke overstiger 4 uker
17 Trykknappskalaen viser hvilken dose som er innstilt (figur N). For doser som korresponderer med hele vridninger vil skalaen tangere det korrekte dosemerket. For doser som korresponderer med antall klikk mellom hele vridninger vil skalaen plassere seg mellom to dosemerker. Kontroller nå at du har riktig dose. Figur N Etter hver hele omdreining må du påse at trekanten er i linje med doseindikatoren (figur O). Hvis du har stilt inn feil dose, kan du vri hylsteret tilbake (mot venstre) så langt du kan, til trykknappen er helt tilbake. Start på nytt. Når den riktige dosen er innstilt er det klart for å injisere. Figur O Injeksjon av oppløsningen Velg ut et injeksjonssted. Det beste området for injeksjon er vevet med et lag fett mellom hud og muskel: lår, utsiden av overarmen (du kan trenge hjelp av en annen person for å kunne bruke dette stedet), mageregionen (bortsett fra navlen og rundt livet). Om du er uvanlig slank så bruk kun låret eller utsiden av armen til injeksjon. Bytt injeksjonssted hver gang. Rengjør og desinfiser huden der du skal injisere. Vent til huden har tørket. Ta bort kanylbeskyttelsen. Med en hånd klypes forsiktig løs hud. Med den andre hånden holder du i sprøyten som om du holder i en penn. Stikk inn kanylen i huden i en vinkel på cirka 45º. Trykk så trykknappen helt ned (figur P). 17
18 Figur P Hold trykknappen nedtrykket og la kanylen sitte igjen noen sekunder for å la injeksjonsvæsken spre seg under huden, fjern så kanylen. Sett forsiktig tilbake den ytre kanylebeskytteren (figur Q). Figur Q Skru kanylen helt av med kanylebeskytteren ved å vri mot venstre som vist på figur R. Ta den forsiktig av pennen og kast den beskyttede kanylen (figur S). Figur R Figur S 18
19 Sett tilbake beskyttelseshetten med trekanten i linje med doseindikatoren som vist på figur T. Legg så pennen tilbake i kjøleskapet. Figur T 19
Pakningsvedlegg: informasjon til pasienten. Aerius 0,5 mg/ml mikstur, oppløsning desloratadin
 Pakningsvedlegg: informasjon til pasienten Aerius 0,5 mg/ml mikstur, oppløsning desloratadin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: informasjon til pasienten Aerius 0,5 mg/ml mikstur, oppløsning desloratadin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til pasienten. Aerius 5 mg tabletter, filmdrasjerte desloratadin
 Pakningsvedlegg: Informasjon til pasienten Aerius 5 mg tabletter, filmdrasjerte desloratadin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til pasienten Aerius 5 mg tabletter, filmdrasjerte desloratadin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: informasjon til pasienten. Aerius 0,5 mg/ml mikstur, oppløsning desloratadin
 Pakningsvedlegg: informasjon til pasienten Aerius 0,5 mg/ml mikstur, oppløsning desloratadin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: informasjon til pasienten Aerius 0,5 mg/ml mikstur, oppløsning desloratadin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til pasienten. Azomyr 5 mg tabletter, filmdrasjerte desloratadin
 Pakningsvedlegg: Informasjon til pasienten Azomyr 5 mg tabletter, filmdrasjerte desloratadin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til pasienten Azomyr 5 mg tabletter, filmdrasjerte desloratadin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til brukeren. Clarityn 10 mg tablett loratadin
 Pakningsvedlegg: Informasjon til brukeren Clarityn 10 mg tablett loratadin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon som er viktig for
Pakningsvedlegg: Informasjon til brukeren Clarityn 10 mg tablett loratadin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon som er viktig for
Pakningsvedlegg: Informasjon til pasienten. GRANUPAS 4 g enterogranulat para-aminosalisylsyre
 Pakningsvedlegg: Informasjon til pasienten GRANUPAS 4 g enterogranulat para-aminosalisylsyre Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til pasienten GRANUPAS 4 g enterogranulat para-aminosalisylsyre Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til pasienten. Aerius 2,5 mg smeltetabletter desloratadin
 Pakningsvedlegg: Informasjon til pasienten Aerius 2,5 mg smeltetabletter desloratadin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon som er
Pakningsvedlegg: Informasjon til pasienten Aerius 2,5 mg smeltetabletter desloratadin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon som er
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. HBVAXPRO 10 mikrogram, injeksjonsvæske, suspensjon Vaksine mot hepatitt B (rdna)
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN HBVAXPRO 10 mikrogram, injeksjonsvæske, suspensjon Vaksine mot hepatitt B (rdna) Les nøye gjennom dette pakningsvedlegget før du vaksineres. - Ta vare på dette
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN HBVAXPRO 10 mikrogram, injeksjonsvæske, suspensjon Vaksine mot hepatitt B (rdna) Les nøye gjennom dette pakningsvedlegget før du vaksineres. - Ta vare på dette
Pakningsvedlegg: Informasjon til brukeren. Bridion 100 mg/ml injeksjonsvæske, oppløsning sugammadex
 Pakningsvedlegg: Informasjon til brukeren Bridion 100 mg/ml injeksjonsvæske, oppløsning sugammadex Les nøye gjennom dette pakningsvedlegget før dette legemidlet blir gitt til deg. Det inneholder informasjon
Pakningsvedlegg: Informasjon til brukeren Bridion 100 mg/ml injeksjonsvæske, oppløsning sugammadex Les nøye gjennom dette pakningsvedlegget før dette legemidlet blir gitt til deg. Det inneholder informasjon
Pakningsvedlegg: Informasjon til pasienten. Januvia 25 mg filmdrasjerte tabletter sitagliptin
 Pakningsvedlegg: Informasjon til pasienten Januvia 25 mg filmdrasjerte tabletter sitagliptin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til pasienten Januvia 25 mg filmdrasjerte tabletter sitagliptin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til pasienten. Zerbaxa 1 g/0,5 g pulver til konsentrat til infusjonsvæske, oppløsning ceftolozan/tazobaktam
 Pakningsvedlegg: Informasjon til pasienten Zerbaxa 1 g/0,5 g pulver til konsentrat til infusjonsvæske, oppløsning ceftolozan/tazobaktam Dette legemidlet er underlagt særlig overvåking for å oppdage ny
Pakningsvedlegg: Informasjon til pasienten Zerbaxa 1 g/0,5 g pulver til konsentrat til infusjonsvæske, oppløsning ceftolozan/tazobaktam Dette legemidlet er underlagt særlig overvåking for å oppdage ny
B. PAKNINGSVEDLEGG 20
 B. PAKNINGSVEDLEGG 20 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Mozobil 20 mg/ml injeksjonsvæske, oppløsning plerixafor Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta
B. PAKNINGSVEDLEGG 20 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Mozobil 20 mg/ml injeksjonsvæske, oppløsning plerixafor Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta
Pakningsvedlegg: Informasjon til pasienten. Orgalutran 0,25 mg/0,5 ml injeksjonsvæske, oppløsning ganirelix
 Pakningsvedlegg: Informasjon til pasienten Orgalutran 0,25 mg/0,5 ml injeksjonsvæske, oppløsning ganirelix Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder
Pakningsvedlegg: Informasjon til pasienten Orgalutran 0,25 mg/0,5 ml injeksjonsvæske, oppløsning ganirelix Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder
Pakningsvedlegg: Informasjon til brukeren. Paracetduo 500 mg/65 mg tabletter. paracetamol/koffein
 Pakningsvedlegg: Informasjon til brukeren Paracetduo 500 mg/65 mg tabletter paracetamol/koffein Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til brukeren Paracetduo 500 mg/65 mg tabletter paracetamol/koffein Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til brukeren. Galvus 50 mg tabletter Vildagliptin
 Pakningsvedlegg: Informasjon til brukeren Galvus 50 mg tabletter Vildagliptin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon som er viktig
Pakningsvedlegg: Informasjon til brukeren Galvus 50 mg tabletter Vildagliptin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon som er viktig
Pakningsvedlegg: Informasjon til brukeren. Ketorax 5 mg/ml injeksjonsvæske. ketobemidonhydroklorid
 Pakningsvedlegg: Informasjon til brukeren Ketorax 5 mg/ml injeksjonsvæske ketobemidonhydroklorid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til brukeren Ketorax 5 mg/ml injeksjonsvæske ketobemidonhydroklorid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til brukeren
 Pakningsvedlegg: Informasjon til brukeren Trulicity 0,75 mg injeksjonsvæske, oppløsning i ferdigfylt penn Trulicity 1,5 mg injeksjonsvæske, oppløsning i ferdigfylt penn dulaglutid Les nøye gjennom dette
Pakningsvedlegg: Informasjon til brukeren Trulicity 0,75 mg injeksjonsvæske, oppløsning i ferdigfylt penn Trulicity 1,5 mg injeksjonsvæske, oppløsning i ferdigfylt penn dulaglutid Les nøye gjennom dette
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. MODURETIC Mite, 25 mg/2,5 mg, tabletter. hydroklortiazid og amiloridhydroklorid
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN MODURETIC Mite, 25 mg/2,5 mg, tabletter hydroklortiazid og amiloridhydroklorid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN MODURETIC Mite, 25 mg/2,5 mg, tabletter hydroklortiazid og amiloridhydroklorid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta
Novartis Norge AS N-0510 OSLO. Pakningsvedlegg. Vectavir krem
 Novartis Norge AS N-0510 OSLO Vectavir krem Godkjent 10.11.2006 Novartis Side 2 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Vectavir 1% krem Penciklovir Les nøye gjennom dette pakningsvedlegget før du begynner
Novartis Norge AS N-0510 OSLO Vectavir krem Godkjent 10.11.2006 Novartis Side 2 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Vectavir 1% krem Penciklovir Les nøye gjennom dette pakningsvedlegget før du begynner
http://www.felleskatalogen.no/medisin/pasienter/pil-trulicity-lilly-595591
 Side 1 av 13 Pakningsvedlegg: Informasjon til brukeren Trulicity 0,75 mg injeksjonsvæske, oppløsning i ferdigfylt penn Trulicity 1,5 mg injeksjonsvæske, oppløsning i ferdigfylt penn dulaglutid Dette legemidlet
Side 1 av 13 Pakningsvedlegg: Informasjon til brukeren Trulicity 0,75 mg injeksjonsvæske, oppløsning i ferdigfylt penn Trulicity 1,5 mg injeksjonsvæske, oppløsning i ferdigfylt penn dulaglutid Dette legemidlet
Pakningsvedlegg: Informasjon til brukeren. Moduretic Mite 25 mg/2,5 mg, tabletter. hydroklortiazid og amiloridhydroklorid
 Pakningsvedlegg: Informasjon til brukeren Moduretic Mite 25 mg/2,5 mg, tabletter hydroklortiazid og amiloridhydroklorid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
Pakningsvedlegg: Informasjon til brukeren Moduretic Mite 25 mg/2,5 mg, tabletter hydroklortiazid og amiloridhydroklorid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
B. PAKNINGSVEDLEGG 24
 B. PAKNINGSVEDLEGG 24 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Evoltra 1 mg/ml konsentrat til infusjonsvæske klofarabin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta
B. PAKNINGSVEDLEGG 24 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Evoltra 1 mg/ml konsentrat til infusjonsvæske klofarabin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta
Pakningsvedlegg: Informasjon til brukeren. Trulicity 0,75 mg injeksjonsvæske, oppløsning i ferdigfylt penn
 Pakningsvedlegg: Informasjon til brukeren Trulicity 0,75 mg injeksjonsvæske, oppløsning i ferdigfylt penn Trulicity 1,5 mg injeksjonsvæske, oppløsning i ferdigfylt penn Dulaglutid Dette legemidlet er underlagt
Pakningsvedlegg: Informasjon til brukeren Trulicity 0,75 mg injeksjonsvæske, oppløsning i ferdigfylt penn Trulicity 1,5 mg injeksjonsvæske, oppløsning i ferdigfylt penn Dulaglutid Dette legemidlet er underlagt
Pakningsvedlegg: Informasjon til brukeren. Firazyr 30 mg injeksjonsvæske, oppløsning i ferdigfylt sprøyte Icatibant
 Pakningsvedlegg: Informasjon til brukeren Firazyr 30 mg injeksjonsvæske, oppløsning i ferdigfylt sprøyte Icatibant Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det
Pakningsvedlegg: Informasjon til brukeren Firazyr 30 mg injeksjonsvæske, oppløsning i ferdigfylt sprøyte Icatibant Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det
Pakningsvedlegg: Informasjon til brukeren. Diproderm øredråper 0,05 %, oppløsning. betametason
 PAKNINGSVEDLEGG Pakningsvedlegg: Informasjon til brukeren Diproderm øredråper 0,05 %, oppløsning betametason Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder
PAKNINGSVEDLEGG Pakningsvedlegg: Informasjon til brukeren Diproderm øredråper 0,05 %, oppløsning betametason Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder
Pakningsvedlegg. Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet.
 Pakningsvedlegg Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. Scheriproct stikkpiller og kombinasjonspakning: Ta vare på dette pakningsvedlegget. Du kan få behov for å lese
Pakningsvedlegg Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. Scheriproct stikkpiller og kombinasjonspakning: Ta vare på dette pakningsvedlegget. Du kan få behov for å lese
Viktig sikkerhetsinformasjon for å redusere risikoen for immunrelaterte bivirkninger. Informasjon til pasienter
 Pasientveiledning BAVENCIO (avelumab) Viktig sikkerhetsinformasjon for å redusere risikoen for immunrelaterte bivirkninger Informasjon til pasienter Dette legemidlet er underlagt særlig overvåking for
Pasientveiledning BAVENCIO (avelumab) Viktig sikkerhetsinformasjon for å redusere risikoen for immunrelaterte bivirkninger Informasjon til pasienter Dette legemidlet er underlagt særlig overvåking for
Denne brosjyren gir deg informasjon og råd om bruk av Volibris, også kalt ambrisentan.
 Informasjon til pasienter som har fått forskrevet Volibris Bruk av hva du må vite Denne brosjyren gir deg informasjon og råd om bruk av Volibris, også kalt ambrisentan. Les den nøye. Ta vare på brosjyren
Informasjon til pasienter som har fått forskrevet Volibris Bruk av hva du må vite Denne brosjyren gir deg informasjon og råd om bruk av Volibris, også kalt ambrisentan. Les den nøye. Ta vare på brosjyren
Pakningsvedlegg: Informasjon til brukeren
 Pakningsvedlegg: Informasjon til brukeren Synflorix injeksjonsvæske, suspensjon i ferdigfylt sprøyte Vaksine mot pneumokokkinfeksjon (polysakkarid, konjugert, adsorbert) Les nøye gjennom dette pakningsvedlegget
Pakningsvedlegg: Informasjon til brukeren Synflorix injeksjonsvæske, suspensjon i ferdigfylt sprøyte Vaksine mot pneumokokkinfeksjon (polysakkarid, konjugert, adsorbert) Les nøye gjennom dette pakningsvedlegget
Pakningsvedlegg: Informasjon til brukeren. TRUSOPT 20 mg/ml øyedråper, oppløsning, uten konserveringsmiddel dorzolamid
 Pakningsvedlegg: Informasjon til brukeren TRUSOPT 20 mg/ml øyedråper, oppløsning, uten konserveringsmiddel dorzolamid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
Pakningsvedlegg: Informasjon til brukeren TRUSOPT 20 mg/ml øyedråper, oppløsning, uten konserveringsmiddel dorzolamid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. Glustin 15 mg tabletter Pioglitazon
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Glustin 15 mg tabletter Pioglitazon Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget. Du kan få
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Glustin 15 mg tabletter Pioglitazon Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget. Du kan få
Din behandling med XALKORI (krizotinib) - viktig sikkerhetsinformasjon
 Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig. Du kan bidra ved å melde enhver mistenkt bivirkning. Se avsnitt 4 i pakningsvedlegget for informasjon
Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig. Du kan bidra ved å melde enhver mistenkt bivirkning. Se avsnitt 4 i pakningsvedlegget for informasjon
Retningslinjer for bruk av KEYTRUDA. (pembrolizumab) Viktig sikkerhetsinformasjon til pasienter
 Retningslinjer for bruk av KEYTRUDA (pembrolizumab) Viktig sikkerhetsinformasjon til pasienter Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig.
Retningslinjer for bruk av KEYTRUDA (pembrolizumab) Viktig sikkerhetsinformasjon til pasienter Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig.
Santen Oy B. PAKNINGSVEDLEGG
 B. PAKNINGSVEDLEGG 18 Pakningsvedlegg: Informasjon til pasienten IKERVIS 1 mg/ml øyedråper, emulsjon ciklosporin (ciclosporin) Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
B. PAKNINGSVEDLEGG 18 Pakningsvedlegg: Informasjon til pasienten IKERVIS 1 mg/ml øyedråper, emulsjon ciklosporin (ciclosporin) Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
Pakningsvedlegg: Informasjon til brukeren. Taloxa tabletter 600 mg Taloxa mikstur, suspensjon 120 mg/ml. felbamat
 Pakningsvedlegg: Informasjon til brukeren Taloxa tabletter 600 mg Taloxa mikstur, suspensjon 120 mg/ml felbamat Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder
Pakningsvedlegg: Informasjon til brukeren Taloxa tabletter 600 mg Taloxa mikstur, suspensjon 120 mg/ml felbamat Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder
B. PAKNINGSVEDLEGG 1
 B. PAKNINGSVEDLEGG 1 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Eulexin 250 mg tabletter flutamid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget.
B. PAKNINGSVEDLEGG 1 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Eulexin 250 mg tabletter flutamid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget.
Retningslinjer for bruk av KEYTRUDA. (pembrolizumab) Viktig sikkerhetsinformasjon til pasienter
 Retningslinjer for bruk av KEYTRUDA (pembrolizumab) Viktig sikkerhetsinformasjon til pasienter Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig.
Retningslinjer for bruk av KEYTRUDA (pembrolizumab) Viktig sikkerhetsinformasjon til pasienter Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig.
Retningslinjer for bruk av KEYTRUDA. (pembrolizumab) Viktig sikkerhetsinformasjon til pasienter
 Retningslinjer for bruk av KEYTRUDA (pembrolizumab) Viktig sikkerhetsinformasjon til pasienter Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig.
Retningslinjer for bruk av KEYTRUDA (pembrolizumab) Viktig sikkerhetsinformasjon til pasienter Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig.
Irbesartan Zentiva inneholder laktose. Dersom du ikke tåler visse sukkertyper (for eksempel laktose), kontakt legen før du tar dette legemidlet.
 Du må fortelle legen din hvis du tror du er gravid (eller om du tror du kan komme til å bli gravid). Irbesartan Zentiva er ikke anbefalt tidlig i svangerskapet, og må ikke benyttes hvis du er mer enn tre
Du må fortelle legen din hvis du tror du er gravid (eller om du tror du kan komme til å bli gravid). Irbesartan Zentiva er ikke anbefalt tidlig i svangerskapet, og må ikke benyttes hvis du er mer enn tre
Pakningsvedlegg: Informasjon til brukeren. Pneumovax injeksjonsvæske, oppløsning i ferdigfylt sprøyte. Vaksine mot pneumokokkpolysakkarid
 For voksne og barn over 2 år. Pakningsvedlegg: Informasjon til brukeren Pneumovax injeksjonsvæske, oppløsning i ferdigfylt sprøyte Vaksine mot pneumokokkpolysakkarid Les nøye gjennom dette pakningsvedlegget
For voksne og barn over 2 år. Pakningsvedlegg: Informasjon til brukeren Pneumovax injeksjonsvæske, oppløsning i ferdigfylt sprøyte Vaksine mot pneumokokkpolysakkarid Les nøye gjennom dette pakningsvedlegget
Otezla 10 mg tabletter, filmdrasjerte Otezla 20 mg tabletter, filmdrasjerte Otezla 30 mg tabletter, filmdrasjerte apremilast
 Pakningsvedlegg: Informasjon til pasienten Otezla 10 mg tabletter, filmdrasjerte Otezla 20 mg tabletter, filmdrasjerte Otezla 30 mg tabletter, filmdrasjerte apremilast Dette legemidlet er underlagt særlig
Pakningsvedlegg: Informasjon til pasienten Otezla 10 mg tabletter, filmdrasjerte Otezla 20 mg tabletter, filmdrasjerte Otezla 30 mg tabletter, filmdrasjerte apremilast Dette legemidlet er underlagt særlig
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. DepoCyte 50 mg injeksjonsvæske, suspensjon Cytarabin
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN DepoCyte 50 mg injeksjonsvæske, suspensjon Cytarabin Les nøye gjennom dette pakningsvedlegget før du får begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget.
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN DepoCyte 50 mg injeksjonsvæske, suspensjon Cytarabin Les nøye gjennom dette pakningsvedlegget før du får begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget.
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. INVANZ 1 g pulver til konsentrat til infusjonsvæske, oppløsning ertapenem
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN INVANZ 1 g pulver til konsentrat til infusjonsvæske, oppløsning ertapenem Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. Det inneholder
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN INVANZ 1 g pulver til konsentrat til infusjonsvæske, oppløsning ertapenem Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. Det inneholder
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. ADCIRCA 20 mg filmdrasjerte tabletter tadalafil
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN ADCIRCA 20 mg filmdrasjerte tabletter tadalafil Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget.
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN ADCIRCA 20 mg filmdrasjerte tabletter tadalafil Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget.
Pakningsvedlegg: Informasjon til pasienten. Janumet 50 mg/850 mg filmdrasjerte tabletter sitagliptin/metforminhydroklorid
 Pakningsvedlegg: Informasjon til pasienten Janumet 50 mg/850 mg filmdrasjerte tabletter sitagliptin/metforminhydroklorid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
Pakningsvedlegg: Informasjon til pasienten Janumet 50 mg/850 mg filmdrasjerte tabletter sitagliptin/metforminhydroklorid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Silgard, injeksjonsvæske, suspensjon Vaksine mot humant papillomavirus [Type 6, 11, 16, 18] (rekombinant, adsorbert) Les nøye gjennom dette pakningsvedlegget før
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Silgard, injeksjonsvæske, suspensjon Vaksine mot humant papillomavirus [Type 6, 11, 16, 18] (rekombinant, adsorbert) Les nøye gjennom dette pakningsvedlegget før
Din behandling med XALKORI (crizotinib) - viktig sikkerhetsinformasjon
 Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig. Du kan bidra ved å melde enhver mistenkt bivirkning. Se avsnitt 4 i pakningsvedlegget for informasjon
Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig. Du kan bidra ved å melde enhver mistenkt bivirkning. Se avsnitt 4 i pakningsvedlegget for informasjon
Pakningsvedlegg: Informasjon til brukeren. Xolair 150 mg pulver og væske til injeksjonsvæske, oppløsning Omalizumab
 Pakningsvedlegg: Informasjon til brukeren Xolair 150 mg pulver og væske til injeksjonsvæske, oppløsning Omalizumab Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det
Pakningsvedlegg: Informasjon til brukeren Xolair 150 mg pulver og væske til injeksjonsvæske, oppløsning Omalizumab Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det
Pakningsvedlegg: Informasjon til brukeren. Norcuron 10 mg pulver til injeksjonsvæske, oppløsning vekuroniumbromid
 PAKNINGSVEDLEGG 1 Pakningsvedlegg: Informasjon til brukeren Norcuron 10 mg pulver til injeksjonsvæske, oppløsning vekuroniumbromid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette
PAKNINGSVEDLEGG 1 Pakningsvedlegg: Informasjon til brukeren Norcuron 10 mg pulver til injeksjonsvæske, oppløsning vekuroniumbromid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette
Pakningsvedlegg: Informasjon til pasienten. Olumiant 2 mg filmdrasjerte tabletter Olumiant 4 mg filmdrasjerte tabletter baricitinib
 Pakningsvedlegg: Informasjon til pasienten Olumiant 2 mg filmdrasjerte tabletter Olumiant 4 mg filmdrasjerte tabletter baricitinib Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon
Pakningsvedlegg: Informasjon til pasienten Olumiant 2 mg filmdrasjerte tabletter Olumiant 4 mg filmdrasjerte tabletter baricitinib Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon
Pakningsvedlegg: Informasjon til brukeren. Ifirmasta 300 mg tabletter, filmdrasjerte Irbesartan
 Pakningsvedlegg: Informasjon til brukeren Ifirmasta 300 mg tabletter, filmdrasjerte Irbesartan Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til brukeren Ifirmasta 300 mg tabletter, filmdrasjerte Irbesartan Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til brukeren. Trulicity 0,75 mg injeksjonsvæske, oppløsning i ferdigfylt penn
 Pakningsvedlegg: Informasjon til brukeren Trulicity 0,75 mg injeksjonsvæske, oppløsning i ferdigfylt penn Trulicity 1,5 mg injeksjonsvæske, oppløsning i ferdigfylt penn Dulaglutid Dette legemidlet er underlagt
Pakningsvedlegg: Informasjon til brukeren Trulicity 0,75 mg injeksjonsvæske, oppløsning i ferdigfylt penn Trulicity 1,5 mg injeksjonsvæske, oppløsning i ferdigfylt penn Dulaglutid Dette legemidlet er underlagt
Pakningsvedlegg: Informasjon til pasienten. Janumet 50 mg/1000 mg filmdrasjerte tabletter sitagliptin/metforminhydroklorid
 Pakningsvedlegg: Informasjon til pasienten Janumet 50 mg/1000 mg filmdrasjerte tabletter sitagliptin/metforminhydroklorid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
Pakningsvedlegg: Informasjon til pasienten Janumet 50 mg/1000 mg filmdrasjerte tabletter sitagliptin/metforminhydroklorid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
Pakningsvedlegg: Informasjon til brukeren. Vyndaqel 20 mg myke kapsler Tafamidis
 Pakningsvedlegg: Informasjon til brukeren Vyndaqel 20 mg myke kapsler Tafamidis Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig. Du kan bidra ved
Pakningsvedlegg: Informasjon til brukeren Vyndaqel 20 mg myke kapsler Tafamidis Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig. Du kan bidra ved
Pakningsvedlegg: Informasjon til brukeren. INVANZ 1 g pulver til konsentrat til infusjonsvæske, oppløsning ertapenem
 Pakningsvedlegg: Informasjon til brukeren INVANZ 1 g pulver til konsentrat til infusjonsvæske, oppløsning ertapenem Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det
Pakningsvedlegg: Informasjon til brukeren INVANZ 1 g pulver til konsentrat til infusjonsvæske, oppløsning ertapenem Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det
Pakningsvedlegg: Informasjon til brukeren
 Pakningsvedlegg: Informasjon til brukeren PegIntron 150 mikrogram pulver og væske til injeksjonsvæske, oppløsning, i ferdigfylt penn peginterferon alfa-2b Les nøye gjennom dette pakningsvedlegget før du
Pakningsvedlegg: Informasjon til brukeren PegIntron 150 mikrogram pulver og væske til injeksjonsvæske, oppløsning, i ferdigfylt penn peginterferon alfa-2b Les nøye gjennom dette pakningsvedlegget før du
Pakningsvedlegg: Informasjon til brukeren
 Pakningsvedlegg: Informasjon til brukeren Onbrez Breezhaler 150 mikrogram inhalasjonspulver, harde kapsler Onbrez Breezhaler 300 mikrogram inhalasjonspulver, harde kapsler Indakaterol maleat Les nøye gjennom
Pakningsvedlegg: Informasjon til brukeren Onbrez Breezhaler 150 mikrogram inhalasjonspulver, harde kapsler Onbrez Breezhaler 300 mikrogram inhalasjonspulver, harde kapsler Indakaterol maleat Les nøye gjennom
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. Ipreziv 20 mg tabletter Ipreziv 40 mg tabletter Ipreziv 80 mg tabletter azilsartanmedoksomil
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Ipreziv 20 mg tabletter Ipreziv 40 mg tabletter Ipreziv 80 mg tabletter azilsartanmedoksomil Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet.
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Ipreziv 20 mg tabletter Ipreziv 40 mg tabletter Ipreziv 80 mg tabletter azilsartanmedoksomil Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet.
Pakningsvedlegg: Informasjon til brukeren. Comtess 200 mg tabletter, filmdrasjerte Entakapon
 Pakningsvedlegg: Informasjon til brukeren Comtess 200 mg tabletter, filmdrasjerte Entakapon Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til brukeren Comtess 200 mg tabletter, filmdrasjerte Entakapon Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til brukeren
 Pakningsvedlegg: Informasjon til brukeren Adempas 0,5 mg tabletter, filmdrasjerte Adempas 1 mg tabletter, filmdrasjerte Adempas 1,5 mg tabletter, filmdrasjerte Adempas 2 mg tabletter, filmdrasjerte Adempas
Pakningsvedlegg: Informasjon til brukeren Adempas 0,5 mg tabletter, filmdrasjerte Adempas 1 mg tabletter, filmdrasjerte Adempas 1,5 mg tabletter, filmdrasjerte Adempas 2 mg tabletter, filmdrasjerte Adempas
Viktig sikkerhetsinformasjon
 Viktig sikkerhetsinformasjon Din veiledning om YERVOY for YERVOY TM Informasjonsbrosjyre pasientertil pasient Dette opplæringsmateriellet er et obligatorisk vilkår for markedsføringstillatelsen for å minske
Viktig sikkerhetsinformasjon Din veiledning om YERVOY for YERVOY TM Informasjonsbrosjyre pasientertil pasient Dette opplæringsmateriellet er et obligatorisk vilkår for markedsføringstillatelsen for å minske
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. Ipstyl Autogel 60 mg/90 mg/120 mg injeksjonsvæske, oppløsning i ferdigfylt sprøyte lanreotid
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Ipstyl Autogel 60 mg/90 mg/120 mg injeksjonsvæske, oppløsning i ferdigfylt sprøyte lanreotid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet.
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Ipstyl Autogel 60 mg/90 mg/120 mg injeksjonsvæske, oppløsning i ferdigfylt sprøyte lanreotid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet.
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. Creon 10000 harde enterokapsler. Creon 25000 harde enterokapsler. Creon 40000 harde enterokapsler
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Creon 10000 harde enterokapsler Creon 25000 harde enterokapsler Creon 40000 harde enterokapsler pankreatin Les nøye gjennom dette pakningsvedlegget før du begynner
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Creon 10000 harde enterokapsler Creon 25000 harde enterokapsler Creon 40000 harde enterokapsler pankreatin Les nøye gjennom dette pakningsvedlegget før du begynner
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. EZETROL 10 mg tabletter ezetimib
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN EZETROL 10 mg tabletter ezetimib Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget. Du kan få behov
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN EZETROL 10 mg tabletter ezetimib Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget. Du kan få behov
Pakningsvedlegg: Informasjon til brukeren. PegIntron 50 mikrogram pulver og væske til injeksjonsvæske, oppløsning peginterferon alfa-2b
 Pakningsvedlegg: Informasjon til brukeren PegIntron 50 mikrogram pulver og væske til injeksjonsvæske, oppløsning peginterferon alfa-2b Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette
Pakningsvedlegg: Informasjon til brukeren PegIntron 50 mikrogram pulver og væske til injeksjonsvæske, oppløsning peginterferon alfa-2b Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette
Viktig informasjon til pasienter som starter på behandling med MAVENCLAD
 Viktig sikkerhetsinformasjon MAVENCLAD 10 mg tabletter kladribin Pasientveiledning Viktig informasjon til pasienter som starter på behandling med MAVENCLAD Melding av bivirkninger Kontakt lege dersom du
Viktig sikkerhetsinformasjon MAVENCLAD 10 mg tabletter kladribin Pasientveiledning Viktig informasjon til pasienter som starter på behandling med MAVENCLAD Melding av bivirkninger Kontakt lege dersom du
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. Focetria injeksjonsvæske, suspensjon
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Focetria injeksjonsvæske, suspensjon Vaksine mot pandemisk influensa (H1N1) (inaktivert, overflateantigen, med adjuvans) Den mest oppdaterte informasjonen ligger
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Focetria injeksjonsvæske, suspensjon Vaksine mot pandemisk influensa (H1N1) (inaktivert, overflateantigen, med adjuvans) Den mest oppdaterte informasjonen ligger
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. Canesten kombinasjonspakning (vaginaltabletter 100 mg og krem 1 %) klotrimaziol
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Canesten kombinasjonspakning (vaginaltabletter 100 mg og krem 1 %) klotrimaziol Les nøye gjennom dette pakningsvedlegget. Det inneholder informasjon som er viktig
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Canesten kombinasjonspakning (vaginaltabletter 100 mg og krem 1 %) klotrimaziol Les nøye gjennom dette pakningsvedlegget. Det inneholder informasjon som er viktig
Pakningsvedlegg: Informasjon til pasienten. Colrefuz 500 mikrogram tabletter. kolkisin
 Pakningsvedlegg: Informasjon til pasienten Colrefuz 500 mikrogram tabletter kolkisin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon som er
Pakningsvedlegg: Informasjon til pasienten Colrefuz 500 mikrogram tabletter kolkisin Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon som er
Pakningsvedlegg: Informasjon til brukeren. Aranesp 60 mikrogram injeksjonsvæske, oppløsning i ferdigfylt sprøyte
 Pakningsvedlegg: Informasjon til brukeren Aranesp 10 mikrogram injeksjonsvæske, oppløsning i ferdigfylt sprøyte Aranesp 15 mikrogram injeksjonsvæske, oppløsning i ferdigfylt sprøyte Aranesp 20 mikrogram
Pakningsvedlegg: Informasjon til brukeren Aranesp 10 mikrogram injeksjonsvæske, oppløsning i ferdigfylt sprøyte Aranesp 15 mikrogram injeksjonsvæske, oppløsning i ferdigfylt sprøyte Aranesp 20 mikrogram
B. PAKNINGSVEDLEGG 28
 B. PAKNINGSVEDLEGG 28 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Cerezyme 200 E pulver til konsentrat til infusjonsvæske, oppløsning Imiglukerase Les nøye gjennom dette pakningsvedlegget før du begynner
B. PAKNINGSVEDLEGG 28 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Cerezyme 200 E pulver til konsentrat til infusjonsvæske, oppløsning Imiglukerase Les nøye gjennom dette pakningsvedlegget før du begynner
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. Puregon 150 IE/0,18 ml injeksjonsvæske, oppløsning follitropin beta
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Puregon 150 IE/0,18 ml injeksjonsvæske, oppløsning follitropin beta Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. Ta vare på dette
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Puregon 150 IE/0,18 ml injeksjonsvæske, oppløsning follitropin beta Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. Ta vare på dette
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. Protopic 0,03 % salve Takrolimusmonohydrat
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Protopic 0,03 % salve Takrolimusmonohydrat Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. Det inneholder informasjon som er viktig
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Protopic 0,03 % salve Takrolimusmonohydrat Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. Det inneholder informasjon som er viktig
Pakningsvedlegg: Informasjon til brukeren
 Pakningsvedlegg: Informasjon til brukeren ZOSTAVAX Pulver og væske til injeksjonsvæske, suspensjon i ferdigfylt sprøyte Vaksine mot helvetesild (levende) Les nøye gjennom dette pakningsvedlegget før du
Pakningsvedlegg: Informasjon til brukeren ZOSTAVAX Pulver og væske til injeksjonsvæske, suspensjon i ferdigfylt sprøyte Vaksine mot helvetesild (levende) Les nøye gjennom dette pakningsvedlegget før du
CAPRELSA. Vandetanib CAPRELSA (VANDETANIB) DOSERINGS- OG MONITORERINGSVEILEDNING FOR PASIENTER OG PASIENTENS OMSORGSPERSONER (PEDIATRISK BRUK)
 CAPRELSA Vandetanib Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig. Du kan bidra ved å melde enhver mistenkt bivirkning. Se avsnitt 4 i pakningsvedlegget
CAPRELSA Vandetanib Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig. Du kan bidra ved å melde enhver mistenkt bivirkning. Se avsnitt 4 i pakningsvedlegget
Pakningsvedlegg: Informasjon til brukeren Karvea 150 mg filmdrasjerte tabletter irbesartan
 Pakningsvedlegg: Informasjon til brukeren Karvea 150 mg filmdrasjerte tabletter irbesartan Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til brukeren Karvea 150 mg filmdrasjerte tabletter irbesartan Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Veiledning for administrering av hetteglass og sprøyter (for pasienter, leger, sykepleiere, farmasøyter.)
 VEILEDNING FOR Å STARTE MED APIDRA 10 ml HETTEGLASS Apidra 100 E/ml injeksjonsvæske, oppløsning er en klar, fargeløs, vandig oppløsning uten synlige partikler. Hvert hetteglass inneholder 10 ml oppløsning
VEILEDNING FOR Å STARTE MED APIDRA 10 ml HETTEGLASS Apidra 100 E/ml injeksjonsvæske, oppløsning er en klar, fargeløs, vandig oppløsning uten synlige partikler. Hvert hetteglass inneholder 10 ml oppløsning
Pakningsvedlegg: Informasjon til brukeren. Temodal 2,5 mg/ml pulver til infusjonsvæske, oppløsning. temozolomid
 Pakningsvedlegg: Informasjon til brukeren Temodal 2,5 mg/ml pulver til infusjonsvæske, oppløsning temozolomid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder
Pakningsvedlegg: Informasjon til brukeren Temodal 2,5 mg/ml pulver til infusjonsvæske, oppløsning temozolomid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder
Tilberedning og injeksjon
 Se s. 2 og 10 for anbefalt dosering Tilberedning og injeksjon qilaris 150 mg pulver til injeksjonsvæske, oppløsning Veiledning for pasienter og helsepersonell om klargjøring og administrering av ILARIS
Se s. 2 og 10 for anbefalt dosering Tilberedning og injeksjon qilaris 150 mg pulver til injeksjonsvæske, oppløsning Veiledning for pasienter og helsepersonell om klargjøring og administrering av ILARIS
Pasientveiledning Lemtrada
 Pasientveiledning Lemtrada Viktig sikkerhetsinformasjon Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig. Du kan bidra ved å melde enhver mistenkt
Pasientveiledning Lemtrada Viktig sikkerhetsinformasjon Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig. Du kan bidra ved å melde enhver mistenkt
Pakningsvedlegg: Informasjon til brukeren. Nasonex 50 mikrogram/dose nesespray, suspensjon. mometasonfuroat
 Pakningsvedlegg: Informasjon til brukeren Nasonex 50 mikrogram/dose nesespray, suspensjon mometasonfuroat Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder
Pakningsvedlegg: Informasjon til brukeren Nasonex 50 mikrogram/dose nesespray, suspensjon mometasonfuroat Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder
VIKTIG SIKKERHETSINFORMASJON FOR PASIENTER SOM FÅR BEHANDLING MED RIXATHON (RITUKSIMAB)
 FOR PASIENTER SOM FÅR BEHANDLING (RITUKSIMAB) VED IKKE-ONKOLOGISKE INDIKASJONER 2 3 I denne håndboken vil du få svar på noen av spørsmålene du kanskje har vedrørende bivirkninger og potensiell risiko ved
FOR PASIENTER SOM FÅR BEHANDLING (RITUKSIMAB) VED IKKE-ONKOLOGISKE INDIKASJONER 2 3 I denne håndboken vil du få svar på noen av spørsmålene du kanskje har vedrørende bivirkninger og potensiell risiko ved
Pakningsvedlegg: Informasjon til brukeren. Emend 80 mg harde kapsler aprepitant
 Pakningsvedlegg: Informasjon til brukeren Emend 80 mg harde kapsler aprepitant Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon som er viktig
Pakningsvedlegg: Informasjon til brukeren Emend 80 mg harde kapsler aprepitant Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon som er viktig
Pakningsvedlegg: Informasjon til brukeren. Esmeron 10 mg /ml injeksjonsvæske, oppløsning rokuroniumbromid
 PAKNINGSVEDLEGG 1 Pakningsvedlegg: Informasjon til brukeren Esmeron 10 mg /ml injeksjonsvæske, oppløsning rokuroniumbromid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
PAKNINGSVEDLEGG 1 Pakningsvedlegg: Informasjon til brukeren Esmeron 10 mg /ml injeksjonsvæske, oppløsning rokuroniumbromid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
Din veileder til Lemilvo (Aripiprazol)
 Din veileder til Lemilvo (Aripiprazol) Informasjonsbrosjyre for pasient/pårørende 2 Informasjonsbrosjyre for pasient/pårørende - Aripiprazole Innledning Du har fått diagnosen bipolar I lidelse av legen
Din veileder til Lemilvo (Aripiprazol) Informasjonsbrosjyre for pasient/pårørende 2 Informasjonsbrosjyre for pasient/pårørende - Aripiprazole Innledning Du har fått diagnosen bipolar I lidelse av legen
Pakningsvedlegg: Informasjon til brukeren. Temodal 5 mg harde kapsler. Temodal 250 mg harde kapsler
 Pakningsvedlegg: Informasjon til brukeren Temodal 5 mg harde kapsler Temodal 20 mg harde kapsler Temodal 100 mg harde kapsler Temodal 140 mg harde kapsler Temodal 180 mg harde kapsler Temodal 250 mg harde
Pakningsvedlegg: Informasjon til brukeren Temodal 5 mg harde kapsler Temodal 20 mg harde kapsler Temodal 100 mg harde kapsler Temodal 140 mg harde kapsler Temodal 180 mg harde kapsler Temodal 250 mg harde
Viktig informasjon for pasienter
 Ditt navn: Din adresse: Ditt telefonnummer: Din leges navn: _ Din leges adresse: _ Behandling av psoriasis med Stelara Viktig informasjon for pasienter Din leges telefonnummer: _ Her kan du notere legens
Ditt navn: Din adresse: Ditt telefonnummer: Din leges navn: _ Din leges adresse: _ Behandling av psoriasis med Stelara Viktig informasjon for pasienter Din leges telefonnummer: _ Her kan du notere legens
Pakningsvedlegg: Informasjon til brukeren. Nitro-Dur 5 mg/24 timer, depotplaster Nitro-Dur 10 mg/24 timer, depotplaster glyseroltrinitrat
 Pakningsvedlegg: Informasjon til brukeren Nitro-Dur 5 mg/24 timer, depotplaster Nitro-Dur 10 mg/24 timer, depotplaster glyseroltrinitrat Les nøye gjennom dette pakningsvedlegget før du begynner å bruke
Pakningsvedlegg: Informasjon til brukeren Nitro-Dur 5 mg/24 timer, depotplaster Nitro-Dur 10 mg/24 timer, depotplaster glyseroltrinitrat Les nøye gjennom dette pakningsvedlegget før du begynner å bruke
COSMEGEN brukes i behandlingen av visse former for nyrekreft (Wilms tumor), muskelkreft (rhabdomyosarkom), kreft i testikler og livmor.
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN COSMEGEN 0,5 mg injeksjons-/infusjonssubstans Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget.
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN COSMEGEN 0,5 mg injeksjons-/infusjonssubstans Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget.
Pakningsvedlegg: Informasjon til brukeren. Kineret 100 mg/0,67 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte anakinra
 Pakningsvedlegg: Informasjon til brukeren Kineret 100 mg/0,67 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte anakinra Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
Pakningsvedlegg: Informasjon til brukeren Kineret 100 mg/0,67 ml injeksjonsvæske, oppløsning i ferdigfylt sprøyte anakinra Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
Pakningsvedlegg: Informasjon til brukeren. TRUSOPT 20 mg/ml øyedråper, oppløsning dorzolamid
 Pakningsvedlegg: Informasjon til brukeren TRUSOPT 20 mg/ml øyedråper, oppløsning dorzolamid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til brukeren TRUSOPT 20 mg/ml øyedråper, oppløsning dorzolamid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til brukeren Bondil 250 mikrogram uretralstift Bondil 500 mikrogram uretralstift Bondil 1000 mikrogram uretralstift
 Pakningsvedlegg: Informasjon til brukeren Bondil 250 mikrogram uretralstift Bondil 500 mikrogram uretralstift Bondil 1000 mikrogram uretralstift alprostadil Les nøye gjennom dette pakningsvedlegget før
Pakningsvedlegg: Informasjon til brukeren Bondil 250 mikrogram uretralstift Bondil 500 mikrogram uretralstift Bondil 1000 mikrogram uretralstift alprostadil Les nøye gjennom dette pakningsvedlegget før
FORSTEO 20 mikrogram/80 mikroliter, injeksjonsvæske, oppløsning i ferdigfylt penn Teriparatide
 Pakningsvedlegg: Informasjon til brukeren FORSTEO 20 mikrogram/80 mikroliter, injeksjonsvæske, oppløsning i ferdigfylt penn Teriparatide Les nøye gjennom dette pakningsvedlegget før du begynner å bruke
Pakningsvedlegg: Informasjon til brukeren FORSTEO 20 mikrogram/80 mikroliter, injeksjonsvæske, oppløsning i ferdigfylt penn Teriparatide Les nøye gjennom dette pakningsvedlegget før du begynner å bruke
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. RENITEC Comp Mite tabletter (enalaprilmaleat/hydroklortiazid)
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN RENITEC Comp Mite tabletter (enalaprilmaleat/hydroklortiazid) Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget.
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN RENITEC Comp Mite tabletter (enalaprilmaleat/hydroklortiazid) Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget.
Pakningsvedlegg: Informasjon til brukeren RotaTeq, oral oppløsning Rotavirusvaksine, levende
 Pakningsvedlegg: Informasjon til brukeren RotaTeq, oral oppløsning Rotavirusvaksine, levende Les nøye gjennom dette pakningsvedlegget før barnet vaksineres. Det inneholder informasjon som er viktig for
Pakningsvedlegg: Informasjon til brukeren RotaTeq, oral oppløsning Rotavirusvaksine, levende Les nøye gjennom dette pakningsvedlegget før barnet vaksineres. Det inneholder informasjon som er viktig for
Pakningsvedlegg: Informasjon til pasienten. KEYTRUDA 50 mg pulver til konsentrat til infusjonsvæske, oppløsning pembrolizumab
 Pakningsvedlegg: Informasjon til pasienten KEYTRUDA 50 mg pulver til konsentrat til infusjonsvæske, oppløsning pembrolizumab Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon
Pakningsvedlegg: Informasjon til pasienten KEYTRUDA 50 mg pulver til konsentrat til infusjonsvæske, oppløsning pembrolizumab Dette legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon
Trinn-for-trinn bruksanvisning til Enbrel 25 mg og 50 mg ferdigfylt penn MYCLIC
 Trinn-for-trinn bruksanvisning til Enbrel 25 mg og 50 mg ferdigfylt penn MYCLIC For ytterligere informasjon les Enbrel pakningsvedlegg før bruk Innholdsfortegnelse Viktig å huske før du begynner...3 Hvordan
Trinn-for-trinn bruksanvisning til Enbrel 25 mg og 50 mg ferdigfylt penn MYCLIC For ytterligere informasjon les Enbrel pakningsvedlegg før bruk Innholdsfortegnelse Viktig å huske før du begynner...3 Hvordan
Fendrix, injeksjonsvæske, suspensjon Vaksine mot hepatitt B (rdna) (med adjuvans, adsorbert)
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Fendrix, injeksjonsvæske, suspensjon Vaksine mot hepatitt B (rdna) (med adjuvans, adsorbert) Les nøye gjennom dette pakningsvedlegget før du får denne vaksinen.
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Fendrix, injeksjonsvæske, suspensjon Vaksine mot hepatitt B (rdna) (med adjuvans, adsorbert) Les nøye gjennom dette pakningsvedlegget før du får denne vaksinen.
Pakningsvedlegg: Informasjon til pasienten. Tredaptive 1000 mg/20 mg tabletter med modifisert frisetting nikotinsyre/laropiprant
 Pakningsvedlegg: Informasjon til pasienten Tredaptive 1000 mg/20 mg tabletter med modifisert frisetting nikotinsyre/laropiprant Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
Pakningsvedlegg: Informasjon til pasienten Tredaptive 1000 mg/20 mg tabletter med modifisert frisetting nikotinsyre/laropiprant Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
Pakningsvedlegg: Informasjon til brukeren. Nasonex 50 mikrogram/dose nesespray, suspensjon. mometasonfuroat
 Pakningsvedlegg: Informasjon til brukeren Nasonex 50 mikrogram/dose nesespray, suspensjon mometasonfuroat Dette legemidlet er reseptfritt. Les nøye gjennom dette pakningsvedlegget før du begynner å bruke
Pakningsvedlegg: Informasjon til brukeren Nasonex 50 mikrogram/dose nesespray, suspensjon mometasonfuroat Dette legemidlet er reseptfritt. Les nøye gjennom dette pakningsvedlegget før du begynner å bruke
