Hver filmdrasjerte tablett inneholder eprosartanmesylat tilsvarende 600 mg eprosartan og 12,5 mg hydroklortiazid.
|
|
|
- Jørgen Amundsen
- 8 år siden
- Visninger:
Transkript
1 1. LEGEMIDLETS NAVN Teveten Comp 600 mg/12,5 mg, filmdrasjerte tabletter. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder eprosartanmesylat tilsvarende 600 mg eprosartan og 12,5 mg hydroklortiazid. For en fullstendig liste over hjelpestoffer, se pkt LEGEMIDDELFORM Tablett, filmdrasjert. Lysebrune, kapselformede, filmdrasjerte tabletter. Inskripsjonen på tabletten er 5147 på den ene siden. 4. KLINISKE OPPLYSNINGER 4.1 Indikasjoner Essensiell hypertensjon. Teveten Comp 600 mg/12,5 mg er indisert hos pasienter med blodtrykk som ikke er tilstrekkelig redusert med eprosartan monoterapi. 4.2 Dosering og administrasjonsmåte Anbefalt dosering er én tablett Teveten Comp 600 mg/12,5 mg én gang daglig, tatt om morgenen. Overgang fra monoterapi med eprosartan til den faste kombinasjonen kan vurderes etter 8 ukers blodtrykkstabilisering. Teveten Comp 600 mg/12,5 mg kan tas uavhengig av måltid. Eldre Ingen dosejustering er påkrevd hos eldre, selv om kun begrenset informasjon er tilgjengelig for denne gruppen. Pediatrisk populasjon Da sikkerhet og effekt ved administrasjon til barn ikke er fastslått, anbefales ikke behandling av barn og ungdom under 18 år med Teveten Comp 600 mg/12,5 mg. Nedsatt leverfunksjon Hos pasienter med mild til moderat nedsatt leverfunksjon anbefales ikke bruk av Teveten Comp 600 mg/12,5 mg, siden det kun foreligger begrenset erfaring med eprosartanmesylat i denne pasientgruppen. Hos pasienter med alvorlig nedsatt leverfunksjon er Teveten Comp 600 mg/12,5 mg kontraindisert (se pkt. 4.3 og 4.4). Nedsatt nyrefunksjon Hos pasienter med mild til moderat nedsatt nyrefunksjon (kreatinin clearence 30 ml/minutt) er dosejustering ikke nødvendig. Teveten Comp 600 mg/12,5 mg er kontraindisert hos pasienter med alvorlig nedsatt nyrefunksjon (se pkt 4.3 og pkt 4.4). 1
2 4.3 Kontraindikasjoner Overfølsomhet overfor eprosartan, sulfonamidderivater (som hydroklortiazid), eller overfor et eller flere av hjelpestoffene listet opp i pkt Andre og tredje trimester av graviditet (se pkt. 4.4 og 4.6). Alvorlig redusert leverfunksjon. Kolestase og obstruktive gallesykdommer. Alvorlig redusert nyrefunksjon (kreatinin clearence <30 ml/minutt). Hemodynamisk signifikant bilateral renovaskulær sykdom eller alvorlig stenose i en enkelt fungerende nyre. Behandlingsresistent hypokalemi eller hyperkalsemi. Refraktorisk hyponatremi. Symptomatisk hyperurikemi/urinsyregikt. 4.4 Advarsler og forsiktighetsregler Hypersensitivitetsreaksjoner overfor hydroklortiazid er mer sannsynlig hos pasienter som har hatt allergier inkludert hypersensitivitet overfor sulfonamiddervierte substanser. Pasienter med risiko for nedsatt nyrefunksjon Noen pasienter hvis nyrefunksjon er avhengig av kontinuerlig naturlig aktivitet i renin-angiotensinaldosteronsystemet (f.eks. pasienter med alvorlig hjertesvikt [NYHA-klassifisering: klasse IV], bilateral nyrearteriestenose eller stenose i arterien til en enkelt fungerende nyre), har risiko for å utvikle oliguri og/eller progressiv azotemi og i sjeldne tilfeller akutt nyresvikt under behandling med en angiotensinkonverterende enzym- (ACE-) hemmer. Disse hendelsene oppstår mer sannsynlig hos pasienter som får samtidig behandling med et diuretikum. Det foreligger ikke tilstrekkelig terapeutiske erfaring med angiotensin-ii-reseptorantagonister, slik som eprosartan, til å kunne bestemme om det er en lignende risiko for å utvikle kompromitterende nyrefunksjon hos disse følsomme pasientene. Nyrefunksjonen skal overvåkes nøye ettersom det er en økt risiko for alvorlig hypotensjon og nedsatt nyrefunksjon hos disse pasientene. Nedsatt nyrefunksjon og nyretransplantasjon Når eprosartan + hydroklortiazid skal brukes hos pasienter med nedsatt nyrefunksjon skal nyrefunksjon, serumkalium og urinsyre vurderes før oppstart av og regelmessig under behandling med eprosartan + hydroklortiazid. Dersom nyrefunksjonen forverres under behandling skal behandling med eprosartan + hydroklortiazid revurderes (se pkt. 4.3). Hydroklortiazidassosiert azotemi kan forekomme hos pasienter med nedsatt nyrefunksjon. Det er ingen erfaring med Teveten Comp 600 mg/12,5 mg hos nyretransplanterte pasienter. Nedsatt leverfunksjon Når eprosartan brukes hos pasienter med lett til moderat nedsatt leverfunksjon bør spesiell forsiktighet utvises grunnet begrenset erfaring hos denne pasientpopulasjonen. Hydroklortiazid bør kun brukes med forsiktighet hos pasienter med lett til moderat nedsatt leverfunksjon da det kan forårsake intrahepatisk kolestase. Endringer i væske- og elektrolyttbalansen kan fremskynde hepatisk koma. Stoffskifte- og endokrine forstyrrelser Hydroklortiazid kan svekke glukosetoleranse og dette kan kreve dosejustering av antidiabetika (se pkt. 4.5). Latent diabetes mellitus kan manifestere seg ved behandling med Teveten Comp 600 mg/12,5 mg. Ved doser på 12,5 mg hydroklortiazid i Teveten Comp 600 mg/12,5 mg ble kun lette stoffskifte- og endrokrine bivirkninger observert (økning i serumkolesterol og triglyserider). Elektrolyttubalanse Hydroklortiazid kan forårsake væske- eller elektrolyttubalanse (hypokalemi, hyponatremi, hyperkalsemi, hypomagnesemi og hypokloremisk alkalose). 2
3 Som for alle pasienter som får behandling med diuretika bør periodisk måling av serumelektrolytter overveies. Kaliumsparende diuretika, kaliumtilskudd eller kaliumholdige salterstatninger bør gis med forsiktighet sammen med eprosartan (se pkt. 4.5). Akutt myopi og sekundær trangvinklet glaukom Hydroklortiazid, et sulfonamid, kan forårsake en idiosynkratisk reaksjon som medfører forbigående myopi og akutt trangvinklet glaukom. Symptomene inkluderer akutt opptreden av nedsatt synsskarphet eller øyesmerte og oppstår vanligvis innen timer til uker etter behandlingsstart. Ubehandlet akutt trangvinklet glaukom kan medføre permanent synstap. Primærbehandling er seponering av hydroklortiazid så snart som mulig. Det kan være nødvendig å vurdere øyeblikkelig medisinsk eller kirurgisk behandling dersom det intraokulære trykket forblir ukontrollert. Risikofaktorer for å utvikle akutt trangvinklet glaukom kan inkludere tidligere sulfonamid- eller penicillinallergi. Hypotensjon Symptomatisk hypotensjon kan forekomme hos pasienter med alvorlig natrium- eller volumdeplesjon, f.eks. som et resultat av høye doser diuretika, saltrestriksjon i dietten, diaré eller oppkast. Natriumog/eller volumdeplesjon bør korrigeres før behandling med Teveten Comp 600 mg/12,5 mg. Aorta- og mitralklaffstenose, hypertrofisk obstruktiv kardiomyopati Som for andre vasodilatorer bør pasienter med aorta- eller mitralklaffstenose eller hypertrofisk obstruktiv kardiomyopati behandles med forsiktighet. Primær hyperaldosteronisme Pasienter med primær hyperaldosteronisme reagerer ikke tilstrekkelig på antihypertensiva som virker via hemming av renin-angiotensin-aldosteron-systemet. Behandling med Teveten Comp 600 mg/12,5 mg anbefales derfor ikke. Hjerte-karsykdom Hittil er det begrenset erfaring hos pasienter med hjerte-karsykdom. Graviditet Angiotensin-II-reseptorantagonister bør ikke initieres under graviditet. Med mindre det anses som essensielt å fortsette behandling med angiotensin-ii-reseptorantagonister, bør pasienter som planlegger graviditet bytte til alternativ antihypertensivbehandling med en etablert sikkerhetsprofil for bruk under graviditet. Ved påvist graviditet bør behandling med angiotensin-ii-reseptorantagonister seponeres umiddelbart og alternativ behandling bør startes hvis det er hensiktsmessig (se pkt. 4.3 og 4.6). Andre advarsler og forsiktighetsregler Det har blitt rapportert at tiaziddiuretika forverrer eller aktiverer systemisk lupus erythematosus. Pasienter med sjeldne arvelige problemer med galaktoseintoleranse, en spesiell form for hereditær laktasemangel (Lapp lactase deficiency) eller glukose-galaktose malabsorpsjon bør ikke ta dette legemidlet. Hydroklortiazid kan gi positive resultater i dopingtester. 4.5 Interaksjon med andre legemidler og andre former for interaksjon Potensielle interaksjoner relatert til både eprosartan og hydroklortiazid: Samtidig bruk anbefales ikke. Litium: Reversible økninger i serumlitium-konsentrasjoner og toksisitet har blitt rapportert ved samtidig administrering av litium med angiotensin converting enzyme-hemmere, og sjeldent, med angiotensin IIreseptorantagonister. I tillegg er renal clearance av litium redusert av tiazider og som følge av dette kan 3
4 risikoen for litiumtoksisitet økes. Derfor anbefales ikke bruk av Teveten Comp 600 mg/12,5 mg og litium i kombinasjon (se pkt 4.4). Hvis bruk av denne kombinasjonen viser seg å være nødvendig, anbefales nøye kontroll av serumlitium-nivåene. Forsiktighet er påkrevet ved samtidig bruk. Baclofen: Potensiering av den antihypertensive effekten kan oppstå. Ikke steroide anti-inflammatoriske legemidler: Som med andre ACE-hemmere kan samtidig bruk av angiotensin II-reseptorantagonister og NSAIDs medføre økt risiko for forverring av nyrefunksjonen, inkludert mulig akutt nyresvikt og økning i serumkalium, særlig hos pasienter med nedsatt nyrefunksjon. Kombinasjonen bør administreres med forsiktighet, særlig hos eldre. Pasienter bør være adekvat hydrert og det bør tas hensyn til kontroll av nyrefunksjonen etter initiering av samtidig behandling, og deretter med jevne mellomrom. Samtidig bruk av losartan med NSAID-et indometacin medførte nedsatt effekt av angiotensin II-reseptorantagonisten, og en klasseeffekt kan ikke utelukkes. Samtidig behandling som det bør tas hensyn til. Amifostin: Potensiering av den antihypertensive effekten kan forekomme. Andre antihypertensiva: Den blodtrykkssenkende effekten av Teveten Comp 600 mg/12,5 mg kan økes ved samtidig bruk av andre antihypertensive legemidler. Alkohol, barbiturater, narkotika eller antidepressiva: Potensiering av ortostatisk hypotensjon kan forekomme. Potensielle interaksjoner relatert til eprosartan: Samtidig bruk anbefales ikke. Legemidler som påvirker kaliumnivåene: Basert på erfaring med bruk av andre legemidler som påvirker renin-angiotensin-systemet kan samtidig bruk av kaliumsparende diuretika, kaliumtilskudd, saltsubstitutter som inneholder kalium eller andre legemidler som kan øke serumkaliumnivåene (f.eks. heparin, ACE-hemmere) føre til økning i serumkalium. Dersom legemidler som påvirker kaliumnivåene foreskrives i kombinasjon med Teveten Comp 600 mg/12,5 mg, anbefales kontroll av kaliumplasmanivåene (se pkt. 4.4). Potensielle interaksjoner relatert til hydroklortiazid: Samtidig bruk anbefales ikke. Legemidler som påvirker kaliumnivåene: Den kalium-uttømmende effekten av hydroklortiazid kan potensieres av samtidig administrering av andre legemidler som forbindes med kaliumtap og hypokalemi (f.eks. andre kaliuretiske diuretika, laksativa, kortikosteroider, ACTH, amfotericin, karbenoksolon, penicillin G natrium eller salisylsyrederivater). Slik samtidig behandling anbefales derfor ikke (se pkt. 4.4). Forsiktighet er påkrevet ved samtidig bruk. Kalsiumsalter og vitamin D: Tiaziddiuretika kan øke serumkalsiumnivåene pga. nedsatt utskillelse. Hvis kalsiumtilskudd eller legemidler som påvirker serumkalsiumnivåene (f. eks. behandling med vitamin D) må foreskrives, bør serumkalsiumnivåene kontrolleres og kalsiumdoseringen justeres i henhold til disse. Kolestyramin og kolestipolresiner: 4
5 Absorpsjon av hydroklortiazid hemmes ved tilstedeværelse av anionbyttende resiner, som kolestyramin eller kolestipol. Imidlertid kan interaksjonen minimeres ved oppdelt inntak av hydroklortiazid og resin på den måten at hydroklortiazid tas minst 4 timer før eller 4-6 timer etter resinet. Digitalisglykosider: Tiazid-indusert hypokalemi eller hypomagnesemi kan fremme begynnelse av digitalisinduserte hjertearytmier. Legemidler som påvirkes av serumkaliumforstyrrelser: Jevnlig kontroll av serumkalium og EKG anbefales når Teveten Comp 600 mg/12,5 mg administreres med legemidler som påvirkes av serumkaliumforstyrrelser (f.eks. digitalisglykosider og antiarytmika) og ved følgende torsades de pointes (ventrikulær takykardi)-induserende legemidler (inkludert noen antiarytmika), siden hypokalemi er en predisponerende faktor for torsades de pointes (ventrikulær takykardi): Klasse Ia-antiarytmika (f.eks. kinidin, hydrokinidin, disopyramid). Klasse III-antiarytmika (f.eks. amiodaron, sotalol, defetilid, ibutilid). Noen antipsykotika (f.eks. tioridazin, klorpromazin, levomepromazin, trifluoperazin, cyamemazin, sulpirid, sultoprid, amisulprid, tiaprid, pimozid, haloperidol, droperidol). Andre (f.eks. bepridil, cisaprid, difemanil, erytromycin IV, halofantrin, mizolastin, pentamidin, terfenadin, vinkamin IV). Ikke-depolariserende muske-skjelettrelaksantia (f.eks. tubokurarin): Effekten av ikke-depolariserende muskelskjelettrelaksantia kan potensieres av hydroklortiazid. Antikolinerge midler (f.eks. atropin, biperiden): Økning i biotilgjengeligheten til tiaziddiuretika ved senkning av gastrointestinal motilitet og magetømmingshastighet. Antidiabetika (orale og insulin): Behandling med tiazid kan påvirke glukosetoleransen. Dosejustering av det antidiabetiske legemidlet kan være nødvendig (se pkt 4.4). Metformin: Metformin bør brukes med forsiktighet pga. risiko for laktisk acidose indusert ved mulig funksjonell nyresvikt i forbindelse med hydroklortiazid. Betablokkere og diazoksid: Den hyperglykemiske effekten av betablokkere og diazoksid kan økes av tiazider. Pressoraminer (f.eks. noradrenalin): Effekten av pressoraminer kan reduseres. Legemidler som brukes i behandling av urinsyregikt (probenecid, sulfinpyrazon og allopurinol): Dosejustering av urikosurika kan være nødvendig siden hydroklortiazid kan øke nivået av serumurinsyre. Doseøkning av probenecid eller sulfinpyrazon kan være nødvendig. Samtidig administrering av tiazid kan øke forekomsten av hypersensitivitetsreaksjoner overfor allopurinol. Amantadin: Tiazider kan øke risikoen for bivirkninger forårsaket av amantadin. Cytotoksiske midler (f.eks. cyklofosfamid, metotreksat): Tiazider kan redusere renal utskillelse av cytotoksiske legemidler og potensiere deres myelosupressive effekter. Tetracykliner: 5
6 Samtidig administrering av tetracykliner og tiazider øker risikoen for tetracyklinindusert økning i urea. Denne interaksjonen gjelder sannsynligvis ikke doksycyklin. Legemidler som senker serumnatriumnivået: Den hyponatremiske effekten av hydroklortiazid kan forsterkes ved samtidig administrering av legemidler som antidepressiva, antipsykotika, antiepileptika, osv. Det bør utvises forsiktighet ved langvarig administrasjon av disse legemidlene. 4.6 Fertilitet, graviditet og amming Graviditet Angiotensin II-reseptorantagonister (AIIRAs): Bruk av eprosartan er ikke anbefalt i første trimester av graviditeten (se pkt. 4.4). Bruk av eprosartan er kontraindisert i andre og tredje trimester av graviditeten (se pkt. 4.3 og 4.4). Det er ikke tilstrekkelig epidemiologisk grunnlag for å konkludere med at eksponering for ACE-hemmere i første trimester fører til økt risiko for teratogenese, men en liten risiko kan ikke utelukkes. Det foreligger ikke kontrollerte epidemiologiske data for risikoen ved bruk av AII-reseptorantagonister, men lignende risiko kan eksistere for denne klassen legemidler. Med mindre videre bruk av AII-reseptorantagonister ansees som helt nødvendig, bør pasienter som planlegger graviditet, bytte til alternativ anti-hypertensiv behandling med en etablert sikkerhetsprofil for bruk under graviditet. Hvis graviditet blir påvist, bør behandling med AII-reseptorantagonister stanses umiddelbart, og hvis hensiktsmessig, alternativ behandling startes. Det er kjent at eksponering for AII-reseptorantagonister i andre og tredje trimester kan påvirke funksjoner hos foster (nedsatt nyrefunksjon, redusert mengde av fostervann, forsinket bendannelse i skallen) og toksisitet hos nyfødte (nyresvikt, hypotensjon, hyperkalemi) hos mennesker. Ultralydundersøkelse for å undersøke nyrefunksjon og kranium anbefales hvis fosteret har blitt eksponert for AIIreseptorantagonister i andre eller tredje trimester av svangerskapet. Spedbarn bør observeres nøye for hypotensjon hvis moren har brukt AII-reseptorantagonister under svangerskapet (se pkt. 4.3 og 4.4). Hydroklortiazid Erfaring med bruk av hydroklortiazid ved graviditet er begrenset, spesielt i første trimester. Dyrestudier er utilstrekkelige. Hydroklortiazid passerer placenta. Basert på hydroklortiazids farmakologiske virkningsmekanisme kan bruk i andre og tredje trimester redusere blodgjennomstrømning mellom placenta og fosteret, og kan hos nyfødte og foster forårsake bivirkninger, som gulsott, elektrolyttforstyrrelser og trombocytopeni. Hydroklortiazid bør ikke brukes ved svangerskapsødem, hypertensjon under svangerskapet eller svangerskapsforgiftning grunnet risikoen for plasmavolumreduksjon og redusert gjennomstrømning i placenta uten noen fordeler på sykdomsforløpet. Hydroklortiazid bør ikke brukes ved essensiell hypertensjon hos gravide, med mindre det i sjeldne tilfeller ikke finnes et terapeutisk alternativ. Amming Angiotensin II-reseptorantagonister (AIIRAs) Ettersom det ikke finnes informasjon vedrørende bruk av Teveten Comp 600 mg/12,5 mg ved amming, er Teveten Comp 600 mg/12,5 mg ikke anbefalt, og det er ønskelig å benytte behandlingsalternativ med bedre etablert sikkerhetsprofil ved amming, spesielt ved amming av nyfødte eller for tidlig fødte spedbarn. Hydroklortiazid Hydroklortiazid skilles ut i små mengder i morsmelk hos mennesker. Høye doser tiazider forårsaker kraftig diurese som kan hemme melkeproduksjonen. Bruk av Teveten Comp 600 mg/12,5 mg anbefales 6
7 ikke ved amming. Dersom Teveten Comp 60 mg/12,5 mg brukes under amming bør dosen holdes så lav som mulig. Fertilitet Det finnes ingen kliniske data vedrørende fertilitet. Ikke-kliniske data for eprosartan viste ingen effekter på mannlig og kvinnelig fertilitet. Det er ingen tilgjengelig preklinisk informasjon om mulige effekter av hydroklortiazid på fertilitet. 4.7 Påvirkning av evnen til å kjøre bil eller bruke maskiner Det er ikke gjennomført studier vedrørende påvirkningen av evnen til å kjøre bil eller bruke maskiner, men basert på de farmakodynamiske egenskaper er det lite sannsynlig at Teveten Comp 600 mg/12,5 mg påvirker denne evnen. Ved bilkjøring eller betjening av maskiner bør det tas med i beregningen at svimmelhet og tretthet kan oppstå under behandling av hypertensjon. 4.8 Bivirkninger a. Sammendrag av sikkerhetsprofilen De vanligst rapporterte bivirkningene hos pasienter som behandles med eprosartan + hydroklortiazid er hodepine og uspesifikke gastrointestinale plager, som oppstår hos henholdsvis ca. 11 % og 8 % av pasientene (vs. 14 % og 8 % med placebo) b. Sammendrag av bivirkninger Bivirkninger som oppsto i placebokontrollerte kliniske studier eller er rapportert fra vitenskapelig litteratur er oppsummert i tabellen nedenfor. Under hver frekvenskategori er bivirkningene listet opp etter data fra eprosartan, kombinasjonen eprosartan + hydroklortiazid og hydroklortiazid alene (se fotnotene til tabellen). BIVIRKNINGER RAPPORTERT I PLACEBOKONTROLLERTE STUDIER OG VITENSKAPELIG LITTERATUR Svært Vanlige Mindre Sjeldne Svært vanlig 1/100 til vanlige 1/ sjeldne e <1/10 1/1000 til til <1/ 1/10 <1/100 <1/ Sykdommer i blod og lymfatiske organer Forstyrrelser i immunsystemet Stoffskifte- og ernæringsbetingede sykdommer Psykiatriske lidelser Hyperglyke mi Leukopeni Hypersensitivi tet Hypokalemi Hyponatremi Hypokloremi Hyperurikemi Urinsyregikt Hyperkolesterolemi Depresjon Angst Insomnia Nervøsitet Forstyrrelser i MedDRA organklassesystem Hemolytisk anemi* Ikke kjent (kan ikke anslås utifra tilgjengelige data) Agranulocytose Aplastisk anemi Trombocytopeni Anafylaktiske reaksjoner Hyperkalsemi Hypomagnesemi Hypertriglyseridemi Anoreksi Rastløshet 7
8 Nevrologiske sykdommer Øyesykdomme r Sykdommer I øre og labyrint Karsykdomme r Pulmonalt ødem * Pneumonitt* Sykdommer i respirasjonsorganer, thorax og mediastinum Gastrointestinale sykdommer Sykdommer i lever og galleveier Hud- og underhudssykd ommer Sykdommer I muskler, bindevev og skjelett Sykdommer i nyre og urinveier Lidelser i kjønnsorganer og brystsykdommer Svært vanlig e 1/10 MedDRA organklassesystem Hodepine** Vanlige 1/100 til <1/10 Svimmelhet Parestesi Hypotensjo n (f.eks. ortostatisk) Rhinitt Uspesifikke gastrointestinale lidelser (f.eks. kvalme, diaré, oppkast) Allergiske hudreaksjoner (f.eks. utslett, pruritus) Mindre vanlige 1/1000 til <1/100 libido Vertigo** Konstipasjon* * Angioødem Muskelkramper** Seksuell dysfunksjon Sjeldne 1/ til <1/1000 Pankreatitt * Svært sjeldne <1/ Ikke kjent (kan ikke anslås utifra tilgjengelige data) Akutt myopi og sekundær trangvinklet glaukom * Vaskulitt Gulsott (intrahepatisk kolestatisk gulsott) Toksisk epidermal nekrolyse Fotosensitivitet Systemisl lupus erythematosus Interstitiell nefritt Nyresvikt/nedsatt nyrefunksjon hos risikopasienter (f.eks. nyrearteriestenose) 8
9 MedDRA organklassesystem Generelle lidelser og reaksjoner på administrasjon s-stedet Svært vanlig e 1/10 Vanlige 1/100 til <1/10 Asteni Mindre vanlige 1/1000 til <1/100 Pyreksi Sjeldne 1/ til <1/1000 * Frekvens basert på data fra vitenskapelig litteratur om hydroklortiazid ** Forekom ikke hyppigere enn i placebogruppen Svært sjeldne <1/ Ikke kjent (kan ikke anslås utifra tilgjengelige data) Melding av mistenkte bivirkninger Melding av mistenkte bivirkninger etter godkjenning av legemidlet er viktig. Det gjør det mulig å overvåke forholdet mellom nytte og risiko for legemidlet kontinuerlig. Helsepersonell oppfordres til å melde enhver mistenkt bivirkning. Dette gjøres via meldeskjema som finnes på nettsiden til Statens legemiddelverk: Field 4.9 Overdosering Begrensede data er tilgjengelig med hensyn til overdosering hos mennesker. Det har vært individuelle rapporter etter markedsføring med doser opp til mg eprosartan. Selv om de fleste pasientene rapporterte ingen symptomer, er det hos én pasient observert sirkulatorisk kollaps etter inntak av mg eprosartan. Personen ble helt frisk igjen. Maksimal inntatt dose av eprosartan + hydroklortiazid var 3600 mg eprosartan/75 mg hydroklortiazid, som ble rapportert i forbindelse med et selvmordsforsøk. Det mest sannsynlige tegnet på overdose vil være hypotensjon. Andre symptomer kan skyldes dehydrering og elektrolyttmangel (hypokalemi, hypokloremi, hyponatremi) og vil mest sannsynlig opptre som kvalme og søvnighet. Behandlingen bør være støttende og symptomatisk. Eprosartan fjernes ikke ved hemodialyse. Det er ikke klarlagt i hvilken grad hydroklortiazid fjernes ved hemodialyse. 5. FARMAKOLOGISKE EGENSKAPER 5.1 Farmakodynamiske egenskaper Farmakoterapeutisk gruppe: Eprosartan og diuretika.atc-kode: C09D A02. Eprosartan Eprosartan er et syntetisk, peroralt virkende ikke-bifenyl, ikke-tetrazol-angiotensin II-reseptor antagonist som bindes selektivt til AT1-reseptoren. Angiotensin II har en sentral rolle i patofysiologien ved hypertensjon. Det er det primært aktive hormonet i renin-angiotensin-aldosteronsystemet og er en potent vasokonstriktor. Eprosartan motvirker effekten av angiotensin II på blodtrykk, renal blodgjennomstrømning og aldosteronsekresjon hos mennesker. Blodtrykkskontroll vedlikeholdes over 24 timer uten at det oppstår postural hypotensjon eller reflekstakykardi etter første dosen. Seponering av behandling med eprosartan medfører ikke hurtig rebound økning av blodtrykket. Eprosartan hemmer ikke renale autoreguleringsmekanismer. Hos friske voksne menn har eprosartan vist å øke gjennomsnittlig blodgjennomstrømning i nyrene. Eprosartan forsterker ikke effekter relatert til bradykinin (ACE-mediert), som for eksempel tørrhoste. 9
10 Hydroklortiazid Hydroklortiazid er et etablert tiaziddiuretikum. Tiazider påvirker elektrolytt reabsorbsjonen fra nyretubulus, og øker utskillelsen av væske, natrium og klorid. Den diuretiske virkningen av hydroklortiazid reduserer plasmavolum, øker plasmarenin aktivitet, øker aldosteronutskillelse med medfølgende økt tap av kalium og bikarbonat i urin og reduksjon av serumkalium. Den antihypertensive virkningen av hydroklortiazid antas å skyldes en kombinert diuretisk og vaskulær aktivitet (reduksjon av vaskulær motstand). Teveten Comp 600 mg/12,5 mg I en placebokontrollert, 8 ukers klinisk studie med 473 pasienter med essensiell hypertensjon ble det vist at kombinasjonen av 600 mg eprosartan og 12,5 mg hydroklortiazid ble godt tolerert og var effektiv. Teveten Comp 600 mg/12,5 mg reduserte systolisk blodtrykk og diastolisk blodtrykk i en klinisk relevant størrelsesorden og var statistisk signifikant bedre enn hver av komponentene alene og placebo, til tross for en høy placeborespons (p=0,08 for sammenlikning av eprosartan alene og placebo). Tolerabiliteten var lik for både eprosartan/hydroklortiazid 600 mg/12,5 mg, eprosartan og placebo. I en annen klinisk studie med pasienter med et diastolisk blodtrykk mellom 98 og 114 mmhg, som ikke var tilstrekkelig behandlet med en 3-ukers behandling med eprosartan 600 mg alene, fikk enten eprosartan/hydroklortiazid 600 mg/12,5 mg eller 600 mg eprosartan alene i 8 uker. Kombinasjonen medførte en signifikant og klinisk relevant ytterligere reduksjon i systolisk og diastolisk blodtrykk hos pasienter som ikke responderte tilfredsstillende på eprosartan monoterapi. Tolerabiliteten var like god for kombinasjonen som for monoterapi. Kun begrensede data foreligger hos pasienter over 80 år. Effekten av kombinasjonen av eprosartan og hydroklortiazid på sykelighet og dødelighet ble ikke undersøkt. Epidemiologiske studier viste at langtidsbehandling med hydroklortiazid reduserer risikoen for kardiovaskulær mortalitet og sykelighet. 5.2 Farmakokinetiske egenskaper Eprosartan Absolutt biologisk tilgjengelighet etter en oral dose eprosartan er ca. 13%. Maksimal plasmakonsentrasjon av eprosartan oppnås 1 til 2 timer etter dosering. Terminal eliminasjonshalveringstid for eprosartan er vanligvis 5 til 9 timer. Eprosartan akkumuleres kun i liten grad (14%) ved langtidsbruk. Administrasjon av eprosartan sammen med mat forsinker absorpsjon, men reduserer ikke biotilgjengeligheten. For doseintervallet mellom 100 mg og 800 mg er det en litt mindre enn doseproporsjonal økning i eprosartaneksponeringen, sannsynligvis pga. de fysisk-kjemiske egenskapene til legemidlet. Plasmaproteinbinding av eprosartan er 98% og påvirkes ikke av kjønn, alder, redusert leverfunksjon eller mild til moderat reduksjon av nyrefunksjonen. Distribusjonsvolumet av eprosartan er omtrent 13 liter. Total plasmaclearance er omtrent 130 ml/min. Etter oral dosering av 14 C eprosartan gjenfinnes omtrent 90% av radioaktiviteten i fæces. Omtrent 7 % utskilles i urin, hvorav 80 % som eprosartan. Både AUC og Cmax-verdiene er forhøyet hos eldre (i gjennomsnitt 2 ganger høyere), men dette krever ingen forandring av dosen. AUC (men ikke Cmax) av eprosartan er forhøyet i gjennomsnitt 40 % hos pasienter med nedsatt leverfunksjon, men dette krever ingen forandring av dosen. Sammenlignet med personer med normal nyrefunksjon var gjennomsnittelig AUC og Cmax ca. 30 % høyere hos pasienter med moderat nedsatt nyrefunksjon (kreatinin clearance ml/min.), ca. 50 % høyere hos pasienter med alvorlig nedsatt nyrefunksjon (kreatinin clearance 5-29 ml/min). Det er ingen forskjell i farmakokinetikken hos menn og kvinner. Det ble vist in vitro at eprosartan ikke hemmer human Cytokrom P450 isoenzymene CYP1A, 2A6, 2C9/8, 2C19, 2D6, 2E og 3A. 10
11 Hydroklortiazid Etter oral administrasjon er absorpsjonen av hydroklortiazid relativt rask. Gitt i fastende tilstand er gjennomsnittlig eliminasjonshalveringstid 5-15 timer. Hydroklortiazid metaboliseres ikke og utskilles hurtig fra nyrene. Minst 61% av en peroral dose utskilles uforandret innen 24 timer. Hydroklortiazid passerer placentabarrieren, men ikke blod-hjernebarrieren, og utskilles i brystmelk. Teveten Comp 600 mg/12,5 mg Samtidig administrasjon av eprosartan og hydroklortiazid har ingen klinisk signifikant effekt på farmakokinetikken av hver av substansene. Biotilgjengeligheten av eprosartan og hydroklortiazid påvirkes ikke av mat, men absorbsjonen forsinkes. Maksimal plasmakonsentrasjon nås etter 4 timer for eprosartan og 3 timer for hydroklortiazid. 5.3 Prekliniske sikkerhetsdata Mulig toksisitet av kombinasjonen eprosartan/hydroklortiazid etter peroral administrasjon ble undersøkt hos rotter og hunder i studier som varte opptil 3 måneder. Det fremkom ingen funn som ekskluderer bruken av terapeutiske doser i mennesker. Det toksikologiske målorganet var nyrene. Kombinasjonen av eprosartan/hydroklortiazid induserte funksjonelle endringer i nyrene (økt serumurea og serum kreatinin). Videre ble tubulær de- og regenerering i nyrene indusert ved høyere doser hos mus og hunder, sannsynligvis ved endret renal hemodynamikk (redusert renal gjennomstrømning som følge av hypotensjon som fører til tubulær hypoksi med tubulær celledegenerering). Videre induserte kombinasjonen juxtaglomerulær cellehyperplasi, reduksjon i parametere for røde blodlegemer og en reduksjon i hjertevekt. Disse effektene synes å skyldes den farmakologiske effekten av høye doser eprosartan og kan også forekomme med ACE-hemmere. Det er ikke kjent hvilken betydning disse funnene har for bruken av terapeutiske doser av kombinasjonen eprosartan/hydroklortiazid hos mennesker. Funn fra in vitro og in vivo studier med eprosartan og hydroklortiazid både alene og i kombinasjon, avdekket ikke et relevant gentoksisk potensial. Karsinogenstudier er ikke utført med kombinasjonen eprosartan/hydroklortiazid. Karsinogene effekter ble ikke observert hos rotter og mus i doser av eprosartan opp til henholdsvis 600 mg eller 2000 mg/kg daglig i løpet av en 2 års periode. Den omfattende erfaring med hydroklortiazid i mennesker har ikke vist en sammenheng mellom bruken og en økning av neoplasmer. Hos drektige kaniner er det vist at eprosartan forårsaket mortalitet både hos mor og foster ved en dose på 10 mg/kg pr. dag kun under den senere delen av drektigheten. Hydroklortiazid økte ikke maternell eller embryo-føtal toksisitet av eprosartan. Kombinasjonen eprosartan/hydroklortiazid gitt peroralt ved doser opp til 3/1 mg/kg daglig (eprosartan/hydroklortiazid) viste ikke utviklingsmessige toksiske effekter hos moren eller avkommet. 6. FARMASØYTISKE OPPLYSNINGER 6.1 Fortegnelse over hjelpestoffer Tablettkjerne: Laktosemonohydrat. Mikrokrystallinsk cellulose. Pregelatinert maisstivelse. Krysspovidon. 11
12 Magnesiumstearat. Renset vann. Drasjering: Polyvinylalkohol. Talkum. Titandioksid (E171). Makrogol Gult jernoksid (E172). Svart jernoksid (E172). 6.2 Uforlikeligheter Ikke relevant. 6.3 Holdbarhet 3 år. 6.4 Oppbevaringsbetingelser Dette legemidlet krever ingen spesielle oppbevaringsbetingelser. 6.5 Emballasje (type og innhold) Hvit PVC/PCTFE/Aluminiumsfolie blister eller hvit PVC/PVDC/Aluminiumsfolie blister. Blisterpakninger: Prøve (ikke for salg): 28 filmdrasjerte tabletter 56 filmdrasjerte tabletter 98 filmdrasjerte tabletter 280 (10x28) filmdrasjerte tabletter 14 filmdrasjerte tabletter. Ikke alle pakningsstørrelser vil nødvendigvis bli markedsført. 6.6 Spesielle forholdsregler for destruksjon og annen håndtering Ingen spesielle forholdsregler. 7. INNEHAVER AV MARKEDSFØRINGSTILLATELSEN Abbott Norge AS, Postboks 1, 1330 Fornebu, Norge. Tlf MARKEDSFØRINGSTILLATELSESNUMMER (NUMRE)
13 9. DATO FOR FØRSTE MARKEDSFØRINGSTILLATELSE / SISTE FORNYELSE / OPPDATERINGSDATO
Eldre Det er ikke nødvendig å justere dosen ved behandling av eldre pasienter.
 1. LEGEMIDLETS NAVN Glucosamin Orifarm 400 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Glukosamin 400 mg (som glukosaminsulfatkaliumklorid). For fullstendig liste over hjelpestoffer
1. LEGEMIDLETS NAVN Glucosamin Orifarm 400 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Glukosamin 400 mg (som glukosaminsulfatkaliumklorid). For fullstendig liste over hjelpestoffer
Eldre Det er ikke nødvendig med dosejustering ved behandling av eldre pasienter.
 1. LEGEMIDLETS NAVN Gluxine 625 mg tablett, filmdrasjert 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder glukosaminsulfatnatriumkloridkompleks, tilsvarende 625 mg glukosamin eller 795
1. LEGEMIDLETS NAVN Gluxine 625 mg tablett, filmdrasjert 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder glukosaminsulfatnatriumkloridkompleks, tilsvarende 625 mg glukosamin eller 795
Tabletten med styrke på 10 mg egner seg ikke til barn med en kroppsvekt under 30 kg.
 1. LEGEMIDLETS NAVN Loratadin Orifarm 10 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 10 mg loratadin. Hjelpestoff med kjent effekt: laktose For fullstendig liste over
1. LEGEMIDLETS NAVN Loratadin Orifarm 10 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 10 mg loratadin. Hjelpestoff med kjent effekt: laktose For fullstendig liste over
Pediatrisk populasjon: Legemidlet bør ikke brukes til barn siden det ikke finnes tilgjengelige sikkerhetsdata.
 1. LEGEMIDLETS NAVN Kaliumklorid Orifarm 750 mg depottabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En depottablett inneholder 750 mg kaliumklorid. For fullstendig liste over hjelpestoffer, se pkt.
1. LEGEMIDLETS NAVN Kaliumklorid Orifarm 750 mg depottabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En depottablett inneholder 750 mg kaliumklorid. For fullstendig liste over hjelpestoffer, se pkt.
Hver filmdrasjerte tablett inneholder 120 mg feksofenadinhydroklorid tilsvarende 112 mg feksofenadin.
 1. LEGEMIDLETS NAVN Altifex 120 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder 120 mg feksofenadinhydroklorid tilsvarende 112 mg feksofenadin.
1. LEGEMIDLETS NAVN Altifex 120 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder 120 mg feksofenadinhydroklorid tilsvarende 112 mg feksofenadin.
En filmdrasjert tablett inneholder 1884,60 mg glukosaminsulfat natriumklorid tilsvarende 1500 mg glukosaminsulfat eller 1178 mg glukosamin.
 1. LEGEMIDLETS NAVN Dolenio 1178 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En filmdrasjert tablett inneholder 1884,60 mg glukosaminsulfat natriumklorid tilsvarende 1500 mg glukosaminsulfat
1. LEGEMIDLETS NAVN Dolenio 1178 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En filmdrasjert tablett inneholder 1884,60 mg glukosaminsulfat natriumklorid tilsvarende 1500 mg glukosaminsulfat
Lyngonia anbefales ikke til bruk hos barn og ungdom under 18 år (se pkt. 4.4 Advarsler og forsiktighetsregler ).
 1. LEGEMIDLETS NAVN Lyngonia filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjert tablett inneholder: 361-509 mg ekstrakt (som tørket ekstrakt) fra Arctostaphylos uva-ursi
1. LEGEMIDLETS NAVN Lyngonia filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjert tablett inneholder: 361-509 mg ekstrakt (som tørket ekstrakt) fra Arctostaphylos uva-ursi
Hjelpestoffer med kjent effekt: sorbitol (256 mg/ml), metylparahydroksybenzoat (1 mg/ml) og etanol (40 mg/ml)
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Solvipect comp 2,5 mg/ml + 5 mg/ml mikstur, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 ml mikstur inneholder: Etylmorfinhydroklorid 2,5 mg Guaifenesin 5
PREPARATOMTALE 1. LEGEMIDLETS NAVN Solvipect comp 2,5 mg/ml + 5 mg/ml mikstur, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 ml mikstur inneholder: Etylmorfinhydroklorid 2,5 mg Guaifenesin 5
Én ml inneholder 0,1 mg desmopressinacetat tilsvarende 89 mikrogram desmopressin.
 1. LEGEMIDLETS NAVN Minirin 0,1 mg/ml nesedråper, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Én ml inneholder 0,1 mg desmopressinacetat tilsvarende 89 mikrogram desmopressin. For fullstendig
1. LEGEMIDLETS NAVN Minirin 0,1 mg/ml nesedråper, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Én ml inneholder 0,1 mg desmopressinacetat tilsvarende 89 mikrogram desmopressin. For fullstendig
PREPARATOMTALE 2. KVALITATIV OG KVANTITATIV SAMMENSETNING
 1. LEGEMIDLETS NAVN Mesasal 500 mg stikkpiller PREPARATOMTALE 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Mesalazin 500 mg For fullstendig liste over hjelpestoffer, se pkt. 6.1. 3. LEGEMIDDELFORM Stikkpiller
1. LEGEMIDLETS NAVN Mesasal 500 mg stikkpiller PREPARATOMTALE 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Mesalazin 500 mg For fullstendig liste over hjelpestoffer, se pkt. 6.1. 3. LEGEMIDDELFORM Stikkpiller
Bør bare brukes på gynekologiske- eller fødeavdelinger med nødvendig utrustning. Minprostin skal
 1. LEGEMIDLETS NAVN Minprostin 0,5 mg / 2,5 ml endocervikalgel 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Dinoproston (prostaglandin E2) 0,2 mg/ml For fullstendig liste over hjelpestoffer se pkt. 6.1.
1. LEGEMIDLETS NAVN Minprostin 0,5 mg / 2,5 ml endocervikalgel 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Dinoproston (prostaglandin E2) 0,2 mg/ml For fullstendig liste over hjelpestoffer se pkt. 6.1.
Hver kapsel inneholder glukosaminsulfat-kaliumkloridkompleks, tilsvarende 400 mg glukosamin eller 509 mg glukosaminsulfat.
 1. LEGEMIDLETS NAVN Glucosamin Pharma Nord 400 mg kapsel, hard 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver kapsel inneholder glukosaminsulfat-kaliumkloridkompleks, tilsvarende 400 mg glukosamin eller
1. LEGEMIDLETS NAVN Glucosamin Pharma Nord 400 mg kapsel, hard 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver kapsel inneholder glukosaminsulfat-kaliumkloridkompleks, tilsvarende 400 mg glukosamin eller
Obstipasjon. Forberedelse før røntgenundersøkelse eller tømming av colon før operative inngrep.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Dulcolax 5 mg enterotabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Bisakodyl 5 mg Hjelpestoffer: Laktosemonohydrat Sakkarose 34,9 mg 23,4 mg For fullstendig liste
PREPARATOMTALE 1. LEGEMIDLETS NAVN Dulcolax 5 mg enterotabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Bisakodyl 5 mg Hjelpestoffer: Laktosemonohydrat Sakkarose 34,9 mg 23,4 mg For fullstendig liste
Hver filmdrasjerte tablett inneholder eprosartanmesylat tilsvarende 600 mg eprosartan.
 1. LEGEMIDLETS NAVN Teveten 600 mg, filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder eprosartanmesylat tilsvarende 600 mg eprosartan. For fullstendig
1. LEGEMIDLETS NAVN Teveten 600 mg, filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder eprosartanmesylat tilsvarende 600 mg eprosartan. For fullstendig
1. LEGEMIDLETS NAVN. Addex - Kaliumklorid 1 mmol/ml, konsentrat til infusjonsvæske 2. KVALITATIV OG KVANTITATIV SAMMENSETNING
 1. LEGEMIDLETS NAVN Addex - Kaliumklorid 1 mmol/ml, konsentrat til infusjonsvæske 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Kaliumklorid 74,6 mg/ml, tilsvarende 1 mmol/ml Elektrolyttprofilen til 1 ml
1. LEGEMIDLETS NAVN Addex - Kaliumklorid 1 mmol/ml, konsentrat til infusjonsvæske 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Kaliumklorid 74,6 mg/ml, tilsvarende 1 mmol/ml Elektrolyttprofilen til 1 ml
Èn filmdrasjert tablett inneholder 320 mg valsartan og 25 mg hydroklortiazid.
 1. LEGEMIDLETS NAVN Diovan Comp 80 mg/12,5 mg filmdrasjerte tabletter Diovan Comp 160 mg/12,5 mg filmdrasjerte tabletter Diovan Comp 160 mg/25 mg filmdrasjerte tabletter Diovan Comp 320 mg/12,5 mg filmdrasjerte
1. LEGEMIDLETS NAVN Diovan Comp 80 mg/12,5 mg filmdrasjerte tabletter Diovan Comp 160 mg/12,5 mg filmdrasjerte tabletter Diovan Comp 160 mg/25 mg filmdrasjerte tabletter Diovan Comp 320 mg/12,5 mg filmdrasjerte
PREPARATOMTALE. Hjelpestoff(er) med kjent effekt: Cetylalkohol 1,10 % w/w, stearylalkohol 0,50 % w/w and propylenglykol 2,00 % w/w
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Bettamousse 1mg/g (0,1 %) skum 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 g skum inneholder 1 mg betametason (0,1 %) som valerat Hjelpestoff(er) med kjent effekt: Cetylalkohol
PREPARATOMTALE 1. LEGEMIDLETS NAVN Bettamousse 1mg/g (0,1 %) skum 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 g skum inneholder 1 mg betametason (0,1 %) som valerat Hjelpestoff(er) med kjent effekt: Cetylalkohol
Glukosaminhydroklorid-magnesiumsulfat kompleks (2:1), tilsvarende 400 mg glukosamin og tilsvarende 509 mg glukosaminsulfat.
 1. LEGEMIDLETS NAVN Perigona 400 mg filmdrasjert tablett 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Glukosaminhydroklorid-magnesiumsulfat kompleks (2:1), tilsvarende 400 mg glukosamin og tilsvarende 509
1. LEGEMIDLETS NAVN Perigona 400 mg filmdrasjert tablett 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Glukosaminhydroklorid-magnesiumsulfat kompleks (2:1), tilsvarende 400 mg glukosamin og tilsvarende 509
Hver filmdrasjert tablett inneholder 100 mg losartankalium og 12,5 mg hydroklortiazid.
 1. LEGEMIDLETS NAVN Losatrix Comp 100 mg/12,5 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjert tablett inneholder 100 mg losartankalium og 12,5 mg hydroklortiazid.
1. LEGEMIDLETS NAVN Losatrix Comp 100 mg/12,5 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjert tablett inneholder 100 mg losartankalium og 12,5 mg hydroklortiazid.
Hypertensjon. Ødemer i forbindelse med hjertesvikt. Ødemer av annen årsak. Morbus Ménière.
 1. LEGEMIDLETS NAVN ESIDREX 25 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hydroklortiazid 25 mg. For fullstendig liste over hjelpestoffer se pkt. 6.1 3. LEGEMIDDELFORM Tablett Hvite tabletter,
1. LEGEMIDLETS NAVN ESIDREX 25 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hydroklortiazid 25 mg. For fullstendig liste over hjelpestoffer se pkt. 6.1 3. LEGEMIDDELFORM Tablett Hvite tabletter,
Obstipasjon. Forberedelse før røntgenundersøkelse eller tømming av colon før operative inngrep.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Dulcolax 10 mg stikkpiller 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Bisakodyl 10 mg For fullstendig liste over hjelpestoffer se pkt. 6.1 3. LEGEMIDDELFORM Stikkpille
PREPARATOMTALE 1. LEGEMIDLETS NAVN Dulcolax 10 mg stikkpiller 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Bisakodyl 10 mg For fullstendig liste over hjelpestoffer se pkt. 6.1 3. LEGEMIDDELFORM Stikkpille
PREPARATOMTALE. 1 tablett inneholder 750 mg glukosaminhydroklorid tilsvarende 625 mg glukosamin.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Samin 625 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 tablett inneholder 750 mg glukosaminhydroklorid tilsvarende 625 mg glukosamin. For hjelpestoffer,
PREPARATOMTALE 1. LEGEMIDLETS NAVN Samin 625 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 tablett inneholder 750 mg glukosaminhydroklorid tilsvarende 625 mg glukosamin. For hjelpestoffer,
4. KLINISKE OPPLYSNINGER 4.1 Indikasjoner Urinveisinfeksjoner forårsaket av mecillinamfølsomme mikroorganismer
 1. LEGEMIDLETS NAVN Selexid 1 g pulver til injeksjonsvæske, oppløsning. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hvert hetteglass inneholder: Mecillinam 1 gram For fullstendig liste over hjelpestoffer,
1. LEGEMIDLETS NAVN Selexid 1 g pulver til injeksjonsvæske, oppløsning. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hvert hetteglass inneholder: Mecillinam 1 gram For fullstendig liste over hjelpestoffer,
PREPARATOMTALE 1. LEGEMIDLETS NAVN
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Irbesartan/Hydroklortiazid Actavis 150 mg/12,5 mg filmdrasjerte tabletter. Irbesartan/Hydroklortiazid Actavis 300 mg/12,5 mg filmdrasjerte tabletter. Irbesartan/Hydroklortiazid
PREPARATOMTALE 1. LEGEMIDLETS NAVN Irbesartan/Hydroklortiazid Actavis 150 mg/12,5 mg filmdrasjerte tabletter. Irbesartan/Hydroklortiazid Actavis 300 mg/12,5 mg filmdrasjerte tabletter. Irbesartan/Hydroklortiazid
Til voksne over 18 år: Syreoverskudd, ulcus pepticum, pyrose, kardialgi og dyspepsi.
 1. LEGEMIDLETS NAVN Titralac 50 mg, tablett 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En tablett inneholder 50 mg kalsiumkarbonat Hjelpestoffer med kjent effekt: Én tablett inneholder hvetestivelse (70
1. LEGEMIDLETS NAVN Titralac 50 mg, tablett 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En tablett inneholder 50 mg kalsiumkarbonat Hjelpestoffer med kjent effekt: Én tablett inneholder hvetestivelse (70
Virkestoff: Hver kapsel inneholder: Balsalaziddinatrium 750mg, tilsvarende 262,5mg mesalazin. INN: Balsalazid For hjelpestoffer se pkt. 6.1.
 1. LEGEMIDLETS NAVN COLAZID, 750 mg, kapsler 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoff: Hver kapsel inneholder: Balsalaziddinatrium 750mg, tilsvarende 262,5mg mesalazin. INN: Balsalazid For
1. LEGEMIDLETS NAVN COLAZID, 750 mg, kapsler 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoff: Hver kapsel inneholder: Balsalaziddinatrium 750mg, tilsvarende 262,5mg mesalazin. INN: Balsalazid For
Hvit eller nesten hvite, 8 mm runde flate tabletter med bokstaven L på den ene siden og med delestrek på den andre siden av tabletten.
 1. LEGEMIDLETS NAVN Loratadin Actavis 10 mg tabletter. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 10 mg loratadin. Hver tablett inneholder 75 mg laktosemonohydrat. For fullstendig
1. LEGEMIDLETS NAVN Loratadin Actavis 10 mg tabletter. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 10 mg loratadin. Hver tablett inneholder 75 mg laktosemonohydrat. For fullstendig
Én ml inneholder 1 mg dokusatnatrium (natriumdioktylsulfosuksinat) og 250 mg sorbitol (E 420).
 Dette preparatet har markedsføringstillatelse for både human og veterinær bruk. Preparatomtale for veterinær bruk finnes nederst i dokumentet. 1. LEGEMIDLETS NAVN Klyx (1 mg/ml) / (250 mg/ml) rektalvæske,
Dette preparatet har markedsføringstillatelse for både human og veterinær bruk. Preparatomtale for veterinær bruk finnes nederst i dokumentet. 1. LEGEMIDLETS NAVN Klyx (1 mg/ml) / (250 mg/ml) rektalvæske,
PREPARATOMTALE. Hver filmdrasjerte tablett inneholder 320 mg valsartan og 25 mg hydroklortiazid.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Valsartan/Hydrochlorothiazide Teva 320 mg/12,5 mg tabletter, filmdrasjerte Valsartan/Hydrochlorothiazide Teva 320 mg/25 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV
PREPARATOMTALE 1. LEGEMIDLETS NAVN Valsartan/Hydrochlorothiazide Teva 320 mg/12,5 mg tabletter, filmdrasjerte Valsartan/Hydrochlorothiazide Teva 320 mg/25 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV
En gul, filmdrasjert, oval, bikonveks tablett med skråkant, merket med M på den ene siden av
 1. LEGEMIDLETS NAVN Asolzid 50 mg/12,5 mg filmdrasjerte tabletter Asolzid 100 mg/12,5 mg filmdrasjerte tabletter Asolzid 100 mg/25 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING
1. LEGEMIDLETS NAVN Asolzid 50 mg/12,5 mg filmdrasjerte tabletter Asolzid 100 mg/12,5 mg filmdrasjerte tabletter Asolzid 100 mg/25 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING
Natriumbehov [mmol] = (ønsket nåværende serumnatrium) total kroppsvæske [liter]
![Natriumbehov [mmol] = (ønsket nåværende serumnatrium) total kroppsvæske [liter] Natriumbehov [mmol] = (ønsket nåværende serumnatrium) total kroppsvæske [liter]](/thumbs/39/19534687.jpg) PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Natriumklorid B. Braun 1 mmol/ml konsentrat til infusjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 ml konsentrat til infusjonsvæske inneholder:
PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Natriumklorid B. Braun 1 mmol/ml konsentrat til infusjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 ml konsentrat til infusjonsvæske inneholder:
Valsartan/Hydrochlorthiazid Actavis 320 mg/12,5 mg filmdrasjerte tabletter Valsartan/Hydrochlorthiazid Actavis 320 mg/25 mg filmdrasjerte tabletter
 1. LEGEMIDLETS NAVN Valsartan/Hydrochlorthiazid Actavis 320 mg/12,5 mg filmdrasjerte tabletter Valsartan/Hydrochlorthiazid Actavis 320 mg/25 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING
1. LEGEMIDLETS NAVN Valsartan/Hydrochlorthiazid Actavis 320 mg/12,5 mg filmdrasjerte tabletter Valsartan/Hydrochlorthiazid Actavis 320 mg/25 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING
Antidot etter høydose metotreksat. I kombinasjon med fluorouracil til behandling av colorektalcancer i avansert stadium.
 1. LEGEMIDLETS NAVN Calciumfolinate Teva 15 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Kalsiumfolinat tilsvarende 15 mg folinsyre For fullstendig liste over hjelpestoffer se pkt. 6.1 3. LEGEMIDDELFORM
1. LEGEMIDLETS NAVN Calciumfolinate Teva 15 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Kalsiumfolinat tilsvarende 15 mg folinsyre For fullstendig liste over hjelpestoffer se pkt. 6.1 3. LEGEMIDDELFORM
VEDLEGG I PREPARATOMTALE
 VEDLEGG I PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Rasilez HCT 150 mg/12,5 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder 150 mg aliskiren (som
VEDLEGG I PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Rasilez HCT 150 mg/12,5 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder 150 mg aliskiren (som
1. LEGEMIDLETS NAVN. Mørk grå-fiolett, bikonveks, kapsel formet, filmdrasjert tablett med delestrek (diameter ca. 8,1 x 17,7 mm).
 1. LEGEMIDLETS NAVN Valsartan ratiopharm 320 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En filmdrasjert tablett inneholder 320 mg valsartan. For fullstendig liste over hjelpestoffer
1. LEGEMIDLETS NAVN Valsartan ratiopharm 320 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En filmdrasjert tablett inneholder 320 mg valsartan. For fullstendig liste over hjelpestoffer
Olmetec Comp 20 mg/25 mg tablett, filmdrasjert: Hver filmdrasjerte tablett inneholder 20 mg olmesartanmedoksomil og 25 mg hydroklortiazid.
 1. LEGEMIDLETS NAVN Olmetec Comp 20 mg/12,5 mg tabletter, filmdrasjerte Olmetec Comp 20 mg/25 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Olmetec Comp 20 mg/12,5 mg tablett,
1. LEGEMIDLETS NAVN Olmetec Comp 20 mg/12,5 mg tabletter, filmdrasjerte Olmetec Comp 20 mg/25 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Olmetec Comp 20 mg/12,5 mg tablett,
Valsartan/Hydrochlorothiazide Sandoz 160 mg / 25 mg filmdrasjerte tabletter
 1. LEGEMIDLETS NAVN Valsartan/Hydrochlorothiazide Sandoz 80 mg / 12,5 mg filmdrasjerte tabletter Valsartan/Hydrochlorothiazide Sandoz 160 mg / 12,5 mg filmdrasjerte tabletter Valsartan/Hydrochlorothiazide
1. LEGEMIDLETS NAVN Valsartan/Hydrochlorothiazide Sandoz 80 mg / 12,5 mg filmdrasjerte tabletter Valsartan/Hydrochlorothiazide Sandoz 160 mg / 12,5 mg filmdrasjerte tabletter Valsartan/Hydrochlorothiazide
Dette preparatet har markedsføringstillatelse for både human og veterinær bruk. Preparatomtale for veterinær bruk finnes nederst i dokumentet.
 Dette preparatet har markedsføringstillatelse for både human og veterinær bruk. Preparatomtale for veterinær bruk finnes nederst i dokumentet. 1. LEGEMIDLETS NAVN Pyrisept 2. KVALITATIV OG KVANTITATIV
Dette preparatet har markedsføringstillatelse for både human og veterinær bruk. Preparatomtale for veterinær bruk finnes nederst i dokumentet. 1. LEGEMIDLETS NAVN Pyrisept 2. KVALITATIV OG KVANTITATIV
Brannskader: Brannsåret skal først renses, og deretter påføres kremen hele det affiserte området i et 3-5 mm tykt lag.
 1. LEGEMIDLETS NAVN Flamazine 10 mg/g krem 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Sølvsulfadiazin 10 mg/g (1 %) For fullstendig liste over hjelpestoffer se pkt. 6.1. 3. LEGEMIDDELFORM Krem 4. KLINISKE
1. LEGEMIDLETS NAVN Flamazine 10 mg/g krem 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Sølvsulfadiazin 10 mg/g (1 %) For fullstendig liste over hjelpestoffer se pkt. 6.1. 3. LEGEMIDDELFORM Krem 4. KLINISKE
1. LEGEMIDLETS NAVN. Vallergan 10 mg filmdrasjert tablett 2. KVALITATIV OG KVANTITATIV SAMMENSETNING. Alimemazintartrat 10 mg
 1. LEGEMIDLETS NAVN Vallergan 10 mg filmdrasjert tablett 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Alimemazintartrat 10 mg For fullstendig liste over hjelpestoffer se pkt 6.1. 3. LEGEMIDDELFORM Tabletter,
1. LEGEMIDLETS NAVN Vallergan 10 mg filmdrasjert tablett 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Alimemazintartrat 10 mg For fullstendig liste over hjelpestoffer se pkt 6.1. 3. LEGEMIDDELFORM Tabletter,
Eldre Det er ikke nødvendig å redusere dosen ved behandling av eldre pasienter.
 1. LEGEMIDLETS NAVN Gluxine 400 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder glukosaminsulfat-natriumkloridkompleks, tilsvarende 400 mg glukosamin eller
1. LEGEMIDLETS NAVN Gluxine 400 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder glukosaminsulfat-natriumkloridkompleks, tilsvarende 400 mg glukosamin eller
VEDLEGG I PREPARATOMTALE
 VEDLEGG I PREPARATOMTALE 1 1. LEGEMIDLETS NAVN CoAprovel 150 mg/12,5 mg tabletter. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 150 mg irbesartan og 12,5 mg hydroklortiazid. Hjelpestoff
VEDLEGG I PREPARATOMTALE 1 1. LEGEMIDLETS NAVN CoAprovel 150 mg/12,5 mg tabletter. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 150 mg irbesartan og 12,5 mg hydroklortiazid. Hjelpestoff
1. LEGEMIDLETS NAVN. Hjelpestoff(er) med kjent effekt: Isomalt 1830,0 mg (E953) og 457,6 mg flytende maltitol (E965).
 1. LEGEMIDLETS NAVN Solvivo 0,6 mg/1,2 mg sugetablett med mintsmak Solvivo 0,6 mg/1,2 mg sugetablett med honning- og sitronsmak 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver sugetablett inneholder: amylmetakresol
1. LEGEMIDLETS NAVN Solvivo 0,6 mg/1,2 mg sugetablett med mintsmak Solvivo 0,6 mg/1,2 mg sugetablett med honning- og sitronsmak 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver sugetablett inneholder: amylmetakresol
Overfølsomhet overfor virkestoffet eller overfor ett eller flere av hjelpestoffene listet opp i pkt. 6.1. Hyperkalsemi.
 1. LEGEMIDLETS NAVN Etalpha 0,25 mikrogram kapsel, myk Ethalpa 0, 5 mikrogram kapsel, myk Ethalpa 1 mikrogram kapsel, myk 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 kapsel inneholder: Alfakalsidol 0,25
1. LEGEMIDLETS NAVN Etalpha 0,25 mikrogram kapsel, myk Ethalpa 0, 5 mikrogram kapsel, myk Ethalpa 1 mikrogram kapsel, myk 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 kapsel inneholder: Alfakalsidol 0,25
PREPARATOMTALE. Atacand Plus Mite 8 mg/12,5 mg tabletter er hvite, ovale, bikonvekse med delestrek på begge sider og
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Atacand Plus Mite 8 mg/12,5 mg tabletter Atacand Plus 16 mg/12,5 mg tabletter Atacand Plus 32 mg/12,5 mg tabletter Atacand Plus 32 mg/25 mg tabletter 2. KVALITATIV OG
PREPARATOMTALE 1. LEGEMIDLETS NAVN Atacand Plus Mite 8 mg/12,5 mg tabletter Atacand Plus 16 mg/12,5 mg tabletter Atacand Plus 32 mg/12,5 mg tabletter Atacand Plus 32 mg/25 mg tabletter 2. KVALITATIV OG
Reisesyke, brekninger, svimmelhet, medikamentelt fremkalt kvalme og kvalme ved strålebehandling. Menieres syndrom.
 1. LEGEMIDLETS NAVN Marzine 50 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Syklizinhydroklorid 50 mg For fullstendig liste over hjelpestoffer se pkt. 6.1. 3. LEGEMIDDELFORM Tabletter 4. KLINISKE
1. LEGEMIDLETS NAVN Marzine 50 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Syklizinhydroklorid 50 mg For fullstendig liste over hjelpestoffer se pkt. 6.1. 3. LEGEMIDDELFORM Tabletter 4. KLINISKE
4.1 Indikasjoner Sporelementtilskudd for å dekke basale til moderat økte behov ved parenteral ernæring.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Addaven, konsentrat til infusjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Addaven inneholder: 1 ml 1 ampulle (10 ml) Kromklorid (6H2O) 5,33 mikrog
PREPARATOMTALE 1. LEGEMIDLETS NAVN Addaven, konsentrat til infusjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Addaven inneholder: 1 ml 1 ampulle (10 ml) Kromklorid (6H2O) 5,33 mikrog
PREPARATOMTALE. Duphalac mikstur, oppløsning med fruktsmak inneholder 667 mg laktulose pr. 1 ml. Én 15 ml dosepose inneholder 10 g laktulose.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Duphalac 667 mg/ml mikstur, oppløsning med fruktsmak 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Duphalac mikstur, oppløsning med fruktsmak inneholder 667 mg laktulose
PREPARATOMTALE 1. LEGEMIDLETS NAVN Duphalac 667 mg/ml mikstur, oppløsning med fruktsmak 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Duphalac mikstur, oppløsning med fruktsmak inneholder 667 mg laktulose
Hver filmdrasjerte tablett inneholder eprosartanmesylat tilsvarende 600 mg eprosartan og 12,5 mg hydroklortiazid.
 1. LEGEMIDLETS NAVN Teveten Comp 600 mg/12,5 mg, filmdrasjerte tabletter. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder eprosartanmesylat tilsvarende 600 mg eprosartan
1. LEGEMIDLETS NAVN Teveten Comp 600 mg/12,5 mg, filmdrasjerte tabletter. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder eprosartanmesylat tilsvarende 600 mg eprosartan
VEDLEGG I PREPARATOMTALE
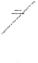 VEDLEGG I PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Rasitrio 150 mg/5 mg/12,5 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder 150 mg aliskiren (som
VEDLEGG I PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Rasitrio 150 mg/5 mg/12,5 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder 150 mg aliskiren (som
Hver tablett inneholder natriumalginat 250 mg, natriumhydrogenkarbonat 133,5 mg og kalsiumkarbonat 80 mg.
 PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Galieve tyggetabletter med peppermyntesmak 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder natriumalginat 250 mg, natriumhydrogenkarbonat 133,5 mg
PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Galieve tyggetabletter med peppermyntesmak 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder natriumalginat 250 mg, natriumhydrogenkarbonat 133,5 mg
PREPARATOMTALE (SPC) 1 tablett inneholder: Fenoksymetylpenicillinkalium 400 mg resp. 650 mg. For fullstendig liste over hjelpestoffer se pkt. 6.1.
 PREPARATOMTALE (SPC) 1. LEGEMIDLETS NAVN Weifapenin 400 mg og 650 mg tabletter. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 tablett inneholder: Fenoksymetylpenicillinkalium 400 mg resp. 650 mg. For fullstendig
PREPARATOMTALE (SPC) 1. LEGEMIDLETS NAVN Weifapenin 400 mg og 650 mg tabletter. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 tablett inneholder: Fenoksymetylpenicillinkalium 400 mg resp. 650 mg. For fullstendig
Orale og intestinale Candida-infeksjoner. Som tilleggsbehandling til andre lokalt appliserte legemidler med nystatin som profylakse mot re-infeksjon.
 1. LEGEMIDLETS NAVN Nystimex 100 000 IE/ml mikstur, suspensjon 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 ml inneholder 100 000 IE nystatin. Hjelpestoffer: Metylparahydroksybenzoat 1 mg Natrium 1,2 mg/ml,
1. LEGEMIDLETS NAVN Nystimex 100 000 IE/ml mikstur, suspensjon 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 ml inneholder 100 000 IE nystatin. Hjelpestoffer: Metylparahydroksybenzoat 1 mg Natrium 1,2 mg/ml,
PREPARATOMTALE. 4.1 Indikasjoner Forebygging av urinveistoksisitet i forbindelse med administrering av oxazafosforiner (cyklofosfamid, ifosfamid).
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Uromitexan 400 mg og 600 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Mesna 400 mg/tablett og 600 mg/tablett For hjelpestoffer, se punkt 6.1. 3. LEGEMIDDELFORM
PREPARATOMTALE 1. LEGEMIDLETS NAVN Uromitexan 400 mg og 600 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Mesna 400 mg/tablett og 600 mg/tablett For hjelpestoffer, se punkt 6.1. 3. LEGEMIDDELFORM
PREPARATOMTALE. Loratadin er indisert for symptomatisk behandling av allergisk rhinitt og kronisk idiopatisk urtikaria.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Loratadin Hexal, 10 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 10 mg loratadin. Hjelpestoff(er) med kjent effekt: En tablett inneholder
PREPARATOMTALE 1. LEGEMIDLETS NAVN Loratadin Hexal, 10 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 10 mg loratadin. Hjelpestoff(er) med kjent effekt: En tablett inneholder
Hver filmdrasjerte tablett inneholder 100 mg losartankalium tilsvarende 91,52 mg losartan og 12,5 mg hydroklortiazid.
 1. LEGEMIDLETS NAVN /Hydrochlorothiazide Krka 100 mg/12,5 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder 100 mg losartankalium tilsvarende
1. LEGEMIDLETS NAVN /Hydrochlorothiazide Krka 100 mg/12,5 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder 100 mg losartankalium tilsvarende
Virkestoff: Benazepril 2,3 mg (tilsvarende 2,5 mg benazeprilhydroklorid)
 1. VETERINÆRPREPARATETS NAVN Benakor vet. 2,5 mg, filmdrasjerte tabletter til katt 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Én tablett inneholder: Virkestoff: Benazepril 2,3 mg (tilsvarende 2,5 mg benazeprilhydroklorid)
1. VETERINÆRPREPARATETS NAVN Benakor vet. 2,5 mg, filmdrasjerte tabletter til katt 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Én tablett inneholder: Virkestoff: Benazepril 2,3 mg (tilsvarende 2,5 mg benazeprilhydroklorid)
Vedlegg II. Endringer til relevante avsnitt i preparatomtale og pakningsvedlegg
 Vedlegg II Endringer til relevante avsnitt i preparatomtale og pakningsvedlegg 1 For preparater som inneholder angiotensinkonverterende enyzymhemmerne (ACEhemmere) benazepril, kaptopril, cilazapril, delapril,
Vedlegg II Endringer til relevante avsnitt i preparatomtale og pakningsvedlegg 1 For preparater som inneholder angiotensinkonverterende enyzymhemmerne (ACEhemmere) benazepril, kaptopril, cilazapril, delapril,
PREPARATOMTALE. Page 1
 PREPARATOMTALE Page 1 1. LEGEMIDLETS NAVN Oftagel 2,5 mg/g øyegel 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Karbomer 974P 2,5 mg/g Hjelpestoff(er) med kjent virkning: benzalkoniumklorid (0,06 mg/g) For
PREPARATOMTALE Page 1 1. LEGEMIDLETS NAVN Oftagel 2,5 mg/g øyegel 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Karbomer 974P 2,5 mg/g Hjelpestoff(er) med kjent virkning: benzalkoniumklorid (0,06 mg/g) For
PREPARATOMTALE. Hvit, rund tablett, uten filmdrasjering, preget med ucb på én side og delestrek på den andre siden.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Postafen 25 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett med Postafen inneholder 25 mg meklozinhydroklorid. For fullstendig liste over hjelpestoffer
PREPARATOMTALE 1. LEGEMIDLETS NAVN Postafen 25 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett med Postafen inneholder 25 mg meklozinhydroklorid. For fullstendig liste over hjelpestoffer
2. KVALITATIV OG KVANTITATIV SAMMENSETNING
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Keflex 500 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Cefaleksinmonohydrat, tilsvarende 500 mg cefaleksin pr. tablett. For hjelpestoffer, se pkt. 6.1. 3.
PREPARATOMTALE 1. LEGEMIDLETS NAVN Keflex 500 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Cefaleksinmonohydrat, tilsvarende 500 mg cefaleksin pr. tablett. For hjelpestoffer, se pkt. 6.1. 3.
1. LEGEMIDLETS NAVN. Polaramin, 2 mg tablett 2. KVALITATIV OG KVANTITATIV SAMMENSETNING. Deksklorfeniraminmaleat 2 mg
 PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Polaramin, 2 mg tablett 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Deksklorfeniraminmaleat 2 mg For fullstendig liste over hjelpestoffer, se pkt. 6.1. 3. LEGEMIDDELFORM
PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Polaramin, 2 mg tablett 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Deksklorfeniraminmaleat 2 mg For fullstendig liste over hjelpestoffer, se pkt. 6.1. 3. LEGEMIDDELFORM
Hver filmdrasjerte tablett inneholder 100 mg losartankalium, ekvivalent med 91,52 mg losartan, og 25 mg hydroklortiazid.
 1. LEGEMIDLETS NAVN /Hydrochlorothiazide Krka 100 mg/25 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder 100 mg losartankalium, ekvivalent med
1. LEGEMIDLETS NAVN /Hydrochlorothiazide Krka 100 mg/25 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder 100 mg losartankalium, ekvivalent med
Citalopram bør gis som en enkelt daglig dose på 20 mg. Avhengig av individuell respons kan dosen økes til maksimalt 40 mg daglig.
 Citalopram og risiko for QT-forlengelse PREPARATOMTALE citalopram 10, 20, 30 og 40 mg tabletter 4.2. Dosering og administrasjonsmåte Depresjon Citalopram bør gis som en enkelt daglig dose på 20 mg. Avhengig
Citalopram og risiko for QT-forlengelse PREPARATOMTALE citalopram 10, 20, 30 og 40 mg tabletter 4.2. Dosering og administrasjonsmåte Depresjon Citalopram bør gis som en enkelt daglig dose på 20 mg. Avhengig
1 ml inneholder: Betametasondipropionat tilsvarende betametason 0,5 mg og salisylsyre 20 mg.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Diprosalic liniment, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 ml inneholder: Betametasondipropionat tilsvarende betametason 0,5 mg og salisylsyre 20 mg.
PREPARATOMTALE 1. LEGEMIDLETS NAVN Diprosalic liniment, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 ml inneholder: Betametasondipropionat tilsvarende betametason 0,5 mg og salisylsyre 20 mg.
Hver tablett inneholder 10 mg lisinopril (som dihydrat) og 12,5 mg hydroklortiazid.
 1. LEGEMIDLETS NAVN Lisinopril/Hydroklortiazid Mylan 10 mg/12,5 mg tabletter Lisinopril/Hydroklortiazid Mylan 20 mg/12,5 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Lisinopril/Hydroklortiazid
1. LEGEMIDLETS NAVN Lisinopril/Hydroklortiazid Mylan 10 mg/12,5 mg tabletter Lisinopril/Hydroklortiazid Mylan 20 mg/12,5 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Lisinopril/Hydroklortiazid
Candanzid 8 mg/12,5 mg: hver tablett inneholder 77 mg laktosemonohydrat. Candanzid 16 mg/12,5 mg: hver tablett inneholder 69 mg laktosemonohydrat.
 1. LEGEMIDLETS NAVN Candanzid 8 mg/12,5 mg tabletter Candanzid 16 mg/12,5 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Én tablett inneholder 8 mg kandesartalcileksetil og 12,5 mg hydroklortiazid.
1. LEGEMIDLETS NAVN Candanzid 8 mg/12,5 mg tabletter Candanzid 16 mg/12,5 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Én tablett inneholder 8 mg kandesartalcileksetil og 12,5 mg hydroklortiazid.
Losartan/Hydrochlorothiazide Bluefish 50 mg/12,5 mg tablett, filmdrasjert Losartan/Hydrochlorothiazide Bluefish 100 mg/25 mg tablett, filmdrasjert
 1. LEGEMIDLETS NAVN /Hydrochlorothiazide Bluefish 50 mg/12,5 mg tablett, filmdrasjert /Hydrochlorothiazide Bluefish 100 mg/25 mg tablett, filmdrasjert 2. KVALITATIV OG KVANTITATIV SAMMENSETNING /Hydrochlorothiazide
1. LEGEMIDLETS NAVN /Hydrochlorothiazide Bluefish 50 mg/12,5 mg tablett, filmdrasjert /Hydrochlorothiazide Bluefish 100 mg/25 mg tablett, filmdrasjert 2. KVALITATIV OG KVANTITATIV SAMMENSETNING /Hydrochlorothiazide
Tablett, filmdrasjert Hvit, rund, bikonveks, filmdrasjert tablett. Merket med A på den ene siden og delestrek på den andre.
 1. LEGEMIDLETS NAVN Cetirizin Bluefish 10 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En filmdrasjert tablett inneholder 10 mg cetirizindihydroklorid. For fullstendig liste over
1. LEGEMIDLETS NAVN Cetirizin Bluefish 10 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En filmdrasjert tablett inneholder 10 mg cetirizindihydroklorid. For fullstendig liste over
Hypertensjon ½-2 tabletter gitt som en eller fordelt på flere doser. Bruk lavest mulige dose som er nødvendig for å oppnå ønsket respons.
 1. LEGEMIDLETS NAVN Moduretic Mite 25 mg/2,5 mg, tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hydroklortiazid 25 mg og amiloridhydroklorid 2,5 mg. For fullstendig liste over hjelpestoffer se pkt.
1. LEGEMIDLETS NAVN Moduretic Mite 25 mg/2,5 mg, tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hydroklortiazid 25 mg og amiloridhydroklorid 2,5 mg. For fullstendig liste over hjelpestoffer se pkt.
PREPARATOMTALE. Den første dosen skal tas om kvelden (ved sengetid). Depottabletten skal svelges hel.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Xatral 5 mg depottabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Alfuzosinhydroklorid 5 mg For fullstendig liste over hjelpestoffer, se pkt. 6.1. 3. LEGEMIDDELFORM
PREPARATOMTALE 1. LEGEMIDLETS NAVN Xatral 5 mg depottabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Alfuzosinhydroklorid 5 mg For fullstendig liste over hjelpestoffer, se pkt. 6.1. 3. LEGEMIDDELFORM
Hver filmdrasjert tablett inneholder 300 mg irbesartan og 25 mg hydroklortiazid.
 1. LEGEMIDLETS NAVN CoAprovel 300 mg/25 mg filmdrasjerte tabletter. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjert tablett inneholder 300 mg irbesartan og 25 mg hydroklortiazid. Hjelpestoff:
1. LEGEMIDLETS NAVN CoAprovel 300 mg/25 mg filmdrasjerte tabletter. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjert tablett inneholder 300 mg irbesartan og 25 mg hydroklortiazid. Hjelpestoff:
Særlige forholdsregler for personer som gir veterinærpreparatet til dyr
 PREPARATOMTALE 1. VETERINÆRLEGEMIDLETS NAVN Fortekor vet. 20 mg, tabletter til hund 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoff: Benazeprilhydroklorid 20 mg Se punkt 6.1 for komplett liste over
PREPARATOMTALE 1. VETERINÆRLEGEMIDLETS NAVN Fortekor vet. 20 mg, tabletter til hund 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoff: Benazeprilhydroklorid 20 mg Se punkt 6.1 for komplett liste over
Hjelpestoff med kjent effekt: 8 mg/12,5 mg 16 mg/12,5 mg 32 mg/12,5 mg 32 mg/25 mg Laktose 73,06 65,46 142,79 130,91
 1. LEGEMIDLETS NAVN Candesartan/Hydrochlorothiazide Krka 8 mg/12,5 mg tabletter Candesartan/Hydrochlorothiazide Krka 16 mg/12,5 mg tabletter Candesartan/Hydrochlorothiazide Krka 32 mg/12,5 mg tabletter
1. LEGEMIDLETS NAVN Candesartan/Hydrochlorothiazide Krka 8 mg/12,5 mg tabletter Candesartan/Hydrochlorothiazide Krka 16 mg/12,5 mg tabletter Candesartan/Hydrochlorothiazide Krka 32 mg/12,5 mg tabletter
Pediatrisk populasjon Man har ingen erfaring med bruk av Silkis på barn (se 4.4. Spesielle advarsler og forsiktighetsregler for bruken).
 1. LEGEMIDLETS NAVN Silkis 3 mikrogram per g salve 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Ett gram salve inneholder 3 mikrogram kalsitriol (INN) For fullstendig liste over hjelpestoffer se pkt. 6.1.
1. LEGEMIDLETS NAVN Silkis 3 mikrogram per g salve 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Ett gram salve inneholder 3 mikrogram kalsitriol (INN) For fullstendig liste over hjelpestoffer se pkt. 6.1.
Hver tablett inneholder 10 mg loratadin. Hjelpestoff med kjent effekt: Hver Clarityn 10 mg tablett inneholder 71,3 mg laktosemonohydrat.
 1. LEGEMIDLETS NAVN Clarityn 10 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 10 mg loratadin. Hjelpestoff med kjent effekt: Hver Clarityn 10 mg tablett inneholder 71,3
1. LEGEMIDLETS NAVN Clarityn 10 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 10 mg loratadin. Hjelpestoff med kjent effekt: Hver Clarityn 10 mg tablett inneholder 71,3
Hver tablett inneholder 150 mg irbesartan og 12,5 mg hydroklortiazid.
 1. LEGEMIDLETS NAVN CoAprovel 150 mg/12,5 mg tabletter. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 150 mg irbesartan og 12,5 mg hydroklortiazid. Hjelpestoff: Hver filmdrasjert tablett
1. LEGEMIDLETS NAVN CoAprovel 150 mg/12,5 mg tabletter. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 150 mg irbesartan og 12,5 mg hydroklortiazid. Hjelpestoff: Hver filmdrasjert tablett
1. LEGEMIDLETS NAVN. Irbesartan Amneal 75 mg tabletter. Irbesartan Amneal 150 mg tablett. Irbesartan Amneal 300 mg tablett
 1. LEGEMIDLETS NAVN Irbesartan Amneal 75 mg tabletter Irbesartan Amneal 150 mg tabletter Irbesartan Amneal 300 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 75 mg irbesartan.
1. LEGEMIDLETS NAVN Irbesartan Amneal 75 mg tabletter Irbesartan Amneal 150 mg tabletter Irbesartan Amneal 300 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 75 mg irbesartan.
Behandlingsområdet vaskes med såpe og vann og deretter tørkes med håndkle e.l. før påføringen.
 1. LEGEMIDLETS NAVN Wartec 5 mg/ml liniment, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Podofyllotoksin 5 mg/ml For fullstendig liste over hjelpestoffer, se pkt. 6.1. 3. LEGEMIDDELFORM Liniment,
1. LEGEMIDLETS NAVN Wartec 5 mg/ml liniment, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Podofyllotoksin 5 mg/ml For fullstendig liste over hjelpestoffer, se pkt. 6.1. 3. LEGEMIDDELFORM Liniment,
PREPARATOMTALE. 50 mg/12,5 mg: Hver tablett inneholder 50 mg losartankalium og 12,5 mg hydroklortiazid.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN /Hydrochlorothiazide Teva 50 mg/12,5 mg tabletter, filmdrasjerte /Hydrochlorothiazide Teva 100 mg/25 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING
PREPARATOMTALE 1. LEGEMIDLETS NAVN /Hydrochlorothiazide Teva 50 mg/12,5 mg tabletter, filmdrasjerte /Hydrochlorothiazide Teva 100 mg/25 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING
PREPARATOMTALE. Effekt og sikkerhet hos barn under 12 år er ikke undersøkt. Erfaring med langtidsbehandling er begrenset.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Kestine 10 mg tabletter, filmdrasjerte Kestine 20 mg tabletter,filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Ebastin 10 mg og 20 mg Hjelpestoff med kjent effekt:
PREPARATOMTALE 1. LEGEMIDLETS NAVN Kestine 10 mg tabletter, filmdrasjerte Kestine 20 mg tabletter,filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Ebastin 10 mg og 20 mg Hjelpestoff med kjent effekt:
Pakningsvedlegg: Informasjon til brukeren. Teveten Comp 600 mg/12,5 mg filmdrasjerte tabletter. eprosartan og hydroklortiazid
 Pakningsvedlegg: Informasjon til brukeren Teveten Comp 600 mg/12,5 mg filmdrasjerte tabletter eprosartan og hydroklortiazid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
Pakningsvedlegg: Informasjon til brukeren Teveten Comp 600 mg/12,5 mg filmdrasjerte tabletter eprosartan og hydroklortiazid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
Dosering Doseringen justeres individuelt på grunnlag av pasientens alder, kroppsvekt og kliniske tilstand.
 PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Kalium-Natrium-Glucose Braun infusjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1000 ml infusjonsvæske inneholder: Virkestoffer: Glukose (i form
PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Kalium-Natrium-Glucose Braun infusjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1000 ml infusjonsvæske inneholder: Virkestoffer: Glukose (i form
Forskrivningsregel: For 500 mg tabletter skal behandlingen være instituert av sykehus eller spesialist i indremedisin.
 1. LEGEMIDLETS NAVN FUROSEMID 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Furosemid 20 mg, 40 og 500 mg. 3. LEGEMIDDELFORM Tabletter. Reseptpliktig gruppe C. Forskrivningsregel: For 500 mg tabletter skal
1. LEGEMIDLETS NAVN FUROSEMID 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Furosemid 20 mg, 40 og 500 mg. 3. LEGEMIDDELFORM Tabletter. Reseptpliktig gruppe C. Forskrivningsregel: For 500 mg tabletter skal
Hver tablett inneholder 120 mg feksofenadinhydroklorid, tilsvarende 112 mg feksofenadin. For fullstendig liste over hjelpestoffer se pkt. 6.1.
 1. LEGEMIDLETS NAVN Telfast 120 mg, filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 120 mg feksofenadinhydroklorid, tilsvarende 112 mg feksofenadin. For fullstendig
1. LEGEMIDLETS NAVN Telfast 120 mg, filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 120 mg feksofenadinhydroklorid, tilsvarende 112 mg feksofenadin. For fullstendig
PREPARATOMTALE. Hvit, bikonveks, ovalformet filmdrasjert tablett med "LH" inngravert på en side og glatt på den andre.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN /Hydrochlorothiazide Teva 100 mg/12,5 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 100 mg losartankalium og 12,5 mg
PREPARATOMTALE 1. LEGEMIDLETS NAVN /Hydrochlorothiazide Teva 100 mg/12,5 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 100 mg losartankalium og 12,5 mg
Feksofenadin er en farmakologisk aktiv metabolitt av terfenadin.
 PREPARATOMTALE (SPC) 1. LEGEMIDLETS NAVN TELFAST 180 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 180 mg feksofenadinhydroklorid, tilsvarende 168 mg feksofenadin.
PREPARATOMTALE (SPC) 1. LEGEMIDLETS NAVN TELFAST 180 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder 180 mg feksofenadinhydroklorid, tilsvarende 168 mg feksofenadin.
Preparatomtale (SPC) Inneholder også cetylalkohol, stearylalkohol og propylenglykolalginat.
 Preparatomtale (SPC) 1. LEGEMIDLETS NAVN Brevoxyl 40 mg/g krem 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 gram inneholder benzoylperoksid 40 mg. Inneholder også cetylalkohol, stearylalkohol og propylenglykolalginat.
Preparatomtale (SPC) 1. LEGEMIDLETS NAVN Brevoxyl 40 mg/g krem 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 gram inneholder benzoylperoksid 40 mg. Inneholder også cetylalkohol, stearylalkohol og propylenglykolalginat.
1. LEGEMIDLETS NAVN 2. KVALITATIV OG KVANTITATIV SAMMENSETNING
 1. LEGEMIDLETS NAVN /Hydroklortiazid Actavis 50 mg/12,5 mg filmdrasjerte tabletter /Hydroklortiazid Actavis 100 mg/12,5 mg filmdrasjerte tabletter /Hydroklortiazid Actavis 100 mg/25 mg filmdrasjerte tabletter
1. LEGEMIDLETS NAVN /Hydroklortiazid Actavis 50 mg/12,5 mg filmdrasjerte tabletter /Hydroklortiazid Actavis 100 mg/12,5 mg filmdrasjerte tabletter /Hydroklortiazid Actavis 100 mg/25 mg filmdrasjerte tabletter
Obstipasjon. Forberedelse før røntgenundersøkelse eller tømming av colon før operative inngrep.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Dulcolax 5 mg enterotabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Bisakodyl 5 mg Hjelpestoffer: Laktosemonohydrat Sakkarose 34,9 mg 23,4 mg For fullstendig liste
PREPARATOMTALE 1. LEGEMIDLETS NAVN Dulcolax 5 mg enterotabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Bisakodyl 5 mg Hjelpestoffer: Laktosemonohydrat Sakkarose 34,9 mg 23,4 mg For fullstendig liste
En tablett inneholder 750 mg glukosaminhydroklorid tilsvarende 625 mg glukosamin
 1. LEGEMIDLETS NAVN Flexove 625 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En tablett inneholder 750 mg glukosaminhydroklorid tilsvarende 625 mg glukosamin For fullstendig liste over hjelpestoffer,
1. LEGEMIDLETS NAVN Flexove 625 mg tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En tablett inneholder 750 mg glukosaminhydroklorid tilsvarende 625 mg glukosamin For fullstendig liste over hjelpestoffer,
PREPARATOMTALE (SPC) FOR. Panodil, filmdrasjert tablett
 1. LEGEMIDLETS NAVN Panodil 500 mg tabletter. Panodil 1 g tabletter. PREPARATOMTALE (SPC) FOR Panodil, filmdrasjert tablett 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Paracetamol 500 mg og 1 g. For fullstendig
1. LEGEMIDLETS NAVN Panodil 500 mg tabletter. Panodil 1 g tabletter. PREPARATOMTALE (SPC) FOR Panodil, filmdrasjert tablett 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Paracetamol 500 mg og 1 g. For fullstendig
PREPARATOMTALE 1. LEGEMIDLETS NAVN. Glucos. B. Braun 50 mg/ml infusjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Glucos. B. Braun 50 mg/ml infusjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1000 ml infusjonsvæske inneholder: Glukose, vannfri (55,0 g som glukosemonohydrat)
PREPARATOMTALE 1. LEGEMIDLETS NAVN Glucos. B. Braun 50 mg/ml infusjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1000 ml infusjonsvæske inneholder: Glukose, vannfri (55,0 g som glukosemonohydrat)
1. VETERINÆRPREPARATETS NAVN. Canidryl 100 mg tabletter til hund 2. KVALITATIV OG KVANTITATIV SAMMENSETNING. Virkestoff: Karprofen 100 mg/tablett
 1. VETERINÆRPREPARATETS NAVN Canidryl 100 mg tabletter til hund 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoff: Karprofen 100 mg/tablett Hjelpestoffer: Se punkt 6.1 for komplett liste over hjelpestoffer.
1. VETERINÆRPREPARATETS NAVN Canidryl 100 mg tabletter til hund 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoff: Karprofen 100 mg/tablett Hjelpestoffer: Se punkt 6.1 for komplett liste over hjelpestoffer.
VEDLEGG I PREPARATOMTALE
 VEDLEGG I PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Irbesartan Teva 75 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjert tablett inneholder 75 mg irbesartan. For fullstendig
VEDLEGG I PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Irbesartan Teva 75 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjert tablett inneholder 75 mg irbesartan. For fullstendig
Fenazon-Koffein Runde, flate, hvite tabletter med delestrek på en side og merket N2 på den andre siden.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Fenazon-Koffein tabletter Fenazon-Koffein Sterke tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver Fenazon-Koffein tablett inneholder 500 mg fenazon og 100 mg
PREPARATOMTALE 1. LEGEMIDLETS NAVN Fenazon-Koffein tabletter Fenazon-Koffein Sterke tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver Fenazon-Koffein tablett inneholder 500 mg fenazon og 100 mg
PREPARATOMTALE. Effekt og sikkerhet hos barn under 12 år er ikke undersøkt. Erfaring med langtidsbehandlinger begrenset.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Kestine 10 mg smeltetabletter Kestine 20 mg smeltetabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Ebastin 10 mg og 20 mg Hjelpestoff med kjent effekt: aspartam 1
PREPARATOMTALE 1. LEGEMIDLETS NAVN Kestine 10 mg smeltetabletter Kestine 20 mg smeltetabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Ebastin 10 mg og 20 mg Hjelpestoff med kjent effekt: aspartam 1
VEDLEGG I PREPARATOMTALE
 VEDLEGG I PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Irbesartan/Hydrochlorothiazide Teva 150 mg/12,5 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjert tablett inneholder
VEDLEGG I PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Irbesartan/Hydrochlorothiazide Teva 150 mg/12,5 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjert tablett inneholder
Milde til moderate lokale smerter i forbindelse med overfladiske bløtdelskader.
 1. LEGEMIDLETS NAVN Orudis 2,5 % gel 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Ketoprofen 2,5 %. For fullstendig liste over hjelpestoffer, se pkt. 6.1. 3. LEGEMIDDELFORM Gel Til utvortes bruk. 4. KLINISKE
1. LEGEMIDLETS NAVN Orudis 2,5 % gel 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Ketoprofen 2,5 %. For fullstendig liste over hjelpestoffer, se pkt. 6.1. 3. LEGEMIDDELFORM Gel Til utvortes bruk. 4. KLINISKE
Tablett, filmdrasjert Hvit, til offwhite filmdrasjert tablett, med delestrek på ene siden og merket med 10 på den andre.
 1. LEGEMIDLETS NAVN Cetirizin ratiopharm 10 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder cetirizin dihydroklorid 10 mg. Hjelpestoffer med
1. LEGEMIDLETS NAVN Cetirizin ratiopharm 10 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder cetirizin dihydroklorid 10 mg. Hjelpestoffer med
