Årsrapport 2016 med resultater og forbedringstiltak
|
|
|
- Susanne Aas
- 6 år siden
- Visninger:
Transkript
1 Nasjonalt kvalitetsregister for prostatakreft Årsrapport 2016 med resultater og forbedringstiltak
2 Anbefalt referanse: Årsrapport 2016 med resultater og forbedringstiltak fra Nasjonalt kvalitetsregister for prostatakreft. Oslo: Kreftregisteret, ISBN: Side 2 av 114
3 FORORD Prostatakreft er vår mest utbredte kreftsykdom og blir årlig påvist hos 5000 norske menn. Mens median alder ved diagnose er 69 år, er alderen betraktelig høyere, 83 år, for pasienter som dør av prostatakreft. Prostatakreft er også den vanligste kreftsykdommen hos menn som lever med kreft. I dag er det kun en av fem prostatakreftpasienter som forventes å dø av sin kreft. Målt i 5 års relativ overlevelse er prostatakreft vår 3. minst dødelige kreftsykdom. Når gjennomsnittlig levetid med sykdommen i tillegg er 15 år, tar det tid før endringer i utredning og behandling kan sees på harde endepunkter som nedgang i dødelighet. Et kvalitetsregisters primære oppgave er å måle etterlevelse av faglige retningslinjer. Videre er det også en forventning både blant pasienter og helsemyndigheter om at kvalitetsregistrene skal avspeile kvaliteten på helsetjenesten og avdekke eventuelle forskjeller geografisk og mellom ulike aktører. Et intuitivt kvalitetsmål ved kreftbehandling er for mange overlevelse og videre sykdomsutvikling etter behandling. Siden etableringen av prostatakreftregisteret i 2004 har det vært en pågående diskusjon om hvordan man skal definere og måle kvalitetsindikatorer for diagnostikk og behandling av prostatakreft. Fordi mange lever lenge med sin sykdom, kan det ta mange år før man ser effekter av endret diagnostikk eller behandling på langtidsoverlevelse. I denne perioden kan tjenestetilbudet være betydelig omorganisert og nye behandlinger være innført, noe som gjør tidligere data uaktuelle. Det finnes ingen etablerte internasjonale mål for hva som er god kvalitet på prostatakreftomsorg, ikke minst fordi forventet gevinst må veies opp mot mulige bivirkninger siden forløpet oftest er meget langt uansett behandling. Kvalitetsindikatorene sammen med prosentvise mål som i denne rapporten er fremstilt i kapittel 1.2, er valgt ut fra grundige, men skjønnsmessige vurderinger av referansegruppen. Det er mange forhold som spiller inn når man velger behandling, og mye av behandlingen som gis i dag kan dokumentere liten eller usikker gevinst. Målsetningen med rapporten er både å beskrive utredning og behandling og i hvilken grad denne praksis varierer gjennom ulike deskriptive tabeller og figurer. Vi håper at introduksjon av utvalgte kvalitetsmål vil bidra til å bedre omsorg av prostatakreftpasienter i landet. Resultatene i denne rapporten må vurderes med forsiktighet. Rapportering av kliniske data til denne rapporten er ikke komplett. I tillegg har Kreftregisteret foreløpig ingen data over hvordan pasientene opplever kvaliteten av sin behandling. I 2017 har registeret iverksatt et prosjekt for å måle pasientenes opplevelse av resultater av behandling av prostatakreft, støttet av Movember. Gjennom prosjektet håper vi å få kunnskap om pasientopplevd kvalitet og ikke minst bivirkninger av behandling fra pasienter behandlet over hele landet. Dette prosjektet sammen med fremstilling av sykehusenes praksis og resultater i forhold til andre sykehus og de foreslåtte kvalitetsmål, håper vi i neste omgang kan bidra til en enda bedre helsetjeneste for pasienten. Erik Skaaheim Haug Leder av referansegruppen Giske Ursin Direktør, Kreftregisteret Side 3 av 114
4 ÅRSRAPPORT SAMMENDRAG Sammendrag Kvalitetsindikatorer Utvikling av kvalitetsindikatorer Summary in english REGISTERBESKRIVELSE Bakgrunn og formål Bakgrunn for registeret Registerets formål Juridisk hjemmelsgrunnlag Faglig ledelse og databehandlingsansvar Aktivitet i styringsgruppe/referansegruppe RESULTATER Definisjoner Forekomst, dødelighet og prevalens Diagnostikk PSA ved diagnosetidspunkt Gleason score ved diagnosetidspunkt Risikogrupper ved diagnosetidspunkt Behandling med kurativ intensjon Behandlingsvalg Radikal prostatektomi Strålebehandling Dødelighet, dødsårsaker og overlevelse METODER FOR DATAFANGST Rapportering av klinisk informasjon Rapportering av klinisk informasjon innen 60 dager Rapportering av patologiinformasjon Rapportering av strålebehandlingsdata Rapportering fra andre kilder METODISK KVALITET Antall registreringer Metode for beregning av dekningsgrad Tilslutning Dekningsgrad Prosedyrer for intern sikring av datakvalitet Metoder for validering av data i registeret Vurdering av datakvalitet Statistisk metode FAGUTVIKLING OG KVALITETSFORBEDRING AV TJENESTEN Pasientgruppe som omfattes av registeret Side 4 av 114
5 6.2 Registerets spesifikke kvalitetsmål Lavrisiko pasienter som er radikal behandlet Høyrisiko prostatakreft som er radikal behandlet Lymfeknutedisseksjon i forbindelse med prostatektomi for høyrisiko kreft Ufri rand (margin) etter en prostatektomi for pt2 cancer Videre arbeid med kvalitetsmål Nasjonale kvalitetsindikatorer Pasientrapporterte resultat- og erfaringsmål (PROM og PREM) Sosiale og demografiske ulikheter i helse Bidrag til utvikling av nasjonale retningslinjer, nasjonale kvalitetsindikatorer o.l Etterlevelse av nasjonale retningslinjer Identifisering av kliniske forbedringsområder Tiltak for klinisk kvalitetsforbedring initiert av registeret Evaluering av tiltak for klinisk kvalitetsforbedring (endret praksis) Pasientsikkerhet FORMIDLING AV RESULTATER Resultater tilbake til deltakende fagmiljø Resultater til administrasjon og ledelse Resultater til pasienter Offentliggjøring av resultater til institusjonsnivå SAMARBEID OG FORSKNING Samarbeid med andre helse- og kvalitetsregistre Vitenskapelige arbeider Oversikt over publikasjoner med bruk av data fra Prostatakreftregisteret Doktorgrader PLAN FOR FORBEDRINGSTILTAK MOMENTLISTE Datafangst Metodisk kvalitet Fagutvikling og kvalitetsforbedring av tjenesten Formidling av resultater Samarbeid og forskning STADIEVURDERING REFERANSER TIL VURDERING AV STADIUM VEDLEGG Forfattere og andre bidragsytere til årsrapporten Referansegruppen for Nasjonalt kvalitetsregister for prostatakreft Klinisk TNM, prostatakreft Ekstra analyser Utredning Behandlingsvalg Tidligere publikasjoner med data fra prostatakreftregisteret Side 5 av 114
6 11.6 Figuroversikt Tabelloversikt REFERANSER Side 6 av 114
7 Del 1 Årsrapport Side 7 av 114
8 1 SAMMENDRAG 1.1 Sammendrag I første halvdel av 1990-tallet og fram til rundt 2005 ser vi at det har vært en rask økning i nye tilfeller av prostatakreft for alle aldersgrupper. Ca. fire ganger flere menn mellom år lever med prostatakreft i dag sammenlignet med i år Fra midten av 1990-tallet har det vært en nedgang i dødeligheten for alle aldersgrupper. PSA-verdi ved diagnose faller jevnt, noe som tyder på at det screenes for mye prostatakreft uten at det eksisterer et formelt screening-program. Praksis ved utredning av pasienter med PSA <4 synes å variere noe, mens bruk av PSA uten symptomer er mindre blant de eldste. Rapporteringspraksis bidrar sannsynligvis også i stor grad til forskjeller mellom fylkene, selv om fylkesvise forskjeller i bruk av PSA ikke kan utelukkes. Fordeling av Gleason score ved diagnosetidspunktet har i Norge vært stabil over tid. Det observeres noe forskjell i fordeling av høyeste Gleason score ved diagnosetidspunktet mellom patologilaboratoriene i Norge, men på landsbasis har også denne fordelingen vært relativt stabil de seneste årene. Samsvaret mellom Gleason score i siste prøve før operasjon og i påfølgende prostatektomipreparat er om lag 50 %, og reflekterer i stor grad utfordringer knyttet til diagnostikk av prostatakreft. Forbedringer i bildediagnostikk og økende bruk av målrettede biopsier kan muligens gi bedre samsvar i fremtiden. Ulik praksis ved rapportering og bruk av MR, men også ulik vurdering av ct-stadium og Gleason-grad mellom sykehusene, kan bidra til ulik fordeling i risikogruppene mellom fylkene. En reell geografisk forskjell i sykdomsstadium kan likevel ikke utelukkes. Andelen menn som gjennomførte behandling med kurativ intensjon har vært stabilt siste ti år. Bare for menn mellom år observeres en fortsatt økning i andelen radikal behandling. Det er tydelige endringer å se for risikogruppene: andel behandlete menn med lavrisikokreft er kontinuerlig fallende og andelen menn som ble behandlet for høyrisikokreft har steget lenge, men ser ut til ha stabilisert seg de siste årene, noe som er en ønsket utvikling. Andel menn som opereres for lavrisikokreft er fortsatt fallende, samtidig som antall menn som opereres for høyrisikosykdom er stigende. Pasientene får i all hovedsak sin behandling i egen region. Det er fortsatt stor variasjon i preoperativ stadievurdering, hvilket kan tilskrives forskjeller i implementering av MR i stadievurderingen før operasjon. Både absolutt antall og andel menn som gjennomførte primær kurativt strålebehandlet av totalt antall behandlet med kurativ intensjon har gått ned. Bruken av postoperativ strålebehandling synes å gå noe ned for pasienter operert etter En tredje del av menn som ble operert for lokalavansert kreft (pt3) i 2012 måtte gjennomføre postoperativ strålebehandling innen tre år. De betydelige forskjellene mellom sykehusene tyder på ulik behandlingspraksis. Beregninger av overlevelse etter en prostatakreftdiagnose i et populasjonsbasert materiale må ta hensyn til risikogrupper, alder, behandling samt død av andre årsaker. Noen forskjeller i overlevelse mellom fylkene kan sees, men disse kan skyldes tilfeldig variasjon. Side 8 av 114
9 1.2 Kvalitetsindikatorer Denne rapporten presenterer fire mål for behandlingskvaliteten. Lavrisikopasienter har ingen dokumentert effekt av radikal behandling, men målet er < 20 % da pasienters preferanser og spesielle forhold likevel kan resultere i radikal behandling. Behandling av høyrisiko-sykdom er indisert når pasientene ikke har reduserte leveutsikter av annen årsak, og målet er derfor satt til > 70 %. Lymfeknutedisseksjon i forbindelse med prostatektomi ved høyrisiko sykdom er anbefalt i nasjonale og internasjonale retningslinjene, og det bør være gjennomførbart hos > 80 %. Fravær av kreft i snittflaten (fri margin) bør være regelen hos pasienter med kreft avgrenset til prostata. Minimale områder med ufri margin har ikke vist vesentlig betydning for prognose eller etterbehandling og er en risiko ved valg av nervesparende teknikk for å bedre funksjonelt resultat hos utvalgte pasienter, men andelen ufri margin bør være < 20 %. For en lengre redegjørelse for valg av kvalitetsmål se avsnitt 6.2. Det er i tillegg satt kvalitetsmål for dekningsgrad og rapporteringsgrad. Dekningsgrad er hvor stor andel av alle pasienter med prostatakreft som finnes i registeret. Rapporteringsgrad viser for hvor stor andel av pasientene den behandlende helseinstitusjon har meldt detaljert informasjon om utredning og kirurgi. Side 9 av 114
10 Mål Rapporteringsgrad klinisk utredningsmelding 68% >80 Rapporteringsgrad klinisk kirurgimelding 75% >80 Andel lavrisikopasienter som er radikalt behandlet 17% <20 Andel høyrisikopasienter som er radikalt behandlet 76% >70 Andel høyrisikopasienter som har fått lymfeknutedisseksjoner under prostatektomi 87% >80 Andel fri rand - pt2 85% >80 Dekningsgrad 99% > Andel (%) Figur 1 Kvalitetsmål fra årsrapport 2016 fra Nasjonalt kvalitetsregister for prostatakreft. Norge, prosent. 1.3 Utvikling av kvalitetsindikatorer Denne rapporten fremmer for første gang kvalitetsmål. Referansegruppen har foreslått syv markører som vist i Figur 1. I fremtiden kan flere markører bli inkludert, og fem mulige markører er oppført i Figur 2. Side 10 av 114
11 Andel fri rand - pt3 65% Andel pasienter med pt2 som har fått postoperativ strålebehandling 7% Andel pasienter med pt3 som har fått postoperativ strålebehandling 32% Andel pasienter hvor det er samsvar mellom pre- og postoperativ gleasonscore 52% Andel pasienter hvor det er samsvar mellom pre- og postoperativt T-stadium 66% Andel (%) Figur 2 Utviklingsindikatorer for årsrapport 2016 fra Nasjonalt kvalitetsregister for prostatakreft. Norge, prosent. Lokalavanserte svulster (pt3) er en heterogen gruppe ut fra omfanget av ekstraprostatisk vekst, og det har variert i hvilken grad gruppen har blitt tilbudt operasjon. Et senter der mange pasienter med avanserte svulster opereres vil få en høyere andel med ufrie marginer, samtidig er det enighet om at fri margin bør tilstrebes. Så lenge registeret ikke kan redegjøre for den underliggende variasjon vil ikke referansegruppen innføre et kvalitetsmål for pt3 tumorer. Patologiforeningen arbeider med standardisering av patologirapporten. Dette vil fremtidig kunne føre til beskrivelse av et distinkt mål også for lokalavanserte svulster. Indikasjonen for postoperativ strålebehandling er ikke fullstendig avklart i retningslinjene og bruken varierer også basert på hvor tett pasientene følges. Referansegruppen har ikke innført noe kvalitetsmål for dette, men følger parameteren da postoperativ stråling klart er forbundet med økte bivirkninger og ressursbruk. Riktig sykdomsklassifisering før behandling er vesentlig for riktig beslutning og godt resultat. Per i dag skjer det store endringer i diagnostikken, særlig ved bruk av MR til å angi T-stadium og til å rette biopsiene mot tumor. Dette er foreløpig lite beskrevet i retningslinjene og det er foreløpig ikke kjent hvordan dette kan bedre treffsikkerhet for T-stadium og Gleason-score før og etter operasjon. Side 11 av 114
12 Referansegruppen håper man i fremtiden kan bruke dette som en kvalitetsindikator som kan fremme treffsikkerheten i diagnostikken 1.4 Summary in english In Norway, the prostate cancer incidence rate in men increased rapidly between 1990s and 2005 (figure 3). Today there are four times more men (between the age of 65 and 74) living with prostate cancer compared to the year The prostate cancer mortality rates have decreased for all age groups from the mid-1990s. Men diagnosed with prostate cancer, that have not spread to other organs, are more likely to die from other causes than from prostate cancer (figure 44). The use of PSA testing alone (prostate-specific antigen) in the diagnostic work-up of men without lower urinary tract symptoms (LUTS), seems to continue to increase compared to last year s report. There are large regional variations in the use of PSA testing alone (figure 11 and 12). However, the clinical forms have caused uncertainties as to how diagnostic work up should be reported, meaning that these variations may not be caused by differences in clinical practice, but by administrative reasons. In June 2017 the cancer registry published new clinical forms which hopefully will eliminate the risk of misinterpreting the questions. The national overview of Gleason score groups at time of diagnosis have been relatively stable over time (figure 16). There are differences between the pathology laboratories in Gleason score (figure 17), the reason for this is not known and may be caused by differences in the patient population, differences in interpreting Gleason score, et.c.. There are also large variations when comparing Gleason score before surgery (biopsy) with Gleason score in the surgical tissue sample (figure 18). Increased use of MRI and targeted needle biopsies may give even higher concordance between the first and final tissue sample in the future. Information about MRI and PI-RADS were added to the new clinical forms mentioned above. The proportion of men with high-risk disease that undergo radical prostatectomy have increased from 5 percent to about 40 percent during the period (figure 22). This indicates an increased use of radical prostatectomy in patients with locally advanced cancer (ct3). The number of patients receiving radiation therapy as primary treatment has been relatively stable over the last years (table 5 in the appendix). There are regional differences in the use of postoperative radiation therapy in the period , but it seems to stabilize (table 11 in appendix). Side 12 av 114
13 2 REGISTERBESKRIVELSE 2.1 Bakgrunn og formål Bakgrunn for registeret Nasjonalt Program for Prostatacancer (NPPC) ble startet opp i 2003 og registeret fikk nasjonal status i Siden oppstarten av Prostatakreftregisteret i 2004 har opplysninger om pasienter blitt registrert i registeret Registerets formål Registeret skal bidra til å styrke kvaliteten på helsehjelp til pasienter med prostatakreft. Registeret skal også drive, fremme og gi grunnlag for forskning for å utvikle ny viten om kreftsykdommens årsaker, diagnose og sykdomsforløp, samt behandlingseffekter. Ref. Kreftregisterforskriften Juridisk hjemmelsgrunnlag Helseregisterloven av nr 4 11 og Kreftregisterforskriften. 2.3 Faglig ledelse og databehandlingsansvar Kreftregisteret er databehandlingsansvarlig. Faglig ledelse av Prostatakreftregisteret gjøres i tett samarbeid med referansegruppen. Referansegruppen for Nasjonalt kvalitetsregister for Prostatakreft består av urologer, onkologer, patologer og radiologer fra hele landet 1. Leder for referansegruppen er Urolog Erik Skaaheim Haug, og onkolog Arne Berg er nestleder. 2.4 Aktivitet i styringsgruppe/referansegruppe Referansegruppemøter arrangeres to ganger årlig. Det siste året har referansegruppen fokusert på kvalitetsmål for registeret, revisjon av eksisterende kliniske meldeskjemaer samt nytt strålebehandlingsskjema. I tillegg har innhold i årsrapporten fra prostatakreftregisteret vært fast innlegg på møtene. I oktober 2014 ble det nedsatt en arbeidsgruppe for årsrapporten fra registeret. Arbeidsgruppen består av 5 referansegruppemedlemmer og 3 representanter fra Kreftregisteret. Denne gruppen har hatt to møter i løpet av 2017; ett i januar og ett i mai. Ellers har korrespondansen foregått hovedsakelig via e-post. Hele referansegruppen har fått tilsendt rapporten med muligheter for å gi tilbakemeldinger og innspill før publisering. Kreftregisteret har et godt samarbeid med Kreftforeningen og i samråd med dem har vi etablert et brukerpanel der representanter fra alle relevante pasientforeninger er invitert. Brukerpanelet hadde møte i Kreftregisteret 29. mai 2017 og pasientrepresentantene kom med tilbakemeldinger på utkast til presentasjon av resultater. Et nytt brukerpanelmøte er planlagt 22. november Brukerpanelmøtene erstatter foreløpig pasientrepresentasjon i referansegruppen for prostatakreftregisteret. 1 En oversikt over referansegruppemedlemmer finnes i kapittel 11.2 Side 13 av 114
14 3 RESULTATER 3.1 Definisjoner Begrep Adjuvant behandling Aktiv overvåkning Aldersstandardisert insidens- /dødelighetsrate Behandling med kurativ intensjon Behandling med livsforlengende- og symptomforebyggende intensjon Dødelighet Dødelighetsrate Forekomst Insidensrate Gleason score Forklaring Tilleggsbehandling for å redusere risikoen for tilbakefall Aktiv overvåkning har som målsetting å unngå eller utsette kurativ behandling for dermed å unngå eller utsette unødvendige bivirkninger knyttet til behandlingen. Pasienter i aktiver overvåkning følges med PSAmålinger, rebiopsier og i økene grad MR av prostata. Ved tegn til progresjon av sykdommen avsluttes overvåkningen og pasienten får behandling med helbredende intensjon. En aldersstandardisert rate er et vektet gjennomsnitt av aldersspesifikke rater. Ved å aldersstandardisere rater kan befolkningsgrupper, for eksempel fylker, regioner eller land, med ulik alderssammensetning sammenlignes. Om målet er å fjerne hele kreften kan behandlingen for eksempel hete «helbredende», «kurativ» eller «radikal». For denne rapporten har vi valgt begrepet «kurativ» eller «kurativ intensjon». De behandlingsvalgene som er aktuelle for å helbrede prostatakreft er operasjon og strålebehandling. Andre behandlingsvalg med kurativ intensjon er svært sjelden og omtales ikke i rapporten (f. eks. prostatektomi eller høy intensitet ultralyd behandling etter kurativ strålebehandling). Når det ikke er mulig med å fjerne hele kreftsvulsten blir behandlingens mål livsforlengende, symptomforebyggende eller symptomlindrende. Ofte brukes ordet «palliativ» for slik behandling. Palliativ behandling omtales ikke i denne rapporten. Sykdomsspesifikk mortalitet, eller dødelighet, er antallet personer som dør av en spesifikk sykdom i en definert populasjon innen en gitt tidsperiode, og er begrepet som benyttes i rapporten når ikke annet er angitt. I denne rapporten er populasjonen Norges mannlige befolkning, sykdommen er prostatakreft, og tidsperiodene er kalenderår. Denne form for dødelighet skiller seg fra total dødelighet som er dødelighet uavhengig av dødsårsak. Dødelighetsraten uttrykkes i denne rapporten som antall dødsfall av prostatakreft per personår. Insidens, eller forekomst, er antall nye tilfeller av en sykdom i en definert populasjon innen en gitt tidsperiode. I denne rapporten er populasjonen Norges mannlige befolkning, og tidsperiodene er kalenderår. Antall nye tilfeller som oppstår i en populasjon (forekomsten/insidensen) delt på antall personår som var under risiko for å bli rammet av kreft i den aktuelle periode. Raten uttrykkes som antall tilfeller per personår. Gleason score settes ved mikroskopisk undersøkelse av en vevsprøve. Det er en av de viktigste prognostiske faktorene ved prostatakreft. Den settes sammen av to Gleason grader, som hver kan være fra 1-5. Gleason score må minst være 2 og kan maksimalt være 10. Etter siste revisjon av Gleasonsystemet, er Gleason score 6 i praksis den laveste Side 14 av 114
15 score som settes i nålebiopsier. i Den graden det sees mest av i tumorvevet, settes som den første, og den andre graden er den det sees nest mest av. For eksempel: Gleason grad: 3+4= score 7. I nålebiopsier skal imidlertid høyeste grad alltid angis, og i mange tilfeller blir derfor Gleason score; dominerende grad + høyeste grad. En høy Gleason score tyder på en relativ aggressiv tumor. ii Det er også innført en ny gradering iii av Gleason score som fordeler Gleason score inn i de prognostiske gruppene 1 til 5 (gradgrupper) i henhold til ISUP (International Society for Urologicl Pathology). Ved å benytte et mer forenklet graderingssystem hvor gruppe 1 er de laveste, i motsetning til Gleason grad 6, vil det potensielt kunne redusere overbehandlingen av prostatakreft. For å forhindre forveksling av resultater er det anbefalt å rapportere både gammelt og nytt graderingssystem inntil det nye graderingssystemet blir mer praktisert og akseptert av klinikerne. Grad- gruppe 1: Gleason score 6 Grad-gruppe 2: Gleason score 3+4=7a Grad-gruppe 3: Gleason score 4+3=7b Grad-gruppe 4: Gleason score 8 Grad-gruppe 5: Gleason score 9-10 Kurativ Prevalens Postoperativ strålebehandling PSA Relativ overlevelse Risikogrupper Helbredende, se behandling med kurativ intensjon Prevalens er antallet eller andelen av en populasjon som på et tidspunkt har eller har hatt den aktuelle sykdommen. I denne rapporten gjelder det alle menn som på et eller annet tidspunkt har fått en prostatakreftdiagnose, og fremdeles er i live. Begrepet «postoperativ strålebehandling» som brukes i rapporten ( ), inkluderer strålebehandling rett etter operasjon og strålebehandling som er gitt etter tilbakefall av prostatakreft inntil 3 år etter operasjon. I begge disse tilfellene betegnes strålebehandlingen som kurativ. PSA (prostataspesifikt antigen) er et protein som produseres i prostata. PSAens biologiske funksjon er å frigjøre sædcellene fra ejakulatet. Menn har også litt PSA i blodet og PSA blir derfor målbart med en blodprøve. PSA-nivået kan øke ved benign prostatahyperplasi (BPH) og prostatitt, men også ved prostatakreft. PSA-nivået benyttes i tidlig diagnostikk av prostatakreft. I Norge er det til nå ikke anbefalt med PSA-screening av symptomfrie menn uten arvelig belastning. iv Måling av PSA brukes også i oppfølging av menn som har fått behandling for prostatakreft, fordi forhøyet PSA verdi kan gi indikasjon om tilbakefall. Overlevelse blant kreftpasienter delt på forventet overlevelse for en tilsvarende gruppe personer i befolkningen, som ikke har denne kreften, men ellers er sammenlignbar (samme kjønn og alder). v Risikogruppering er en av faktorene som brukes ved valg av behandling og oppgis som lavrisiko, middels risiko (kalles også intermediær risiko) og høyrisiko. vi Mange av resultatene i denne rapporten er fordelt på risikogrupper. I denne rapporten oppgis risikogruppering for Pasienter med lokalisert eller lokalavansert prostatakreft stadium ct1-ct3 Ingen spredning til lymfeknuter (N0/NX) Ingen spredning til andre organer (M0) Side 15 av 114
16 PSA lavere 100 ng/ml Alder under 80 år, generelt god almenntilstand og fravær av annen kreftdiagnose Risikogruppene er basert på EAU Guidelines on Prostate Cancer vii før revisjon i 2015: Lavrisiko: ct1-2a og PSA 10 ng/ml og Gleason score 6. Middels risiko 2 /intermediær risiko: ct2b-2c eller PSA>10<20 ng/ml eller Gleason score 7. Høyrisiko: ct 3a eller PSA >20 ng/ml eller Gleason score Revidert risikogruppering vil bli tatt i bruk fra og med neste rapport som utgis i 2018 TNM Klinisk TNM (ctnm) er en av de viktigste prognostiske faktorene for sannsynlig sykdomsforløp og en av faktorene som brukes som grunnlag for valg av behandling. 3 TNM står for tumor, node (lymfeknute) og metastasis (metastase/dattersvulst), og er et mål på kreftsykdommens utbredelse i kroppen. T beskriver primærtumorens utbredelse, N eventuell spredning til regionale lymfeknuter, og M omhandler status for fjernmetastasering (spredning av kreftsykdommen til andre organer). Tallene som settes etter disse tre bokstavene, angir sykdommens utbredelse, for eksempel T2 N0 M0. viii Det skilles i mellom klinisk TNM (ctnm) og patologisk TNM (ptnm). Klinisk TNM blir satt av legen som utreder pasienten og gjenspeiler funn tilgjengelig før behandling, inkludert klinisk undersøkelse, bildediagnostikk og svar på vevsprøver. Klinisk TNM stadium er viktig når behandling og prognose vurderes. Patologisk TNM settes av patolog ved undersøkelse av et operasjonspreparat, og er blant annet viktig for å vurdere om det trengs supplerende behandling (adjuvant terapi). ix 2 I årsrapport 2014 ble D Amicos kriterier benyttet, som inkluderer ct2c i høyrisikogruppen. Dermed inkluderer gruppen for middels risiko en større andel pasienter i årets rapport, enn i fjorårets. 3 For klinisk TNM-oversikt for prostatakreft, se kapittel 11.3 Side 16 av 114
17 3.2 Forekomst, dødelighet og prevalens Tabell 1 viser antall nye pasienter som ble diagnostisert med prostatakreft, antall som døde av prostatakreft samt antallet personer som lever med prostatakreft i Norge fra oppstarten av Prostatakreftregisteret i 2004 og fram til I 2016 fikk over 1100 flere pasienter prostatakreft enn i 2004, og antallet pasienter som lever med, eller etter behandling, for en prostatakreftdiagnose er mer enn doblet i løpet av samme periode. På tross av den kraftige økningen i antallet pasienter som blir diagnostisert med prostatakreft per år, har antallet som dør av prostatakreft holdt seg relativt stabilt gjennom hele perioden. Tabell 1 Antall nye pasienter, antall døde av prostatakreft og personer som lever med prostatakreft. Norge, År Forekomst Dødelighet Prevalens * Utviklingen i forekomst (insidensrater) av prostatakreft fra 1960 til 2015 er vist i figur 3. Vi ser at det har vært en gradvis økning i både forekomst fram til rundt Etter 1990 og fram til midten av 1990-tallet ser vi at det har vært en raskere økning i forekomsten for alle aldersgrupper. I denne perioden ble blodprøven PSA innført i Norge og det er grunn til å tro at mye av økningen skyldes en mer aktiv leting etter sykdommen. Forekomsten har økt videre også etter 1995 og fram til rundt Etter dette ser vi en markant nedgang for menn over 85 år og en stabilisering for menn under 85 år. figur 4 viser at det rundt 2005 har vært en kraftig økning av pasienter som for oppdaget kreften når den fortsatt en lokalisert til prostata eller har spredd seg til regionale lymfeknuter. Denne økningen passer med økningen i forekomst, som forklart over. Totalt ble 5087 pasienter diagnostisert med prostatakreft i Omtrent en fjerdedel var 75 år eller eldre på diagnosetidspunktet (figur 5). Aldersfordelingen i de ulike risikogruppene for pasienter som er regnet som aktuelle for kurativ behandling er vist i figur 6. Utviklingen i dødelighet (dødelighetsrater) vises i figur 7. Dødeligheten av prostatakreft har økt langsomt fram til midt på 1990-tallet, bortsett fra for menn 85 år og eldre der vi ser en raskere økning fra , tilsvarende økningen i forekomsten i samme periode. Fra midten av 1990-tallet har det vært en nedgang i dødeligheten for alle aldersgrupper menn hadde prostatakreft som dødsårsak i Ca. ¾ av mennene var over 75 år når de døde, mens omtrent 5% var under 65 år (figur 8). Figur 10 viser at det i dag er fire ganger så mange menn mellom år som lever med prostatakreft enn i år Figur 9 viser at det særlig er pasienter med lokalisert prostatakreft som diagnostiseres hyppigere. Økningen i andel pasienter med regional spredning kan skyldes bedre diagnostikk med MR og lymfeknutefjerning som ikke var praksis tidligere, da regional spredning ikke ble undersøkt. Sammendrag: I første halvdel av 1990-tallet og fram til rundt 2005 ser vi at det har vært en økning i påvisning av prostatakreft for alle aldersgrupper. Ca. fire ganger flere menn mellom år lever med prostatakreft i dag enn i år Fra midten av 1990-tallet har det vært en nedgang i dødeligheten for alle aldersgrupper. 4 Kreftregisteret har pr. 25. august 2017 ikke mottatt all data fra Dødsårsaksregisteret for Dødelighetstall for 2016 kan derfor ikke publiseres. Side 17 av 114
18 Insidensrate (pr personår) Figur 3 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Prostatakreft Diagnoseår: Dekningsgrad: >99% Alder: Figur 3 Insidensrater for prostatakreft pr personår for ulike aldersgrupper. Aldersstandardisert insidensrate (pr personår) Figur 4 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Prostatakreft Diagnoseår: Dekningsgrad: >99% Stadium ved diagnose: Lokalisert Regional spredning Primærmetastatisk Figur 4 Stadium ved diagnose. Side 18 av 114
19 % 24% 21% Figur 5 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Prostatakreft Diagnoseår: 2016 Dekningsgrad: >99% Antall % % 8% % 4% 2% Aldersgrupper Figur 5 Forekomst av prostatakreft, aldersgruppert. Andel (%) Lav risiko, N = Andel (%) Intermediær risiko, N = Figur 6 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Diagnostisert prostatakreft, <80 år. Diagnoseår: 2016 Dekningsgrad: >99% Intermediær risiko = middels risiko, se definisjoner Høy risiko, N = 859 Mangler informasjon, N = Andel (%) Andel (%) Figur 6 Risikogrupper, aldersfordeling. Side 19 av 114
20 Mortalitetsrate (pr personår) Figur 7 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Diagnostisert med prostatakreft Diagnoseår: Dekningsgrad: >99% Alder: Figur 7 Dødelighetsrater for prostatakreft pr personår, gruppert etter alder ved død % 24% Figur 8 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Diagnostisert prostatakreft Dødsår: 2015 Dekningsgrad: >99% 17% Antall % % 9% 50 3% Aldersgrupper Figur 8 Alder ved død av prostatakreft. Side 20 av 114
21 Prevalens Figur 9 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Diagnostisert med prostatakreft Diagnoseår: Dekningsgrad: >99% Stadium ved diagnose: Lokalisert Regional spredning Primærmetastatisk Figur 9 Prevalens etter stadium ved diagnose. Prevalens Figur 10 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Diagnostisert med prostatakreft Diagnoseår: Dekningsgrad: >99% Alder: Figur 10 Prevalens, aldersgruppert (alder ved diagnose). Side 21 av 114
22 3.3 Diagnostikk PSA ved diagnosetidspunkt Figur 11 og figur 12 viser pasientene der legen har rapportert at forhøyet PSA var hovedårsaken til at pasienten ble utredet 5 i Den fylkesvise oversikten viser at det kan være regionale forskjeller i bruk av PSA-testing, men mye tyder på at rapporteringspraksisen sannsynligvis varierer mye mellom avdelingene. Det har vært ulike kliniske meldeskjemaer for rapportering til Prostatakreftregisteret de siste årene, og alternativene under spørsmålet «årsak til utredning» har variert. I 2016 er det rapportert at 70 % av nydiagnostiserte pasienter under 70 år og 53% av pasientene over 70 år har blitt sendt til utredning for prostatakreft på grunn av en forhøyet PSA alene. For aldersgruppen år blir 3 av 5 menn utredet kun som en følge av forhøyet PSA-verdi. Tidligere har en fjerdedel av pasientene startet utredning på grunn av urinveissymptomer (LUTS Lower Urinary Tract Symptoms). PSA tas rutinemessig ved vannlatingsproblemer hos menn, noe som gir mulighet for ulik vektlegging mellom avdelingene ved rapportering. I fremtiden vil man derfor heller rapportere hvem som utredes for LUTS i tillegg til høy PSA, da dette vil gi en riktigere fremstilling. Palpasjonsfunn ved DRE (digital rektal eksplorasjon), tilfeldig funn ved cystoprostatektomi og metastasemistanke kan være andre årsaker til utredning. I tråd med at bruken av PSA-prøver har økt, har også PSA-verdien ved diagnose falt, noe som fremstilles ved at andelen som har PSA <10 ved diagnose har økt jevnt fra 27% i 2004 til 51% i 2016 (se figur 13). Norge har ikke hatt et formelt screeningprogram for prostatakreft med bruk av PSA, men utbredt bruk av PSA, såkalt vill-screening, kan også være med å forklare den høye norske forekomsten av prostatakreft. Ser man figur 13 i sammenheng med figur 9 underbygger det påstanden om at norske menn tar PSA i økende grad for å avdekke prostatakreft og at dette medfører at flere lokaliserte prostatakreftsvulster oppdages. Figur 14 viser den fylkesvise fremstillingen av fordelingen i ulike PSA-intervaller av diagnostiserte pasienter. Figuren er vanskelig å tolke, men en variasjon på 0-14% av pasienter som har <4 i PSA ved diagnose kan antyde at praksis lokalt på sykehusene kan variere i forhold til når man starter utredning av pasienter for prostatakreft. De fleste fylkene ligger imidlertid tett opp til landsgjennomsnittet. Figur 15 viser ikke uventet at de eldste har gjennomsnittlig høyest PSA verdi ved diagnose. Dette kan både skyldes at eldre menn oftere har avansert sykdom (jfr. figur 6), og at PSA oftere tas på grunn av symptomer (jfr. figur 12). Sammendrag: PSA-verdi ved diagnose faller jevnt, noe som tyder på at det screenes for mye prostatakreft uten at det eksisterer et formelt screening-program. Praksis ved utredning av pasienter med PSA <4 synes å variere noe, mens bruk av PSA uten symptomer er mindre blant de eldste. Rapporteringspraksis bidrar sannsynligvis også i stor grad til forskjeller mellom fylkene, selv om fylkesvise forskjeller i bruk av PSA ikke kan utelukkes. 5 Utdypende data over angitt hovedårsak til utredning finnes i vedlegg 11-1, vedlegg 11-2, vedlegg 11-3 og vedlegg Side 22 av 114
23 Norge 70% Pasienter Meldt / Diagnostisert 1792 / 2680 Nord-Trøndelag Finnmark 30% 34% 33 / / 40 Sør-Trøndelag Telemark 52% 53% 52 / / 87 Troms Nordland Hordaland Oppland Rogaland Østfold Møre og Romsdal Aust-Agder Sogn og Fjordane Hedmark Akershus Oslo Vest-Agder Vestfold Buskerud 59% 60% 62% 65% 68% 69% 69% 70% 71% 74% 79% 81% 81% 83% 86% 49 / / / / / / / / / / / / / / / Andel (%) Figur 11 Utredet kun på grunn av forhøyet PSA, <70 år, Norge og fylker. Figur 11 Datakilde: Klinisk primærutredningsmelding Inklusjonskriterier: Diagnostisert prostatakreft, <70 år, utfylt PSA-verdi ved diagnose. Eksklusjonskriterier: Utredet med andre metoder i tillegg til PSA Diagnoseår: 2016 Rapporteringsgrad: 68% Side 23 av 114
24 Norge 53% Pasienter Meldt / Diagnostisert 1482 / 2407 Nord-Trøndelag Finnmark 17% 20% 47 / / 30 Sør-Trøndelag Sogn og Fjordane 27% 28% 44 / / 58 Telemark Oppland Troms Møre og Romsdal Hordaland Nordland Østfold Hedmark Buskerud Aust-Agder Vest-Agder Vestfold Rogaland Akershus Oslo 35% 38% 42% 43% 45% 49% 51% 53% 54% 60% 60% 64% 67% 69% 75% 54 / / / / / / / / / / / / / / / Andel (%) Figur 12 Utredet kun på grunn av forhøyet PSA, >70 år, Norge og fylker. Figur 12 Datakilde: Klinisk primærutredningsmelding Inklusjonskriterier: Diagnostisert prostatakreft, >70 år, utfylt PSA-verdi ved diagnose. Eksklusjonskriterier: Utredet med andre metoder i tillegg til PSA Diagnoseår: 2016 Rapporteringsgrad: 68% Side 24 av 114
25 2016 8% 51% 22% 13% 6% Pasienter Meldt / Diagnostisert 3379 / % 49% 23% 15% 5% 3881 / % 47% 23% 16% 7% 3954 / % 45% 25% 17% 7% 4088 / % 45% 25% 20% 5% 4662 / 4822 Diagnoseår % 5% 5% 38% 38% 42% 26% 25% 25% 22% 21% 24% 7% 9% 8% 4711 / / / % 36% 24% 25% 9% 3976 / % 33% 25% 27% 10% 4063 / % 29% 26% 29% 11% 3561 / % 30% 24% 28% 13% 3521 / % 25% 31% 13% 3669 / Andel (%) PSA<4 4 PSA<10 10 PSA<20 20 PSA<100 PSA>100 Figur 13 Gruppert PSA-verdi ved diagnosetidspunkt, fra Figur 13 Datakilde: Klinisk primærutredningsmelding Inklusjonskriterier: Diagnostisert prostatakreft, utfylt PSA-verdi ved diagnose i klinisk melding Diagnoseår: Rapporteringsgrad: 68% Side 25 av 114
26 Pasienter Meldt / Diagnostisert Norge 8% 51% 22% 13% 6% 3379 / 5037 Østfold 12% 63% 19% 5% 196 / 463 Akershus 6% 53% 23% 13% 5% 513 / 613 Oslo 8% 60% 19% 12% 313 / 409 Hedmark 7% 50% 25% 11% 7% 175 / 228 Oppland 12% 40% 24% 19% 5% 156 / 183 Buskerud 8% 50% 23% 13% 6% 220 / 265 Vestfold 10% 49% 24% 15% 203 / 250 Telemark 8% 48% 20% 15% 9% 132 / 152 Aust-Agder 59% 27% 14% 22 / 110 Vest-Agder 7% 49% 18% 20% 6% 45 / 200 Rogaland 8% 59% 17% 12% 288 / 443 Hordaland 6% 47% 26% 15% 6% 356 / 419 Sogn og Fjordane 5% 51% 19% 19% 6% 43 / 101 Møre og Romsdal 10% 58% 15% 11% 6% 198 / 298 Sør-Trøndelag 13% 48% 22% 14% 96 / 286 Nord-Trøndelag 9% 37% 32% 18% 79 / 132 Nordland 11% 40% 30% 13% 6% 166 / 226 Troms 9% 49% 23% 14% 5% 107 / 162 Finnmark 14% 39% 22% 14% 11% 51 / Andel (%) PSA<4 4 PSA<10 10 PSA<20 20 PSA<100 PSA>100 Figur 14 Gruppert PSA-verdi ved diagnosetidspunkt, fylker. Figur 14 Datakilde: Klinisk primærutredningsmelding Inklusjonskriterier: Diagnostisert prostatakreft, utfylt PSA-verdi ved diagnose i klinisk melding Diagnoseår: 2016 Rapporteringsgrad: 68% Fylke angitt i grått har en rapporteringsgrad under 60%, og resultat må tolkes med forsiktighet. Side 26 av 114
27 Median PSA Aldersgrupper Figur 15 Median PSA-verdi ved diagnosetidspunkt, aldersgrupper. Figur 15 Datakilde: Klinisk primærutredningsmelding Inklusjonskriterier: Diagnostisert prostatakreft, utfylt PSA-verdi ved diagnose i klinisk melding Diagnoseår: 2016 Rapporteringsgrad: 68% Side 27 av 114
28 3.3.2 Gleason score ved diagnosetidspunkt Figur 16 viser at det har vært relativt stabil fordeling av Gleason score ved diagnosetidspunktet for pasienter diagnostisert med prostatakreft i perioden (for definisjon av Gleason score se kapittel 3.1). Dette til tross for at en større andel av pasientene har lavere alder (jfr. figur 10) og lavere PSA-verdi ved diagnosetidspunktet (jfr. figur 13). Forklaringen er sannsynligvis dels justering av Gleason-graderingen, bedret bildediagnostikk og økende bruk av målrettede biopsier. Figur 17 viser fordeling av høyeste Gleason score i første vevsprøve som viser kreft ved patologilaboratoriene i Norge. Sammenlignet med funn i rapporter fra tidligere år, er fordelingen mellom Gleason scoren på landsbasis tilnærmet uendret, men det er fortsatt stor spredning i fordelingen av Gleason score mellom patologilaboratoriene. Det er ikke mulig å identifisere én enkeltårsak til forskjellene. Forskjeller i pasientgrunnlaget, variasjon i kvalitet og representativitet av biopsiene og forskjeller i fortolkning av kriteriene som ligger til grunn for Gleason-gradering kan bidra til ulikhetene. I tillegg kan varierende bruk av ultralyd og MR ved biopsitaking (målrettede biopsier) ved de forskjellige sykehusene bidra til forskjellene. Det virker ikke å være regionale forskjeller eller forskjeller mellom små og store sykehus. Sammenlignet med tidligere rapporteringer er det ingen enkeltsykehus som skiller seg vesentlig ut, og alle sykehus viser en viss variasjon i fordeling fra år til år. Dette kan bety at forskjellene skyldes naturlige variasjoner. Figur 18 sammenligner høyeste Gleason score i siste maligne vevsprøve før prostatektomi, med høyeste Gleason score i prostatektomipreparat. Sammenlignet med årsrapport for 2015 har samsvaret i Gleason score før og etter operasjon falt fra 74 % i 2015 til 52 % i 2016 på landsbasis. Denne nedgangen skyldes at man fra 2016 også skiller mellom Gleason score 7a og 7b, mens disse i 2015 ble vurdert som samme grad (Gleason grad 7). Manglende samsvar har flere årsaker, men reflekterer blant annet at svulster i prostata som oftest har variert vekstmønster (flere samtidige Gleason grader), og at biopsier fra slike svulster ofte representerer kun en liten del av den totale svulsten. I tillegg er kriteriene for Gleason-scoring av prostatabiopsier og prostatektomier utformet slik at man må forvente en viss andel avvik mellom dem. Forbedringer i bildediagnostikk og økende bruk av målrettede biopsier kan muligens gi bedre samsvar i fremtiden. Oppsummering: Fordeling av Gleason score ved diagnosetidspunktet har i Norge vært stabil over tid. Det observeres noe forskjell i fordeling av høyeste Gleason score ved diagnosetidspunktet mellom patologilaboratoriene i Norge, men på landsbasis har også denne fordelingen vært relativt stabil de seneste årene. Samsvaret mellom Gleason score i siste prøve før operasjon og i påfølgende prostatektomipreparat er om lag 50 %, og reflekterer i stor grad utfordringer knyttet til diagnostikk av prostatakreft. Forbedringer i bildediagnostikk og økende bruk av målrettede biopsier kan muligens gi bedre samsvar i fremtiden. Side 28 av 114
29 50 40 Andel (%) Diagnoseår 6 7a 7b Figur 16 Gruppert Gleason score ved diagnosetidspunkt. Figur 16 Datakilde: Prostatakreftregisteret, histologisvar etter biopsi/tur-p Inklusjonskriterier: Diagnostisert prostatakreft, kjent Gleason score i første maligne vevsprøve Diagnoseår: Side 29 av 114
30 Norge Helse Sør-Øst Oslo Universitetssykehus Furst Medisinsk Laboratorium Unilabs Laboratoriemedisin Sykehuset Østfold, Fredrikstad Sykehuset Telemark, Skien Sykehuset Innlandet, Lillehammer Vestre Viken, Drammen Sørlandet Sykehus, Kristiansand Ahus Sykehuset i Vestfold, Tønsberg Helse Vest HUS, Gades institutt Stavanger universitetssjukehus Helse Førde Helse-Fonna, Haugesund Helse Midt St. Olavs hospital Helse Møre og Romsdal, Molde Helse Møre og Romsdal, Ålesund Helse Nord UNN, Tromsø Nordlandssykehuset, Bodø 29% 26% 20% 15% 21% 22% 16% 24% 25% 37% 33% 21% 23% 23% 32% 7% 7% 19% 24% 24% 22% 25% 33% 29% 29% 32% 29% 27% 17% 14% 13% 38% 15% 11% 10% 21% 25% 5% 18% 24% 11% 22% 17% 11% 20% 23% 19% 35% 19% 12% 10% 27% 17% 10% 21% 26% 18% 13% 6% 23% 16% 25% 36% 16% 29% 13% 40% 31% 19% 27% 26% 31% 20% 21% 22% 19% 13% 13% 15% 8% 16% 17% 10% 28% 13% 15% 21% 10% 9% 16% 9% 17% 27% 20% 6% 15% 15% 17% 18% 16% Pasienter Meldt / Første vevsprøve 4351 / / / / / / / / / / / / / / / / / / / / Andel (%) 6 7a 7b Figur 17 Gleason score (høyeste) i første maligne vevsprøve. Norge og laboratorier. Figur 17 Datakilde: Prostatakreftregisteret, histologisvar etter vevsprøve. Inklusjonskriterier: Diagnostisert prostatakreft, kjent Gleason score Eksklusjon: De som ikke har vevsprøve Diagnoseår: 2016 Forklaring: Sykehus angitt med grå farge har en rapporteringsprosent på under 60%. Meldt = innsendt klinisk melding. Første vevsprøve = antall registrert via histologisvar. Side 30 av 114
31 Pasienter Norge 52% 30% 18% 1665 Sykehuset Telemark, Skien 65% 23% 12% 57 Helse-Fonna, Haugesund 59% 41% 22 Sykehuset Innlandet, Lillehammer 58% 21% 21% 157 Sørlandet Sykehus, Kristiansand 56% 34% 10% 70 St. Olavs hospital 56% 28% 16% 244 Oslo Universitetssykehus 56% 27% 17% 317 Sykehuset i Vestfold, Tønsberg 54% 30% 16% 89 HUS, Gades institutt 52% 29% 19% 73 Vestre Viken, Drammen 51% 32% 17% 125 Stavanger universitetssjukehus 50% 33% 17% 123 Furst Medisinsk Laboratorium 48% 31% 21% 54 UNN, Tromsø 47% 38% 15% 81 Ahus 47% 28% 25% 98 Sykehuset Østfold, Fredrikstad 41% 36% 23% 87 Nordlandssykehuset, Bodø 32% 54% 14% 41 Helse Førde 12% 65% 23% Andel (%) Samsvar Undergradert Overgradert Figur 18 Samsvar høyeste Gleason score i vevsprøve før prostatektomi, og høyeste Gleason score i prostatektomi. Figur 18 Datakilde: Histologisvar etter biopsi og prostatektomi Inklusjonskriterier: Diagnostisert prostatakreft og operert radikal prostatektomi. Siste maligne vevsprøve før operasjon og vevsprøve fra operasjon. Operasjonsår: 2016 Side 31 av 114
32 3.3.3 Risikogrupper ved diagnosetidspunkt Pasientens risikogruppe settes på bakgrunn av klinisk T-stadium (ct), PSA-verdi og Gleason-score. Sammen med alder og andre sykdommer, er risikogruppeeringen helt grunnleggende ved vurdering av prognose og behandling. Risikogrupperingen i rapporten er gjort på grunnlag av inndelingen til European Association of Urology (EAU) som gjaldt da pasientene ble diagnostisert. Figur 19 antyder at risikogrupperingen er ulikt fordelt mellom fylkene. Forskjellene kan både antyde ulik praksis i diagnostisk vurdering og ulik praksis ved rapportering, men også reell ulik geografisk fordeling. Få lavrisiko-svulster og mange høyrisiko-svulster kan også være uttrykk for en tendens til overvurdering av parameterne som inngår i risikogrupperingen. Vurderingen av diagnostisk kvalitet bør derfor vurderes med samsvar mellom Gleason-score og T-stadium før og etter operasjon (se figur 18 og figur 33). Tidligere ble svulstens størrelse (ct-stadium) vurdert kun på bakgrunn av DRE (digital rektal eksplorasjon) av prostata, som har lav spesifisitet og sensitivitet. Med innføring av MR-prostata må svulstens størrelse (ct) bestemmes på grunnlag av både DRE og MR-prostata, uten at det ennå er klart hvordan informasjonen skal vektes mot hverandre. Bruken av MR har variert mellom avdelinger og det finnes pr. i dag heller ikke nomogrammer 6 til hjelp ved MR-vurdering av stadier. Ved bruk av MR vil enhver synlig tumor få stadium ct2 eller høyere. Dette kan medføre at en pasient tidligere vurdert som ct1c ved DRE, vurderes som ct3 dersom en MR-undersøkelse av samme svulst legges til grunn. Dette vil igjen plassere den samme pasienten i en høyere risikogruppe til tross for at sykdomsstadiet og prognosen reelt sett er den samme. Pasienter diagnostisert med TUR-P 7 vil primært få stadium ct1a/b, selv om stadiet reelt sett ofte er høyere. Figur 20 viser derfor variasjoner som i stor grad kan skyldes metoden som ble brukt for å vurdere ct. Også ulik vurdering av Gleason-score mellom ulike laboratorier vil påvirke fordeling av risikogrupper (figur 17). Tendensen er at pasientene får en høyere Gleason-score etter endringen av Gleasonsystemet i 2006 x. Dette vil igjen kunne medføre en overvurdering av pasientens risiko for sykdomsrelatert død og videre overbehandling. Prostatakreftregisteret reviderte meldingene i I de reviderte meldingene skal ct basert på DRE, ct vurdert på MR og samlet vurdering av ct meldes separat, slik at man i fremtiden sikrere kan risikogruppere pasientene, og vi vil da også kunne vite mer sikkert om det finnes forskjeller i diagnostisk praksis og kvalitet. Det er også behov for risikogrupperinger som i større grad tar opp i seg dagens metoder for å stadievurdere pasientene, og som tar hensyn til flere faktorer, jfr. CAPRA (Cancer of the Prostata Risk Assessment) og NCCN (National Comprehensive Cancer Network). Videre må det etter hvert finnes prognostiske data for de ny-definerte risikogruppene. Oppsummering: Ulik praksis ved rapportering og bruk av MR, men også ulik vurdering av ct-stadium og Gleason-grad mellom sykehusene, kan bidra til ulik fordeling i risikogruppene mellom fylkene. En reell geografisk forskjell i sykdomsstadium kan likevel ikke utelukkes. 6 Et nomogram er en regelmotor og et grafisk hjelpemiddel for utregning. 7 TUR-P (trans uretral reseksjon av prostata), et inngrep via urinrøret der prostatas størrelse reduseres. Operasjonen har til hensikt å redusere prostatas størrelse, men kan også innebære at man oppdager prostatakreft tilfeldig. Side 32 av 114
33 Norge Helse Sør-Øst Sykehuset Østfold, Fredrikstad Vestre Viken, Bærum Ahus, Lørenskog Oslo Universitetssykehus Volvat, Oslo Sykehuset Innlandet, Kongsvinger Sykehuset Innlandet, Hamar Sykehuset Innlandet, Lillehammer Vestre Viken, Drammen Vestre Viken, Hønefoss Sykehuset i Vestfold, Tønsberg Sykehuset Telemark, Skien/Porsgrunn Sørlandet Sykehus Moelv Spesialistsenter Uro-Sør A/S Overnklinikken AS CuraMedica Spesialistsenter AS Helse Vest Helse-Fonna, Haugesund Stavanger universitetssjukehus Haraldsplass Diakonale Sykehus Haukeland universitetssykehus Volvat, Bergen Helse-Førde, Lærdal Helse-Førde, Førde Helse Midt Helse Møre og Romsdal, Kristiansund Helse Møre og Romsdal, Molde Helse Møre og Romsdal, Volda Helse Møre og Romsdal, Ålesund St. Olavs hospital Helse Nord-Trøndelag, Levanger Helse Nord Nordlandssykehuset, Bodø Helgelandsykehuset, Mosjøen UNN, Narvik UNN, Harstad UNN, Tromsø Finnmarkssykehuset, Hammerfest Finnmarkssykehuset, Kirkenes Tromsø Urologiske Spesialistsenter 19% 27% 18% 17% 15% 12% 13% 19% 33% 20% 26% 8% 23% 19% 10% 19% 8% 11% 18% 17% 14% 25% 14% 31% 12% 29% 27% 9% 13% 12% 23% 19% 15% 18% 9% 33% 17% 17% 37% 29% 43% 37% 38% 40% 42% 37% 29% 36% 47% 42% 48% 39% 37% 37% 43% 47% 49% 47% 59% 68% 52% 65% 61% 49% 59% 59% 48% 42% 55% 64% 51% 62% 100% 28% 34% 18% 33% 43% 43% 23% 26% 17% 38% 43% 25% 55% 41% 39% 43% 34% 33% 41% 43% 31% 27% 75% 57% 18% 29% 23% 11% 48% 50% 50% 40% 100% 44% 42% 73% 25% 66% Pasienter Meldt / Diagnostisert 2577 / / / / / / / / / / / / / / / / / / 51 2 / / / / / / 12 7 / / / / / / / / / 67 1 / / / / / 19 6 / Andel (%) Lav risiko Middels risiko Høy risiko Figur 19 Risikogrupper ved diagnosetidspunkt 8. Figur 19 Datakilde: Klinisk primærutredningsmelding, potensielt kurative pasienter Inklusjonskriterier: ct1-3 N0/NX M0, PSA 100 ng/ml, alder < 80 år og fravær av annen kreftdiagnose Eksklusjon: Spesialistsentre med færre enn 10 pasienter. Diagnoseår: 2016 Forklaring: Sykehus angitt med grå farge har en klinisk rapporteringsprosent på under 60%. Meldt: Antall pasienter hvor alle parametere for risikoklassifisering er meldt. Diagnostisert: Antall pasienter <80 år som er diagnostisert. 8 Tilsvarende figur, men fordelt på Norge og fylker, finnes som vedlegg Side 33 av 114
34 Norge Helse Sør-Øst Sykehuset Østfold, Fredrikstad Vestre Viken, Bærum Ahus, Lørenskog Oslo Universitetssykehus Volvat, Oslo Sykehuset Innlandet, Kongsvinger Sykehuset Innlandet, Hamar Sykehuset Innlandet, Lillehammer Vestre Viken, Drammen Vestre Viken, Hønefoss Sykehuset i Vestfold, Tønsberg Sykehuset Telemark, Skien/Porsgrunn Sørlandet Sykehus Moelv Spesialistsenter Uro-Sør A/S Overnklinikken AS CuraMedica Spesialistsenter AS Helse Vest Helse-Fonna, Haugesund Stavanger universitetssjukehus Haraldsplass Diakonale Sykehus Haukeland universitetssykehus Volvat, Bergen Helse-Førde, Lærdal Helse-Førde, Førde Helse Midt Helse Møre og Romsdal, Kristiansund Helse Møre og Romsdal, Molde Helse Møre og Romsdal, Volda Helse Møre og Romsdal, Ålesund St. Olavs hospital Helse Nord-Trøndelag, Levanger Helse Nord Nordlandssykehuset, Bodø Helgelandsykehuset, Mosjøen UNN, Narvik UNN, Harstad UNN, Tromsø Finnmarkssykehuset, Hammerfest Finnmarkssykehuset, Kirkenes Tromsø Urologiske Spesialistsenter 5% 18% 22% 19% 16% 14% 13% 20% 19% 24% 30% 27% 25% 28% 27% 24% 29% 34% 33% 26% 38% 36% 37% 36% 36% 38% 42% 41% 40% 46% 50% 54% 53% 54% 48% 23% 34% 42% 37% 43% 21% 34% 45% 38% 62% 49% 43% 36% 29% 67% 67% 43% 36% 31% 14% 44% 26% 47% 10% 44% 6% 54% 38% 80% 10% 35% 30% 60% 5% 71% 39% 6% 32% 32% 19% 8% 42% 29% 69% 24% 30% 34% 27% 10% 40% 26% 34% 5% 43% 21% 17% 25% 28% 6% 55% 10% 25% 15% 43% 10% 24% 20% 18% 6% 48% 46% 58% 100% 35% 7% 68% 24% 12% 10% 10% 9% 29% 9% 14% 33% Pasienter Meldt / Diagnostisert 3331 / / / / / / / / / / / / / / / / / / 58 7 / / / / / / / / / / / / / / / 81 1 / / / / / 25 6 / Andel (%) ct1 ct2 ct3 ct4 Figur 20 Klinisk tumorstadium (ct) 9. Figur 20 Datakilde: Klinisk primærutredningsmelding Inklusjonskriterier: ct1-3 N0/NX M0, PSA 100 ng/ml, alder < 80 år og fravær av annen kreftdiagnose, utfylt ct i klinisk primærutredningsmelding Eksklusjon: Spesialistsentre med færre enn 10 pasienter. Diagnoseår: 2016 Rapporteringsgrad: 68% Forklaring: Sykehus angitt med grå farge har en klinisk rapporteringsprosent på under 60%. Meldt: Antall pasienter hvor alle parametere for risikoklassifisering er meldt. Diagnostisert: Antall pasienter <80 år som er diagnostisert. 9 Fordeling av klinisk tumorstadium (ct) fordelt på fylker finnes som vedlegg Side 34 av 114
35 3.4 Behandling med kurativ intensjon Behandlingsvalg ved prostatkreft i Norge veiledes av Nasjonalt handlingsprogram for prostatakreft, utgitt av helsedirektorat xi, og Oncology guidelines for prostate cancer utgitt av den europeiske urologforeningen EAU xii Behandlingsvalg Kapittelet om behandlingsmuligheter innledes i det Nasjonale handlingsprogram for prostatakreft med følgende avsnitt: «Prostatakreft har mange fasetter og kan ha et dramatisk aggressivt forløp, men hos andre være langsomt utviklende og kan hos mange pasienter forbli ubehandlet uten at det utvikles kliniske symptomer. Vi vet at sykdomsutvikling er nøye relatert til PSA, Gleason score og T stadium [ ]. Behandlingsanbefalingene må basere seg på pasientens allmenntilstand, sykelighet, forventete levetid, pasientens egne forventninger til behandlingen, og vurdering av antatt behandlingsnytte opp mot risiko for bivirkninger. Valg av behandling er følgelig en prosess hvor pasienten i samråd med legen må ta stilling til forskjellige behandlingsalternativer.» Både prostatektomi (kirurgisk fjerning av prostatakjertelen) og høydosert strålebehandling er etablert som kurativ behandling av prostatakreft. Strålebehandling kombineres ofte med endokrin behandling («hormonell behandling»). Valg av behandling er sterkt avhengig av pasientens alder og kreftsvulstens risikoprofil. Yngre menn med lavrisikokreft blir oftere behandlet med prostatektomi, mens eldre menn med høyrisikokreft hyppigere får tilbud om strålebehandling xiii. Denne seleksjonen observeres også i Norge. Menn som blir operert har en median alder på 63 år og en gjennomsnittlig PSA på 10.1 ng/ml, mens menn som får primær strålebehandling har en median alder på 69 år og en gjennomsnittlig PSA på 14.8 ng/ml. Ikke-randomiserte studier kan ikke konkludere med om prostatektomi er bedre enn strålebehandling. xiv I fjor ble det for første gang publisert en prospektiv, randomisert studie xv som sammenlignet aktiv overvåkning, operasjon og strålebehandling. Denne studien inkluderte vesentlig pasienter med lav og middels/intermediær risiko. Den skandinaviske prostatakreftgruppen (SPCG) gjennomfører for tiden en randomisert studie som sammenligner prostatektomi og strålebehandling for lokalavansert høyrisikokreft (SPCG-15, NCT ). Flere norske sykehus deltar i studien. Behandling av prostatakreft gis vanligvis til hele prostatakjertelen. Med utvikling av multiparametrisk MR er vi i dag ofte i stand til nøyaktig å beskrive kreftutbredelsen i prostata. Dette vil i fremtiden åpne for fokal behandling (behandling kun av svulsten og ikke det friske vevet rundt). Metodene for fokal behandling som er under utvikling er high intensity focused utrasound (HIFU), cryoablasjon, radiofrekvensablasjon, laserablasjon, stereotaktisk strålebehandling og fokal brachyterapi. Per i dag er fokal behandling svært lite anvendt, men eksakte tall foreligger ikke. Aktiv overvåkning er i dag den viktigste strategien for å redusere unødvendig behandling for prostatakreft («overbehandling»). Aktiv overvåkning (AS, Active Surveillance) har som målsetting å unngå eller utsette kurativ behandling for dermed å unngå eller utsette unødvendige bivirkninger knyttet til behandlingen. Pasienter i AS følges med PSA-målinger, biopsier og i økende grad MR av prostata. Ved tegn til progresjon (forverring) av sykdommen avsluttes overvåkingen og pasienten får behandling med helbredende intensjon. Dersom sykdommen er stabil kan man unngå aggressiv behandling og etterhvert også avslutte oppfølgingen. De fleste pasienter i lavrisikogruppen regnes som gode kandidater for aktiv overvåkning, men også utvalgte pasienter med middels risiko kan følges opp på denne måten xvi. Registrering av AS i Prostatakreftregisteret kom først i gang i Mens andel menn rapportert med aktiv overvåkning har økt siden 2009 har andel menn i kategorien ubehandlet observasjon vært forholdsvis stabil. Samtidig faller andelen lav-risiko pasienter som behandles, noe som antyder at kodingen av aktiv overvåking og ubehandlet observasjon ikke er konsekvent. Alle resultater gjelder behandlinger gjennomført i Norge. Et økende antall pasienter søker i dag behandling i utlandet. Kreftregisteret har per i dag ikke opplysninger om disse behandlingene. Side 35 av 114
36 Fagmiljøet antar, med bakgrunn i muntlig kommunikasjon, at det kan dreie seg om >100 pasienter som på grunn av behandling i utlandet, ikke fanges opp i tabeller og figurer i kapittel 3. Andelen menn som fikk helbredende behandling (strålebehandling eller prostatektomi) var stabil fra med svak nedgang de siste årene (figur 21), men det observeres nå klart mindre behandling av lavrisikokreft og mer behandling av middels høy- og høyrisikokreft (figur 22). Denne utviklingen er ønskelig og blir her vist for alle helseregioner og for menn under 75 år. Bare for menn mellom 75 og 79 år øker andelen som får radikal behandling. For behandlingsårene vises en gradvis økning av andel menn < 70 år som opereres med prostatektomi og en korresponderende nedgang for menn som får strålebehandling (figur 21). Trenden er den samme i alle helseregioner (vedlegg 11-10). En stigende andel menn år tilbys behandling med kurativ intensjon, de fleste i form av strålebehandling (vedlegg 11-7). Det observeres fylkesvise forskjeller i bruk av de ulike behandlingsmodalitetene (vedlegg 11-9). Forskjellene vurderes som reelle, men tallene må likevel tolkes med forsiktighet på grunn av ikke komplett innrapportering av kliniske meldinger og forskjeller i utredning. I denne rapporten innføres to nye kvalitetsmål - 1) for andel menn som blir radikal behandlet til tross for lavrisiko prostatakreft (mål < 20%), og 2) for andel menn som behandles radikalt for høyrisiko prostatakreft (mål >70%). På grunn av sen innrapportering av strålebehandlingsdata kan det ikke oppgis nyere tall enn for behandlingsåret 2014 (figur 21). Resultatene for strålebehandling gjenspeiler derfor ikke praksis for Resultatet for alle pasientene samlet viser at andelen pasienter med lavrisiko prostatakreft som behandles radikalt er på et tilfredsstillende nivå. Andelen høyrisikopasienter som blir radikalt behandlet er også innenfor fagmiljøets målsetning. Andelen radikalt behandlet for de ulike risikogruppene er vist på pasientenes bostedsfylke. De fylkesvise forskjellene må tolkes med forsiktighet fordi det er forskjeller mellom enkelt år, i tillegg til en relativ lav innrapporteringsgrad. For videre redegjørelse av kvalitetsmål se avsnitt 6.2. Sammendrag: Andelen menn som gjennomførte behandling med kurativ intensjon har vært stabilt siste ti år. Bare for menn mellom år observeres en fortsatt økning i andelen radikal behandling. Det er tydelige endringer å se for risikogruppene: andel behandlete menn med lavrisikokreft er kontinuerlig fallende og andelen menn som ble behandlet for høyrisikokreft har steget lenge, men ser ut til ha stabilisert seg de siste årene, noe som er en ønsket utvikling. Side 36 av 114
37 50 40 Andel (%) Diagnoseår Prostatektomi Strålebehandling Aktiv overvåkning Ikke lokalbehandlet/annet Figur 21 Behandlingsvalg i Norge. 10 Figur 21 Datakilde: Klinisk informasjon, stråledata, histologisvar etter operasjons og klinisk primærutredningsmelding. Inklusjonskriterier: Diagnostisert prostatakreft, <80 år, stadium ct1-3, N0/NX, M0, PSA 100 ng/ml, og fravær av annen kreftdiagnose. Diagnosesår: Dekningsgrad: >99% 10 Tilsvarende figur fordelt på aldersgrupper finnes som vedlegg Side 37 av 114
38 60 Lav risiko, Antall siste år = Middels risiko, Antall siste år = Andel (%) 30 Andel (%) Diagnoseår Diagnoseår 60 Høy risiko, Antall siste år = Andel (%) Prostatektomi Strålebehandling Aktiv overvåkning Ikke lokalbehandlet/annet Diagnoseår Figur 22 Behandlingsvalg, fordelt på risikogrupper. Registrering av aktiv overvåkning begynte i Figur 22 Datakilde: Klinisk informasjon, stråledata, histologisvar etter operasjons og klinisk primærutredningsmelding Inklusjonskriterier: Diagnostisert prostatakreft, <80 år, stadium ct1-3, N0/NX, M0, PSA 100 ng/ml, fravær av annen kreftdiagnose Diagnoseår: Dekningsgrad: >99% 11 Tilsvarende figur i tabellform fordelt på behandlingsvalg og risikogrupper finnes som vedlegg I tillegg finnes vedlegg 11-9 med oversikt behandlingsvalg, fylke og risikogrupper, og vedlegg med oversikt over behandlingsvalg fordelt på helseforetak, Side 38 av 114
39 Norge 77% Pasienter 483 Sogn og Fjordane Østfold Vest-Agder 100% 100% 100% Telemark Møre og Romsdal Oslo Oppland 94% 93% 89% 89% Aust-Agder Nord-Trøndelag Akershus Buskerud Nordland Sør-Trøndelag Rogaland 83% 82% 77% 74% 74% 73% 71% Vestfold 64% 14 Hordaland Hedmark 56% 59% Finnmark 50% 6 Troms 38% Andel (%) Figur 23 Aktiv overvåking for lav-risikogruppen, Norge og fylker. Figur 23 Datakilde: Prostatakreftregisteret, klinisk primærutredningsmelding Inklusjonskriterier: Diagnostisert prostatakreft, <80 år, stadium ct1-3, N0/NX, M0, PSA 100 ng/ml, fravær av annen kreftdiagnose Diagnoseår: 2015 og 2016 Rapporteringsgrad: 68% Lav total andel på grunn av mangelfull rapportering til Kreftregisteret. Figuren viser andelen pasienter det var mulig å risikogruppere. Side 39 av 114
40 Norge 17% Pasienter 578 Vestfold 0% 18 Telemark Akershus 7% 8% Hedmark Vest-Agder Sogn og Fjordane Sør-Trøndelag Hordaland Oslo Østfold Møre og Romsdal Oppland Buskerud Aust-Agder Rogaland Nord-Trøndelag Troms 13% 14% 15% 16% 16% 17% 18% 19% 19% 20% 21% 22% 22% 23% Nordland Finnmark 30% 33% Andel (%) Figur 24 Radikalt behandlede, lavrisikogruppen 12. Norge og fylker. Figur 24 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Diagnostisert prostatakreft, <80 år, stadium ct1-3, N0/NX, M0, PSA 100 ng/ml, fravær av annen kreftdiagnose Behandlingsår: 2013 og Kvalitetsmål: 20% Lav total andel på grunn av mangelfull rapportering til Kreftregisteret. Figuren viser andelen pasienter det var mulig å risikogruppere. 12 Begrunnelse for valg av kvalitetsmål finnes i avsnitt Side 40 av 114
41 Norge 76% Pasienter 1050 Nord-Trøndelag Hordaland Troms Oppland Finnmark Møre og Romsdal Rogaland Sogn og Fjordane Aust-Agder Telemark Buskerud Sør-Trøndelag Vest-Agder Vestfold Akershus Oslo 90% 90% 89% 88% 88% 87% 84% 80% 79% 77% 77% 76% 75% 74% 70% 69% Nordland 63% 32 Østfold Hedmark 57% 55% Andel (%) Figur 25 Radikalt behandlede, høyrisikogruppen 13. Norge og fylker. Figur 25 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Diagnostisert prostatakreft, <80 år, stadium ct1-3, N0/NX, M0, PSA 100 ng/ml, fravær av annen kreftdiagnose Behandlingsår: 2013 og 2014 Kvalitetsmål: 70% Lav total andel på grunn av mangelfull rapportering til Kreftregisteret. Figuren viser andelen pasienter det var mulig å risikogruppere. 13 Begrunnelse for valg av kvalitetsmål finnes i avsnitt Side 41 av 114
42 Norge 51% 46% Pasienter 1363 Helse Sør-Øst Ahus, Lørenskog 55% 43% 64 Oslo Universitetssykehus 45% 53% 448 Sykehuset Innlandet, Hamar 61% 38% 196 Vestre Viken, Drammen 65% 31% 90 Sykehuset i Vestfold, Tønsberg 29% 71% 82 Sykehuset Telemark, Skien/Porsgrunn 60% 36% 79 Sørlandet Sykehus 50% 50% 15 Helse Vest Stavanger universitetssjukehus 49% 47% 72 Haukeland universitetssykehus 8% 60% 32% 93 Helse Midt St. Olavs hospital 50% 49% 119 Helse Nord Nordlandssykehuset, Bodø 56% 44% 32 UNN, Tromsø 12% 43% 45% Andel (%) Lav risiko Middels risiko Høy risiko Figur 26 Risikogruppering (preoperativt) av prostatektomerte pasienter, operasjonssykehus. Figur 26 Datakilde: Klinisk primærutredningsmelding Inklusjonskriterier: Mottatt utfylt klinisk radikal prostatektomimelding, <80 år, ct1-3, N0/NX, M0, PSA 100ng/mL, WHO-status0-1 og fravær av annen kreftdiagnose. Diagnoseår: 2016 Rapporteringsgrad: 68% Lav total andel på grunn av mangelfull rapportering til Kreftregisteret. Figuren viser andelen pasienter det var mulig å risikogruppere. Side 42 av 114
43 Norge Østfold Akershus Oslo Hedmark Oppland Buskerud Vestfold 40% 42% 40% 38% 42% 45% 44% 40% Pasienter Telemark 55% 157 Aust-Agder 28% 67 Vest-Agder 34% 67 Rogaland 45% 250 Hordaland 24% 263 Sogn og Fjordane 33% 58 Møre og Romsdal 51% 229 Sør-Trøndelag 32% 146 Nord-Trøndelag 47% 89 Nordland Troms 41% 42% Finnmark 35% Andel (%) Figur 27 Radikal prostatektomi. Bostedsfylke og Norge 14. Figur 27 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Alle kurative pasienter <80 år, stadium ct1-3, N0/NX, M0, PSA 100 ng/ml, og fravær av annen kreftdiagnose Diagnoseår: 2014 og 2015 (pasienter operert til og med 2016) Dekningsgrad: >99% Med «pasienter» menes antall pasienter Kreftregisteret har data til å risikovurdere. 14 Oversikt over alle radikale prostatektomier utført ved sykehus i Norge i perioden finnes som vedlegg Side 43 av 114
44 Norge 24% Pasienter 3061 Østfold Akershus Oslo Hedmark 19% 20% 19% 19% Oppland 28% 160 Buskerud Vestfold Telemark 14% 15% 18% Aust-Agder 25% 83 Vest-Agder Rogaland Hordaland 33% 34% 36% Sogn og Fjordane Møre og Romsdal Sør-Trøndelag Nord-Trøndelag Nordland Troms Finnmark 22% 25% 25% 26% 26% 20% 23% Andel (%) Figur 28 Kurativ strålebehandling, fylker. Figur 28 Datakilde: Stråledata Inklusjonskriterier: Alle kurative pasienter <80 år, stadium ct1-3, N0/NX, M0, PSA 100 ng/ml, fravær av annen kreftdiagnose og datagrunnlag for å risikovurdering. Diagnoseår: 2013 og 2014 Andel pasienter Kreftregisteret har data til å risikovurdere. Side 44 av 114
45 3.4.2 Radikal prostatektomi Ved radikal prostatektomi fjernes hele prostata, og hele, eller deler av, sædblærene. Inngrepet gjøres i narkose, enten som robotassistert laparoskopisk prostatektomi (kikkhullsoperasjon) eller som åpen kirurgi. Andelen lavrisikopasienter som behandles med radikal prostatektomi er stadig fallende (figur 29). I årets rapport vises også innenlands pasientmigrasjon, som viser at pasienter i all hovedsak får utført operativ behandling for sin prostatakreft innenfor egen region (figur 30). Klinisk stadievurdering (ct) viser fortsatt stor variasjon, større enn forventet ut fra forskjeller i pasientpopulasjonen (figur 31). Postoperativ stadievurdering av prostatasvulsten (pt) viser noe mindre variasjon (figur 32), hvilket samlet indikerer forskjeller mellom institusjonene i anvendelse av klassifiseringsverktøyene. Spesielt vet vi at praksis varierer i bruk av MR i fastsettelse av ct. Samsvar mellom preoperativ stadievurdering og postopertivt stadium etter histologisk undersøkelse av prostatektomipreparatet er mindre variert (figur 33). For landet som helhet 67%, med variasjon mellom sykehusene fra 58% - 80%. Undergradering er fortsatt klart viktigste årsak til manglende samsvar, for 26% av pasientene. Fra og med 2017 skal MR-vurdering inngå i rapporteringen til Prostatakreftregisteret, slik at slike forskjeller kan synliggjøres. Sammendrag: Andel menn som opereres for lavrisikokreft er fortsatt fallende, samtidig som antall menn som opereres for høyrisikosykdom er stigende. Pasientene får i all hovedsak sin behandling i egen region. Det er fortsatt stor variasjon i preoperativ stadievurdering, hvilket kan tilskrives forskjeller i implementering av MR i stadievurderingen før operasjon. Side 45 av 114
46 Andel (%) Figur 29 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Kurative pasienter som har fått utført prostatektomi <80 år, stadium ct1-3, N0/NX, M0, PSA 100 ng/m og fravær av annen kreftdiagnose Diagnoseår: Diagnoseår Lav risiko Middels risiko Høy risiko Figur 29 Prostatektomi i de ulike risikogruppene. Antall Fylke Østfold Akershus Oslo Hedmark Oppland Buskerud Vestfold Telemark Aust-Agder Vest-Agder Rogaland Hordaland Sogn og Fjordane Møre og Romsdal Sør-Trøndelag Nord-Trøndelag Nordland Troms Finnmark Sykehus Andel Ahus, Lørenskog 5% Oslo Universitetssykehus 26% Sykehuset Innlandet, Hamar 11% Vestre Viken, Drammen 6% Sykehuset i Vestfold, Tønsberg 6% Sykehuset Telemark, Skien/Porsgrunn 5% Sørlandet Sykehus 4% Stavanger universitetssjukehus 6% Haukeland universitetssykehus 10% St. Olavs hospital 15% Nordlandssykehuset, Bodø 2% UNN, Tromsø 6% Figur 30 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Fått utført prostatektomi Operasjonsår: 2016 Helseregion: Sør-Øst Vest Midt Nord Figur 30 Pasientmigrasjon for operasjon 2016, bostedsfylke Andel pasienter behandlet i utlandet vises ikke. Side 46 av 114
47 Norge 69% 30% Pasienter 1363 Helse Sør-Øst Ahus, Lørenskog 85% 15% 64 Oslo Universitetssykehus 63% 36% 448 Sykehuset Innlandet, Hamar 73% 27% 196 Vestre Viken, Drammen 83% 17% 90 Sykehuset i Vestfold, Tønsberg 45% 55% 82 Sykehuset Telemark, Skien/Porsgrunn 79% 21% 79 Sørlandet Sykehus 53% 47% 15 Helse Vest Stavanger universitetssjukehus 71% 29% 72 Haukeland universitetssykehus 86% 14% 93 Helse Midt St. Olavs hospital 59% 41% 119 Helse Nord Nordlandssykehuset, Bodø 94% 6% 32 UNN, Tromsø 69% 31% Andel (%) ct1-2 ct3 Figur 31 Preoperativ klinisk tumorstadium (ct) for 2016, sykehus 16. Figur 31 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Mottatt utfylt klinisk prostatektomimelding. Diagnoseår: 2016 Rapporteringsgrad: 75% Kliniske prostatektomimeldinger rapportert etter er ikke inkludert i denne figuren på grunn av revidert utforming på skjema. 16 Tilsvarende figur fordelt på fylker finnes som vedlegg Side 47 av 114
48 Pasienter Meldt / Operert Norge 55% 45% 1819 / 1826 Helse Sør-Øst Ahus, Lørenskog 71% 29% 89 / 89 Oslo Universitetssykehus 40% 59% 468 / 470 Sykehuset Innlandet, Hamar 54% 46% 199 / 199 Vestre Viken, Drammen 52% 48% 104 / 104 Sykehuset i Vestfold, Tønsberg 38% 61% 101 / 103 Sykehuset Telemark, Skien/Porsgrunn 54% 46% 94 / 94 Sørlandet Sykehus 54% 46% 76 / 76 Helse Vest Stavanger universitetssjukehus 55% 45% 108 / 108 Haukeland universitetssykehus 67% 33% 172 / 174 Helse Midt St. Olavs hospital 71% 29% 266 / 267 Helse Nord Nordlandssykehuset, Bodø 70% 30% 33 / 33 UNN, Tromsø 69% 31% 109 / Andel (%) Figur 32 Fordeling patologisk tumorstadium (pt) pr. sykehus. Figur 32 Datakilde: Prostatakreftregisteret, histologisvar etter prostatektomi Inklusjonskriterier: Fått utført prostatektomi Operasjonsår: 2016 Rapporteringsgrad: 100% pt2 pt3 Side 48 av 114
49 Norge 66% 26% 8% Pasienter 1318 Sykehuset i Vestfold, Tønsberg 79% 18% 68 Nordlandssykehuset, Bodø 78% 22% 32 St. Olavs hospital 73% 10% 17% 120 Haukeland universitetssykehus 73% 24% 89 UNN, Tromsø 72% 15% 13% 67 Ahus, Lørenskog 71% 24% 5% 59 Sykehuset Innlandet, Hamar 67% 27% 6% 195 Sykehuset Telemark, Skien/Porsgrunn 65% 28% 7% 78 Stavanger universitetssjukehus 63% 27% 10% 71 Oslo Universitetssykehus 61% 32% 7% 438 Sørlandet Sykehus 60% 27% 13% 15 Vestre Viken, Drammen 59% 37% Andel (%) Samsvar Undergradert Overgradert Figur 33 Samsvar klinisk tumorstadium (ct) og patologisk tumorstadium (pt). Figur 33 Datakilde: Prostatakreftregisteret, klinisk primærutredningsmelding og histologisvar etter prostatektomi Inklusjonskriterier: Mottatt klinisk primærutredningsmelding og fått utført prostatektomi Operasjonsår: 2016 Side 49 av 114
50 Lymfeknutedisseksjon under radikal prostatektomi Utvidet lymfeknutedisseksjon 17 anbefales hos alle pasienter som får utført radikal prostatektomi for høyrisiko prostatakreft, samt for intermediær/middels risiko der man vurderer at risiko for lymfeknutemetastaser er > 5% (EAU Guidelines). For enkeltpasienter kan det være medisinske grunner for å fravike denne anbefalingen, men for årets rapport har referansegruppen satt 80% som mål til etterlevelse for høyrisikopasienter. For 2016 ser vi en positiv utvikling ved at flere pasienter får utført lymfeknutedisseksjon. Oslo universitetssykehus ligger under målet på 80%, og en mulig årsak til dette kan være at Oslo får tilsendt pasienter fra hele landet, når operasjonen er mer komplisert. Norge 87% Pasienter 493 Stavanger universitetssjukehus 100% 23 Vestre Viken, Drammen 100% 22 Haukeland universitetssykehus 100% 39 St. Olavs hospital 100% 53 Sykehuset i Vestfold, Tønsberg 98% 46 Ahus, Lørenskog 95% 24 Nordlandssykehuset, Bodø 93% 17 Sykehuset Innlandet, Hamar 89% 46 Sykehuset Telemark, Skien/Porsgrunn 83% 27 UNN, Tromsø 82% 38 Oslo Universitetssykehus 70% Andel (%) Figur 34 Lymfeknutedisseksjoner 18/19 under prostatektomi, høyrisiko (vurdert før operasjon) 20 Figur 34 Datakilde: Prostatakreftregisteret, histologisvar etter operasjon Inklusjonskriterier: Pasienter <80 år, stadium ct1-3, N0/NX, M0, PSA 100 ng/ml og fravær av annen kreftdiagnose som har fått utført lymfeknutedisseksjon under prostatektomi Operasjonsår: 2015 og 2016 Dekningsgrad: >99% Kvalitetsmål: 80% 17 Utvidet lymfeknutedisseksjon = fjerning av alle nærliggende lymfeknuter for å oppdage spredning 18 Tabell med oversikt over antall prostatektomier i de ulike risikogruppene, og hvorvidt det er uført lymfeknutedisseksjon for operasjonsår , finnes som vedlegg Tabell over antall lymfeknutedisseksjoner under prostatektomi, og antall negative/positive funn for operasjonsår , finnes som vedlegg Begrunnelse for valg av kvalitetsmål finnes i avsnitt Side 50 av 114
51 Reseksjonrender i radikal prostatektomi Ufrie reseksjonrender innebærer at det er kreftceller igjen etter operasjon eller at marginen mellom svulsten som er fjernet og gjenværende vev er for liten. Dette gir økt risiko for tilbakefall som kun vises med stigende PSA, og innebærer at pasienten trenger strålebehandling etter operasjon med belastende bivirkninger som konsekvens. Det er forventet at flere operasjoner ved lokalavansert prostatakreft (T3-T4) vil gi økt andel ufri reseksjonsrand i denne pasientgruppen. I gruppen lokalisert prostatakreft (T1-T2) er målsettingen at det operative inngrepet er kurativt, med frie reseksjonrender. Vi ser da også av figurene at andelen ufri rand er klart lavere ved T2 enn ved T3 (figur 35 og figur 36). For årets rapport har vi innført som kvalitetsmål at andelen pasienter som har ufri rand etter operasjon ved pt2 bør være under 20%. Tilsvarende mål for ufri rand ved pt3 ble ikke satt, men fremmet som et utviklingsmål. For en redegjørelse for valg av kvalitetsmål se avsnitt 6.2. Årets rapport viser en nokså betydelig variasjon mellom institusjoner, for både pt2 (5% - 32%) og pt3 (22% - 63%). Det er også variasjon innen samme institusjon fra (vises som horisontal klammer ved hver søyle). En tolkning av forskjellene mellom hver institusjon og det nasjonale gjennomsnittet skal gjøres med forsiktighet på grunn av naturlig variasjon i pasientgrunnlaget. Det er viktig å være oppmerksom på at økt fokus på funksjonelt resultat etter operasjon (eksempelvis så lite nerveskader som mulig) kan bidra til at andelen pasienter med ufri reseksjonsrand varierer. De nylig reviderte meldeskjemaene til prostatakreftregisteret tar hensyn til dette ved at sykehuset kan registrere om det er brukt nervesparende prosedyre ved operasjonen. Side 51 av 114
52 Norge 15% Pasienter Meldt / Operert 986 / 1012 Sykehuset i Vestfold, Tønsberg 5% 38 / 38 Haukeland universitetssykehus 6% 114 / 116 Vestre Viken, Drammen 6% 52 / 54 UNN, Tromsø 11% 73 / 75 Oslo Universitetssykehus 11% 184 / 195 Stavanger universitetssjukehus 12% 58 / 59 Sykehuset Telemark, Skien/Porsgrunn 14% 51 / 51 Ahus, Lørenskog 15% 61 / 63 St. Olavs hospital 21% 184 / 188 Sykehuset Innlandet, Hamar 24% 108 / 108 Nordlandssykehuset, Bodø 27% 22 / 24 Sørlandet Sykehus 32% 41 / Andel ufri margin (%) Figur 35 Ufri reseksjonsrand for prostatektomier ved pt2 prostatakreft 21. Figur 35 Datakilde: Prostatakreftregisteret, histologisvar etter operasjon Inklusjonskriterier: Prostatektomier, pt2 Operasjonsår: 2015 og 2016 Dekningsgrad: >99% Kvalitetsmål: 20% Meldt er antall pasienter Kreftregisteret har mottatt histologisvar etter operasjon. 21 Begrunnelse for valg av kvalitetsmål finnes i avsnitt Side 52 av 114
53 Norge 35% Pasienter Meldt / Operert 791 / 814 Vestre Viken, Drammen 22% 46 / 49 UNN, Tromsø 22% 32 / 34 Sørlandet Sykehus 26% 35 / 35 Oslo Universitetssykehus 27% 274 / 283 Sykehuset i Vestfold, Tønsberg 30% 60 / 62 Haukeland universitetssykehus 35% 54 / 56 Sykehuset Telemark, Skien/Porsgrunn 35% 43 / 43 Sykehuset Innlandet, Hamar 40% 88 / 90 Nordlandssykehuset, Bodø 40% 10 / 10 Stavanger universitetssjukehus 54% 48 / 49 St. Olavs hospital 58% 77 / 78 Ahus, Lørenskog 63% 24 / Andel ufri margin (%) Figur 36 Ufri reseksjonsrand for prostatektomier ved pt3 prostatakreft. Figur 36 Datakilde: Prostatakreftregisteret, histologiremisse etter prostatektomi Inklusjonskriterier: Prostatektomier, pt3 Operasjonsår: 2015 og 2016 Dekningsgrad: >99% Mål: Ikke satt Meldt er antall pasienter Kreftregisteret har mottatt histologisvar etter operasjon. Side 53 av 114
54 3.4.3 Strålebehandling Strålebehandling som primærbehandling Strålebehandling som primærbehandling innebærer at pasienten får strålebehandling med kurativ intensjon istedenfor operasjon. Høyt dosert strålebehandling med kurativ intensjon kan gis som ekstern strålebehandling, brachyterapi 22, eller som kombinasjon av de to teknikkene. Denne rapporten skiller ikke mellom de ulike typene stråleteknikker som kan brukes. For pasienter med middels/intermediær- eller høyrisikokreft kombineres strålebehandlingen som regel med endokrin behandling («hormonell behandling»). Strålebehandling gis mot hele prostatakjertelen og avhengig av sykdommens risikoprofil inkluderes deler av, eller hele sædblærene (vesiculae seminales). Ved høy risiko for spredning til lymfeknuter kan også bekkenlymfeknuter inngå i behandlingsområdet. Tross økende antall prostatakreftdiagnoser har antallet pasienter som gjennomførte primær strålebehandling i perioden (vedlegg 11-8) falt. Også andelen pasienter med nyoppdaget prostatakreft som ble primært strålebehandlet har derfor falt. Utviklingen kan observeres i alle helseregioner uavhengig av klinisk risikogruppe. Bare i aldersgruppen år observeres fortsatt økende bruk av strålebehandling (figur 3 i vedlegg). Sammendrag: Både absolutt antall og andel menn som gjennomførte primær kurativt strålebehandlet av totalt antall behandlet med kurativ intensjon har gått ned. 22 Brachyterapi = Indre strålebehandling, der en strålekilde plasseres i eller i nærheten av svulsten Side 54 av 114
55 Andel (%) Diagnoseår Lav risiko Middels risiko Høy risiko Figur 37 Kurativ strålebehandling i de ulike risikogruppene. Figur 37 Datakilde: Stråledata Inklusjonskriterier: Mottatt kurativ strålebehandling Diagnoseår: Side 55 av 114
56 Postoperativ strålebehandling Postoperativ strålebehandling er strålebehandling som gis etter operasjon. Strålebehandlingen gis enten adjuvant eller som salvage behandling. Adjuvant strålebehandling er en tilleggsbehandling som gis direkte etter operasjon (som regel innen 6 måneder). For at behandlingen skal kalles adjuvant kan det ikke være påvist restsykdom eller målbar PSA etter operasjon. Salvage strålebehandling gis ved gjenværende sykdom eller ved tilbakefall opp til tre år etter behandling og har fortsatt kurativ intensjon. Datagrunnlaget for denne rapporten gjør det ikke mulig å skille mellom adjuvant og salvage stråling og registeret bruker derfor det samlende begrepet «postoperativ strålebehandling» for all strålebehandling som er utført inntil 3 år etter radikal operasjon. Strålefeltet ved postoperativ strålebehandling inkluderer alltid operasjonsfeltet («prostatasengen» eller «prostatatomten»), men kan også omfatte et større bekkenfelt for å dekke eventuelle lymfeknutemetastaser. Holdningen til postoperativ strålebehandling har variert over tid og mellom behandlingssteder. Mens noen pasienter har fått umiddelbar stråling ved ufri margin etter operasjon, selv om PSA ikke har vært målbar (PSA < 0,2 ng/ml), har andre avdelinger avventet utvikling av målbar PSA hos pasienten. Videre vil også hyppigheten av kontroller være bestemmende for hvor raskt tilbakefall i form av stigende PSA oppdages og dermed hvor raskt pasienten eventuelt får salvage strålebehandling. Postoperativ stråling øker risikoen for kronisk urinlekkasje, endetarmsproblemer og ereksjonsproblemer, men kan være en del av en planlagt multimodal behandling hos pasienter med høyrisikosykdom. Høy Gleason score og høyt T-stadium øker risikoen for ufri margin etter operasjon og spredning til lymfeknutene (N+-sykdom), og øker dermed behovet for postoperativ stråling. Dersom et sykehus behandler mange lavrisiko pasienter vil dette også kunne gi en lav andel postoperativ strålebehandling ved sykehuset. Bruk av postoperativ stråling som kvalitetsmarkør har dermed sine begrensninger, ikke minst med tanke på vurdering av forskjeller mellom avdelinger. Andelen menn som har fått postoperativ strålebehandling har økt frem til 2009 (figur 38). Etter 2009 ligger andelene tilsynelatende stabilt på et lavere nivå. Det er viktig å vise hvor lang tid etter operasjon strålebehandlingen blir gitt. Postoperativ strålebehandling er derfor delt opp i 3 intervaller, de som får strålebehandling fra 0-1 år etter operasjon, 1-2 år etter operasjon, og 2-3 år etter operasjon. Vi vet at postoperativ behandling forekommer senere enn tre år etter operasjon. xvii Observasjonsintervallet på 3 år medfører at resultatene ikke nødvendigvis reflekterer dagens praksis. Den økende andelen menn med intermediær/middels og høyrisikokreft som ble operert har økt behovet for postoperativ strålebehandling. figur 39 viser andelen menn som fått strålebehandling etter operasjon for pt2 svulst, og viser store variasjoner i landet sammenlignet med landsgjennomsnittet. Andelen menn som strålebehandles etter operasjon for lokalavansert kreft (stadium pt3) var 32% for operasjonsår 2012 (figur 40) og 60% for menn operert for høy risikokreft med ufrie marginer (figur 41). Forskjellene mellom sykehus må tolkes forsiktig, men indikerer trolig ulik praksis med tanke på indikasjonsstilling og oppfølging av pasientene. Oppsummering: Bruken av postoperativ strålebehandling synes å gå noe ned for pasienter operert etter En tredje del av menn som ble operert for lokalavansert kreft (pt3) i 2012 måtte gjennomføre postoperativ strålebehandling innen tre år. De betydelige forskjellene mellom sykehusene tyder på ulik behandlingspraksis. Side 56 av 114
57 25 20 Andel bestrålt postoperativt(%) % 3% 3% 5% 3% 4% 4% 3% 5% 4% 7% 7% 3% 5% 11% 3% 5% 9% 2% 4% 12% 2% 4% 3% 11% 10% 10% 5 5% 5% 5% Operasjonsår Tid etter operasjon: 1 år 2 år 3 år Figur 38 Pasienter som fikk postoperativ strålebehandling 23. Figur 38 Datakilde: Histologisvar etter operasjon og stråledata Inklusjonskriterier: Mottatt postoperativ strålebehandling Behandlingsår: Oversikt over antall pasienter som har fått postoperativ strålebehandling fordelt på de regionale helseforetakene, operasjonsår , finnes som vedlegg Side 57 av 114
58 Norge 7% pt2 Pasienter 1466 Helse Sør-Øst Vestre Viken, Hønefoss 0% 38 Vestre Viken, Drammen 2% 45 Vestre Viken, Bærum 3% 31 Sørlandet Sykehus 4% 80 Oslo Universitetssykehus 6% 442 Sykehuset i Vestfold, Tønsberg 10% 61 Ahus, Lørenskog 14% 72 Sykehuset Innlandet, Hamar 37 Helse Vest Helse-Fonna, Haugesund 0% 11 Haukeland universitetssykehus 5% 102 Stavanger universitetssjukehus 8% 106 Helse-Førde, Førde 18% 11 Helse Midt St. Olavs hospital 4% 277 Helse Nord UNN, Tromsø 9% 126 Nordlandssykehuset, Bodø 13% Andel (%) Tid etter operasjon: 1 år 2 år 3 år Figur 39 Postoperativ strålebehandling ved stadium pt2 pr. opererende sykehus. Figur 39 Datakilde: histologisvar etter operasjon og stråledata Inklusjonskriterier: Mottatt postoperativ strålebehandling, stadium pt2 Operasjonsår: 2011 og 2012, tre års observasjonstid Sykehuset Innlandet, Hamar har inkomplett innrapportering av bl.a. patologisk stadium (pt) og angis derfor uten andel. Side 58 av 114
59 Norge 32% pt3 Pasienter 1151 Helse Sør-Øst Sørlandet Sykehus Vestre Viken, Drammen Vestre Viken, Hønefoss 21% 22% 24% Oslo Universitetssykehus Sykehuset i Vestfold, Tønsberg 31% 33% Vestre Viken, Bærum Sykehuset Innlandet, Hamar Ahus, Lørenskog Helse Vest 44% 47% Stavanger universitetssjukehus 32% 72 Haukeland universitetssykehus Helse Midt 43% 30 St. Olavs hospital Helse Nord 26% 101 UNN, Tromsø Nordlandssykehuset, Bodø 42% 42% Andel (%) Tid etter operasjon: 1 år 2 år 3 år Figur 40 Postoperativ strålebehandling ved lokalavansert prostatakreft stadium pt3 pr. opererende sykehus. Figur 40 Datakilde: Histologisvar etter operasjon eller klinisk kirurgimelding, stråledata. Inklusjonskriterier: Mottatt postoperativ strålebehandling, stadium pt3 Operasjonsår: 2011 og 2012, tre års observasjonstid Sykehuset Innlandet, Hamar har inkomplett innrapportering av bl.a. patologisk stadium (pt) og angis derfor uten andel. Side 59 av 114
60 Lav risiko, N = 470 Middels risiko, N = Andel (%) 30 Andel (%) Tid siden operasjon (år) Tid siden operasjon (år) Høy risiko, N = Andel (%) Fri rand Ufri rand Tid siden operasjon (år) Figur 41 Postoperativ strålebehandling for de ulike risikogruppene, opp til 3 år etter operasjon. Figur 41 Datakilde: Histologisvar etter operasjon og stråledata Inklusjonskriterier: Mottatt postoperativ strålebehandling Operasjonsår: 2012 Side 60 av 114
61 3.5 Dødelighet, dødsårsaker og overlevelse Prostatakreftbehandling har en svært lav dødelighet som en direkte følge av utredning og behandling. I Norge er det på landsbasis null til ett dødsfall årlig innen 30 dager etter prostatektomi. I rapporten er det derfor ikke vist analyser på dette med sammenligninger på sykehus- eller fylkesnivå. Sannsynligheten for å dø av prostatakreft versus andre årsaker er analysert i figur 42. Alle disse dødsårsakene øker kraftig med alder. Kvaliteten av dødsårsak-kodingen er usikker hos de eldste, men i aldersgruppene opp til 79 år er det sannsynlig at årsaken til død er ført korrekt på dødsattesten. For pasienter som får helbredende behandling er det lite forskjeller i prostatadødelighet mellom ulike aktive behandlingsvalg (figur 43). Dette inkluderer også pasientgruppen som fikk overvåkning, hvor dødeligheten også er veldig lav. For de ulike risikogruppene er det imidlertid som forventet forskjeller i sannsynligheten for å dø av prostatakreft (figur 44). Den relative overlevelsen 5 år etter operasjon er svært god selv for høyrisikopasienter og er ca 98%. De nordligste fylkene ser ut til å ha en trend med lavere relativ overlevelse i høyrisikogruppen (figur 45) men dette er ikke signifikant og kan skyldes tilfeldigheter. Figuren for relativ overlevelse for pasienter med spredning ved diagnosetidspunkt (figur 47) viser et nasjonalt nitt på 36%, og dette kan indikere forskjeller i behandlingsvalg mellom fylkene. Funnene kan imidlertid også skyldes tilfeldig variasjon siden konfidensintervallene for alle fylker overlapper med konfidensintervallene for landsgjennomsnittet. Sammendrag: Beregninger av overlevelse etter en prostatakreftdiagnose i et populasjonsbasert materiale må ta hensyn til risikogrupper, alder, behandling samt død av andre årsaker. Noen forskjeller i overlevelse mellom fylkene kan sees, men disse kan skyldes tilfeldig variasjon. Side 61 av 114
62 <55 år år Sannsynlighet Sannsynlighet Tid siden diagnose (år) Tid siden diagnose (år) år 75+ år Sannsynlighet Sannsynlighet Tid siden diagnose (år) Tid siden diagnose (år) Død av prostatakreft Død av annen kreft Død av andre årsaker Figur 42 Dødelighet og dødsårsaker, aldersgrupper, 0-10 år etter diagnose. Figur 42 Datakilde: Dødsårsaksregisteret og prostatakreftregisteret Diagnoseår: Side 62 av 114
63 Radikal kirurgi Kurativ strålebehandling Sannsynlighet Sannsynlighet Tid siden diagnose (år) Tid siden diagnose (år) Aktiv overvåkning Ikke behandlet Sannsynlighet Sannsynlighet Tid siden diagnose (år) Tid siden diagnose (år) Død av prostatakreft Død av annen kreft Død av andre årsaker Figur 43 Dødelighet og dødsårsaker for ulike behandlingsvalg Figur 43 Datakilde: Prostatakreftregisteret, dødsårsaksregisteret, histologisvar, stråledata og klinisk primærutredningsmelding. Inklusjonskriterier: Påvist prostatakreft, <80 år, stadium ct1-3, N0/NX, M0, PSA 100 ng/ml, og fravær av annen kreftdiagnose Diagnoseår: Aktiv overvåkning ble begynt registrert i Side 63 av 114
64 Lav risiko Middels risiko Høy risiko Sannsynlighet Sannsynlighet Sannsynlighet Tid siden diagnose (år) Tid siden diagnose (år) Tid siden diagnose (år) Regionale Lymfeknutemetastaser Primærmetastatisk Sannsynlighet Sannsynlighet Død av prostatakreft Død av annen kreft Død av andre årsaker Tid siden diagnose (år) Tid siden diagnose (år) Figur 44 Dødelighet og dødsårsaker for risikogrupper og metastatisk sykdom år etter diagnose. Figur 44 Datakilde: Prostatakreftregisteret, dødsårsaksregisteret og klinisk primærutredningsmelding. Inklusjonskriterier: Påvist prostatakreft, <75år for risikogruppene og ingen aldersbegrensning for metastatisk sykdom. Diagnoseår: Side 64 av 114
65 Pasienter Norge 98% 4129 Møre og Romsdal 102% 276 Aust-Agder 102% 89 Østfold 101% 318 Troms 101% 118 Sør-Trøndelag 100% 261 Vest-Agder 99% 120 Oslo 99% 303 Akershus 99% 442 Buskerud 99% 284 Sogn og Fjordane 99% 111 Rogaland 98% 327 Oppland 97% 166 Nord-Trøndelag 96% 121 Hordaland 96% 347 Hedmark 96% 202 Vestfold 95% 221 Nordland 95% 191 Telemark 94% 169 Finnmark 93% års relativ overlevelse (%) Figur 45 Relativ overlevelse 5 år etter diagnose, høyrisikogruppen. Norge og fylker. Prosent. Figur 45 Datakilde: Prostatakreftregisteret og klinisk primærutredningsmelding Periodevindu: Side 65 av 114
66 Norge 36% Pasienter 797 Aust-Agder 57% 31 Rogaland 47% 79 Telemark 43% 35 Møre og Romsdal 41% 60 Hordaland 40% 61 Oppland 38% 31 Hedmark 37% 29 Buskerud 35% 28 Akershus 35% 68 Sør-Trøndelag 33% 56 Vestfold 33% 58 Østfold 33% 50 Nordland 32% 41 Vest-Agder 30% 23 Troms 30% 28 Finnmark 30% 8 Oslo 30% 61 Nord-Trøndelag 29% 28 Sogn og Fjordane 26% års relativ overlevelse (%) Figur 46 Relativ overlevelse 5 år etter diagnose, metastaser på diagnosetidspunktet (primærmetastatisk). Figur 46 Datakilde: Prostatakreftregisteret Periodevindu: Side 66 av 114
67 4 METODER FOR DATAFANGST Innmelding til Kreftregisteret er obligatorisk for leger som utreder, behandler og følger opp prostatakreftpasienter og krever ikke samtykke fra pasientene. Meldeplikten til Kreftregisteret er beskrevet i Kreftregisterforskriften 2-1. Kreftregisteret innhenter også rutinemessig data fra andre registre. 4.1 Rapportering av klinisk informasjon Rapportering av klinisk informasjon om utredning, behandling og oppfølging av kreftpasienter gjøres av behandlende lege, eller annet personell på sykehusene. Klinisk informasjon kan kun meldes elektronisk (fra og med ). Kreftregisteret utvikler elektroniske meldeskjemaer for rapportering av kliniske kreftdata via en portal på Norsk Helsenett (KREMT- Kreftregisterets elektroniske meldetjeneste på Det er mulig å rapportere inn klinisk informasjon via andre systemer, forutsatt at Kreftregisterets meldingsspesifikasjoner benyttes. Elektroniske kliniske meldinger for prostatakreft ble gjort tilgjengelig for rapportering via KREMT Kvalitetsregisteret har følgende meldinger: Primærutreding (publisert revidert skjema ) Utredning kun på bakgrunn av metastase (nytt skjema fra ) Radikal prostatektomi (publisert revidert skjema ) Strålebehandling (nytt fra ) KREMT har funksjoner for å gjøre arbeidet med rapportering enklere. Purringer på manglende meldinger og kvittering for innsendte meldinger, er tilgjengelige i KREMT-portalen. Det er også mulig å mellomlagre skjema. For å motivere til rapportering er det utarbeidet administrativ og klinisk statistikk som gir sykehusene oppdaterte resultater for sin enhet. Denne statistikken blir oppdatert daglig. Andelen kliniske meldinger som sendes inn spontant, uten at Kreftregisteret må etterspørre meldingen, er om lag 50 prosent. Kreftregisteret bruker derfor mye ressurser på å purre etter manglende informasjon. Rapporteringsgraden øker med antall ganger klinisk informasjon etterspørres, derfor purrer Kreftregisteret flere ganger på samme type informasjon hvis purringen ikke blir besvart. Kreftregisteret mottar også data fra alle landets stråleavdelinger elektronisk. I prostatakreftregisteret har vi fra i tillegg en egen strålemelding i KREMT fordi dataene som kommer direkte fra stråleenhetene ikke gir all den informasjonen som er nødvendig for å vurdere kvaliteten på helsetjenesten Rapportering av klinisk informasjon innen 60 dager Prostatakreftregisteret begynte for diagnoseår 2015 å presentere en analyse for å se på hvor fort helsetjenesten melder inn klinisk informasjon (ref. Kreftregisterforskriften 2-1 og frist på 60 dager). Vi har tatt utgangspunkt i diagnosedato og sett på hvor mange dager det har gått frem til meldingen er sendt inn. For diagnoseår 2016 klarte kun 6 institusjoner å melde inn over 80% av meldingene sine innen 60 dager etter at diagnosen var satt. Det nasjonale snittet er 34% (se figur 48). For kliniske prostatektomimeldinger klarte kun én institusjon å melde inn over 80% av meldingene sine etter kirurgi innen 60 dager. Det nasjonale snittet var 38% (se figur 50). Resultatet av disse to analysene kan gi et inntrykk av at det er store variasjoner mellom institusjonene i forhold til melderutiner, i tillegg til at Kreftregisteret mistenker at mange ikke melder inn krefttilfellet eller behandlingen før de mottar purringer fra Kreftregisteret, som nevnt tidligere i rapporten. Side 67 av 114
68 4.2 Rapportering av patologiinformasjon Patologiinformasjon, det vil si patologens vurdering av celle- og vevsprøver, er vesentlig for kvalitetsregisteret for å bekrefte diagnosen kreft, men gir også opplysninger om celletyper, biomarkører m.m. Rapportering av patologiinformasjon gjøres fra patologilaboratoriene ved at Kreftregisteret mottar kopi av patologiremissen, enten på papir eller elektronisk. Patologiinformasjonen er i all hovedsak i fritekst, supplert med håndtegnede bilder som ansatte i Kreftregisteret bearbeider manuelt etter interne regler i kvalitetsregisteret. Intern registreringsløsning for utvidet registrering av patologiinformasjon for prostatakreft ble tilgjengelig i 2009, og innebærer at detaljert patologinformasjon blir registrert i kvalitetsregister for prostatakreft fra og med (det vil si på prostatakreftpasienter som fikk sin diagnose fra 2009 og fremover). På grunn av svikt i den rutinemessige rapporteringen fra Patologiavdelingen ved Helse Fonna mangler Kreftregisteret foreløpig patologibesvarelser for siste halvdel av 2016 fra dette laboratoriet. 4.3 Rapportering av strålebehandlingsdata I motsetning til individuelle meldinger fra klinikere og patologiavdelinger, rapporteres strålebehandlingsdata samlet, en eller flere ganger per år, fra de respektive stråleavdelingene. Behandlingsdata genereres som uttrekk fra databasene i strålebehandlingssentrene. Det er noen praktiske problemer med denne formen for rapportering, blant annet knyttet til ulik definisjon av behandlet målvolum og ulik rapportering av dose per målvolum (f. eks. 50 Gy i 2 Gy fraksjoner mot prostata og vesiculae seminales pluss en boost mot prostata med 24 Gy i 2 Gy fraksjoner). Dette krever manuell gjennomgang av dataene fra stråleenhetene. Dette kan være tidkrevende og har sannsynligvis vært noe av årsaken til manglende rapportering av stråledata for 2015 fra en del sykehus. Det er planlagt introduksjon av en klinisk strålemelding fra juni 2017 som kan bedre rapporteringen av strålebehandlingen. Omfanget av den kliniske strålemeldingen kan begrenses ved forbedring av melderutiner ved strålesentrene. 4.4 Rapportering fra andre kilder Norsk pasientregister sender informasjon om kreftdiagnoser og kreftrelaterte opphold, hvert tertial. Opplysningene brukes i hovedsak til å purre etter informasjon om kreftpasienter som ikke er registrert i Kreftregisteret. Dødsårsaksregisteret sender inn opplysninger om kreftrelaterte dødsfall og dødsårsaker hvert år. Informasjonen brukes blant annet til kvalitetssikring for å komplettere opplysninger som mangler i Kreftregisteret. Folkeregisteret sender kopi av det sentrale personregisteret til Kreftregisteret hver måned. Folkeregisterdataene er vesentlige grunnlagsdata for å vite om personer i Kreftregisteret eksempelvis er emigrert eller døde. Side 68 av 114
69 5 METODISK KVALITET 5.1 Antall registreringer Ved uttrekk av data den hadde det for behandlingsår 2016 blitt registrert 9371 patologimeldinger og 4894 kliniske meldinger i prostatakreftregisteret. Registeret har detaljerte opplysninger om pasienter med prostatakreft. 5.2 Metode for beregning av dekningsgrad Komplettheten i Kreftregisteret for utvalgte kreftformer er estimert for perioden ved hjelp av en capture-recapture metode xviii. Capture-recapture metoden sammenligner antall tilfeller registrert ved hjelp av ulike meldingstyper. I denne analysen brukte vi kliniske meldinger, patologimeldinger og dødsattester. Når man har funnet hvor mange tilfeller som er registrert med klinisk melding, patologi og/eller dødsattest, kan man ved hjelp av en matematisk formel estimere komplettheten i registeret. Rapporteringsgrad for utredningsmeldingen er beregnet som andelen av tilfellene diagnostisert med prostatakreft i 2016 hvor det er mottatt og registrert en utredningsmelding. Tilsvarende er rapporteringsgraden for kirurgimeldingen regnet ut som andelen av de opererte hvor det er mottatt og registrert en kirurgimelding. 5.3 Tilslutning Alle leger som yter helsehjelp til pasienter med prostatakreft har meldeplikt til Kreftregisteret. Dette inkluderer rapportering til kvalitetsregister for prostatakreft. Alle helseinstitusjoner som diagnostiserer eller behandler prostatakreft er tilsluttet prostatakreftregisteret. Alle svar på vevsprøver blir rapportert fra patologiavdelingene til Kreftregisteret, men enkelte avdelinger ved sykehusene har ikke etablert gode rutiner for rapportering av klinisk informasjon. Rapportering av klinisk informasjon knyttet til prostatektomi er etablert som rutine ved de fleste sykehusene som utfører dette inngrepet. Klinisk informasjon om diagnose og utredning har en lavere rapporteringsgrad. Figur 47 viser at det er store forskjeller mellom sykehusene for rapportering av utredning til prostatakreftregisteret og registeret fikk utredningsmelding på 68% av pasientene i Det er flere sykehus som har et stort forbedringspotensial for å etablere rutiner for rapportering av utredingsmelding. Figur 48 viser at kun 34% av utredningsmeldingene ble rapportert til Kreftregisteret innen 60 dager etter diagnose. Figur 49 viser at Prostatakreftregisteret har fått kliniske melding om prostatektomi på 75% av pasientene i 2016, så også her finnes rom for forbedring. Figur 50 viser at kun 38% av meldingen om prostatektomi rapporteres til prostatakreftregisteret innen 60 dager etter operasjon. Side 69 av 114
70 Norge Urologiklinikken AS Haraldsplass Diakonale Sykehus Volvat, Fredrikstad Sykehuset Innlandet, Kongsvinger Aleris, Oslo Helse Nord-Trøndelag, Levanger Uro-Sør A/S Sykehuset Innlandet, Lillehammer Overnklinikken AS Moelv Spesialistsenter Volvat, Bergen Vestre Viken, Bærum Helse Møre og Romsdal, Kristiansund Helgelandsykehuset, Mosjøen Aleris sykehus og medisinsk senter Trondheim Urologiklinikken i Trondheim Sykehuset Telemark, Skien/Porsgrunn Ahus, Lørenskog Helse Møre og Romsdal, Molde Finnmarkssykehuset, Hammerfest Helse Møre og Romsdal, Volda Volvat, Oslo Vestre Viken, Hønefoss Finnmarkssykehuset, Kirkenes Vestre Viken, Drammen Sykehuset Innlandet, Tynset Sykehuset i Vestfold, Tønsberg Helse-Førde, Lærdal Haukeland universitetssykehus CuraMedica Spesialistsenter AS Stavanger Urologiske Senter AS UNN, Harstad Nordlandssykehuset, Bodø Oslo Universitetssykehus UNN, Tromsø Sykehuset Innlandet, Hamar Stavanger universitetssjukehus Helse Møre og Romsdal, Ålesund Helse-Fonna, Haugesund Tromsø Urologiske Spesialistsenter Helse-Førde, Førde Urologisk Klinikk Sørlandet Sykehus Privatsykehuset Haugesund AS St. Olavs hospital Sykehuset Østfold, Fredrikstad Nøtterøy Legesenter Private leger UNN, Narvik Ski urologiske senter Klinikk Røa Parsennklinikken Østsiden kirurgiske praksis Helse Nord-Trøndelag, Namsos 0% 0% 0% 0% 0% 29% 26% 24% 23% 17% 15% 14% 12% 9% 9% 7% 52% 62% 68% 88% 88% 88% 86% 86% 86% 84% 84% 82% 80% 80% 79% 77% 76% 75% 73% 73% 70% 69% 67% 100% 100% 100% 100% 99% 99% 98% 98% 97% 96% 95% 94% 93% 93% 92% 92% Pasienter Innrapporteringsgrad (%) Figur 47 Rapporteringsgrad av klinisk primærutredningsmelding ved prostatakreft. Figur 47 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Innsendt klinisk primærutredningsmelding for prostatakreft. Diagnoseår: 2016 Side 70 av 114
71 Norge Aleris, Oslo Volvat, Fredrikstad Overnklinikken AS Vestre Viken, Bærum Volvat, Bergen Aleris sykehus og medisinsk senter Trondheim Helse Møre og Romsdal, Molde Haraldsplass Diakonale Sykehus Helgelandsykehuset, Mosjøen Moelv Spesialistsenter Volvat, Oslo Haukeland universitetssykehus Stavanger Urologiske Senter AS Helse Møre og Romsdal, Kristiansund Ahus, Lørenskog Vestre Viken, Drammen Helse Møre og Romsdal, Ålesund Vestre Viken, Hønefoss Stavanger universitetssjukehus Sykehuset Innlandet, Lillehammer Helse Nord-Trøndelag, Levanger Finnmarkssykehuset, Hammerfest Urologiklinikken AS Urologiklinikken i Trondheim Finnmarkssykehuset, Kirkenes Sykehuset Innlandet, Tynset Sykehuset Innlandet, Kongsvinger UNN, Tromsø Helse Møre og Romsdal, Volda Nordlandssykehuset, Bodø Helse-Førde, Førde Sykehuset Telemark, Skien/Porsgrunn Sykehuset Innlandet, Hamar Nøtterøy Legesenter Private leger Urologisk Klinikk Sørlandet Sykehus Sykehuset Østfold, Fredrikstad Oslo Universitetssykehus UNN, Harstad Helse-Fonna, Haugesund Tromsø Urologiske Spesialistsenter St. Olavs hospital Sykehuset i Vestfold, Tønsberg Uro-Sør A/S UNN, Narvik Parsennklinikken Østsiden kirurgiske praksis CuraMedica Spesialistsenter AS Privatsykehuset Haugesund AS Klinikk Røa Helse-Førde, Lærdal Helse Nord-Trøndelag, Namsos Ski urologiske senter 34% 94% 89% 89% 88% 85% 81% 79% 78% 78% 77% 76% 68% 65% 60% 57% 47% 46% 37% 37% 31% 27% 23% 20% 20% 20% 20% 18% 16% 14% 14% 12% 11% 11% 9% 9% 8% 7% 7% 6% 4% 4% 4% 3% 3% 2% 0% 0% 0% 0% 0% 0% 0% 0% 0% Meldinger Andel (%) Figur 48 Rapportert innen 60 dager etter ferdig utredning Figur 48 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Innsendt klinisk primærutredningsmelding Diagnoseår: 2016 Side 71 av 114
72 Pasienter Norge 75% 1829 Sykehuset Innlandet, Hamar 98% 199 Nordlandssykehuset, Bodø 94% 34 Oslo Universitetssykehus 94% 472 UNN, Tromsø 89% 109 Vestre Viken, Drammen 86% 101 Sykehuset Telemark, Skien/Porsgrunn 84% 94 Ahus, Lørenskog 71% 89 Sykehuset i Vestfold, Tønsberg 67% 103 Stavanger universitetssjukehus 67% 108 Haukeland universitetssykehus 53% 174 St. Olavs hospital 45% 267 Sørlandet Sykehus 20% Innrapporteringsgrad (%) Figur 49 Rapporteringsgrad for klinisk melding etter radikal prostatektomi. Figur 49 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Utfylt og innsendt klinisk melding etter prostatektomi Diagnoseår:2016 Side 72 av 114
73 Norge 38% Meldinger 1829 Sykehuset Innlandet, Hamar 95% 199 Vestre Viken, Drammen 67% 101 Stavanger universitetssjukehus 53% 108 Haukeland universitetssykehus 45% 174 Nordlandssykehuset, Bodø 41% 34 Ahus, Lørenskog 39% 89 Oslo Universitetssykehus 30% 472 St. Olavs hospital 28% 267 UNN, Tromsø 21% 109 Sykehuset Telemark, Skien/Porsgrunn 10% 94 Sykehuset i Vestfold, Tønsberg 5% 103 Sørlandet Sykehus 0% Andel (%) Figur 50 Rapportert innen 60 dager etter utført kirurgi Figur 50 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Innsendt klinisk prostatektomimelding Diagnoseår: 2016 Side 73 av 114
74 5.4 Dekningsgrad Alle pasienter med prostatakreft (ICD10 C61) i Norge skal være inkludert i registeret. Dekningsgraden for pasienter diagnostisert med prostatakreft i 2016 er beregnet til 99,30 %. For alle kreftformer samlet er dekningsgraden i ,4 %. Se kapittel 5.2. for metode. Mål for dekningsgrad: Høy: 98 % eller mer Moderat: 95 % eller mer, men under 98 % Lav: Under 95 % 5.5 Prosedyrer for intern sikring av datakvalitet Kvalitetssikring av data gjøres som en integrert del av kode- og registreringsprosessen. I tillegg bidrar følgende eksempler med å sikre datakvaliteten i Kreftregisteret: Flere uavhengige kilder rapporterer inn opplysninger Opplysningene rapporteres inn på flere tidspunkter i sykdomsforløpet Medarbeiderne har unik kompetanse på koding av krefttilfeller i henhold til Kreftregisterets egen kodebok og internasjonale kodeverk IT-systemene har regler og sperrer for ulogiske kombinasjoner, feilaktige opplysninger med mer Kreftregisteret gjør analyser og kontrollkjøringer som avdekker inkonsistens i dataene Datauttrekk til forskere gir mulighet til å kontrollere et mindre datasett av opplysninger som kan avdekke enkeltfeil (for eksempel feiltasting av sykehuskoder) eller systematiske ulikheter som skyldes ulik tolkning av kodeverk og regler 5.6 Metoder for validering av data i registeret Kreftregisteret får innrapportert og henter inn opplysninger fra ulike kilder, noe som sikrer høy grad av validitet og kompletthet av registrerte data (for de ulike kildene se kapittel 4). Hvis det mangler kliniske meldinger (for eksempel etter mottak av et patologisvar som viser kreft), purres institusjonen med oppfordring om å sende inn opplysninger. Manglende patologimeldinger fra patologiavdelingene etterspørres også. Kreftregisterets stab av ansatte med spesialkompetanse på koding og registrering av krefttilfeller kvalitetssikrer informasjon om hvert enkelt tilfelle som en integrert del av arbeidsprosessen. I tillegg er det etablert faste kvalitetssikringsrutiner som gjennomføres ved avslutning av hver årgang. Det er ennå ikke planlagt en formell studie av validiteten i prostatakreftregisteret. I september 2017 publiserte Kreftregisteret en studie som vurderte kvaliteten på dataene i Nasjonalt kvalitetsregister for tykk- og endetarmskreft 24. Studien brukte metodene «reabstracting and recoding», og 1400 pasientjournaler ble gjennomgått for å trekke ut relevante opplysninger til registeret. Deretter ble de nye opplysningene sammenliknet med dataene i registeret. Studien konkluderer med at kvaliteten på data som er entydig definert og data som kvalitetssikres fra flere kilder har god til meget god kvalitet. Denne konklusjonen antas gjelde også for prostatakreftregisteret, fordi opplysninger til registeret hentes inn og bearbeides på stort sett samme måte som i tykk- og endetarmskreftregisteret Side 74 av 114
75 5.7 Vurdering av datakvalitet En helhetlig vurdering av datakvalitet i prostatakreftregisteret vil bli utført i en senere årsrapport. Sentrale kliniske variabler (for eksempel tumorstadie ct og PSA) er stort sett angitt i meldingene som sendes inn, og dermed ligger komplettheten av disse variablene tett opp til den kliniske rapporteringsgraden. Under vises komplettheten for 2016 for noen sentrale variabler fra patologimeldinger: Tumorstadie pt: omtrent 99.5 % Status for reseksjonsrand: omtrent 99 % Gleason score i nålebiopsi: omtrent 97 % Gleason score i prostatektomi: omtrent 99 % 5.8 Statistisk metode Deler av den statistikken som presenteres i rapporten er basert på enkle opptellinger eller fremstillinger av gjennomsnitt, median og andeler. For å sikre at tilfeldig variasjon ikke påvirker resultatene i for stor grad er det satt krav til en viss utvalgsstørrelse for de ulike analysene. Kriteriene for utvalgsstørrelse kan variere og er derfor spesifisert for de analysene der det er behov for dette. I noen analyser der det presenteres resultater på sykehusnivå vises det det også konfidensintervaller (usikkerhetsmargin) for de tilhørende estimatene. Dette for å illustrere at det er knyttet usikkerhet til estimatene, og at eventuelle forskjeller kan skyldes tilfeldige variasjoner. Metodene som er brukt for beregning av disse konfidensintervallene legger til rette for sammenligning mellom hver institusjon/region og landsgjennomsnittet, men legger ikke til rette for sammenligninger mellom institusjoner/regioner. Ved slike parvise sammenligninger vil tilfeldig variasjon spille en større rolle, noe som vil reflekteres i bredere konfidensintervaller enn de som presenteres i denne rapporten. Det er gjort analyser på utvikling i insidens og mortalitet over tid. Aldersspesifikke rater er beregnet som antall tilfeller per personår for hvert kalenderår (det brukes 18 aldersgrupper; 0-4,5-9,...,85+). Aldersstandardiserte rater, som er et vektet gjennomsnitt av de aldersspesifikke ratene, er beregnet ved å bruke avrundede vekter basert på den norske middelbefolkningen i Dette er også standarden Kreftregisteret bruker i den årlige publikasjonen Cancer in Norway1 25. For å bedre kunne illustrere trender over tid er det i noen figurer presentert glattede rater, beregnet ved hjelp av vektet lokal regresjon (LOWESS). Alle insidensrater er basert på uttrekk fra Kreftregisterets insidensdatabase, som er tilnærmet komplett til og med 31. desember Uttrekket til denne rapporten ble gjort 15. august Dødelighetsrater er kun tilgjengelig til og med 31. desember 2015 fordi Dødsårsaksregisteret ennå ikke er oppdatert for Kreftregisteret har komplett oppfølging med hensyn til dødstidspunkt for alle pasienter til og med 31. desember Dette danner grunnlaget for forløpsanalysene (overlevelsesanalysene) i rapporten. I en forløpsanalyse ønsker man å følge opp en gruppe personer (en kohort) fra et gitt starttidspunkt (for eksempel diagnosedato) til de opplever en hendelse av interesse, for eksempel død eller tilbakefall. For en del av pasientene i kohorten vet man ikke om de opplever hendelsen siden de enten har forsvunnet ut av kohorten på et tidspunkt, eller siden de ikke har opplevd hendelsen ved siste oppdaterte oppfølgingsdato. I statistikken kalles dette sensurering, noe som må tas hensyn til for å kunne estimere korrekte andeler/sannsynligheter. Den mest brukte metoden for å gjøre slike analyser er den såkalte Kaplan-Meier metoden 26. Estimater for totaloverlevelse og andel postoperativt bestrålt er beregnet ved hjelp av denne metoden. Relativ overlevelse er en metode for å estimere andelen pasienter som dør av sin kreftsykdom i en hypotetisk verden der man ikke kan dø av andre årsaker. Dette estimeres mer konkret ved å sammenligne dødeligheten for personer diagnostisert med en viss type kreft med dødeligheten for en 25 Cancer Registry of Norway. Cancer in Norway Cancer incidence, mortality, survival and prevalence in Norway. Oslo: Cancer Registry of Norway, Kaplan, E. L.; Meier, P.: Nonparametric estimation from incomplete observations. J. Amer. Statist. Assn. 53: , Side 75 av 114
76 sammenlignbar kreftfri befolkning. Relativ overlevelse er nyttig for å sammenligne overlevelse over tid eller mellom regioner og institusjoner. Det finnes ulike metoder for å estimere relativ overlevelse. Estimatene i denne rapporten er basert på den såkalte Ederer2-metoden 27. For beregning av relativ overlevelse for diagnoseår hvor vi har fem års oppfølgingstid tilgjengelig bruker vi kohortmetoden 28. Her følger vi pasientene fra diagnosetidspunktet til sensurering eller hendelse. I en situasjon hvor man ønsker å estimere fem års relativ overlevelse der man har pasienter med oppfølging til og med fem år kan man bruke complete approach. I et nylig opprettet register hvor man kun har pasienter som er diagnostisert fra og med 2011 vil man bruke all ( complete ) tilgjengelig oppfølgingstid. Pasienter diagnostisert i 2011 vil ha fulle fem års oppfølging, mens pasienter diagnostisert i senere år bidrar med den oppfølgingstiden de har. Man kan se på dette som en variant av kohortmetoden der ikke alle pasientene har full oppfølgingstid, men denne metoden gir mer oppdaterte estimater for nylig diagnostiserte pasienter. For diagnoseår hvor vi ikke har nok oppfølgingstid tilgjengelig, typisk de fem siste årene, bruker vi periodetilnærmingen for å estimere overlevelsen med så oppdatert overlevelseserfaring som mulig 23. I stedet for å følge pasientene i en kohort fra diagnosedato til død eller sensurering, så definerer vi en periode (periodevindu) hvor pasienter bidrar med overlevelseserfaring. Pasientene trenger da ikke å bli diagnostisert med kreft i perioden. I denne rapporten har vi valgt å bruke et femårig periodevindu ( ) for å få nok styrke og så oppdaterte overlevelsesestimat som mulig. Det betyr at for å estimere 1 5 års relativ overlevelse benytter vi overlevelseserfaring fra pasienter diagnostisert i periodevinduet, men på grunn av for kort oppfølging må også pasienter diagnostisert forut for perioden inkluderes. Pasienter diagnostisert i årene bidrar med henholdsvis 5, 4 5, 2 4 og 1 3 års oppfølgingstid. For å synliggjøre dødeligheten av prostatakreft presenteres det kurver som viser den faktiske sannsynligheten for å dø av prostatakreft sammenlignet med sannsynligheten for å dø av hjerte- karsykdommer og andre årsaker. Dette er estimater som blir beregnet ved hjelp av såkalt competing risk analyse. Competing risk beskriver situasjoner der man er interessert i en spesifikk hendelse (død som følge av prostatakreft), men der andre hendelser (død som følge av andre årsaker) forhindrer oss i å observere hendelsen vi primært er interessert i. Metoden som er brukt for å estimere sannsynlighetene er en såkalt ikke-parametrisk metode 29. Alle statistiske analyser ble utført med Stata versjon Ederer, F., and Heise, H. (1959), "Instructions to Ibm 650 Programmers in Processing Survival Computations," Technical, End Results Evaluation Section, National Cancer Institute. 28 Brenner H, Rachet B. Hybrid analysis for up-to-date long-term survival rates in cancer registries with delayed recording of incident cases. Eur J Cancer 2004;40: Gooley T.A., Leisenring W., Crowley J., and Storer B.E. Estimation of failure probabilities in the presence of competing risks: new representations of old estimators. Statistics in Medicine 1999; 18: StataCorp Stata Statistical Software: Release 15. College Station, TX: StataCorp LLC Side 76 av 114
77 6 FAGUTVIKLING OG KVALITETSFORBEDRING AV TJENESTEN 6.1 Pasientgruppe som omfattes av registeret Alle menn som har fått påvist prostatakreft (ICD 10 C61) i Norge fra er inkludert i Prostatakreftregisteret. 6.2 Registerets spesifikke kvalitetsmål Lavrisiko pasienter som er radikal behandlet Ingen studier viser en overlevelsesgevinst med primær radikal behandling for menn med lavrisikokreftxix/xx/xxi. Aktiv overvåkning medfører en svært lav risiko for prostatakreftdødelighet xxii/ xxiii Aktiv overvåkning anbefales derfor som strategi for denne gruppen både av EAU guidelines og Norsk Handlingsprogram prostatakreft. I Sverige begynner en stor andel av pasientene med lav risikokreft med aktiv overvåkning, for svenske pasienter med meget lav risiko er andelen 90% i 2015 og for pasienter med lav risiko prostatakreft er andelen 72%. Også i Norge er utviklingen positiv, i 2014 var andelen menn med lav risiko som likevel valgte radikal behandling primært ca. 17%. En nylig publikasjon av Vickers gruppe ved memorial Sloan Kettering Cancer Centre i New York viste at dedikerte spesialister kan oppnå 93% oppslutning om aktiv overvåkning, men selv etter kommunikasjonstrening kunne en gruppe på fem spesialister bare oppnå 81% oppslutning. Da registeret foreløpig ikke kan skille meget lav fra lav risiko, har referansegruppen valgt < 20% som kvalitetsmål for radikal behandling i lavrisikogruppen Høyrisiko prostatakreft som er radikal behandlet Menn som har en høyrisiko-kreft uten spredning og som ikke gjennomfører en radikal behandling etter diagnosen har en høy sannsynlighet for å dø av sin kreft. Dette gjelder selv menn i høy alder som man ellers kunne anta ville dø av andre årsakerxxiv. Vi vet også at menn med høyrisiko-kreft kan helbredes med høydosert strålebehandling xxv/xxvi og med operasjon xxvii/ xxviii. I 2014 ble tre av fire menn under 80 år radikalt behandlet etter diagnose med en høyrisiko prostatakreft. Denne andelen er lite endret de siste årene (tabell 5 i vedlegget) Det vil nødvendigvis være en andel menn der radikal behandling ikke skal anbefales på grunn av tilleggssykdommer eller at en operasjon ikke lar seg gjennomføre pga svulstens plassering (teknisk inoperabilitet) eller som ikke ønsker slik behandling. For en del av disse menn foreligger også kontraindikasjoner mot strålebehandling. Referansegruppen har derfor valgt som kvalitetsmål at >70% av menn med en høyrisikokreft uten spredning skal behandles enten med kurativ strålebehandling eller operasjon. Side 77 av 114
78 6.2.3 Lymfeknutedisseksjon i forbindelse med prostatektomi for høyrisiko kreft En ny systematisk oversiktsartikkel xxix finner ingen dokumentasjon for at en lymfeknutedisseksjon 31 fører til et bedre behandlingsresultat. Det gjelder uavhengig av type disseksjon (begrenset, standard eller utvidet reseksjon). Forfatterne er nøye med å fremheve at deres konklusjon ikke utelukker at utvalgte grupper eller pasienter kan ha effekt av lymfeknutedisseksjon, for eksempel høyrisikopasienter. Det er godt dokumentert at en lymfeknutedisseksjon medfører bivirkninger og at pasientenes bivirkninger øker med omfang av disseksjonen. Det er enighet om at lymfeknutedisseksjon er en god prosedyre for å fastsette stadium (sykdomsutbredelse) som gir prognostisk informasjon. En disseksjon kan være grunnlag for å anbefale tilleggsbehandlinger som hormonbehandling eller strålebehandling. EAU anbefaler i sine aktuelle retningslinjer en utvidet lymfeknutedisseksjon ved prostatakreft med høy risiko for tilbakefall og dersom beregnet risiko for lymfeknutespredning overskrider 5% for alle svulster (grad A anbefaling). I Nasjonalt handlingsprogram er det formulert et krav til lymfeknutedisseksjon ved høyrisiko prostatakreft (grad C anbefaling). På landsbasis utføres 87% av alle prostataoperasjoner for høyrisikokreft med en lymfeknutedisseksjon. Registeret har ingen opplysninger om komplikasjoner på nasjonal basis. Referansegruppen har innført som kvalitetsmål at >80% bør få utført lymfeknutedisseksjon ved operasjon for høyrisikokreft Ufri rand (margin) etter en prostatektomi for pt2 cancer Kurativ kreftkirurgi har som mål å fjerne kreften, og kirurgen bør streve etter å oppnå en fri margin. Når patologen påviser kreftceller i snittkanten er det ansett som et uønsket resultat etter en prostatektomi. En ufri margin øker risikoen for et tilbakefall som påvises med forhøyet PSA men det er usikkert om det øker risikoen for utvikling av metastaser eller død av prostatakreftxxx/xxxi. Ufri margin eller tilbakefall som påvises med forhøyet PSA medfører ofte at pasienten trenger videre behandling med postoperativ strålebehandling xxxii og hermed ytterligere bivirkninger. Nervesparende operasjonsteknikk reduserer risikoen for postoperativ impotens og inkontinens32, men øker samtidig risikoen for en ufri margin. xxxiii Å velge en nervesparende operasjonsteknikk krever som regel at kreften er innenfor prostatakjertelens kapsel (lokalisert sykdom T2-stadium). En slik vurdering før operasjonen er beheftet med usikkerhet (klinisk T2 stadium). På den andre siden forventes fri margin dersom kreften viser seg å være lokalisert i prostata etter operasjonen (patologisk T2 stadium). Vurderingen av om operasjonsmargingen er fri eller ikke, er ikke et objektivt mål, men vurderes av den enkelte patolog, og en vurdering om det foreligger ufrie marginer eller ikke, kan variere mellom ulike patologer. I publikasjoner beskrives til dels store variasjoner på andel ufri margin. Sooriakumaran et al. xxxiv analyserte resultatene fra 14 internasjonale sentre og fant en rate på ufri margin på 18% og andelen pt2 tumorer var 67%. Andre studier har vist andel ufri margin i samme størrelsesorden. Referansegruppen har valgt å sette et kvalitetsmål for ufri margin ved operasjon for kreftsvulster lokalisert i prostata (pt2), og mener alle sykehus bør kunne oppnå en andel ufri margin for lokalisert kreft som ikke er større enn 20% Videre arbeid med kvalitetsmål Referansegruppen prioriterer arbeidet med å finne flere gode kvalitetsmål. De fleste kvalitetsmålene 31 Lymfeknutedisseksjon = å fjerne lymfeknuter i en operasjon 32 Inkontinens betyr her urin- eller tarmlekkasje Side 78 av 114
79 Prostatakreftregisteret har så langt, er mest interessante for fagfolk. For å kunne publisere resultater som er mer relevante for pasientene, er arbeidet med å legge til rette for innsamling av pasientrapporterte resultatmål et prioritert arbeidsområde. Fra mars 2017 ble utsending av spørreskjemaer begynt og resultater fra dette vil først kunne bli tilgjengelig i årsrapporten for operasjonsåret Nasjonale kvalitetsindikatorer Ingen av kvalitetsmålene over har ennå status som nasjonale kvalitetsindikatorer. 5 års relativ overlevelse etter prostatakreft er i dag en nasjonal indikator sammen med utvalgte parametere fra pakkeforløpet. Helsedirektoratet, Kreftregisteret og referansegruppen til prostatakreftregisteret samarbeider i 2017 om å etablere nye og bedre nasjonale indikatorer for prostatakreft. 6.3 Pasientrapporterte resultat- og erfaringsmål (PROM og PREM) Pasientrapporterte resultat- og erfaringsmål er så langt ikke inkludert i prostatakreftregisteret, med registeret brukes som pilotregister for innsamling av PROMs (Patient Reported Outcome Measures). De første invitasjonene til prostatakreftpasienter ble sendt ut i mars 2017, og så langt ligger responsraten på rundt 50 %. Pasienter diagnostisert med prostatakreft til og med 2019 vil bli invitert til studien. En kontrollgruppe blir også invitert. Movemberstiftelsen finansierer studien, og Regional komité for medisinsk og helsefaglig forskningsetikk har godkjent prosjektet. Innsamling av pasientrapporterte resultater kan bidra til at pasienter får bedre behandling og oppfølging og bedre livskvalitet. Sykehus med nødvendig etisk godkjenning kan få en kopi av pasientens svar. Slik kan sykehusene bruke PROMs-dataene til pasientoppfølging og kvalitetssikring av egen virksomhet. Det er et viktig mål for studien å sette opp et system for innsamling av PROMs nasjonalt, som også kan brukes for andre kreftformer. Kreftregisteret avventer derfor resultater fra pilotprosjektet før pasientrapporterte data blir inkludert i flere kvalitetsregister. 6.4 Sosiale og demografiske ulikheter i helse Registeret har tilgang til data for å gjøre analyser på demografiske ulikheter som for eksempel alder, kjønn, bosted på diagnosetidspunktet, behandlingsinstitusjon og dato for død. Kreftregisteret har i tillegg tilgang til opplysninger om hvorvidt personen er emigrert eller bosatt i Norge, men har ikke tilgang til flyttehistorikk. Analyser på eventuelle forskjeller mellom sykehusene vil avhenge av klinisk rapporteringsgrad. Det er en forutsetning at komplettheten av dataene er høy, for å kunne vurdere hvorvidt pasientene får tilgang til like bra utredning, behandling og oppfølging/kontroll i hele landet. I denne rapporten er flere resultater presentert med utgangspunkt i pasientens bosted og ikke bare behandlende sykehus. Det er viktig å kunne avdekke om det er eventuelle forskjeller i helsehjelpen som blir gitt, på bakgrunn av hvor pasientene er bosatt. I 2016 startet flere forskningsprosjekter ved Kreftregisteret med kreft hos innvandrere som tema. Dette er viktig kunnskap for å kunne overvåke sosiale ulikheter i helse, og Kreftregisteret har spilt inn behovet for å kunne registrere landbakgrunn til Helse- og omsorgsdepartementet. Det er foreløpig ikke planlagt regelmessig å samle inn data som kan belyse sosiale ulikheter for pasientene kvalitetsregisteret. For å få tilgang til slike data fra Statistisk sentralbyrå, må Kreftregisteret per i dag søke om konsesjon fra Datatilsynet. Et phd-arbeid ved Kreftregisteret, som ser på regionale ulikheter i kreftforekomst og overlevelse, ble ferdigstilt Bosted, inntekt og utdanning var noen av flere forhold som ble vurdert. Side 79 av 114
80 6.5 Bidrag til utvikling av nasjonale retningslinjer, nasjonale kvalitetsindikatorer o.l. Prostatakreftregisteret er det uro-onkologiske miljøets viktigste samlede oversikt over den diagnostiske og behandlingsmessige aktiviteten som foregår innenfor prostatakreft. De nasjonale retningslinjene ligger i stor grad på etterskudd med tanke på å implementere endringer i internasjonale retningslinjer og studier. Noen avdelinger kan derfor ligge i forkant av nasjonale praksisendringer. En stor utfordring for registeret har tidligere vært forsinkelse i ferdigstillelse av data. Med etablering av elektronisk innmelding gjennom KREMT er tidligere etterslep tatt igjen. Med innføring av mer relevante skjemaer for behandling og oppfølging, regner man med at komplettheten og kvaliteten på data om norsk behandlingspraksis og resultater vil øke. 6.6 Etterlevelse av nasjonale retningslinjer Referansegruppen for prostatakreftregisteret og handlingsprogramgruppen i Helsedirektoratet settes sammen uavhengig av hverandre. Prostatakreftregisteret ble etablert mange år før det nasjonale handlingsprogrammet og har i mindre grad vært konstruert for å måle etterlevelse av nasjonale retningslinjer. Dette fokuseres det imidlertid på nå, men dette arbeidet er også avhengig av en mer dynamisk og varslet oppdatering av det nasjonale handlingsprogrammet for prostatakreft. Nasjonale retningslinjer for utredning, behandling og oppfølging av prostatakreft finnes på Identifisering av kliniske forbedringsområder Rapporten viser en trend mot flere operasjoner, og operasjon også ved lokalavansert og høyrisiko sykdom, på bekostning av primær strålebehandling. Dette er en praksis som er i tråd med internasjonale trender, men likevel dårlig dokumentert. Det er usikkert om randomiserte studier mellom operasjon og stråling vil kunne gjennomføres og registerdata vil da være av stor betydning. Det er ulik behandlingspraksis ved de ulike sykehusene både i andel pasienter som blir primært strålebehandlet og andelen som blir operert. Videre ser man at andelen postoperative strålebehandlinger øker. Berettigelsen av dette vil kreve ytterligere vurdering av data i årene fremover. Videre analyser må vurdere økningen og forbruk av postoperativ strålebehandling i forhold til risikogrupper, men også forhold knyttet til kirurgi, som operasjonsvolum og utførelse av nervesparende teknikk, da andelen pasienter som blir postoperativt strålebehandlet varierer mellom sykehusene. Det vil være et naturlig fokus for referansegruppen å avdekke bakgrunnen for forskjellene mellom regionene og sykehusene, og diskutere de ulike strategier videre for en bedre samstemming. 6.8 Tiltak for klinisk kvalitetsforbedring initiert av registeret Utover de løpende tiltak beskrevet i rapporten jobbes det nå aktivt med å innhente pasientrapporterte resultater (Patient Reported Outcome Measures PROMs). Bivirkninger etter behandling er en faktor av vesentlig betydning ved vurdering av type behandling og hvorvidt behandlingen bør settes i gang for den enkelte pasienten. Innføringen av MR i diagnostikken ved prostatakreft krever innsamling av variabler til registeret for å måle bruken av MR, men også effekten av denne praksisen. Det har derfor blitt jobbet med å revidere kliniske meldeskjemaer for å få inn disse variablene, og de ble tatt i bruk fra Det er nedsatt en gruppe av patologer fra de fire helseregionene som et samarbeid med Den norske patologforening for å revidere og utarbeide en ny mal for standardisert patologibeskrivelse av prostatabiopsier og operasjonspreparater. Side 80 av 114
81 Referansegruppen og registeret legger til grunn at sikreste måte å motivere for rapportering av data er at data blir publisert og at avdelingene synliggjøres, ikke bare på klinisk rapporteringsgrad, men også på resultater. Parallelt er man bevisst på at registervariablene skal være så entydig definert som mulig. 6.9 Evaluering av tiltak for klinisk kvalitetsforbedring (endret praksis) Prostatakreftregisteret har de siste årene hatt fokus på blant annet status for reseksjonrender i prostatektomi på sykehusnivå (fri/ufri rand etter prostatektomi). Forskjellene mellom sykehusene i andelen frie reseksjonrender, som har blitt presentert i tidligere rapporter fra registeret, har blitt bredt diskutert i fagmiljøet. Fra 2009 og frem til 2016 har det derfor vært en kontinuerlig forbedring av reseksjonrender ved prostatektomi ved alle opererende avdelinger. Forbedringen gjenspeiler ikke bare bedret kirurgisk teknikk, men også større bevissthet i patologi-vurderingen Pasientsikkerhet Prostatakreftregisteret har per i dag ingen rapportering av komplikasjoner eller uønskede hendelser. Side 81 av 114
82 7 FORMIDLING AV RESULTATER Kreft er en gruppe sykdommer som utredes, behandles og følges opp over lang tid. Det innebærer at kreftstatistikk som er sammenstilt fra flere kilder, tidligst kan publiseres året etter diagnoseåret. Prostatakreftregisteret publiserer en årsrapport hver høst, men har tidligere ikke vært a jour med å kode inn og kvalitetssikre data var første året det ble publisert data for det foregående operasjonsåret. I forhold til stråledata så mangler fortsatt rapportering fra et helseforetak i Resultater tilbake til deltakende fagmiljø De viktigste resultatene fra prostatakreftregisteret blir publisert i årsrapporten og er dermed allment tilgjengelig. Fagmiljøet får tilsendt rapporten via deltakerne i referansegruppen, men skal også få den tilsendt gjennom linjen i sitt regionale helseforetak. Tidligere har resultatene blitt presentert i relevante fagfora som Kirurgisk høstmøte og Onkologisk forum. I år er det planlagt å presentere resultatene på Onkologisk forum. Resultatene fra registeret blir også kjent for fagmiljøet gjennom publisering av forskningsprosjekter som bruker data fra registeret. Via Kreftregisterets meldetjeneste (KREMT) på Norsk Helsenett har sykehusene tilgang til statistikk basert på elektronisk innsendt klinisk informasjon for eget sykehus sammenlignet med et landsgjennomsnitt. Fra Prostatakreftregisteret er disse statistikkene tilgjengelig: Alder ved diagnosetidspunktet Hovedårsak til utredning Median PSA-verdi ved diagnosetidspunktet angitt i µg/l Tid fra første konsultasjon til diagnose Bruk av bildediagnostikk ct ved diagnosetidspunktet ct basert på DRE ved diagnosetidspunktet Oppfølging/tiltak etter utredning Preoperativ ct Preoperativ ctnm Median preoperativ Gleason score Median preoperativ PSA-verdi Tid fra diagnosedato til operasjonsdato Type kirurgi Kreftregisteret mangler i dag tillatelse i Kreftregisterforskriften for å gi helseinstitusjonene tilgang til personidentifiserbare opplysninger de selv har sendt inn om sine egne pasienter 33. Vi har bedt om at Helse- og omsorgsdepartementet endrer dette ved oppdatering av Kreftregisterforskriften. Inntil denne endringen er på plass, kan helseinstitusjonene skrive databehandleravtaler med Kreftregisteret og få dataene tilbakerapportert. De fleste helseinstitusjoner har allerede etablert databehandleravtale eller er i dialog om å utarbeide avtale. 7.2 Resultater til administrasjon og ledelse Kreftregisteret sender ut årsrapportene til de regionale helseforetakene, slik at rapportene kan brukes i kvalitetsforbedrende arbeid regionalt og i de lokale helseforetakene. Rapportene sendes også til kontaktpersoner og avdelingsledere. 33 For mer informasjon, se Kreftregisterets nettsider: Side 82 av 114
83 Etter publisering av årsrapportene i 2016 ble Kreftregisteret invitert til fagdirektør/fagsjefmøtene i Helse Sør-Øst, Helse Vest og Helse Nord (høsten 2016 og våren 2017). Kreftregisteret presenterte resultater for hver helseregion og spesielt sykehus i helseregionen som avvek fra nasjonale resultater ble trukket frem. 7.3 Resultater til pasienter På publiseres resultater fra kvalitetsregistrene som er tilpasset pasienter og publikum. Disse sidene driftes av Nasjonalt servicemiljø for medisinske kvalitetsregistre. I forbindelse med offentliggjøringen av årsrapportene lages det nyhetssaker som publiseres på Kreftregisterets hjemmesider ( og i andre nyhetsmedier. Årsrapportene ligger tilgjengelig på begge disse nettsidene. Årsrapporten for prostatakreftregisteret vil bli sendt til Prostatakreftforeningen slik at de kan gjøre resultatene tilgjengelig for sine medlemmer. Rapporten vil også bli sent til regionalt brukerutvalg i de Regionale helseforetakene. Resultatene vil bli diskutert på møtet i brukerpanelet som Kreftregisteret arrangerer i november Offentliggjøring av resultater til institusjonsnivå Registeret offentliggjør resultater på institusjonsnivå eller fylkesnivå. Alle regionale helseforetak får tilsendt årsrapportene for kvalitetsregistrene på kreftområdet i god tid før publisering slik at de kan gå gjennom sine egne resultater og forberede seg før rapportene blir allment tilgjengelige. Det er også mulig for hver enkelt institusjon å henvende seg til Kreftregisteret for å få en nærmere gjennomgang og utdyping av sine resultater. I 2017 sendes årsrapporten fra Kreftregisteret til RHFene 1. oktober, og offentliggjøringen er planlagt til 13. november. Side 83 av 114
84 8 SAMARBEID OG FORSKNING 8.1 Samarbeid med andre helse- og kvalitetsregistre Kreftregisteret har et tett samarbeid med de andre nordiske kreftregistrene. Årlig møtes representanter fra alle de nordiske landene for å lære av hverandre og etablere samarbeidsområder. Kreftregisteret og prostatakreftregisteret samarbeider også med andre norske helse- og kvalitetsregistre. Våren 2017 ble det satt i gang et samarbeidsprosjekt mellom Kreftregisteret og Norsk pasientregister. Målet er å vurdere komplettheten på informasjon om prostatektomi og strålebehandling ved å gjøre dekningsgradsanalyser på prosedyrekoder registrert hos Norsk pasientregister 8.2 Vitenskapelige arbeider Det er gitt ut data fra Prostatakreftregisteret til åtte ulike forskningsprosjekter i 2016, i tillegg til en rekke utleveringer av generell statistikk og tabeller. I første halvdel av 2017 ble det gitt ut data til fire forskningsprosjekter Oversikt over publikasjoner med bruk av data fra Prostatakreftregisteret : Kirsti Aas, Karol Axcrona, Rune Kvåle, Bjørn Møller, Tor Åge Myklebust, Ulrika Axcrona, Sophie Dorothea Fosså, 10-Year Mortality in Men with NonMetastatic Prostate Cancer in Norway, Urology (2017), /j.urology Kvåle, R., Myklebust, T.Å., Engholm, G., Heinävaara, S., Wist, E. and Møller, B. (2017), Prostate and breast cancer in four Nordic countries: A comparison of incidence and mortality trends across countries and age groups Int. J. Cancer. doi: /ijc Vatne K, Stensvold A, Myklebust TÅ, Møller B, Svindland A og Fosså SD. Pre- and postprostatectomy variables associated with pelvic post-operative radiotherapy in prostate cancer patients: a national registry-based study, Acta Oncologica, DOI: / X Sæter, T., Vlatkovic, L., Waaler, G., Servoll, E., Nesland, J. M., Axcrona, K. and Axcrona, U. (2017), Intraductal Carcinoma of the Prostate on Diagnostic Needle Biopsy Predicts Prostate Cancer Mortality: A Population-Based Study. Prostate, 77: doi: /pros : Sigrun Dahl, Milada Cvancarova, Alv A. Dahl & Sophie D. Foss å (2016) Work ability in prostate cancer survivors after radical prostatectomy, Scandinavian Journal of Urology,50:2, , DOI: / Sæter, T., Bogaard, M., Vlatkovic, L., Waaler, G., Servoll, E., Nesland, J. M., Axcrona, K. and Axcrona, U. (2016), The relationship between perineural invasion, tumor grade, reactive stroma and prostate cancer-specific mortality: A clinicopathologic study on a population-based cohort. Prostate, 76: doi: /pros : 34 Oversikt over publikasjoner fra tidligere år enn angitt her finnes i vedlegg. Side 84 av 114
85 Dahl S, Loge JH, Berge V, Cvanvarova M, Dahl AA, Fosså SD. Life 3 Years after Surgery. Influence of Radical Prostatectomy for Prostate Cancer on Work Status and Working. J Cancer Surviv Jun;9(2):172-9 Dahl S., Cvancarova M., Dahl, AA., Fosså, SD. Work ability in prostate cancer survivors after radiaval prostatectomy. Scand J Urol. 2016;50(2): Doktorgrader Pågående doktorgrader som utgår med data fra prostatakreftregisteret. For tiden benyttes kliniske data fra Prostatakreftregisteret i Kari Vatne sin doktorgradstudie, Kirsti Aas sin postdoktor studie og Rune Kvåle sin postdoktor studie Ferdigstilte doktorgrader som utgår fra prostatakreftregisteret Changing Epidemiological Patterns of Prostate Cancer: A Nordic Perspective. Incidence, Mortality, Diagnostic Procedures and Treatment. Rune Kvåle, Ferdigstilte doktorgrader med bidrag fra prostatakreftregisteret Adverse effects and global quality of life after curative treatment for prostate cancer a populationbased cross-sectional survey. Anne Edvardsen Kyrdalen, Outcomes after Curative Treatment of Prostate Cancer Adverse Effects and Surgical Margins. Eivind Andreas Svaboe Steinsvik, Prostate Cancer Progression and Mortality Focus on β-blocker use and β2-adrenergic receptor level. Helene Hartvedt Grytli, Side 85 av 114
86 Del 2 Plan for forbedringstiltak Side 86 av 114
87 9 MOMENTLISTE 9.1 Datafangst Det er svært viktig for Nasjonalt kvalitetsregister for prostatakreft at bevisstheten om rapportering blant sykehusledelse og helsepersonell øker. Ikke alle helseinstitusjoner har gode nok rutiner for å følge opp rapportering til Kreftregisteret. Her må helseinstitusjonene selv gå inn og definere rutiner og prosedyrer som skal gjelde lokalt hos dem, men Kreftregisteret bistår gjerne i dette arbeidet. Kreftregisteret samarbeider nært med flere miljøer og leverandører av IKT-løsninger for å sørge for en så hensiktsmessig datafangst som mulig. Eksempler på samarbeidsprosjekter er: Økt bruk av klinisk relevante data fra Norsk Pasientregister Innhenting av data om medikamentell behandling fra fagsystemer på sykehusene Samarbeid med patologimiljøet om å utarbeide løsninger for mer strukturert, elektronisk rapportering av patologiinformasjon Ehelsedirektoratet jobber med prosjektet «Digital patologi» der elektronisk rapportering til Kreftregisteret inngår på sikt Samarbeid med EPJ-leverandørene for å implementere meldeskjemaene i journalsystemene 9.2 Metodisk kvalitet Kreftregisteret arbeider kontinuerlig med å forbedre rutiner for datafangst, databehandling og intern kvalitetssikring. Analyser og presentasjon av resultatene gjøres av Kreftregisterets egne statistikere. 9.3 Fagutvikling og kvalitetsforbedring av tjenesten På bakgrunn av en artikkel om feilkoding av PSA i National Cancer Institutes SEER database xxxv, skal det foretas en kvalitetssikring av PSA-tallene fra Resultatene vil bli publisert i årsrapport for 2017 årgangen. Referansegruppen har revidert primærutredningsskjemaet, hvor blant annet mer detaljerte MR-data og bruk av multidisiplinære team (MDT) skal kunne meldes. Kirurgiskjema og et primær strålebehandlingsskjema er også utviklet. Alle de nye meldingene ble satt i drift Referansegruppen og Kreftregisteret jobber i tillegg med å kartlegge muligheten for å samle inn PSAdata fra laboratoriene. Det vil da bli mulig å samle inn data om tilbakefall av prostatakreft. Referansegruppen og Kreftregisteret er spesielt opptatt av arbeidet med å innføre PROMs for prostatakreft (se kapittel 6.3). 9.4 Formidling av resultater Det er viktig for fagmiljøet og Kreftregisteret at resultatene fra kvalitetsregisteret blir brukt i kvalitetsforbedring av helsetjenesten og det er viktig at resultatene blir offentlig kjent. Resultatene skal fortsatt formidles gjennom følgende kanaler: I årsrapporter etter årsrapportmal fra Nasjonalt servicemiljø På nettsidene for den nasjonale resultattjenesten På Kreftregisterets nettsider for kvalitetsregistre på kreftområdet Som klinisk statistikk via KREMT-portalen på Norsk Helsenett Som administrativ statistikk via KREMT-portalen på Norsk Helsenett Kvalitetsregisteret jobber aktivt med formidling av årsrapporten som sendes direkte til sykehus og pasientforeningen. Hvert år trekkes også de viktigste resultatene frem i egne pressemeldinger. Side 87 av 114
88 9.5 Samarbeid og forskning Både Kreftregisteret og referansegruppen har ansvar for å initiere relevante forskningsprosjekter som kan nyttiggjøre seg av dataene i prostatakreftregisteret. Side 88 av 114
89 Del 3 Stadievurdering Side 89 av 114
90 10 REFERANSER TIL VURDERING AV STADIUM Tabell 2 Vurderingspunkter for stadium Prostatakreftregisteret Nr Beskrivelse Ikke Kapittel Ja Nei aktuell Stadium 2 1 Er i drift og samler data fra HF i alle helseregioner 3, Presenterer resultater på nasjonalt nivå Har en konkret plan for gjennomføring av dekningsgradsanalyser Har en konkret plan for gjennomføring av analyser og løpende rapportering av resultater på sykehusnivå tilbake til deltakende enheter , Har en oppdatert plan for videre utvikling av registeret Del II Stadium 3 6 Kan redegjøre for registerets datakvalitet Har beregnet dekningsgrad mot uavhengig datakilde 5.2, 5.3, Har dekningsgrad over 60 % Registrerende enheter kan få utlevert egne aggregerte og nasjonale resultater 7.1, 7.2 Presenterer deltakende enheters etterlevelse av de viktigste 10 nasjonale retningslinjer der disse finnes Har identifisert kliniske forbedringsområder basert på analyser 11 fra registeret Brukes til klinisk kvalitetsforbedringsarbeid 6.8, 6.9 Side 90 av 114
91 13 Resultater anvendes vitenskapelig Presenterer resultater for PROM/PREM Har en oppdatert plan for videre utvikling av registeret Del II Stadium 4 Kan dokumentere registerets datakvalitet gjennom 16 valideringsanalyser 5.6, Presenterer oppdatert dekningsgradsanalyse hvert 2. år 5.2, 5.3, Har dekningsgrad over 80% 5.4 Registrerende enheter har løpende (on-line) tilgang til 19 oppdaterte egne og nasjonale resultater Resultater fra registeret er tilpasset og tilgjengelig for pasienter 7.3 Kunne dokumentere at registeret har ført til 21 kvalitetsforbedring/endret klinisk praksis Resultater er ikke presentert i årsrapporten, men data er samlet inn fra mars 2017 og foreløpige resultater er vist på flere nasjonale og internasjonale møter. Side 91 av 114
92 11 VEDLEGG 11.1 Forfattere og andre bidragsytere til årsrapporten Forfattere: Arbeidsgruppen som består av Erik Skaaheim Haug (leder av referansegruppen), Christoph Müller, Tore Knutsen, Øystein Størkersen, Ylva Maria Gjelsvik, Tom Børge Johannesen og Kim Lund Nilsen (kvalitetsregisteransvarlig for Nasjonalt kvalitetsregister for Prostatakreft) Analyser og statistikk: Tor Åge Myklebust Koding, registrering og kvalitetssikring: Ingrid Forberg, Kim Lund Nilsen, Silje Spinnangr Olsen og Tanja Nygård Standardtekster, koordinering, og kvalitetskontroll: Lena Holmström og Liv Marit Rønning Dørum 11.2 Referansegruppen for Nasjonalt kvalitetsregister for prostatakreft Tabell 3 Oversikt over referansegruppens medlemmer, deres spesialitet og tilhørighet. Navn Spesialitet Tilhørighet Axcrona, Karol Urologi Akershus Universitetssykehus Axcrona, Ulrika Patologi Oslo Universitetssykehus Beisland, Christian Urologi Haukeland Universitetssykehus Berg, Arne S. (nestleder) Onkologi Vestre Viken- Drammen sykehus Berge, Viktor Urologi Oslo Universitetssykehus - Aker Christiansen, Ola Urologi Sykehuset Innlandet - Hamar Eri, Lars Magne Urologi Oslo Universitetssykehus - Aker Espeland, Hans Urologi Stavanger Universitetssykehus Fosså, Sophie D Onkologi Oslo Universitetssykehus Gjelsvik, Ylva (PROMs) Rådgiver Kreftregisteret Haug, Erik Skaaheim (leder) Urologi Sykehuset i Vestfold Hoem, Lars Urologi Nordlandssykehuset - Bodø Johannesen, Tom Børge Onkolog Kreftregisteret Johannessen, Dag Clement Onkolog Oslo Universitetssykehus - Ullevål Kjøbli, Eirik Urologi St. Olavs Hospital Klem, Knut Henning Urologi Dr. Klems klinikk Knutsen, Tore Urologi Universitetssykehuset i Nord-Norge Kvåle, Rune Onkolog Kreftregisteret Langørgen, Sverre Radiologi St. Olavs Hospital Mygland, Vegard Urologi Akershus Universitetssykehus Müller, Christoph Onkologi Sørlandet sykehus - Kristiansand Nilsen, Kim Lund (kvalitetsregisteransvarlig) Sykepleier Kreftregisteret Rørvik, Jarle Radiologi Haukeland Universitetssykehus Stensvold, Andreas Onkologi Norsk urologisk cancergruppe (NUCG) Størkersen, Øystein Patologi St. Olavs hospital Svindland, Aud Patologi Oslo Universitetssykehus Side 92 av 114
93 11.3 Klinisk TNM, prostatakreft Tabell 4 Oversikt over klinisk TNM-klassifikasjon, TX T0 T1 T1a T1b T1c T2 T2a T2b T2c T3 T3a T3b T4 NX N0 N1 M0 M1a M1b M1c Primærtumor kan ikke vurderes. Primærtumor ikke påvist. Ingen tumor påvisbar med palpasjon, ultralyd eller annen radiologisk metode, men cancer er påvist ved prostatabiopsier Ikke palpabel tumor, påvist ved TUR-P, <5 % av resektatet. Ikke palpabel tumor, påvist ved TUR-P, >=5% av resektatet. Ikke palpabel tumor, påvist ved nålebiopsi (for eksempel på grunn av forhøyet PSA). Palpabel eller synlig tumor begrenset til prostatakjertelen. Tumor omfatter en halv lapp eller mindre. Tumor omfatter mer enn halvparten av en lapp, men ikke begge lapper. Tumor omfatter begge lapper. Ekstrakapsulær tumorvekst. Ekstrakapsulær vekst (unilateral eller bilateral). Tumor vokser inn i sædblære(r). Tumor er fiksert eller vokser inn i nabostruktur(er) annet enn sædblære(r). Spredning til regionale lymfeknuter er ikke vurdert. Ingen regionale lymfeknutemetastaser. Regional(e) lymfeknutemetastase(r). Ingen fjernmetastaser. Klinisk undersøkelse og skjelettscintigrafi eller annen bildediagnostikk har ikke gitt holdepunkter for fjernmetastaser. Metastase(r) til fjern(e) lymfeknute(r). Metastase(r) til skjelett. Annen/andre fjernmetastase(r), med eller uten skjelettmetastase(r). Side 93 av 114
94 11.4 Ekstra analyser Utredning Vedlegg 11-1 Oppgitt hovedårsak til utredning av prostatakreftpasienter diagnostisert i Alle aldre, Norge og fylker. Antall pasienter. Fylke Kun PSA LUTS Andre årsaker Ikke oppgitt Akershus Aust-Agder Buskerud Finnmark Hedmark Hordaland Møre og Romsdal Nordland Nord-Trøndelag Norge Oppland Oslo Rogaland Sogn og Fjordane Sør-Trøndelag Telemark Troms Vest-Agder Vestfold Østfold Side 94 av 114
95 Vedlegg 11-2 Oppgitt hovedårsak til utredning av prostatakreftpasienter diagnostisert i Under 70 år, Norge og fylker. Antall pasienter. Fylke Kun PSA LUTS Andre årsaker Ikke oppgitt Akershus Aust-Agder Buskerud Finnmark Hedmark Hordaland Møre og Romsdal Nordland Nord-Trøndelag Norge Oppland Oslo Rogaland Sogn og Fjordane Sør-Trøndelag Telemark Troms Vest-Agder Vestfold Østfold Side 95 av 114
96 Vedlegg 11-3 Oppgitt hovedårsak til utredning av prostatakreftpasienter diagnostisert i Over 70 år, Norge og fylker. Antall pasienter. Fylke Kun PSA LUTS Andre årsaker Ikke oppgitt Akershus Aust-Agder Buskerud Finnmark Hedmark Hordaland Møre og Romsdal Nordland Nord-Trøndelag Norge Oppland Oslo Rogaland Sogn og Fjordane Sør-Trøndelag Telemark Troms Vest-Agder Vestfold Østfold Side 96 av 114
97 Vedlegg 11-4 Oppgitt hovedårsak til utredning av prostatakreftpasienter i Under 70 år, PSA <10ng/mL, Norge og fylker. Antall pasienter. Fylke Kun PSA LUTS Andre årsaker Ikke oppgitt Akershus Aust-Agder Buskerud Finnmark Hedmark Hordaland Møre og Romsdal Nordland Nord-Trøndelag Norge Oppland Oslo Rogaland Sogn og Fjordane Sør-Trøndelag Telemark Troms Vest-Agder Vestfold Østfold Side 97 av 114
98 Pasienter Meldt / Diagnostisert Norge 19% 47% 34% 2577 / 4402 Østfold 20% 45% 35% 168 / 407 Akershus 17% 47% 36% 385 / 534 Oslo 14% 45% 41% 266 / 363 Hedmark 14% 58% 28% 127 / 195 Oppland 18% 51% 31% 108 / 152 Buskerud 15% 54% 31% 158 / 232 Vestfold 10% 37% 53% 139 / 195 Telemark 23% 38% 39% 78 / 134 Aust-Agder 38% 38% 24% 16 / 99 Vest-Agder 17% 37% 46% 35 / 176 Rogaland 27% 48% 25% 243 / 402 Hordaland 22% 51% 27% 293 / 372 Sogn og Fjordane 10% 45% 45% 31 / 82 Møre og Romsdal 27% 55% 18% 159 / 267 Sør-Trøndelag 21% 45% 34% 73 / 255 Nord-Trøndelag 22% 36% 42% 50 / 108 Nordland 17% 40% 43% 114 / 191 Troms 14% 46% 40% 92 / 151 Finnmark 20% 27% 53% 30 / Andel (%) Lav risiko Middels risiko Høy risiko Vedlegg 11-5 Fordeling av risikogrupper ved diagnosetidspunkt. Norge og fylker. Vedlegg 11-5 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Potensielt kurative pasienter, utfylt klinisk primærutredningsmelding Diagnoseår: 2016 Forklaring: Sykehus i slørete gråfarge har en innrapporteringsprosent for klinisk primærutredningsmelding på under 60%. Rapporteringsgrad: 68% Side 98 av 114
99 Pasienter Meldt / Diagnostisert Norge 30% 43% 24% 3332 / 5037 Østfold 25% 51% 23% 198 / 463 Akershus 21% 56% 22% 509 / 613 Oslo 19% 48% 32% 319 / 409 Hedmark 30% 45% 24% 164 / 228 Oppland 22% 42% 30% 6% 152 / 183 Buskerud 20% 53% 21% 6% 214 / 265 Vestfold 21% 37% 40% 202 / 250 Telemark 40% 33% 26% 133 / 152 Aust-Agder 36% 41% 18% 5% 22 / 110 Vest-Agder 24% 38% 36% 45 / 200 Rogaland 55% 26% 15% 292 / 443 Hordaland 43% 35% 20% 358 / 419 Sogn og Fjordane 30% 30% 37% 43 / 101 Møre og Romsdal 45% 38% 14% 194 / 298 Sør-Trøndelag 25% 42% 32% 88 / 286 Nord-Trøndelag 34% 25% 40% 80 / 132 Nordland 27% 66% 6% 143 / 226 Troms 16% 50% 26% 8% 106 / 162 Finnmark 30% 19% 42% 9% 53 / Andel (%) ct1 ct2 ct3 ct4 Vedlegg 11-6 Fordeling av preoperativt klinisk tumorstadie (ct) Vedlegg 11-6 Datakilde: Prostatakreftregisteret Inklusjonskriterier: Diagnostisert prostatakreft, utfylt ct i klinisk primærutredningsmelding Diagnoseår: 2016 Forklaring: Fylke i slørete farge har en innrapporteringsprosent for klinisk primærutredningsmelding på under 60%. Rapporteringsgrad: 68% Side 99 av 114
100 Behandlingsvalg 100 <70 år år Andel (%) Andel (%) Diagnoseår Diagnoseår år år Andel (%) Andel (%) Diagnoseår Diagnoseår Prostatektomi Strålebehandling Aktiv overvåkning Ikke lokalbehandlet/annet Vedlegg 11-7 Andelen pasienter som fikk prostatektomi, strålebehandling, aktiv overvåkning eller som ikke ble lokalbehandlet/fikk annen behandling i de ulike aldersgruppene. Vedlegg 11-7 Datakilde: Klinisk informasjon, stråledata, operasjonsremisse og klinisk primærutredningsmelding Inklusjonskriterier: Diagnostisert prostatakreft, <80 år, stadium ct1-3, N0/NX, M0, PSA 100 ng/ml, fravær av annen kreftdiagnose Diagnoseår: Side 100 av 114
101 Vedlegg 11-8 Behandlingsvalg for alle pasienter <80 år, stadium ct1-3, N0/NX, M0, PSA 100ng/mL og fravær av annen kreftdiagnose. Sortert på risikogrupper. Diagnoseår Behandling Risikogrupper Radikal kirurgi Alle Radikal kirurgi Lav risiko Radikal kirurgi Middels risiko Radikal kirurgi Høy risiko Kurativ strålebehandling Alle Kurativ strålebehandling Lav risiko Kurativ strålebehandling Middels risiko Kurativ strålebehandling Høy risiko Aktiv overvåkning Alle Aktiv overvåkning Lav risiko Aktiv overvåkning Middels risiko Aktiv overvåkning Høy risiko Ikke behandlet Alle Ikke behandlet Lav risiko Ikke behandlet Middels risiko Ikke behandlet Høy risiko Side 101 av 114
102 Vedlegg 11-9 Behandlingsvalg fordelt på fylker og risikogrupper, diagnoseår Norge og fylker. Behandling Fylke Lav risiko Intermediær risiko Høy risiko Aktiv Overvåkning Akershus Aktiv Overvåkning Aust-Agder Aktiv Overvåkning Buskerud Aktiv Overvåkning Finnmark 2 5 Aktiv Overvåkning Hedmark Aktiv Overvåkning Hordaland Aktiv Overvåkning Møre og Romsdal Aktiv Overvåkning Nordland Aktiv Overvåkning Nord-Trøndelag 3 6 Aktiv Overvåkning Oppland Aktiv Overvåkning Oslo Aktiv Overvåkning Rogaland Aktiv Overvåkning Sogn og Fjordane 3 6 Aktiv Overvåkning Sør-Trøndelag Aktiv Overvåkning Telemark Aktiv Overvåkning Troms Aktiv Overvåkning Vest-Agder Aktiv Overvåkning Vestfold Aktiv Overvåkning Østfold Ingen behandling Akershus Ingen behandling Aust-Agder Ingen behandling Buskerud Ingen behandling Finnmark Ingen behandling Hedmark Ingen behandling Hordaland Ingen behandling Møre og Romsdal Ingen behandling Nordland Ingen behandling Nord-Trøndelag Ingen behandling Oppland Ingen behandling Oslo Ingen behandling Rogaland Ingen behandling Sogn og Fjordane Ingen behandling Sør-Trøndelag Ingen behandling Telemark Ingen behandling Troms Ingen behandling Vest-Agder Ingen behandling Vestfold Ingen behandling Østfold Prostatektomi Akershus Prostatektomi Aust-Agder Side 102 av 114
103 Prostatektomi Buskerud Prostatektomi Finnmark Prostatektomi Hedmark Prostatektomi Hordaland Prostatektomi Møre og Romsdal Prostatektomi Nordland Prostatektomi Nord-Trøndelag Prostatektomi Oppland Prostatektomi Oslo Prostatektomi Rogaland Prostatektomi Sogn og Fjordane Prostatektomi Sør-Trøndelag Prostatektomi Telemark Prostatektomi Troms Prostatektomi Vest-Agder Prostatektomi Vestfold Prostatektomi Østfold Strålebehandling Akershus Strålebehandling Aust-Agder 9 11 Strålebehandling Buskerud Strålebehandling Finnmark Strålebehandling Hedmark 8 18 Strålebehandling Hordaland Strålebehandling Møre og Romsdal Strålebehandling Nordland Strålebehandling Nord-Trøndelag Strålebehandling Oppland Strålebehandling Oslo Strålebehandling Rogaland Strålebehandling Sogn og Fjordane 3 9 Strålebehandling Sør-Trøndelag 8 32 Strålebehandling Telemark 5 10 Strålebehandling Troms Strålebehandling Vest-Agder 6 11 Strålebehandling Vestfold 4 19 Strålebehandling Østfold Side 103 av 114
104 Vedlegg Behandlingsvalg for alle pasienter <80 år, stadium ct1-3, N0/NX, M0, PSA <= 100 ng/ml, og fravær av annen kreftdiagnose. De regionale helseforetakene. Diagnoseår Behandling Radikal kirurgi Radikal kirurgi Radikal kirurgi Radikal kirurgi Helseforetak Helse Sør-Øst Helse Vest Helse Midt Helse Nord Kurativ strålebehandling Kurativ strålebehandling Kurativ strålebehandling Kurativ strålebehandling Helse Sør-Øst Helse Vest Helse Midt Helse Nord Aktiv overvåkning Aktiv overvåkning Aktiv overvåkning Aktiv overvåkning Helse Sør-Øst Helse Vest Helse Midt Helse Nord Ikke behandlet Ikke behandlet Ikke behandlet Ikke behandlet Helse Sør-Øst Helse Vest Helse Midt Helse Nord Side 104 av 114
105 Vedlegg Antall radikale prostatektomier pr. sykehus i Norge, Sykehus Ahus, Lørenskog Diakonhjemmets sykehus Haukeland universitetssykehus Helgelandsykehuset, Mo i Rana Helse Nord-Trøndelag, Levanger Helse-Fonna, Haugesund Helse-Fonna, Stord Helse-Førde, Førde Nordlandssykehuset, Bodø OUS, Aker OUS, Radiumhospitalet OUS, Rikshospitalet St. Olavs hospital St. Olavs hospital, Orkdal Stavanger universitetssjukehus Sykehuset i Vestfold, Tønsberg Sykehuset Innlandet, Hamar Sykehuset Telemark, Porsgrunn Sykehuset Telemark, Skien Sykehuset Østfold, Fredrikstad Sørlandet Sykehus, Arendal Sørlandet Sykehus, Kristiansand UNN, Tromsø Vestre Viken, Bærum Vestre Viken, Drammen Vestre Viken, Hønefoss Side 105 av 114
106 Vedlegg Antall prostatektomier i de ulike risikogruppene, og hvorvidt det er utført lymfeknutedisseksjon. Operasjonsårene Norge. Risikogruppe Operasjonsår Totalt antall Ja Nei Ukjent Lav risiko (9%) 22 (29%) 48 (62%) Lav risiko (17%) 33 (26%) 74 (57%) Lav risiko (9%) 39 (25%) 103 (66%) Lav risiko (12%) 44 (24%) 117 (64%) Lav risiko (11%) 70 (28%) 153 (61%) Lav risiko (11%) 77 (34%) 126 (55%) Lav risiko (5%) 78 (30%) 164 (65%) Lav risiko (9%) 114 (50%) 91 (41%) Lav risiko (6%) 139 (52%) 110 (42%) Lav risiko (3%) 117 (58%) 78 (39%) Lav risiko (3%) 77 (52%) 65 (45%) Lav risiko (7%) 69 (57%) 43 (36%) Lav risiko (10%) 40 (50%) 32 (40%) Middels risiko (26%) 23 (18%) 74 (56%) Middels risiko (20%) 64 (24%) 146 (56%) Middels risiko (29%) 68 (20%) 169 (51%) Middels risiko (23%) 97 (24%) 219 (53%) Middels risiko (26%) 137 (25%) 275 (49%) Middels risiko (28%) 136 (24%) 273 (48%) Middels risiko (27%) 165 (25%) 308 (48%) Middels risiko (23%) 325 (40%) 303 (37%) Middels risiko (18%) 448 (47%) 324 (35%) Middels risiko (20%) 379 (44%) 314 (36%) Middels risiko (18%) 336 (44%) 294 (38%) Middels risiko (20%) 412 (44%) 328 (36%) Middels risiko (26%) 241 (36%) 254 (38%) Høy risiko (24%) 8 (20%) 23 (56%) Høy risiko (29%) 7 (13%) 33 (58%) Høy risiko (40%) 12 (13%) 44 (47%) Høy risiko (42%) 19 (14%) 62 (44%) Høy risiko (57%) 35 (16%) 61 (27%) Høy risiko (62%) 45 (20%) 42 (18%) Høy risiko (64%) 41 (15%) 60 (21%) Høy risiko (66%) 63 (18%) 59 (16%) Høy risiko (64%) 89 (21%) 61 (15%) Høy risiko (68%) 69 (16%) 64 (16%) Høy risiko (69%) 78 (18%) 61 (13%) Høy risiko (75%) 77 (15%) 54 (10%) Høy risiko (73%) 55 (11%) 77 (16%) Side 106 av 114
107 Vedlegg Antall lymfeknutedisseksjoner under prostatektomier, og antall negative/positive funn. Operasjonsårene Norge. Risikogruppe Operasjonsår Totalt antall Ja Nei Ukjent Lav risiko (100%) 0 (0%) 0 (0%) Lav risiko (100%) 0 (0%) 0 (0%) Lav risiko (100%) 0 (0%) 0 (0%) Lav risiko (95%) 1 (5%) 0 (0%) Lav risiko (100%) 0 (0%) 0 (0%) Lav risiko (100%) 0 (0%) 0 (0%) Lav risiko (100%) 0 (0%) 0 (0%) Lav risiko (100%) 0 (0%) 0 (0%) Lav risiko (94%) 1 (6%) 0 (0%) Lav risiko (100%) 0 (0%) 0 (0%) Lav risiko (80%) 1 (20%) 0 (0%) Lav risiko (78%) 2 (22%) 0 (0%) Lav risiko (100%) 0 (0%) 0 (0%) Lav risiko (100%) 0 (0%) 0 (0%) Middels risiko (100%) 0 (0%) 0 (0%) Middels risiko (98%) 0 (0%) 1 (2%) Middels risiko (97%) 2 (2%) 1 (1%) Middels risiko (97%) 3 (3%) 0 (0%) Middels risiko (97%) 3 (2%) 1 (1%) Middels risiko (88%) 10 (6%) 9 (6%) Middels risiko (91%) 6 (3%) 10 (6%) Middels risiko (96%) 7 (4%) 0 (0%) Middels risiko (90%) 16 (9%) 1 (1%) Middels risiko (92%) 14 (8%) 0 (0%) Middels risiko (91%) 10 (7%) 2 (2%) Middels risiko (91%) 16 (8%) 0 (1%) Middels risiko (91%) 15 (9%) 0 (0%) Høy risiko (80%) 2 (20%) 0 (0%) Høy risiko (81%) 3 (19%) 0 (0%) Høy risiko (86%) 5 (14%) 0 (0%) Høy risiko (86%) 8 (14%) 0 (0%) Høy risiko (91%) 10 (8%) 1 (1%) Høy risiko (87%) 17 (12%) 2 (1%) Høy risiko (84%) 19 (10%) 10 (6%) Høy risiko (84%) 36 (16%) 2 (0%) Høy risiko (83%) 45 (17%) 1 (0%) Høy risiko (80%) 56 (19%) 0 (1%) Høy risiko (75%) 75 (25%) 0 (0%) Høy risiko (83%) 68 (17%) 0 (0%) Høy risiko (79%) 76 (21%) 0 (0%) Side 107 av 114
108 Vedlegg Antall pasienter som har fått postoperativ strålebehandling i de regionale helseforetakene, operasjonsårene Tre års obsersvasjonstid. Operasjonsår Helse Sør-Øst Helse Vest Helse Midt Helse Nord (11%) 2 (6%) 3 (12%) 9 (19%) (11%) 19 (26%) 1 (2%) 12 (20%) (12%) 11 (11%) 6 (7%) 17 (21%) (13%) 18 (13%) 11 (9%) 30 (34%) (15%) 34 (15%) 14 (10%) 24 (20%) (18%) 49 (23%) 21 (16%) 33 (24%) (16%) 53 (21%) 20 (11%) 32 (22%) (21%) 44 (15%) 16 (9%) 27 (18%) (15%) 55 (17%) 24 (9%) 30 (20%) Side 108 av 114
109 11.5 Tidligere publikasjoner med data fra prostatakreftregisteret 2014: Holm HV, Fosså SD, Hedlund H, et al. How should continence and incontinence after radical prostatectomy be evaluated? A prospective study of patient-ratings and changes over time Oct;192(4): Storås AH, Sanda MG, Ferrer M, Loge JH, Dahl AA, Steinsvik EAS, Gueda F, Cvancarova M, Fosså SD. Localized prostate cancer in Norway, the United States, and Spain: Between-country differences of variables before treatment among patients eligible for curative treatment. Clin Genitourin Cancer Aug;12(4):e Dahl S, Steinsvik EA, Dahl AA, Loge JH, Cvancarova M, Fosså SD. Return to work and sick leave after radical prostatectomy: A prospective clinical study. Acta Oncol Jun;53(6): Fosså SD, Nilssen Y, Kvåle R, Hernes E, Axcrona K, Møller B. Treatment and 5-year survival in patients with non-metastatic prostate cancer: The Norwegian experience. Urology Jan;83(1): Grytli HH, Fagerland MW, Fosså SD, Taskén KA. Association between use of β-blockers and Prostate Cancer-Specific Survival: A Cohort Study of 3561 Prostate Cancer Patients with High-Risk or Metastatic Disease. Eur Urol Mar;65(3): : Holm HV, Fosså SD, Hedlund H, Dahl AA. Study of generic quality of life in patients operated for postprostatectomy incontinence. Int J Urol Sep;20(9): Steinsvik EAS, Axcrona K, Angelsen A, Beisland C, Dahl AA, Eri LM, Haug ES, Svindland A, Fosså SD. Does a surgeon s annual radical prostatectomy volume predict the risk of positive surgical margins and urinary incontinence at one-year follow-up? Finding from a prospective national study. Scand J Urol Apr;47(2): Grytli HH, Fagerland MW, Fosså SD, Taskén KA, Håheim LL. Use of β-blockers is associated with prostate cancer-specific survival in prostate cancer patients on androgen deprivation therapy. The Prostate Feb 15;73(3): Kyrdalen AE, Dahl AA, Hernes E, Småstuen MC, Fosså SD. A national study of adverse effects and global quality of life among candidates for curative treatment for prostate cancer. BJU Int Feb;111(2): : Steinsvik EAS, Axcrona K, Dahl AA, Eri LM, Stensvold A, Fosså SD. Can sexual bother after radical prostatectomy be predicted preoperatively? Findings from a prospective national study of the relation between sexual function, activity and bother. BJU Int May;109(9): : Hernes E, Kyrdalen A, Kvåle R, Hem E, Klepp O, Axcrona K, Fosså SD. Initial management of prostate cancer: first year experience with the Norwegian National Prostate Cancer Registry. BJU Int Mar;105(6): Kyrdalen AE, Dahl AA, Hernes E, Cvancarova M, Fosså SD. Fatigue in hormone-naïve prostate cancer patients treated with radical prostatectomy or definitive radiotherapy. Prostate Cancer Side 109 av 114
110 Prostatic Dis Jun;13(2): Kvåle R, Møller B, Angelsen A, Dahl O, Fosså SD, Halvorsen OJ, Hoem L, Solberg A, Wahlqvist R, Bray F. Regional trends in prostate cancer incidence, treatment with curative intent and mortality in Norway Cancer Epidemiol Aug;34(4): Kyrdalen AE, Dahl AA, Hernes E, Hem E, Fosså SD. Fatigue in prostate cancer survivors treated with definitive radiotherapy and LHRH analogs. Prostate Sep 15;70(13): : Kvåle R, Møller B, Wahlqvist R, Fosså SD, Berner A, Busch C, Kyrdalen AE, Svindland A, Viset T, Halvorsen OJ. Concordance between Gleason scores of needle biopsies and radical prostatectomy specimens: a population-based study.bju Int Jun;103(12): Grindedal EM, Møller P, Eeles R, Stormorken AT, Bowitz-Lothe IM, Landrø SM, Clark N, Kvåle R, Shanley S, Maehle L. Germ-line mutations in mismatch repair genes associated with prostate cancer. Cancer Epidemiol Biomarkers Prev Sep;18(9): : Kvåle R, Auvinen A, Adami HO, Klint A, Hernes E, Møller B, Pukkala E, Storm HH, Tryggvadottir L, Tretli S, Wahlqvist R, Weiderpass E, Bray F. Interpreting trends in prostate cancer incidence and mortality in the five Nordic countries. J Natl Cancer Inst Dec 19;99(24): : Kvåle R, Skarre E, Tønne A, Kyrdalen AE, Norstein J, Angelsen A, Wahlqvist R, Fosså SD. Curative treatment of prostatic cancer in Norway in 1998 and Tidsskr Nor Laegeforen Mar 23;126(7): Side 110 av 114
111 11.6 Figuroversikt Figur 1 Kvalitetsmål fra årsrapport 2016 fra Nasjonalt kvalitetsregister for prostatakreft. Norge, prosent Figur 2 Utviklingsindikatorer for årsrapport 2016 fra Nasjonalt kvalitetsregister for prostatakreft. Norge, prosent Figur 3 Insidensrater for prostatakreft pr personår for ulike aldersgrupper Figur 4 Stadium ved diagnose Figur 5 Forekomst av prostatakreft, aldersgruppert Figur 6 Risikogrupper, aldersfordeling Figur 7 Dødelighetsrater for prostatakreft pr personår, gruppert etter alder ved død. 20 Figur 8 Alder ved død av prostatakreft Figur 9 Prevalens etter stadium ved diagnose Figur 10 Prevalens, aldersgruppert (alder ved diagnose) Figur 11 Utredet kun på grunn av forhøyet PSA, <70 år, Norge og fylker Figur 12 Utredet kun på grunn av forhøyet PSA, >70 år, Norge og fylker Figur 13 Gruppert PSA-verdi ved diagnosetidspunkt, fra Figur 14 Gruppert PSA-verdi ved diagnosetidspunkt, fylker Figur 15 Median PSA-verdi ved diagnosetidspunkt, aldersgrupper Figur 16 Gruppert Gleason score ved diagnosetidspunkt Figur 17 Gleason score (høyeste) i første maligne vevsprøve. Norge og laboratorier Figur 18 Samsvar høyeste Gleason score i vevsprøve før prostatektomi, og høyeste Gleason score i prostatektomi Figur 19 Risikogrupper ved diagnosetidspunkt Figur 20 Klinisk tumorstadium (ct) Figur 21 Behandlingsvalg i Norge Figur 22 Behandlingsvalg, fordelt på risikogrupper. Registrering av aktiv overvåkning begynte i Figur 23 Aktiv overvåking for lav-risikogruppen, Norge og fylker Figur 24 Radikalt behandlede, lavrisikogruppen. Norge og fylker Figur 25 Radikalt behandlede, høyrisikogruppen. Norge og fylker Figur 26 Risikogruppering (preoperativt) av prostatektomerte pasienter, operasjonssykehus. 42 Figur 27 Radikal prostatektomi. Bostedsfylke og Norge Figur 28 Kurativ strålebehandling, fylker Figur 29 Prostatektomi i de ulike risikogruppene Figur 30 Pasientmigrasjon for operasjon 2016, bostedsfylke Figur 31 Preoperativ klinisk tumorstadium (ct) for 2016, sykehus Figur 32 Fordeling patologisk tumorstadium (pt) pr. sykehus Figur 33 Samsvar klinisk tumorstadium (ct) og patologisk tumorstadium (pt) Figur 34 Lymfeknutedisseksjoner / under prostatektomi, høyrisiko (vurdert før operasjon) Figur 35 Ufri reseksjonsrand for prostatektomier ved pt2 prostatakreft Figur 36 Ufri reseksjonsrand for prostatektomier ved pt3 prostatakreft Figur 37 Kurativ strålebehandling i de ulike risikogruppene Figur 38 Pasienter som fikk postoperativ strålebehandling Figur 39 Postoperativ strålebehandling ved stadium pt2 pr. opererende sykehus Figur 40 Postoperativ strålebehandling ved lokalavansert prostatakreft stadium pt3 pr. opererende sykehus Figur 41 Postoperativ strålebehandling for de ulike risikogruppene, opp til 3 år etter operasjon Figur 42 Dødelighet og dødsårsaker, aldersgrupper, 0-10 år etter diagnose Figur 43 Dødelighet og dødsårsaker for ulike behandlingsvalg Figur 44 Dødelighet og dødsårsaker for risikogrupper og metastatisk sykdom år etter diagnose Figur 45 Relativ overlevelse 5 år etter diagnose, høyrisikogruppen. Norge og fylker. Prosent. 65 Figur 46 Relativ overlevelse 5 år etter diagnose, metastaser på diagnosetidspunktet (primærmetastatisk) Figur 47 Rapporteringsgrad av klinisk primærutredningsmelding ved prostatakreft Figur 48 Rapportert innen 60 dager etter ferdig utredning Figur 49 Rapporteringsgrad for klinisk melding etter radikal prostatektomi Figur 50 Rapportert innen 60 dager etter utført kirurgi Side 111 av 114
112 11.7 Tabelloversikt Tabell 1 Antall nye pasienter, antall døde av prostatakreft og personer som lever med prostatakreft. Norge, Tabell 2 Vurderingspunkter for stadium Prostatakreftregisteret Tabell 3 Oversikt over referansegruppens medlemmer, deres spesialitet og tilhørighet Tabell 4 Oversikt over klinisk TNM-klassifikasjon, Side 112 av 114
113 12 REFERANSER i Epstein et al. (2005). The 2005 International Society of Urological Pathology (ISUP) Consensus Conference on Gleason Grading of Prostatic Carcinoma. Am J Surg Pathol 2005 Sep;29: ii Humphrey (2004). Gleason grading and prognostic factors in carcinoma of the prostate. Modern Pathology (2004) 17, iii iv Helsedirektoratet (2015). v vi Helsedirektoratet (2015): vii Heidenreich et al. (2014): EAU Guidelines on Prostate Cancer. Part 1. Screening, Diagnosis, and Local Treatment with Curative Intent Update Eur Urology 2014 Jan;65: viii Sobin et al. (2009) TNM. Classification of Malignant Tumours. Seventh edition. Wiley-Blackwell. S 7-8. ix Ibid. x Albertsen PC (2008). The face of high risk prostate cancer. World J Urol Jun;26(3): Doi: /s Epub 2008 Apr 10. xi august xii august xiii xiv Hadley J, Yabroff R, Barret MJ, et. al. Comparative effectiveness of prostate cancer treatments: evaluating statistical adjustments for confounding in observational data. J National Cancer Institute 2011; 102; ; Wolff RE, Ryder S, Bossi A., et al.; A systematic review of randomized controlled trials of radiotherapy for localized prostate cancer. Eur J Cancer 2015; 51 (16), xv 10-Year outcomes after monitoring, surgery, or radiotherapy for localized prostate cancer. xvi Helsedirektoratet (2015). xvii Kari Vatne, Andreas Stensvold, Tor Å. Myklebust, Bjørn Møller, Aud Svindland,Rune Kvåle & Sophie D. Fosså (2017): Pre- and post-prostatectomy variables associated with pelvic post-operative radiotherapy in prostate cancer patients: a national registry-based study, Acta Oncologica, DOI: / X xviii Bray F, Parkin DM. Evaluation of data quality in the cancer registry: principles and methods. Part I: comparability, validity and timeliness. European journal of cancer Mar 31;45(5): xix Predicting 15-Year prostate cancer specific mortality after radical prostatectomy. xx There is more to life than death. xxi 10-year outcomes after monitoring, surgery, or radiotherapy for localized prostate cancer. xxii Long-term follow-up of a large active surveillance cohort of patients with prostate cancer. xxiii Metastatic prostate cancer in men initially treated with active surveillance. xxiv Mortality among men with locally advanced prostate cancer managed with noncurative intent: A nationwide study in PCBaSe Sweden. xxv Endocrine treatment, with or without radiotherapy, in locally advanced prostate cancer (SPCG- 7/SFUO-3): an open randomised phase III trial. xxvi Combined androgen deprivation therapy and radiation therapy for locally advanced prostate cance: a randomised, phase 3 trail. Side 113 av 114
114 xxvii Radical prostatectomy or watchful waiting in early prostate cancer. xxviii Radical prostatectomy versus observation for localized prostate cancer. xxix The benefits and harms of different extents of lymph node dissection during radical prostatectomy for prostate cancer: A systematic review. xxx Positive surgical margins after radical prostatectomy: a systematic review and contemporary update. xxxi The impact of solitary and multiple positive surgical margins on hard clinical end points in 1712 adjuvant treatment-naïve pt2-4 N0 radical prostatectomy patients. xxxii Kari Vatne, Andreas Stensvold, Tor Å. Myklebust, Bjørn Møller, Aud Svindland, Rune Kvåle & Sophie D. Fosså (2017): Pre- and post-prostatectomy variables associated with pelvic post-operative radiotherapy in prostate cancer patients: a national registry-based study, Acta Oncologica, DOI: / X xxxiii Risk factors associated with positive surgical margins following radical prostatectomy for clinically localized prostate cancer: can nerve-sparing surgery increase the risk? xxxiv A multinational, multi-institutional study comparing positive surgical margin rates among open, laparoscopic, and robot-assisted radical prostatectomy patients. xxxv Furlow (2015): US National Cancer Institute investigates PSA coding errors. Lancet Oncol June; 16(6):614 Side 114 av 114
115 Årsrapport 2016 Kreftregisteret
Årsrapport. Resultater og forbedringstiltak fra. Nasjonalt kvalitetsregister for prostatakreft
 Årsrapport 2017 Resultater og forbedringstiltak fra Nasjonalt kvalitetsregister for prostatakreft Anbefalt referanse: Årsrapport 2017 med resultater og forbedringstiltak fra Nasjonalt kvalitetsregister
Årsrapport 2017 Resultater og forbedringstiltak fra Nasjonalt kvalitetsregister for prostatakreft Anbefalt referanse: Årsrapport 2017 med resultater og forbedringstiltak fra Nasjonalt kvalitetsregister
Nasjonalt kvalitetsregister for. prostatakreft. Årsrapport 2004-2013 (2014)
 Nasjonalt kvalitetsregister for prostatakreft Årsrapport 2004-2013 (2014) Årsrapport Kreftregisteret FORORD Årsrapporten for 2015 fra Nasjonalt kvalitetsregister for prostatakreft er den tredje rapporten
Nasjonalt kvalitetsregister for prostatakreft Årsrapport 2004-2013 (2014) Årsrapport Kreftregisteret FORORD Årsrapporten for 2015 fra Nasjonalt kvalitetsregister for prostatakreft er den tredje rapporten
Årsrapport. Resultater og forbedringstiltak fra. Nasjonalt kvalitetsregister for prostatakreft
 Årsrapport 2018 Resultater og forbedringstiltak fra Nasjonalt kvalitetsregister for prostatakreft Anbefalt referanse: Årsrapport 2018 med resultater og forbedringstiltak fra Nasjonalt kvalitetsregister
Årsrapport 2018 Resultater og forbedringstiltak fra Nasjonalt kvalitetsregister for prostatakreft Anbefalt referanse: Årsrapport 2018 med resultater og forbedringstiltak fra Nasjonalt kvalitetsregister
Nasjonalt kvalitetsregister for. prostatakreft. Årsrapport 2015
 Nasjonalt kvalitetsregister for prostatakreft Årsrapport 2015 FORORD Utredning og behandling av prostatakreft har i løpet av en 20 årsperiode vært igjennom betydelige endringer. Fra å være en tilstand
Nasjonalt kvalitetsregister for prostatakreft Årsrapport 2015 FORORD Utredning og behandling av prostatakreft har i løpet av en 20 årsperiode vært igjennom betydelige endringer. Fra å være en tilstand
Cancer in Norway 2015
 Cancer in Norway 2015 Kreftinsidens, mortalitet, overlevelse og prevalens i Norge Norsk sammendrag CiN 2015 Image: Shutterstock Norsk sammendrag Kreft i Norge 2015 Hvordan forstå krefttall I vår årlige
Cancer in Norway 2015 Kreftinsidens, mortalitet, overlevelse og prevalens i Norge Norsk sammendrag CiN 2015 Image: Shutterstock Norsk sammendrag Kreft i Norge 2015 Hvordan forstå krefttall I vår årlige
Nasjonalt kvalitetsregister for. lungekreft. «Fra insidens til revisjon»
 Nasjonalt kvalitetsregister for lungekreft «Fra insidens til revisjon» Norsk lungekreft 1996 Norsk lungekreft 1996 Insidens 1500 Mannesykdom Gjennomsnittlig overlevelse
Nasjonalt kvalitetsregister for lungekreft «Fra insidens til revisjon» Norsk lungekreft 1996 Norsk lungekreft 1996 Insidens 1500 Mannesykdom Gjennomsnittlig overlevelse
Nasjonalt kvalitetsregister for. prostatakreft. Årsrapport 2014
 Nasjonalt kvalitetsregister for prostatakreft Årsrapport 214 Årsrapport 214 Kreftregisteret FORORD Denne rapporten representerer et samarbeid mellom Kreftregisteret og representanter fra de kliniske fagmiljøene.
Nasjonalt kvalitetsregister for prostatakreft Årsrapport 214 Årsrapport 214 Kreftregisteret FORORD Denne rapporten representerer et samarbeid mellom Kreftregisteret og representanter fra de kliniske fagmiljøene.
Dødelighet og kirurgi ved prostatakreft - om kvalitet og sammenlignbarhet
 Dødelighet og kirurgi ved prostatakreft - om kvalitet og sammenlignbarhet Erik Skaaheim Haug Leder, referansegruppen NPPC / Urolog Sykehuset i Vestfold Hva er Hagen-effekten?? Nei, det er ikke 80 norske
Dødelighet og kirurgi ved prostatakreft - om kvalitet og sammenlignbarhet Erik Skaaheim Haug Leder, referansegruppen NPPC / Urolog Sykehuset i Vestfold Hva er Hagen-effekten?? Nei, det er ikke 80 norske
[Navn på register] Årsrapport for [årstall] med plan for forbedringstiltak
![[Navn på register] Årsrapport for [årstall] med plan for forbedringstiltak [Navn på register] Årsrapport for [årstall] med plan for forbedringstiltak](/thumbs/91/107086374.jpg) [Navn på register] Årsrapport for [årstall] med plan for forbedringstiltak [OLA NORMANN, MEDEL SVENSSON OG KARI NORMANN] [Dato] Bakgrunn og veiledning til utfylling Bakgrunn En årsrapport fra et medisinsk
[Navn på register] Årsrapport for [årstall] med plan for forbedringstiltak [OLA NORMANN, MEDEL SVENSSON OG KARI NORMANN] [Dato] Bakgrunn og veiledning til utfylling Bakgrunn En årsrapport fra et medisinsk
Erfaring fra offentliggjøring av resultater fra Nasjonalt register for prostatakreft. Helse- og kvalitetsregisterkonferansen 2014
 Erfaring fra offentliggjøring av resultater fra Nasjonalt register for prostatakreft Helse- og kvalitetsregisterkonferansen 2014 Nasjonalt register for prostatakreft Innhold Kliniske opplysninger om pasienter
Erfaring fra offentliggjøring av resultater fra Nasjonalt register for prostatakreft Helse- og kvalitetsregisterkonferansen 2014 Nasjonalt register for prostatakreft Innhold Kliniske opplysninger om pasienter
Nasjonalt kvalitetsregister for. prostatakreft. Årsrapport 2014
 Nasjonalt kvalitetsregister for prostatakreft Årsrapport 214 Årsrapport 214 Kreftregisteret FORORD Denne rapporten representerer et samarbeid mellom Kreftregisteret og representanter fra de kliniske fagmiljøene.
Nasjonalt kvalitetsregister for prostatakreft Årsrapport 214 Årsrapport 214 Kreftregisteret FORORD Denne rapporten representerer et samarbeid mellom Kreftregisteret og representanter fra de kliniske fagmiljøene.
Navn på register Årsrapport for [årstall] med plan for forbedringstiltak
![Navn på register Årsrapport for [årstall] med plan for forbedringstiltak Navn på register Årsrapport for [årstall] med plan for forbedringstiltak](/thumbs/55/37048416.jpg) Navn på register Årsrapport for [årstall] med plan for forbedringstiltak Ola Normann 1, Medel Svensson 2 og Kari Normann 1 1 et Sykehus, et Foretak, et Sted 2 en annen adresse, et annet Sted 21. mai 2015
Navn på register Årsrapport for [årstall] med plan for forbedringstiltak Ola Normann 1, Medel Svensson 2 og Kari Normann 1 1 et Sykehus, et Foretak, et Sted 2 en annen adresse, et annet Sted 21. mai 2015
Årsrapport 2007 inkludert nasjonale tall for Nasjonalt Program for Prostatacancer
 Årsrapport 2007 inkludert nasjonale tall for 2004-2007 Nasjonalt Program for Prostatacancer Innhold 1. Nasjonalt Program for Prostatacancer (NPPC) 2. Registerrapport: Prostatakreft i Norge 2004 2007 3.
Årsrapport 2007 inkludert nasjonale tall for 2004-2007 Nasjonalt Program for Prostatacancer Innhold 1. Nasjonalt Program for Prostatacancer (NPPC) 2. Registerrapport: Prostatakreft i Norge 2004 2007 3.
Årsrapport. Nasjonalt Program for Prostatacancer
 Årsrapport 2008 Inkludert nasjonale tall for 2004-2008 Nasjonalt Program for Prostatacancer Innhold Nasjonalt Program for Prostatacancer (NPPC) Registerrapport: Prostatakreft i Norge 2004-2008 Utvikling
Årsrapport 2008 Inkludert nasjonale tall for 2004-2008 Nasjonalt Program for Prostatacancer Innhold Nasjonalt Program for Prostatacancer (NPPC) Registerrapport: Prostatakreft i Norge 2004-2008 Utvikling
Prostatakre) Diagnos0kk og Screening. Giske Ursin Direktør Kre)registeret
 Prostatakre) Diagnos0kk og Screening Giske Ursin Direktør Kre)registeret Enorm økning i prostatakre) forekomst de siste 20 år Noe nedgang i dødelighet siste 20 år Forekomst Dødelighet Forekomst, dødelighet
Prostatakre) Diagnos0kk og Screening Giske Ursin Direktør Kre)registeret Enorm økning i prostatakre) forekomst de siste 20 år Noe nedgang i dødelighet siste 20 år Forekomst Dødelighet Forekomst, dødelighet
«Prostatasenter Quo vadis???» Karol Axcrona Avdelingssjef, dr.med. Urologisk avdeling Akershus Universitetssykehus 2.11.2015
 «Prostatasenter Quo vadis???» Karol Axcrona Avdelingssjef, dr.med. Urologisk avdeling Akershus Universitetssykehus 2.11.2015 2000-61 år gammel mann med PSA 25 - Ingen vannlatingsplager - Utredning: 6 prostatabiopsier
«Prostatasenter Quo vadis???» Karol Axcrona Avdelingssjef, dr.med. Urologisk avdeling Akershus Universitetssykehus 2.11.2015 2000-61 år gammel mann med PSA 25 - Ingen vannlatingsplager - Utredning: 6 prostatabiopsier
Tallenes tale; Tverrfaglig tilnærming til prostatakreft. Erik Skaaheim Haug, Overlege og forsker
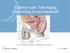 Tallenes tale; Tverrfaglig tilnærming til prostatakreft Erik Skaaheim Haug, Overlege og forsker Erik Skaaheim Haug Overlege dr med, urologisk seksjon, Sykehuset i Vestfold HF, Forsker i deltid, Institutt
Tallenes tale; Tverrfaglig tilnærming til prostatakreft Erik Skaaheim Haug, Overlege og forsker Erik Skaaheim Haug Overlege dr med, urologisk seksjon, Sykehuset i Vestfold HF, Forsker i deltid, Institutt
Fellesregistre - Kreftregisteret. Jan F Nygård Kreftregisteret
 Fellesregistre - Kreftregisteret Jan F Nygård Kreftregisteret Kreftregisteret > Opprettet i 1951 > Samle inn opplysninger om all kreft i Norge (Kreftregisterforskiften); > Formål: Etablere viten og spre
Fellesregistre - Kreftregisteret Jan F Nygård Kreftregisteret Kreftregisteret > Opprettet i 1951 > Samle inn opplysninger om all kreft i Norge (Kreftregisterforskiften); > Formål: Etablere viten og spre
Årsrapport 2016 med resultater og forbedringstiltak
 Nasjonalt kvalitetsregister for tykk- og endetarmskreft Årsrapport 2016 med resultater og forbedringstiltak Anbefalt referanse: Årsrapport 2016 med resultater og forbedringstiltak fra Nasjonalt kvalitetsregister
Nasjonalt kvalitetsregister for tykk- og endetarmskreft Årsrapport 2016 med resultater og forbedringstiltak Anbefalt referanse: Årsrapport 2016 med resultater og forbedringstiltak fra Nasjonalt kvalitetsregister
Klamydia i Norge 2012
 Klamydia i Norge 2012 I 2012 ble det diagnostisert 21 489 tilfeller av genitale klamydiainfeksjoner i Norge. Dette er en nedgang på 4.5 % fra fjoråret. Siden toppåret i 2008 har antall diagnostierte tilfeller
Klamydia i Norge 2012 I 2012 ble det diagnostisert 21 489 tilfeller av genitale klamydiainfeksjoner i Norge. Dette er en nedgang på 4.5 % fra fjoråret. Siden toppåret i 2008 har antall diagnostierte tilfeller
Årsrapport. Resultater og forbedringstiltak fra. Nasjonalt kvalitetsregister for tykk- og endetarmskreft
 Årsrapport 2017 Resultater og forbedringstiltak fra Nasjonalt kvalitetsregister for tykk- og endetarmskreft Anbefalt referanse: Årsrapport 2017 med resultater og forbedringstiltak fra Nasjonalt kvalitetsregister
Årsrapport 2017 Resultater og forbedringstiltak fra Nasjonalt kvalitetsregister for tykk- og endetarmskreft Anbefalt referanse: Årsrapport 2017 med resultater og forbedringstiltak fra Nasjonalt kvalitetsregister
PSA. - en blodprøve til glede og besvær. Barbara Thorsen overlege urologisk avdeling Vårmøte mars 2014
 PSA - en blodprøve til glede og besvær Barbara Thorsen overlege urologisk avdeling Vårmøte mars 2014 1. Hva er PSA? 2. Når skal vi ta PSA? 3. Hva påvirker PSA prøven? 4. Når skal pasienten henvises til
PSA - en blodprøve til glede og besvær Barbara Thorsen overlege urologisk avdeling Vårmøte mars 2014 1. Hva er PSA? 2. Når skal vi ta PSA? 3. Hva påvirker PSA prøven? 4. Når skal pasienten henvises til
Årsrapport til Helse Sør-Øst Nasjonalt kvalitetsregister for barnekreft
 Årsrapport til Helse Sør-Øst Nasjonalt kvalitetsregister for barnekreft Oktober 2013 Side 1 av 15 Postadresse Kontoradresse Telefon: 22 45 13 00 E-post: kreftregisteret@kreftregisteret.no Org. nr.: 974707160
Årsrapport til Helse Sør-Øst Nasjonalt kvalitetsregister for barnekreft Oktober 2013 Side 1 av 15 Postadresse Kontoradresse Telefon: 22 45 13 00 E-post: kreftregisteret@kreftregisteret.no Org. nr.: 974707160
Fotograf: Wilse, A. B. / Oslo byarkiv
 Fotograf: Wilse, A. B. / Oslo byarkiv Fotograf: Wilse, A. B. / Oslo byarkiv Lørdagsseminar 8.november 214 Kampen mot kreft Velkommen ved prodekan Kristin Heggen og professor Marit Bragelien Veierød Kulturelt
Fotograf: Wilse, A. B. / Oslo byarkiv Fotograf: Wilse, A. B. / Oslo byarkiv Lørdagsseminar 8.november 214 Kampen mot kreft Velkommen ved prodekan Kristin Heggen og professor Marit Bragelien Veierød Kulturelt
Validering av resultater fra dekningsgradsanalyse
 Validering av resultater fra dekningsgradsanalyse Cerebral parese 1 Oversikt Tabell 1. Sentrale opplysninger om valideringen Kategori Register Diagnose ICD-10-koder Norsk pasientregister (NPR) Cerebral
Validering av resultater fra dekningsgradsanalyse Cerebral parese 1 Oversikt Tabell 1. Sentrale opplysninger om valideringen Kategori Register Diagnose ICD-10-koder Norsk pasientregister (NPR) Cerebral
Gleason score 50 år! - Hvor står vi nå? Ulrika Axcrona overlege, dr. med. Årsmøte patologiforeningen april, 2016
 Gleason score 50 år! - Hvor står vi nå? Ulrika Axcrona overlege, dr. med. Årsmøte patologiforeningen 14-15 april, 2016 It is the imposing of a pattern on experience, and our recognition of that pattern
Gleason score 50 år! - Hvor står vi nå? Ulrika Axcrona overlege, dr. med. Årsmøte patologiforeningen 14-15 april, 2016 It is the imposing of a pattern on experience, and our recognition of that pattern
Datakvalitet og validering. Ingvild B. M. Tjelmeland Leder for Norsk hjertestansregister
 Datakvalitet og validering Ingvild B. M. Tjelmeland Leder for Norsk hjertestansregister Agenda Hva er hjertestans Hvorfor dokumentere det vi gjør Hvordan dokumentere Hvordan kvalitetssikre data Hvordan
Datakvalitet og validering Ingvild B. M. Tjelmeland Leder for Norsk hjertestansregister Agenda Hva er hjertestans Hvorfor dokumentere det vi gjør Hvordan dokumentere Hvordan kvalitetssikre data Hvordan
Uførepensjon pr. 30. juni 2010 Notatet er skrevet av Marianne Lindbøl
 ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uførepensjon pr. 3. juni 21 Notatet er skrevet av Marianne Lindbøl 26.8.21. // NOTAT Økning i antall uførepensjonister Det er en svak økning i
ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uførepensjon pr. 3. juni 21 Notatet er skrevet av Marianne Lindbøl 26.8.21. // NOTAT Økning i antall uførepensjonister Det er en svak økning i
Uførepensjon pr. 31. mars 2010 Notatet er skrevet av Therese Sundell
 ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uførepensjon pr. 31. mars 21 Notatet er skrevet av Therese Sundell..21. // NOTAT Svak økning i antall uførepensjonister Det er en svak økning
ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uførepensjon pr. 31. mars 21 Notatet er skrevet av Therese Sundell..21. // NOTAT Svak økning i antall uførepensjonister Det er en svak økning
Norsk register for invasiv kardiologi (NORIC) Årsrapport 2012 Plan for forbedringstiltak 2013
 Norsk register for invasiv kardiologi (NORIC) Årsrapport 2012 Plan for forbedringstiltak 2013 SVEIN ROTEVATN 1 1 Hjerteavdelingen, Haukeland Universitetssykehus 31. oktober 2013 Bakgrunn og veiledning
Norsk register for invasiv kardiologi (NORIC) Årsrapport 2012 Plan for forbedringstiltak 2013 SVEIN ROTEVATN 1 1 Hjerteavdelingen, Haukeland Universitetssykehus 31. oktober 2013 Bakgrunn og veiledning
Nasjonalt Kvalitetsregister for Smertebehandling (SmerteReg) Årsrapport for 2013
 Nasjonalt Kvalitetsregister for Smertebehandling (SmerteReg) Årsrapport for 2013 Lars Jørgen Rygh Haukeland Universitetssykehus, Helse Vest RHF 30. September 2014 1 Bakgrunn og veiledning til utfylling
Nasjonalt Kvalitetsregister for Smertebehandling (SmerteReg) Årsrapport for 2013 Lars Jørgen Rygh Haukeland Universitetssykehus, Helse Vest RHF 30. September 2014 1 Bakgrunn og veiledning til utfylling
Om tabellene. Januar - februar 2019
 Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Personer med nedsatt arbeidsevne. Fylke og alder. Tidsserie måned
 Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Om tabellene. Januar - mars 2019
 Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Personer med nedsatt arbeidsevne. Fylke og alder. Tidsserie måned
 Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Personer med nedsatt arbeidsevne. Fylke og alder. Tidsserie måned
 Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Personer med nedsatt arbeidsevne. Fylke og alder. Tidsserie måned
 Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Om tabellene. Januar - mars 2018
 Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer med nedsatt arbeidsevne". Fylke. Antall I alt I alt
Om tabellene. Januar - desember 2018
 Personer med nedsatt arbeidsevne. Fylke og alder. Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer
Personer med nedsatt arbeidsevne. Fylke og alder. Om tabellene "Om statistikken - Personer med nedsatt arbeidsevne" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Personer
Antall varsler. Antall varsler fordelt på måned (7 md)
 Statistikk for Undersøkelsesenheten varsler om alvorlige hendelser i spesialisthelsetjenesten Statens helsetilsyn Statistikken her gjelder varsling av alvorlige hendelser i spesialisthelsetjenesten til
Statistikk for Undersøkelsesenheten varsler om alvorlige hendelser i spesialisthelsetjenesten Statens helsetilsyn Statistikken her gjelder varsling av alvorlige hendelser i spesialisthelsetjenesten til
Kreftregisterets arbeid med RWE
 Kreftregisterets arbeid med RWE Espen Enerly, PhD Forsker Okt 18, 2016 Kreftregisteret Institutt for populasjonsbasert kreftforskning Interessekonflikt Arbeider på Kreftregisteret med HPV-vaksineprosjekter
Kreftregisterets arbeid med RWE Espen Enerly, PhD Forsker Okt 18, 2016 Kreftregisteret Institutt for populasjonsbasert kreftforskning Interessekonflikt Arbeider på Kreftregisteret med HPV-vaksineprosjekter
Patologirapport 2016 Oversikt over rapportering fra patologiavdelingene
 2016 Oversikt over rapportering fra patologiavdelingene Resultater fra nasjonale kvalitetsregistre på kreftområdet: Brystkreft Føflekkreft Gynekologisk kreft Lungekreft Prostatakreft Tykk- og endetarmskreft
2016 Oversikt over rapportering fra patologiavdelingene Resultater fra nasjonale kvalitetsregistre på kreftområdet: Brystkreft Føflekkreft Gynekologisk kreft Lungekreft Prostatakreft Tykk- og endetarmskreft
Statistikk uførepensjon per 31. desember 2010 Notatet er skrevet av
 ARBEIDS- OG VELFERDSDIREKTORATET / SEKSJON FOR STATISTIKK Statistikk uførepensjon per 31. desember 2010 Notatet er skrevet av jostein.ellingsen@nav.no, 15.4.2011. // NOTAT I dette notatet omtaler vi statistikk
ARBEIDS- OG VELFERDSDIREKTORATET / SEKSJON FOR STATISTIKK Statistikk uførepensjon per 31. desember 2010 Notatet er skrevet av jostein.ellingsen@nav.no, 15.4.2011. // NOTAT I dette notatet omtaler vi statistikk
Virksomhetsrapport november 2018
 Virksomhetsrapport november 2018 Styresak 079-2018 Fagdirektør Per Engstrand 20.12.2018 Innhold 1. Oppsummering 2. Kvalitet og pasientbehandling 3. Aktivitet 4. Bemanning 5. Økonomi/finans 6. Vedlegg oversikt
Virksomhetsrapport november 2018 Styresak 079-2018 Fagdirektør Per Engstrand 20.12.2018 Innhold 1. Oppsummering 2. Kvalitet og pasientbehandling 3. Aktivitet 4. Bemanning 5. Økonomi/finans 6. Vedlegg oversikt
Prostatakreft Epidemiologi
 Prostatakreft Epidemiologi Profo Fagdag 15.4.13 Sophie D. Fosså Prof.em Oslo University Hospital, Radiumhospital Disposisjon 1. Insidens og dødelighet 2. PSA screening 3. Behandling 4. Noen resultater
Prostatakreft Epidemiologi Profo Fagdag 15.4.13 Sophie D. Fosså Prof.em Oslo University Hospital, Radiumhospital Disposisjon 1. Insidens og dødelighet 2. PSA screening 3. Behandling 4. Noen resultater
Uføreytelser pr. 31. mars 2008 Notatet er skrevet av Nina Viten,
 ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 31. mars 28 Notatet er skrevet av Nina Viten, nina.viten@nav.no, 24.4.28. // NOTAT Økning i antall mottakere av uføreytelser
ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 31. mars 28 Notatet er skrevet av Nina Viten, nina.viten@nav.no, 24.4.28. // NOTAT Økning i antall mottakere av uføreytelser
Utviklingen i antall uførepensjonister, 31. mars 2011 Notatet er skrevet av
 ARBEIDS- OG VELFERDSDIREKTORATET / SEKSJON FOR STATISTIKK Utviklingen i antall uførepensjonister, 31. mars 2011 Notatet er skrevet av jostein.ellingsen@nav.no, 30.6.2011. // NOTAT I dette notatet omtaler
ARBEIDS- OG VELFERDSDIREKTORATET / SEKSJON FOR STATISTIKK Utviklingen i antall uførepensjonister, 31. mars 2011 Notatet er skrevet av jostein.ellingsen@nav.no, 30.6.2011. // NOTAT I dette notatet omtaler
Fraværet i videregående stabiliserer seg - analyse av foreløpige fraværstall
 Fraværet i videregående stabiliserer seg - analyse av foreløpige fraværstall 2017-18 To år etter fraværsgrensen ble innført viser foreløpige tall at fraværet i videregående holder seg relativt stabilt
Fraværet i videregående stabiliserer seg - analyse av foreløpige fraværstall 2017-18 To år etter fraværsgrensen ble innført viser foreløpige tall at fraværet i videregående holder seg relativt stabilt
Søknad om status som nasjonalt medisinsk kvalitetsregister 2010. Nasjonalt register for føflekkreft. Kreftregisteret
 Søknad om status som nasjonalt medisinsk kvalitetsregister 2010 1 KONTAKTINFORMASJON Registerets navn Nasjonalt register for føflekkreft Registeransvarlig Kreftregisteret Telefon 22451300 E-post ingunn.bjorhovde@kreftregisteret.no
Søknad om status som nasjonalt medisinsk kvalitetsregister 2010 1 KONTAKTINFORMASJON Registerets navn Nasjonalt register for føflekkreft Registeransvarlig Kreftregisteret Telefon 22451300 E-post ingunn.bjorhovde@kreftregisteret.no
Antall varsler. Antall varsler fordelt på måned (7 md)
 Statistikk for Avdeling for varsler og operativt tilsyn varsler om alvorlige hendelser i spesialisthelsetjenesten Statens helsetilsyn Statistikken her gjelder varsling av alvorlige hendelser i spesialisthelsetjenesten
Statistikk for Avdeling for varsler og operativt tilsyn varsler om alvorlige hendelser i spesialisthelsetjenesten Statens helsetilsyn Statistikken her gjelder varsling av alvorlige hendelser i spesialisthelsetjenesten
Antall varsler. Antall varsler fordelt på måned (7 md)
 Statistikk for Undersøkelsesenheten varsler om alvorlige hendelser i spesialisthelsetjenesten Statens helsetilsyn Statistikken her gjelder varsling av alvorlige hendelser i spesialisthelsetjenesten til
Statistikk for Undersøkelsesenheten varsler om alvorlige hendelser i spesialisthelsetjenesten Statens helsetilsyn Statistikken her gjelder varsling av alvorlige hendelser i spesialisthelsetjenesten til
Utviklingen i uførepensjon, 30. september 2011 Notatet er skrevet av
 ARBEIDS- OG VELFERDSDIREKTORATET / SEKSJON FOR STATISTIKK Utviklingen i uførepensjon, 30. september 2011 Notatet er skrevet av jostein.ellingsen@nav.no, 3.11.2011. // NOTAT Formålet med uførepensjon er
ARBEIDS- OG VELFERDSDIREKTORATET / SEKSJON FOR STATISTIKK Utviklingen i uførepensjon, 30. september 2011 Notatet er skrevet av jostein.ellingsen@nav.no, 3.11.2011. // NOTAT Formålet med uførepensjon er
Klamydia og lymfogranuloma venerum (LGV) i Norge 2013
 Klamydia og lymfogranuloma venerum (LGV) i Norge 2013 I 2013 ble det diagnostisert 22 946 av genitale klamydiainfeksjoner (klamydia) i Norge. Av disse var det 26 av LGV som skyldes smitte med en annen
Klamydia og lymfogranuloma venerum (LGV) i Norge 2013 I 2013 ble det diagnostisert 22 946 av genitale klamydiainfeksjoner (klamydia) i Norge. Av disse var det 26 av LGV som skyldes smitte med en annen
Pasientrapporterte resultater i prostatakreftregisteret. Tidlige erfaringer. Ylva Gjelsvik, Kreftregisteret
 Pasientrapporterte resultater i prostatakreftregisteret. Tidlige erfaringer. Ylva Gjelsvik, Kreftregisteret Disposisjon Presentasjon av prosjektet Infrastruktur Responsrater Oppsummering Nasjonalt kvalitetsregister
Pasientrapporterte resultater i prostatakreftregisteret. Tidlige erfaringer. Ylva Gjelsvik, Kreftregisteret Disposisjon Presentasjon av prosjektet Infrastruktur Responsrater Oppsummering Nasjonalt kvalitetsregister
Pakkeforløpet ved Urologisk avd. OUS Overlege dr med Viktor Berge. kurs almennleger 250815
 Pakkeforløpet ved Urologisk avd. OUS Overlege dr med Viktor Berge 1 Pakkeforløp Oppdrag fra HOD til Helsedirektoratet i februar 2014: Pakkeforløp for kreft og diagnoseveiledere for fastlegene etter modell
Pakkeforløpet ved Urologisk avd. OUS Overlege dr med Viktor Berge 1 Pakkeforløp Oppdrag fra HOD til Helsedirektoratet i februar 2014: Pakkeforløp for kreft og diagnoseveiledere for fastlegene etter modell
Forebyggende behandling av latent tuberkulose
 2012 Forebyggende behandling av latent tuberkulose 2001 2010 Forebyggende behandling av latent tuberkulose 2001 2010 Einar Heldal Karin Rønning Turid Mannsåker Ulf Dahle 2 Utgitt av Nasjonalt folkehelseinstitutt
2012 Forebyggende behandling av latent tuberkulose 2001 2010 Forebyggende behandling av latent tuberkulose 2001 2010 Einar Heldal Karin Rønning Turid Mannsåker Ulf Dahle 2 Utgitt av Nasjonalt folkehelseinstitutt
Nasjonalt kvalitetsregister for. tykk- og endetarmskreft. Årsrapport 2014
 Nasjonalt kvalitetsregister for tykk- og endetarmskreft Årsrapport 2014 Årsrapport 2014 Kreftregisteret Forord Denne rapporten representerer et samarbeid mellom Kreftregisteret og representanter fra de
Nasjonalt kvalitetsregister for tykk- og endetarmskreft Årsrapport 2014 Årsrapport 2014 Kreftregisteret Forord Denne rapporten representerer et samarbeid mellom Kreftregisteret og representanter fra de
Uføreytelser pr. 30. september 2008 Notatet er skrevet av Nina Viten,
 ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 3. september 28 Notatet er skrevet av Nina Viten, nina.viten@nav.no, 22.1.28. // NOTAT Antall uføre øker svakt Økningen i antall
ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 3. september 28 Notatet er skrevet av Nina Viten, nina.viten@nav.no, 22.1.28. // NOTAT Antall uføre øker svakt Økningen i antall
Spesialist i allmennmedisin
 Nordisk konferanse UTF Hotel Bristol 21.mai 2015 Fastlege Åge Norman Hansen Spesialist i allmennmedisin Nordisk konferanse UTF Hotel Bristol 21.mai 2015 Hvordan bør fastlegen komme den engstelige mannen
Nordisk konferanse UTF Hotel Bristol 21.mai 2015 Fastlege Åge Norman Hansen Spesialist i allmennmedisin Nordisk konferanse UTF Hotel Bristol 21.mai 2015 Hvordan bør fastlegen komme den engstelige mannen
Klamydia og lymfogranuloma venerum (LGV) i Norge 2015
 Klamydia og lymfogranuloma venerum (LGV) i Norge 2015 I 2015 ble det diagnostisert 25 207 av genitale klamydiainfeksjoner (klamydia) i Norge. Dette tilsvarer 488 diagnostiserte per 100 000 innbyggere (diagnoserate).
Klamydia og lymfogranuloma venerum (LGV) i Norge 2015 I 2015 ble det diagnostisert 25 207 av genitale klamydiainfeksjoner (klamydia) i Norge. Dette tilsvarer 488 diagnostiserte per 100 000 innbyggere (diagnoserate).
Najonalt Kvalitetsregister for Ryggkirurgi
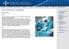 Om registereret Bakgrunn Nasjonalt Kvalitetsregister for Ryggkirurgi (NKR) har som mål å sikre kvaliteten på ryggkirurgi som utføres ved norske sykehus. Målgruppen er pasienter som blir operert for degenerative
Om registereret Bakgrunn Nasjonalt Kvalitetsregister for Ryggkirurgi (NKR) har som mål å sikre kvaliteten på ryggkirurgi som utføres ved norske sykehus. Målgruppen er pasienter som blir operert for degenerative
Årsrapport 2008-2014 Tykktarmskreft 1996-2014 Endetarmskreft
 Nasjonalt kvalitetsregister for tykk- og endetarmskreft Årsrapport 2008-2014 Tykktarmskreft 1996-2014 Endetarmskreft Årsrapport Kreftregisteret FORORD Denne rapporten representerer et samarbeid mellom
Nasjonalt kvalitetsregister for tykk- og endetarmskreft Årsrapport 2008-2014 Tykktarmskreft 1996-2014 Endetarmskreft Årsrapport Kreftregisteret FORORD Denne rapporten representerer et samarbeid mellom
Uføreytelser pr. 30. september 2009 Notatet er skrevet av Nina Viten,
 ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 3. september 29 Notatet er skrevet av Nina Viten, nina.viten@nav.no, 27.1.29. // NOTAT Antall uføre øker svakt Økningen i antall
ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 3. september 29 Notatet er skrevet av Nina Viten, nina.viten@nav.no, 27.1.29. // NOTAT Antall uføre øker svakt Økningen i antall
Økende antall, avtakende vekst
 Uføreytelser pr. 3 september 27 Kvartalsvis statistikknotat fra Statistikk og utredning i Arbeids- og velferdsdirektoratet. Notatet er skrevet av Nina Viten, nina.viten@nav.no. Økende antall, avtakende
Uføreytelser pr. 3 september 27 Kvartalsvis statistikknotat fra Statistikk og utredning i Arbeids- og velferdsdirektoratet. Notatet er skrevet av Nina Viten, nina.viten@nav.no. Økende antall, avtakende
Nasjonalt kvalitetsregister for. tykk- og endetarmskreft. 2008 2014 Tykktarmskreft 1996 2014 Endetarmskreft. Årsrapport
 Nasjonalt kvalitetsregister for tykk- og endetarmskreft Årsrapport 2008 2014 Tykktarmskreft 1996 2014 Endetarmskreft Årsrapport Kreftregisteret Årsrapport Nasjonalt kvalitetsregister for tykk- og endetarmskreft
Nasjonalt kvalitetsregister for tykk- og endetarmskreft Årsrapport 2008 2014 Tykktarmskreft 1996 2014 Endetarmskreft Årsrapport Kreftregisteret Årsrapport Nasjonalt kvalitetsregister for tykk- og endetarmskreft
Overlevelse i Norge, blir vi bedre? Resultater fra Norsk hjertestansregister
 Overlevelse i Norge, blir vi bedre? Resultater fra Norsk hjertestansregister Ingvild Tjelmeland, leder for Norsk hjertestansregister Nasjonal kompetansetjeneste for prehospital akuttmedisin (NAKOS) Agenda
Overlevelse i Norge, blir vi bedre? Resultater fra Norsk hjertestansregister Ingvild Tjelmeland, leder for Norsk hjertestansregister Nasjonal kompetansetjeneste for prehospital akuttmedisin (NAKOS) Agenda
Søknad om status som nasjonalt medisinsk kvalitetsregister 2010. Nasjonalt register for brystkreft. Kreftregisteret. Oslo Universitetssykehus
 Søknad om status som nasjonalt medisinsk kvalitetsregister 2010 1 KONTAKTINFORMASJON Registerets navn Nasjonalt register for brystkreft Registeransvarlig Kreftregisteret Telefon 22451300 E-post monica.johansen@kreftregisteret.no;
Søknad om status som nasjonalt medisinsk kvalitetsregister 2010 1 KONTAKTINFORMASJON Registerets navn Nasjonalt register for brystkreft Registeransvarlig Kreftregisteret Telefon 22451300 E-post monica.johansen@kreftregisteret.no;
Uføreytelser pr. 30. juni 2008 Notatet er skrevet av Nina Viten,
 ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 3. juni 28 Notatet er skrevet av Nina Viten, nina.viten@nav.no, 26.8.28. // NOTAT Antall uføre øker svakt Økningen i antall mottakere
ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 3. juni 28 Notatet er skrevet av Nina Viten, nina.viten@nav.no, 26.8.28. // NOTAT Antall uføre øker svakt Økningen i antall mottakere
KREFTFORENINGENS FORVENTNINGER - PASIENTENS ROLLE I KVALITETSREGISTRE
 KREFTFORENINGENS FORVENTNINGER - PASIENTENS ROLLE I KVALITETSREGISTRE SIDSEL SANDVIG, SPESIALRÅDGIVER KREFTFORENINGEN, 12.12.2014 Politisk påvirkningsarbeid kvalitetsregistre, bakgrunn Helsetjenestekvalitet
KREFTFORENINGENS FORVENTNINGER - PASIENTENS ROLLE I KVALITETSREGISTRE SIDSEL SANDVIG, SPESIALRÅDGIVER KREFTFORENINGEN, 12.12.2014 Politisk påvirkningsarbeid kvalitetsregistre, bakgrunn Helsetjenestekvalitet
Utvalgte helsetjenester til barn i Norge. Notat
 Utvalgte helsetjenester til barn i Norge Notat 2017 SKDE notat Oktober 2017 Forfattere Toril Bakken og Bård Uleberg Oppdragsgiver Hans Petter Fundingsrud (UNN, Tromsø) Forsidefoto: Colourbox Alle rettigheter
Utvalgte helsetjenester til barn i Norge Notat 2017 SKDE notat Oktober 2017 Forfattere Toril Bakken og Bård Uleberg Oppdragsgiver Hans Petter Fundingsrud (UNN, Tromsø) Forsidefoto: Colourbox Alle rettigheter
Norsk diabetesregister for voksne. Karianne Fjeld Løvaas
 Norsk diabetesregister for voksne Karianne Fjeld Løvaas Organisering og drift Registeret finansieres av Helse Vest. Haukeland universitetssykehus er eier og databehandlingsansvarlig Daglige drift er lagt
Norsk diabetesregister for voksne Karianne Fjeld Løvaas Organisering og drift Registeret finansieres av Helse Vest. Haukeland universitetssykehus er eier og databehandlingsansvarlig Daglige drift er lagt
Fravær i videregående skole skoleåret
 Fravær i videregående skole skoleåret 21-19 Tre år etter fraværsgrensen ble innført ser vi at dagsfraværet i videregående holder seg stabilt med fjorårets nivå, men med en liten økning i timefraværet fra
Fravær i videregående skole skoleåret 21-19 Tre år etter fraværsgrensen ble innført ser vi at dagsfraværet i videregående holder seg stabilt med fjorårets nivå, men med en liten økning i timefraværet fra
GSI 2014/15: Voksne i grunnskoleopplæring
 GSI 2014/15: Voksne i grunnskoleopplæring Innledning Tall fra Grunnskolens informasjonssystem (GSI) per 1.10.2014 er tilgjengelige på www.udir.no/gsi fra og med 12. desember 2014. Alle tall og beregninger
GSI 2014/15: Voksne i grunnskoleopplæring Innledning Tall fra Grunnskolens informasjonssystem (GSI) per 1.10.2014 er tilgjengelige på www.udir.no/gsi fra og med 12. desember 2014. Alle tall og beregninger
Uføreytelser pr. 31. desember 2009 Notatet er skrevet av Marianne Næss Lindbøl,
 ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 31. desember 29 Notatet er skrevet av Marianne Næss Lindbøl, 4.2.21. // NOTAT Antall uføre øker fortsatt Økningen i antall mottakere
ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 31. desember 29 Notatet er skrevet av Marianne Næss Lindbøl, 4.2.21. // NOTAT Antall uføre øker fortsatt Økningen i antall mottakere
HEPATITT B OG C-SITUASJONEN I NORGE 2013
 HEPATITT B OG C-SITUASJONEN I NORGE 2013 Den epidemiologiske situasjonen for hepatitt B og C overvåkes gjennom nominative meldinger fra leger og laboratorier til Meldingssystem for smittsomme sykdommer
HEPATITT B OG C-SITUASJONEN I NORGE 2013 Den epidemiologiske situasjonen for hepatitt B og C overvåkes gjennom nominative meldinger fra leger og laboratorier til Meldingssystem for smittsomme sykdommer
SmerteReg Årsrapport for 2014
 SmerteReg Årsrapport for 2014 Daglig leder SmerteReg Overlege Lars Jørgen Rygh, KSK, HUS 30.09.2015 Innhold Del I Årsrapport... 3 1. Sammendrag... 3 2. Registerbeskrivelse... 4 2.1 Bakgrunn og formål...
SmerteReg Årsrapport for 2014 Daglig leder SmerteReg Overlege Lars Jørgen Rygh, KSK, HUS 30.09.2015 Innhold Del I Årsrapport... 3 1. Sammendrag... 3 2. Registerbeskrivelse... 4 2.1 Bakgrunn og formål...
Fortsatt økning i tilgangen til uføreytelser, men veksten er avtakende
 Statistikk over uføreytelser første kvartal 27 Kvartalsvis statistikknotat fra Statistikk og utredning i Arbeids- og velferdsdirektoratet. Notatet er skrevet av Heidi Vannevjen, heidi.vannevjen@nav.no.
Statistikk over uføreytelser første kvartal 27 Kvartalsvis statistikknotat fra Statistikk og utredning i Arbeids- og velferdsdirektoratet. Notatet er skrevet av Heidi Vannevjen, heidi.vannevjen@nav.no.
Om tabellene. Periode:
 Om tabellene "Om statistikken - Mottakere av arbeidsavklaringspenger" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Mottakere av arbeidsavklaringspenger (AAP)". Fylke. Antall
Om tabellene "Om statistikken - Mottakere av arbeidsavklaringspenger" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Mottakere av arbeidsavklaringspenger (AAP)". Fylke. Antall
Mottakere av arbeidsavklaringspenger. Fylke og alder. Tidsserie måned
 Om tabellene "Om statistikken - Mottakere av arbeidsavklaringspenger" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Mottakere av arbeidsavklaringspenger (AAP)". Fylke. Antall
Om tabellene "Om statistikken - Mottakere av arbeidsavklaringspenger" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Mottakere av arbeidsavklaringspenger (AAP)". Fylke. Antall
Om tabellene. Periode:
 Om tabellene "Om statistikken - Mottakere av arbeidsavklaringspenger" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Mottakere av arbeidsavklaringspenger (AAP)". Fylke. Antall
Om tabellene "Om statistikken - Mottakere av arbeidsavklaringspenger" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Mottakere av arbeidsavklaringspenger (AAP)". Fylke. Antall
Mottakere av arbeidsavklaringspenger. Fylke og alder. Tidsserie måned
 Om tabellene "Om statistikken - Mottakere av arbeidsavklaringspenger" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Mottakere av arbeidsavklaringspenger (AAP)". Fylke. Antall
Om tabellene "Om statistikken - Mottakere av arbeidsavklaringspenger" finner du på nav.no ved å følge lenken under relatert informasjon på siden "Mottakere av arbeidsavklaringspenger (AAP)". Fylke. Antall
Utviklingen i reinnleggelser fra 2011 til 2016 Somatiske sykehus
 Nr. 14/2017 Utviklingen i reinnleggelser fra 2011 til 2016 Somatiske sykehus Analysenotat 14/17 SAMDATA Spesialisthelsetjenesten Publikasjonens tittel: Utviklingen i reinnleggelser fra 2011 til 2016. Somatiske
Nr. 14/2017 Utviklingen i reinnleggelser fra 2011 til 2016 Somatiske sykehus Analysenotat 14/17 SAMDATA Spesialisthelsetjenesten Publikasjonens tittel: Utviklingen i reinnleggelser fra 2011 til 2016. Somatiske
Dekningsgradsanalyse 2015 Nasjonalt medisinsk kvalitetsregister for barne- og ungdomsdiabetes
 Nasjonal tjeneste for validering og dekningsgradsanalyser Dekningsgradsanalyse 2015 Nasjonalt medisinsk kvalitetsregister for barne- og ungdomsdiabetes 1 Oversikt Tabell 1 Sentrale opplysninger om dekningsgradsanalysen
Nasjonal tjeneste for validering og dekningsgradsanalyser Dekningsgradsanalyse 2015 Nasjonalt medisinsk kvalitetsregister for barne- og ungdomsdiabetes 1 Oversikt Tabell 1 Sentrale opplysninger om dekningsgradsanalysen
Over personer vil få en kreftdiagnose i Norge i 2015.
 Over 30 000 personer vil få en kreftdiagnose i Norge i 2015. Hvordan har utviklingen vært? Hvordan blir den fremover? Hva kan vi bidra med? Steinar Tretli, PhD, Professor Kreftregisteret/ NTNU- ISM Litt
Over 30 000 personer vil få en kreftdiagnose i Norge i 2015. Hvordan har utviklingen vært? Hvordan blir den fremover? Hva kan vi bidra med? Steinar Tretli, PhD, Professor Kreftregisteret/ NTNU- ISM Litt
Nasjonalt kvalitetsregister for ryggkirurgi (NKR)
 Nasjonal tjeneste for validering og dekningsgradsanalyser Dekningsgradsanalyse Nasjonalt kvalitetsregister for ryggkirurgi - ryggoperasjoner 1 Oversikt Tabell 1. Sentrale opplysninger om dekningsgradsanalysen
Nasjonal tjeneste for validering og dekningsgradsanalyser Dekningsgradsanalyse Nasjonalt kvalitetsregister for ryggkirurgi - ryggoperasjoner 1 Oversikt Tabell 1. Sentrale opplysninger om dekningsgradsanalysen
Kreftregisterets hoveddatabase:
 Kreftregisterets hoveddatabase: kilder, datakvalitet og tilgjengelighet perspektiv fremover Fagdag ved Kreftregisterets 60-årsjubileum 27.9.2012 Bjørn Møller, Avd. leder Registeravdelingen, Kreftregisteret
Kreftregisterets hoveddatabase: kilder, datakvalitet og tilgjengelighet perspektiv fremover Fagdag ved Kreftregisterets 60-årsjubileum 27.9.2012 Bjørn Møller, Avd. leder Registeravdelingen, Kreftregisteret
Kan man rekruttere pasienter fra Kreftregisteret til kliniske studier?
 Kan man rekruttere pasienter fra Kreftregisteret til kliniske studier? Big data og biomedisinsk næringsutvikling Fra genomikk til real world data 7.5. 2015 Bjørn Møller, Avdelingsleder Registeravdelingen,
Kan man rekruttere pasienter fra Kreftregisteret til kliniske studier? Big data og biomedisinsk næringsutvikling Fra genomikk til real world data 7.5. 2015 Bjørn Møller, Avdelingsleder Registeravdelingen,
Prostatakreft Forekomst og forløp Aktuell kurativ behandling
 Prostatakreft Forekomst og forløp Aktuell kurativ behandling Overlege Jon Reidar Iversen Enhet for urologisk kreft Avdeling for Kreftbehandling Ullevål 2011 Oslo Universitetssykehus, Ullevål Ullevål 2011
Prostatakreft Forekomst og forløp Aktuell kurativ behandling Overlege Jon Reidar Iversen Enhet for urologisk kreft Avdeling for Kreftbehandling Ullevål 2011 Oslo Universitetssykehus, Ullevål Ullevål 2011
Kreftregisteret. Hvilke data har vi og hva kan være særlig relevant for industrien? LMI
 Kreftregisteret Hvilke data har vi og hva kan være særlig relevant for industrien? LMI 09.09.2019 Lena.holmstrom@kreftregisteret.no Kreftregisteret Populasjonsbasert helseregister Helseregisterloven 11
Kreftregisteret Hvilke data har vi og hva kan være særlig relevant for industrien? LMI 09.09.2019 Lena.holmstrom@kreftregisteret.no Kreftregisteret Populasjonsbasert helseregister Helseregisterloven 11
Uføreytelser pr. 31. mars 2009 Notatet er skrevet av Nina Viten,
 ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 31. mars 29 Notatet er skrevet av Nina Viten, nina.viten@nav.no, 16.6.29. // NOTAT Økning i antall mottakere av uføreytelser
ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 31. mars 29 Notatet er skrevet av Nina Viten, nina.viten@nav.no, 16.6.29. // NOTAT Økning i antall mottakere av uføreytelser
Om kvalitet i behandling. Andreas Stensvold MD, PhD Avdelingssjef Sykehuset Øs;old 3 november 2014
 Om kvalitet i behandling Andreas Stensvold MD, PhD Avdelingssjef Sykehuset Øs;old 3 november 2014 Bindinger Avdelingssjef Sykehuset Øs4old med budsje8ansvar Utdannet onkolog fra Radiumhospitalet Tidligere
Om kvalitet i behandling Andreas Stensvold MD, PhD Avdelingssjef Sykehuset Øs;old 3 november 2014 Bindinger Avdelingssjef Sykehuset Øs4old med budsje8ansvar Utdannet onkolog fra Radiumhospitalet Tidligere
- Forslag til retningslinjer for helsetjenesten når helsepersonell er smittet med blodbårent virus
 Se mottakertabell Deres ref.: Vår ref.: 12/10119-3 Saksbehandler: Sverre Harbo Dato: 17.12.2012 Høring - Helsepersonell smittet med blodbårent virus - Forslag til retningslinjer for helsetjenesten når
Se mottakertabell Deres ref.: Vår ref.: 12/10119-3 Saksbehandler: Sverre Harbo Dato: 17.12.2012 Høring - Helsepersonell smittet med blodbårent virus - Forslag til retningslinjer for helsetjenesten når
Saksframlegg til styret
 Saksframlegg til styret Møtedato 22.12.16 Sak nr: 070/2016 Sakstype: Orienteringssak Nasjonale kvalitetsindikatorer pr november 2016 Trykte vedlegg: ingen Bakgrunn for saken I styremøtene i september og
Saksframlegg til styret Møtedato 22.12.16 Sak nr: 070/2016 Sakstype: Orienteringssak Nasjonale kvalitetsindikatorer pr november 2016 Trykte vedlegg: ingen Bakgrunn for saken I styremøtene i september og
Kreft i Norge Nøkkeltall for utvalgte kreftformer. Kreftregisteret 23. oktober, 2017
 Kreft i Norge 2016 Nøkkeltall for utvalgte kreftformer Kreftregisteret 23. oktober, 2017 Redaktør: Inger Kristin Larsen Skrivegruppe: IK Larsen, B Møller, TB Johannesen, S Larønningen, TE Robsahm, TK Grimsrud,
Kreft i Norge 2016 Nøkkeltall for utvalgte kreftformer Kreftregisteret 23. oktober, 2017 Redaktør: Inger Kristin Larsen Skrivegruppe: IK Larsen, B Møller, TB Johannesen, S Larønningen, TE Robsahm, TK Grimsrud,
Screening for prostatakreft (?) Olbjørn Klepp, overlege/prof II, Kreftavd. Helse Sunnmøre / NTNU
 Screening for prostatakreft (?) Olbjørn Klepp, overlege/prof II, Kreftavd. Helse Sunnmøre / NTNU CANCER PROSTATAE Minst hver 8. nordmann (hver 5. av dagens yngre?) vil få påvist prostatakreft 4 400 nye
Screening for prostatakreft (?) Olbjørn Klepp, overlege/prof II, Kreftavd. Helse Sunnmøre / NTNU CANCER PROSTATAE Minst hver 8. nordmann (hver 5. av dagens yngre?) vil få påvist prostatakreft 4 400 nye
Ungdom utenfor opplæring og arbeid status fra oppfølgingstjenesten (OT) per 1. februar 2012
 Ungdom utenfor opplæring og arbeid status fra oppfølgingstjenesten (OT) per 1. februar 2012 Sammendrag Tall fra fylkeskommunene per 1. februar 2012 viser at 20 090 ungdommer var i oppfølgingstjenestens
Ungdom utenfor opplæring og arbeid status fra oppfølgingstjenesten (OT) per 1. februar 2012 Sammendrag Tall fra fylkeskommunene per 1. februar 2012 viser at 20 090 ungdommer var i oppfølgingstjenestens
Inngang til lungekreft utredning. Emnekurs radiologi Rogaland 2018 Michael Schubert
 Inngang til lungekreft utredning Emnekurs radiologi Rogaland 2018 Michael Schubert «Målgrupper for retningslinjene er spesialister innen medisin, kirurgi, onkologi, radiologi og patologi og allmennleger.
Inngang til lungekreft utredning Emnekurs radiologi Rogaland 2018 Michael Schubert «Målgrupper for retningslinjene er spesialister innen medisin, kirurgi, onkologi, radiologi og patologi og allmennleger.
Fritt behandlingsvalg
 Fritt behandlingsvalg Status for godkjenningsordningen per ial Rapport IS-2769 Innhold Innhold 1 Sammendrag 3 1. Tilgang på leverandører 5 2. Utvikling i pasienter og aktivitet 6 Utvikling i antall pasienter
Fritt behandlingsvalg Status for godkjenningsordningen per ial Rapport IS-2769 Innhold Innhold 1 Sammendrag 3 1. Tilgang på leverandører 5 2. Utvikling i pasienter og aktivitet 6 Utvikling i antall pasienter
Uføreytelser pr. 30. juni 2009 Notatet er skrevet av Nina Viten,
 ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 3. juni 29 Notatet er skrevet av Nina Viten, nina.viten@nav.no, 25.8.29. // NOTAT Antall uføre øker svakt Økningen i antall mottakere
ARBEIDS- OG VELFERDSDIREKTORATET / STATISTIKK OG UTREDNING Uføreytelser pr. 3. juni 29 Notatet er skrevet av Nina Viten, nina.viten@nav.no, 25.8.29. // NOTAT Antall uføre øker svakt Økningen i antall mottakere
Årsrapport 2012. - kortversjon. Nasjonalt Program for Prostatacancer Prostatacancerregisteret
 Årsrapport 2012 - kortversjon Nasjonalt Program for Prostatacancer Prostatacancerregisteret Innhold Innhold... 2 Introduksjon... 3 Rapportering fra sykehusene... 4 Variabler som inngår og rapportering
Årsrapport 2012 - kortversjon Nasjonalt Program for Prostatacancer Prostatacancerregisteret Innhold Innhold... 2 Introduksjon... 3 Rapportering fra sykehusene... 4 Variabler som inngår og rapportering
