Kjemiske og elektrokjemiske reaksjoner og likevekter
|
|
|
- Ranveig Thorstensen
- 6 år siden
- Visninger:
Transkript
1 MENA11; Mteriler, energi og nnoteknologi - Kp. 6 Kjemiske og elektrokjemiske reksjoner og likevekter Litt repetisjon om G og K Likevekter Truls Norby Kjemisk institutt Universitetet i Oslo Senter for Mterilvitenskp og nnoteknologi (SMN) Forskningsprken FERMiO Gustdlleen 1 49 Oslo Syre-bse Løselighet Kompleksering Red-oks Elektrokjemi truls.norby@kjemi.uio.no 1
2 Kort repetisjon fr Kp. ; Hv skjer i et lukket system? Δ r H = Δ r G + TΔ r S Δ r G = Δ r H TΔ r S Δ r G = Δ r H TΔ r S Δ r G = Δ r G + RTlnQ Spontne prosesser: Δ r G = Δ r H TΔ r S < Likevekt: Δ r G = Δ r H TΔ r S = Likevekt: Δ r G = -RTlnK
3 Repetisjon: Relsjon mellom Gibbs energi-forndring og reksjons-kvotient Q: Ved likevekt: r G = : Ved likevekt: Q = K, likevektskonstnten (mssevirkningskoeffisienten) ln b d c B A D C r r RT G G likevekt B A D C r RT G b d c ln Q RT G RT G G r B A D C r r ln ln b d c K G RT G K RT G K r r r likevekt B A D C RTln - eller ln eller ) exp( b d c
4 Repetisjon: r G og K r G sier noe om energiblnsen når Q = 1. K sier noe om hv Q må bli for å oppveie dette. Eksempel: H (g) + O (g) = H O(g) G r Reksjonen er energetisk gunstig hvis p H, p O, p HO = 1. rg K exp( ) 1 RT Produktene kommer i stor overvekt før likevekt oppnås. I dette kpittelet skl vi bruke slike relsjoner når vi gjør oss kjent med typiske og viktige kjemiske reksjoner og likevekter. 4
5 Autoprotolyse: Vnn; utoprotolyse-likevekten H O(l) = H + (q) + OH - (q) eller H O(l) = H O + (q) + OH - (q) K W H [ HO ( q)] [ OH ( q)] O ( q) OH ( q) 1M 1M [ HO ( q)][ OH ( q)] H O( l) H O( l) H O( l) Likevektskonstnter er i prinsippet benevningsløse, men vi bruker likevel ofte benevning for sikkerhets skyld eller pg. fktiske omgjøringer; 14 K W, 98 [ HO ( q)][ OH ( q)] 1,* 1 M 5
6 Autoprotolyse i rent vnn To species: H O + (q) og OH - (q) Vi trenger to uvhengige ligninger for å finne løsningen : Likevekt: Elektronøytrlitet: ved innsetting: 14 K W, 98 [ HO ( q)][ OH ( q)] 1,* 1 M [ HO ( q)] [ OH ( q)] K W,98 [ H O [ OH [ H O ( q)] ( q)] [ H O ( q)][ H O K W,98 ( q)] [ H O 1,*1 7 M ( q)] 1,*1 7 M ( q)] 1,*1 14 M ph log[ H O ( q)] 7 poh log[ OH ( q)] 7 6
7 Brønsted-syrer og -bser Brønsted-syre: Stoff som vgir protoner HA(q) + H O(l) = H O + (q) + A - (q) K H O ( q) A ( q) HA( q) Eks. vnn som syre: H O(l) = H O + (q) + OH - (q) H O(l) og OH - (q) er korresponderende syre-bse-pr K Brønsted-bse: Stoff som opptr protoner B(q) + H O(l) = BH + (q) + OH - (q) K b Eks.: A - (q) + H O(l) = HA(q) + OH - (q) HA(q) og A - (q) er korresponderende syre-bse-pr Eks. vnn som bse: H O(l) = H O + (q) + OH - (q) H O + (q) og H O(l) er korresponderende syre-bse-pr 7
8 Sterke og svke syrer og bser Sterk syre: K > 1 Sterk bse: K b > 1 Eks. (K >>1): HCl, H SO 4, HNO Eks. (K b >>1): ingen!? H O + er en sterk syre OH - er en sterk bse Svk syre: K < 1 Svk bse: K b < 1 Eks. (K << 1): CH COOH, HCOOH, (COOH), H CO, H O Eks. (K b << 1): NH, CH COO -, HCOO -, HCO -, H O For korresponderende syre-bse-pr: K *K b =K w eller pk +pk b =14. Den korresponderende bsen til en sterk syre er en meget svk bse. Den korresponderende bsen til en svk syre er en svk bse. Og omvendt! 8
9 Svk, enprotisk syre; eks.:mursyre ph som funksjon v [HCOOH(q)] = c ved trdisjonell metode: Reksjonsligning: Før fortynning: HCOOH(q) + H O(l) = H O + (q) + HCOO - (q) Etter fortynning, før likevekt: c Etter reksjon: Etter likevekt: c - x x x Likevekt Hvis ph : x c : -log H O x K ( q) H O H O ( q) HCOO ( q) ( q) 1 HCOOH( q) log K - K 1 c log c 1 ( pk c x x log c ) Ellers, mer generell løsning : x K x K x c K K 4K c 9
10 Svk, enprotisk syre; eks.:mursyre, fortstt HCOOH(q) + H O(l) = H O + (q) + HCOO - (q) ph som funksjon v [HCOOH(q)] = c ved mer generell metode. Tre ukjente, tre ligninger: Likevekt : K H O ( q) HCOO ( q) HCOOH( q) H O ( q) HCOO ( q) [ OH ( )] Elektronøy trlitet : q Mssebln se: Setter inn : HCOO ( q) HCOOH( q) HCOOH( q) H O ( q) HCOO ( q) H O ( q) K HCOOH( q) c H O ( dvs.smme løsning som ved trdisjonell måte. q) osv. 1
11 Svk bse + sterk syre Beregning v ph i en blnding v HCOON(q) og HCl(q). «Trdisjonell metode» Eksempel: Blnder L 1 M HCOON og 1 L 1 M HCl: Reksjonsligning: HCOOH(q) + H O(l) = H O + (q) + HCOO - (q) Før fortynning: 1 1 Etter fortynning:,5,75 Etter reksjon:,5,5 Etter likevekt:,5 - x x,5 + x N + (q) og Cl - (q) er tilskuer-ion 11
12 Svk syre + sterk bse ph i en blnding v HCOOH(q) og NOH(q). Trdisjonell metode Eksempel: Blnder L 1 M HCOOH og 1 L 1 M NOH. Bruker bse-reksjonen (K b = K w /K ) i stedet for syre-reksjonen: Reksjonsligning: HCOO - (q) + H O(l) = OH - (q) + HCOOH(q) Før fortynning: 1 1 Etter fortynning:,5,75 Etter reksjon:,5,5 Etter likevekt:,5 - x x,5 + x N + (q) er tilskuer-ion 1
13 Buffer v mursyre og dens ntriumslt (ntriumformit) ph i en buffer v HCOOH(q) og HCOO - (q); trdisjonell metode Eksempel: blnder 1 L 1 M HCOOH og 1 L 1 M HCOON. Reksjonsligning: HCOOH(q) + H O(l) = H O + (q) + HCOO - (q) Før fortynning: 1 1 Etter fortynning:,5,5 Etter reksjon: (ingen sterk syre/bse) Etter likevekt:,5 - x x,5 + x Likevekt : Hvis x ph -log K H O ( q) HCOO ( q),5: x H O ( q) K H O ( q) log K pk HCOOH( q) x(,5 x),5 x N + (q) er et tilskuer-ion 1
14 Buffer v mursyre og ntriumformit, fortstt ph i en buffer v HCOOH(q) og HCOO - (q). Eksempel: blnder 1 L 1 M HCOOH og 1 L 1 M HCOON. HCOOH(q) + H O(l) = H O + (q) + HCOO - (q) Tre ukjente, tre ligninger: Likevekt : K H O ( q) HCOO ( q) HCOOH( q) H O ( q) N ( q) HCOO ( q) [ OH ( )] Elektronøy trlitet : q Mssebln se: HCOO ( q) HCOOH( q) HCOO ( q) HCOOH( q) Setter inn, etter fortynning: K H O ( q) N ( q) H O ( q) HCOOH ( q) HCOO ( q) N ( q) H O ( q) osv. 14
15 Buffer Hvis A og B er korresponderende pr v svk syre og svk bse, og [A],[B] >> [H O + ],[OH - ] hr vi en buffer. ph pk log B A Bufferen kn regere med sterk syre eller sterk bse og omgjør denne til svk bse eller svk syre; A/B-forholdet endres med dette litt, men ph bufres og endrer seg lite så lenge mn ikke overskrider bufferkpsiteten. 15
16 Toprotisk syre; okslsyre HOOC-COOH eller (COOH) Okslsyre brukes i syntese-lboppgven. Den er toprotisk: (COOH) (q) + H O(l) = H O + (q) + HOOC-COO - (q) K 1 HOOC-COO - (q) + H O(l) = H O + (q) + (COO) - (q) K Syrestyrken vtr som hovedregel med 5 størrelsesordener per proton for flerprotiske syrer: K = K 1 /1 5 pk = pk Delvis protolysert okslsyre, HOOC-COO - (q), er en mfolytt: HOOC-COO - (q) = (COOH) (q) + (COO) - (q) 16
17 Andre syre-bse-begrep Trivielt, men likevel nyttig: Et surt stoff er et stoff som regerer med et bsisk stoff, og omvendt. CO(s) + CO (g) = CCO (s) N O(s) + SO (g) = N SO (s) Et surt stoff er et stoff som vsplter H + fr vnn: SO (g) + H O(l) = H SO (q) H SO (q) + H O(l) = HSO - (q) + H O + (q) Et bsisk stoff er et stoff som vsplter OH - fr vnn: CO(s) + H O(l) = C + (q) + OH - (q) Lewis syre: Elektron-pr-kseptor Lewis bse: Elektron-pr-donor Generell Lewis type reksjon: A + :B = A:B Eksempel: H + + :OH - = H:O:H Eksempel: H B + :NH = H B:NH Lewis-syre-bse-begrepet dekker lle ndre begrep, mens det omvendte ikke nødvendigvis er snt. 17
18 Løselighet Løsning til nøytrle molekyler: Løsning til ioner: C 1 H O 11 (s) = C 1 H O 11 (q) C H 5 OH(l) = C H 5 OH(q) CO (g) = CO (q) Lett løselig: AgNO (s) = Ag + (q) + NO - (q) Tungt løselig: AgCl(s) = Ag + (q) + Cl - (q) K K sp [ Ag [ Ag ( q)][ Cl AgCl( s) ( q)][ Cl ( q)] ( q)] 1,8*1 1 M K sp ; løselighetsprodukt 18
19 Kompleksering Løste species, særlig små og ldde, hr en tendens til å binde til seg lignder; vnnmolekyler (dipol/lewis bse). Hvor mnge, kn være bsert på skjønn. ndre løste species. Ligndene koordineres normlt i symmetriske strukturer oktedrisk (6 lignder) tetredrisk (4 lignder) plnkvdrtisk (4 lignder) Eksempel: [Cu(H O) 6 ] + hekskvkopper(ii)ktion (lysblått) [Cu(NH ) 4 (H O) ] + eller [Cu(NH ) 4 ] + tetrminkopper(ii)ktion (intenst mørkblått) Amin-lignden bindes sterkest, slik t denne likevekten er drevet lngt til høyre. 19
20 Kompleksering; Cu-komplekser, forts. Utfelling v kopperhydroksid: [Cu(H O) 6 ] + (q) + OH - (q) = Cu(OH) (s) + 6H O(l) eller [Cu(H O) 6 ] + (q) + OH - (q) = Cu(H O) 4 (OH) (s) + H O(l) Løsning v kopperhydroksid: Cu(OH) (s) + 6H O(l) = [Cu(H O) 6 ] + (q) + OH - (q) K [[ Cu( H O) ] ( q)][ OH ( q)] Ksp [[ Cu( HO) 6] ( q)][ OH ( q)] 1* Cu( OH ) ( s) M Forenklet (vnlig) beskrivelse v løsning v kopperhydroksid: Cu(OH) (s) = Cu + (q) + OH - (q) K [ Cu ( q)][ OH Cu( OH ) ( s) ( q)] K sp [ Cu ( q)][ OH ( q)] 1*1 19 M Løsning v kopperhydroksid i overskudd v mmonikk: Cu(OH) (s) + 4NH (q) = [Cu(NH ) 4 ] + (q) + OH - (q)
21 En- og flertnnete lignder (Mono- og polydentte) H O og NH er eksempler på éntnnete (monodentte) lignder Etylendimin ( en ) er eksempel på en totnnet (bidentt) lignd. Polydentte lignder som kn binde seg til mer enn ett ktion kn virke som nettverksdnnere Benyttes under syntese v mteriler med flere ktioner; holder ktionene homogent fordelt under prosesseringen Eksempel: Sitronsyre H C 6 H 5 O 7 og citrtnionet C 6 H 5 O 7 - er tridentt og egnet til å lge for eksempel superlederen YB Cu O 7 («YBCO»). Figur: Shriver nd Atkins: Inorgnic Chemistry 1
22 Reduksjon og oksidsjon (red-oks) Reduksjon: A + ze - = A z- eller, mer generelt: A c + ze - = A c-z Ldningen på A blir mer negtiv; oksidsjonstllet reduseres med z Oksidsjon: A = A z+ + ze - eller, mer generelt: A c = A c+z + ze - Ldningen på A blir mer positiv; oksidsjonstllet økes med z Eksempel på red-oks-reksjon: Fe + (q) + Cr + (q) = Fe + (q) + Cr + (q) Reduksjon: Fe + (q) + e - = Fe + (q) Oksidsjon: Cr + (q) = Cr + (q) + e -
23 Oksidsjonstll I kjemiske forbindelser er det som regel ikke slik t elektronene er heltllig fordelt og grunnstoffene hr derfor ikke heltllige oksidsjonstilstnder. Det er derfor i prinsippet ikke opplgt hvilke red-oks-prosesser vi egentlig hr, for eksempel i reksjoner som C + O = CO CO + H O = CO + H forbrenning v kull vnn-skift-reksjonen For å få oversikt over kjemien er det imidlertid nyttig å tillegge grunnstoffene formelle oksidsjonstll i kjemiske forbindelser, som om elektronene vr heltllig fordelt i det vi kller en rent ionisk modell
24 Formelle oksidsjonstll (repetisjon) Tillegges grunnstoffene i et sett regler for forbindelser mellom ulike grunnstoffer. Tr hensyn til elektronegtivitet og ntll vlenselektroner: Fluor hr lltid formelt oksidsjonstll -1 Oksygen hr oksidsjonstll -, -1 eller -½, unnttt i forbindelse med fluor. Hydrogen hr oksidsjonstll +1 eller -1. Andre grunnstoffer hr oksidsjonstll som gis v ntll vlenselektroner og ønsket om å oppnå full oktett i ytre skll, smt v forskjell i elektronegtivitet. Summen v oksidsjonstll skl være lik netto ldning for molekylet/ionet. Eksempel, vnn-skift-reksjonen: CO 1 H O 4 CO H 4
25 Oksidsjon v metller reduksjon v oksider Ellinghm-digrm Vi bruker som eksempel: Ti(s) + O (g) = TiO (s) r G = -RTlnK Reksjonen skjer (går til høyre) ved stndrdbetingelser (1 tm O ) hvis: K > 1 r G < Ellinghm-digrm: r G vs tempertur Figur: Shriver nd Atkins: Inorgnic Chemistry 5
26 Ellinghm-digrm; tempertur-vhengighet G = H - TS r G = r H - T r S Gsser hr stor entropi, S, i forhold til kondenserte fser: Ti(s) + 1/ O (g) = TiO (s) Entropien vtr, r S negtiv, -T r S positiv: r G øker med T C(s) + 1/ O (g) = CO(g) Entropien øker, r S positiv, -T r S negtiv: r G vtr med T Totlreksjon: TiO (s) + C(s) = Ti(s) + CO(g) Figur: Shriver nd Atkins: Inorgnic Chemistry 6
27 Eksempler på industriell fremstilling v grunnstoffer (metller) Fe (totlreksjon, se fig.): Fe O + C = 4Fe + CO Krbotermisk reduksjon Cu, Ni: Røsting v sulfider: Cu S + O = Cu O + SO NiS + 5/ O = NiO + SO med påfølgende reduksjon v oksid, f.eks. krbotermisk eller elektrolytisk Si: Krbotermisk SiO + C = Si + CO Hvordn renses Si? Hv brukes det til? Al: Krbotermisk (> C) eller elektrolytisk: nfe = - r G Hll-Herult: C-elektroder Figur: Shriver nd Atkins: Inorgnic Chemistry 7
28 Elektrokjemi (Smme eksempel som vi strtet med:) Reduksjon: A + ze - = A z- eller, mer generelt: A c + ze - = A c-z Oksidsjon: A = A z+ + ze - eller, mer generelt: A c = A c+z + ze - Eksempel: Fe + (q) + Cr + (q) = Fe + (q) + Cr + (q) Reduksjon: Fe + (q) + e - = Fe + (q) Oksidsjon: Cr + (q) = Cr + (q) + e - Elektrokjemi omhndler reduksjons- og oksidsjonsprosesser (red-oks) der reduksjon og oksidsjon skjer på forskjellig sted. 8
29 Eksempel; Dniell-cellen Elektrokjemiske celler Reduksjon: Cu + (q) + e - = Cu(s) 1 Oksidsjon: Zn(s) = Zn + (q) + e - 1 Totlreksjon: Cu + (q) + Zn(s) = Cu(s) + Zn + (q) Tekst-fremstilling v cellen: Michel Frdy Zn(s) Zn + (q) Cu + (q) Cu(s) Komm skiller stoffer i smme fse Enkle linjer ( ) ngir fsegrenser Dobbel linje ( ) skiller hlvcellene Hvis vi trekker strøm fr cellen får vi F = C/mol elektroner F C/mol Zn C (coulomb) = A s 9
30 Arbeid, Gibbs energiforndring og potensilforskjell (spenning) i en elektrokjemisk celle I en elektrokjemisk celle kn vi gjøre elektrisk rbeid w el i tillegg til volumrbeidet w PV. w w el w PV Elektrisk rbeid utført reversibelt på cellen tilsvrer økningen i cellens Gibbs energi; G w el Det elektriske rbeidet vi gjør (tilfører) er gitt ved ntllet elektroner multiplisert med ldningen (-ne, eller nf for et mol reksjoner) og med potensilforskjellen E fr strtpunktet til sluttpunktet: G = w el = -nee (per reksjonsenhet) G = w el = -nfe (per mol reksjonsenheter) Dette uttrykker blnsen i elektrokjemisk celle ved likevekt (null strøm). Potensilforskjellen for elektroner oppveier forskjellen i Gibbs energi for reksjonen. Hvis elektronene vil gå fr negtiv til positiv elektrode, blir E positiv; w el og G blir d negtive; cellen gjør rbeid; Glvnisk celle (btteri, brenselcelle). Hvis elektronene må gå fr positiv til negtiv elektrode, blir E negtiv; w el og G blir d positive; vi gjør rbeid på cellen; Elektrolytisk celle (elektrolyse, ldning v kkumultor).
31 Cellespenning; Nernst-ligningen Gibbs energiforndring og cellespenning: G nfe Stndrd Gibbs energiforndring og stndrd cellespenning G nfe Smmenhengen mellom de to, G G RT ln Q Gir Nernst-likningen (for hele celler og for ktoder): E E RT nf ln Q 1
32 Ved 98 K Vi liker å bruke log i stedet for ln: log x,44ln x Ved 98 K: RT 98,59 K ln Q log Q nf n slik t vi ofte ser for eksempel Nernst-ligningen skrevet: E E,59 log Q n Husk t dette d gjelder bre ved bruk v log og ved 98 K.
33 Tre måter å ngi stndrd-dt for en elektrokjemisk reksjon: G RT ln K nfe Legg merke til t energiendringer G og G er proporsjonle med ntll mol elektroner i reksjonen (ekstensiv egenskp), mens E og E er uvhengige v ntll mol (intensiv egenskp).
34 Reduksjonspotensiler; refernseelektrode Snn verdi v E for én hlvcelle kn ikke måles. Vi må h en motelektrode en refernseelektrode. Vi definerer derfor en stndrd refernse-hlvcelle; Stndrd hydrogen-elektrode (SHE): H + (q, 1M) + e - = H (g, 1 br) E r G Zn + (q, 1M) + e - = Zn(s) E =? Vi måler: E(Zn +,Zn) - E(H +,H ) = -.76 V Zink-elektroden hr negtiv spenning, Pt-elektroden positiv. Dette betyr t E(Zn +,Zn) SHE = -.76 V Spontn cellereksjon; H + (q) + Zn(s) = H (g) + Zn + (q) E celle = V - (-.76 V) = +.76 V r G = -147 kj/mol Figur: Shriver nd Atkins: Inorgnic Chemistry 4
35 Elektrokjemisk serie (spenningsrekken) Øverst: Stor positiv E(Oks,Red) Oksidert form er et sterkt oksidsjonsmiddel Eks.: F (g) +e - = F - (q) E= +.5 V Hlogener, edelmetllioner, høye oksidsjonstrinn Nederst: Stor negtiv E(Oks,Red) Redusert form er et sterkt reduksjonsmiddel Eks.: Li + (q) + e - = Li(s) E= -.4 V Uedle metller Tbell: Shriver nd Atkins: Inorgnic Chemistry Hvis to hlvreksjoner kombineres vil den som står øverst i spenningsrekken gå til høyre, mens den som står nederst vil gå til venstre (under stndrdbetingelser). 5
36 Hlvceller En elektrokjemisk reksjon eller celle omftter to hlvreksjoner eller hlvceller. Vi kn velge å kombinere dem på to måter: Reduksjon: A + xe - = A x- Oksidsjon: B = B y+ + ye - y x Totl: ya + xb = ya x- + xb y+ G E totl E red yg E oks red xg oks Reduksjon 1: A + xe - = A x- y Reduksjon : B y+ + ye - = B - x Totl: ya + xb = ya x- + xb y+ G E totl E red1 yg E red1 red xg red 6
37 Øvelser 7
38 Kinetikk og overpotensiler Reksjoner krever ktivering; ktiveringsenergi Kn uttrykkes som ktiveringspotensil; overpotensil E op = -ΔG kt /nf Overpotensilet er krkteristisk for hver delreksjon Eks.: Reduksjon og oksidsjon v vnn hr ofte rundt.6 V i overpotensil 8
39 Termodynmikk, kinetikk, ktlyse Eksempel: Oksidsjon v mmonikk 9
40 Oppsummering Kpittel 6 Et mål med kpittelet hr vært å gjøre seg kjent med Viktige typer kjemiske reksjoner og likevekter (syre-bse, oppløsningutfelling, kompleksering, red-oks, elektrokjemi) Beregninger v konsentrsjoner i kjemiske likevektssystemer Måter å fremstille dt for likevekter på Konsentrsjoner i kjemiske likevekter kn beregnes ved å kombinere Likevektskonstnt(er) Msseblnse(r) Elektronøytrlitet Alterntiv (trdisjonell) metodikk i beregninger v bl.. syre-bselikevekter: Finn relevnt reksjonsligning Blnding fortynning Reksjon (sterke syrer eller bser regerer fullstendig) Fininnstilling v likevekt 4
41 Oppsummering, Kp. 6, forts. Mnge prktiske verktøy for likevektsdt: Generelt: G RT ln K nfe Spesielt for red-oks-kjemi: Ellinghm-digrm G vs T for oksidsjoner Spenningsrekken E for reduksjon 41
Kjemiske og elektrokjemiske reaksjoner og likevekter
 MENA11; Mteriler, energi og nnoteknologi - Kp. 6 Kjemiske og elektrokjemiske reksjoner og likevekter Litt repetisjon om G og K Likevekter Truls Norby Kjemisk institutt Universitetet i Oslo Senter for Mterilvitenskp
MENA11; Mteriler, energi og nnoteknologi - Kp. 6 Kjemiske og elektrokjemiske reksjoner og likevekter Litt repetisjon om G og K Likevekter Truls Norby Kjemisk institutt Universitetet i Oslo Senter for Mterilvitenskp
Kjemiske og elektrokjemiske reaksjoner og likevekter
 MENA1001; Mteriler, energi og nnoteknologi - Kp. 6 Kjemiske og elektrokjemiske reksjoner og likevekter Litt repetisjon om G og K Likevekter Truls Norby Kjemisk institutt Universitetet i Oslo Senter for
MENA1001; Mteriler, energi og nnoteknologi - Kp. 6 Kjemiske og elektrokjemiske reksjoner og likevekter Litt repetisjon om G og K Likevekter Truls Norby Kjemisk institutt Universitetet i Oslo Senter for
FASIT (Oppg. bok / ekstra oppg.)
 Fsit 6 FASIT (Oppg. bok / ekstr oppg.).1 Syre-bsereksjoner.1 En syre er et stoff som kn vgi H -ioner. En syre gir sur løsning i vnn. b 1 Syre Sur løsning Syre Syre 5 Sur løsning. HBr H O Br H O b HNO H
Fsit 6 FASIT (Oppg. bok / ekstr oppg.).1 Syre-bsereksjoner.1 En syre er et stoff som kn vgi H -ioner. En syre gir sur løsning i vnn. b 1 Syre Sur løsning Syre Syre 5 Sur løsning. HBr H O Br H O b HNO H
Kjemi og miljø. Elektrokjemi Dette kompendiet dekker følgende kapittel i Rystad & Lauritzen: 10.1, 10.2, 10.3, 10.4 og 10.5
 1 Kjemi og miljø Elektrokjemi Dette kompendiet dekker følgende kapittel i Rystad & Lauritzen: 10.1, 10.2, 10.3, 10.4 og 10.5 Kapittel 10 Elektrokjemi 2 10.1 Repetisjon av viktige begreper: 2 10.2 Elektrokjemiske
1 Kjemi og miljø Elektrokjemi Dette kompendiet dekker følgende kapittel i Rystad & Lauritzen: 10.1, 10.2, 10.3, 10.4 og 10.5 Kapittel 10 Elektrokjemi 2 10.1 Repetisjon av viktige begreper: 2 10.2 Elektrokjemiske
Studie av overføring av kjemisk energi til elektrisk energi og omvendt. Vi snakker om redoks reaksjoner
 Kapittel 19 Elektrokjemi Repetisjon 1 (14.10.02) 1. Kort repetisjon redoks Reduksjon: Når et stoff tar opp elektron Oksidasjon: Når et stoff avgir elektron 2. Elektrokjemiske celler Studie av overføring
Kapittel 19 Elektrokjemi Repetisjon 1 (14.10.02) 1. Kort repetisjon redoks Reduksjon: Når et stoff tar opp elektron Oksidasjon: Når et stoff avgir elektron 2. Elektrokjemiske celler Studie av overføring
Universitetet i Oslo Det matematisk-naturvitenskapelige fakultet
 Universitetet i Oslo Det matematisk-naturvitenskapelige fakultet Eksamen i KJM1100 Generell kjemi Eksamensdag: Fredag 15. januar 2016 Oppgavesettet består av 17 oppgaver med følgende vekt (også gitt i
Universitetet i Oslo Det matematisk-naturvitenskapelige fakultet Eksamen i KJM1100 Generell kjemi Eksamensdag: Fredag 15. januar 2016 Oppgavesettet består av 17 oppgaver med følgende vekt (også gitt i
Kapittel 9 Syrer og baser
 Kapittel 9 Syrer og baser 1. Syre og base (i) Definisjon (ii) Likevektsuttrykk og likevektskonstant (iii) Sterke syrer og sterke baser (iv) Svake syrer og svake baser 2. Vann som både syre og base (amfotært)
Kapittel 9 Syrer og baser 1. Syre og base (i) Definisjon (ii) Likevektsuttrykk og likevektskonstant (iii) Sterke syrer og sterke baser (iv) Svake syrer og svake baser 2. Vann som både syre og base (amfotært)
Elektrokjemi: Studie av overføring av kjemisk energi til elektrisk energi og omvendt.
 1 Kapittel 10 Elektrokjemi Elektrokjemi: Studie av overføring av kjemisk energi til elektrisk energi og omvendt. 1. Repetisjon av viktige begreper: Reduksjon: Når et stoff tar opp elektron: Cu 2+ + 2e
1 Kapittel 10 Elektrokjemi Elektrokjemi: Studie av overføring av kjemisk energi til elektrisk energi og omvendt. 1. Repetisjon av viktige begreper: Reduksjon: Når et stoff tar opp elektron: Cu 2+ + 2e
Når vi snakker om likevektskonstanter for syrer og baser så er det alltid syren eller basen i reaksjon med vann
 Kapittel 16 Syrer og baser Repetisjon 1(30.09.03) 1. Syrer og baser Likevektsuttrykk/konstant Når vi snakker om likevektskonstanter for syrer og baser så er det alltid syren eller basen i reaksjon med
Kapittel 16 Syrer og baser Repetisjon 1(30.09.03) 1. Syrer og baser Likevektsuttrykk/konstant Når vi snakker om likevektskonstanter for syrer og baser så er det alltid syren eller basen i reaksjon med
1. Oppgaver til atomteori.
 1. Oppgaver til atomteori. 1. Hva er elektronkonfigurasjonen til hydrogen (H)?. Fyll elektroner inn i energidiagrammet slik at du får elektronkonfigurasjonen til hydrogen. p 3. Hva er elektronkonfigurasjonen
1. Oppgaver til atomteori. 1. Hva er elektronkonfigurasjonen til hydrogen (H)?. Fyll elektroner inn i energidiagrammet slik at du får elektronkonfigurasjonen til hydrogen. p 3. Hva er elektronkonfigurasjonen
Definisjoner Brønsted, 1923. En syre er et stoff som kan spalte av protoner En base er et stoff som kan ta opp protoner
 Syrer og baser Definisjoner Brønsted, 1923 En syre er et stoff som kan spalte av protoner En base er et stoff som kan ta opp protoner Syrer Genrelt uttrykk HB H + + B - syre H + + korresponderende base
Syrer og baser Definisjoner Brønsted, 1923 En syre er et stoff som kan spalte av protoner En base er et stoff som kan ta opp protoner Syrer Genrelt uttrykk HB H + + B - syre H + + korresponderende base
Fasit oppdatert 10/9-03. Se opp for skrivefeil. Denne fasiten er ny!
 Fasit odatert 10/9-03 Se o for skrivefeil. Denne fasiten er ny! aittel 1 1 a, b 4, c 4, d 4, e 3, f 1, g 4, h 7 a 10,63, b 0,84, c,35. 10-3 aittel 1 Atomnummer gir antall rotoner, mens masse tall gir summen
Fasit odatert 10/9-03 Se o for skrivefeil. Denne fasiten er ny! aittel 1 1 a, b 4, c 4, d 4, e 3, f 1, g 4, h 7 a 10,63, b 0,84, c,35. 10-3 aittel 1 Atomnummer gir antall rotoner, mens masse tall gir summen
Kap 4. Typer av kjemiske reaksjoner og løsningsstøkiometri
 1 Kap 4. Typer av kjemiske reaksjoner og løsningsstøkiometri Vandige løsninger; sterke og svake elektrolytter Sammensetning av løsninger Typer av kjemiske reaksjoner Fellingsreaksjoner (krystallisasjon)
1 Kap 4. Typer av kjemiske reaksjoner og løsningsstøkiometri Vandige løsninger; sterke og svake elektrolytter Sammensetning av løsninger Typer av kjemiske reaksjoner Fellingsreaksjoner (krystallisasjon)
LØSNINGSFORSLAG TIL EKSAMEN AUGUST 2007
 NTNU Norges teknisk-naturvitenskapelige universitet Fakultet for naturvitenskap og teknologi Institutt for materialteknologi TMT1 KJEMI LØSNINGSFORSLAG TIL EKSAMEN AUGUST 007 OPPGAVE 1 a) - ph defineres
NTNU Norges teknisk-naturvitenskapelige universitet Fakultet for naturvitenskap og teknologi Institutt for materialteknologi TMT1 KJEMI LØSNINGSFORSLAG TIL EKSAMEN AUGUST 007 OPPGAVE 1 a) - ph defineres
8. Ulike typer korrosjonsvern. Kapittel 10 Elektrokjemi. 1. Repetisjon av noen viktige begreper. 2. Elektrolytiske celler
 1 Kapittel 10 Elektrokjemi 1. Repetisjon av noen viktige begreper 2. Elektrolytiske celler 3. Galvaniske celler (i) Cellepotensial (ii) Reduksjonspotensialet (halvreaksjonspotensial) (iii) Standardhydrogen
1 Kapittel 10 Elektrokjemi 1. Repetisjon av noen viktige begreper 2. Elektrolytiske celler 3. Galvaniske celler (i) Cellepotensial (ii) Reduksjonspotensialet (halvreaksjonspotensial) (iii) Standardhydrogen
EKSAMENSOPPGAVE. Fag: Generell og uorganisk kjemi. Faglig veileder: Kirsten Aarset Eksamenstid, fra - til: 9.00-14.00 LO 400 K.
 EKSAMENSOPPGAVE Fag: Generell og uorganisk kjemi Gruppe(r): 1KA Fagnr LO 400 K Dato: 14. desember 001 Faglig veileder: Kirsten Aarset Eksamenstid, fra - til: 9.00-14.00 Eksamensoppgaven består av Tillatte
EKSAMENSOPPGAVE Fag: Generell og uorganisk kjemi Gruppe(r): 1KA Fagnr LO 400 K Dato: 14. desember 001 Faglig veileder: Kirsten Aarset Eksamenstid, fra - til: 9.00-14.00 Eksamensoppgaven består av Tillatte
Kapittel 17 Mer om likevekter
 Kapittel 17 Mer om likevekter 1. Mer om syre-base likevekter - Buffer o Definisjon o Hvordan virker en buffer? o Bufferkapasitet o Bufferlignigen o Hvordan lage en buffer med spesifikk ph?. Titrerkurver
Kapittel 17 Mer om likevekter 1. Mer om syre-base likevekter - Buffer o Definisjon o Hvordan virker en buffer? o Bufferkapasitet o Bufferlignigen o Hvordan lage en buffer med spesifikk ph?. Titrerkurver
3. Balansering av redoksreaksjoner (halvreaksjons metoden)
 Kapittel 4 Oksidasjon og reduksjons reaksjoner (redoks reaksjoner) 1. Definisjon av oksidasjon og reduksjon 2. Oksidasjonstall og regler 3. Balansering av redoksreaksjoner (halvreaksjons metoden) Kapittel
Kapittel 4 Oksidasjon og reduksjons reaksjoner (redoks reaksjoner) 1. Definisjon av oksidasjon og reduksjon 2. Oksidasjonstall og regler 3. Balansering av redoksreaksjoner (halvreaksjons metoden) Kapittel
EKSAMENSOPPGAVE. KJE-1001 Introduksjon til kjemi og kjemisk biologi
 Fakultet for naturvitenskap og teknologi EKSAMENSOPPGAVE Eksamen i: KJE-1001 Introduksjon til kjemi og kjemisk biologi Dato: Onsdag 28. februar 2018 Klokkeslett: 09:00-15:00 Sted: Tillatte hjelpemidler:
Fakultet for naturvitenskap og teknologi EKSAMENSOPPGAVE Eksamen i: KJE-1001 Introduksjon til kjemi og kjemisk biologi Dato: Onsdag 28. februar 2018 Klokkeslett: 09:00-15:00 Sted: Tillatte hjelpemidler:
HØGSKOLEN I SØR-TRØNDELAG
 HØGSKOLEN I SØR-TRØNDELAG AVDELING FOR TEKNOLOGI Kandidatnr: Eksamensdato: 09.12.2004 Varighet: 09.00 14.00 Fagnummer: FO120N Fagnavn: Klasse(r): Generell kjemi Studiepoeng: Faglærer(e): Hjelpemidler:
HØGSKOLEN I SØR-TRØNDELAG AVDELING FOR TEKNOLOGI Kandidatnr: Eksamensdato: 09.12.2004 Varighet: 09.00 14.00 Fagnummer: FO120N Fagnavn: Klasse(r): Generell kjemi Studiepoeng: Faglærer(e): Hjelpemidler:
Syrer og baser. Et proton er et hydrogenatom som har mistet sitt eneste elektron. Det beskrives som H +, en positiv ladning.
 Syrer og baser Det finnes flere definisjoner på hva syrer og baser er. Vi skal bruke definisjonen til Brønsted: En Brønsted syre er en proton donor. En Brønsted base er en proton akseptor. 1s 1+ Et proton
Syrer og baser Det finnes flere definisjoner på hva syrer og baser er. Vi skal bruke definisjonen til Brønsted: En Brønsted syre er en proton donor. En Brønsted base er en proton akseptor. 1s 1+ Et proton
EKSAMEN TMT4112 KJEMI
 Eksamen TMT4112, 18. desember-2009 Side 1 av 6 NTNU NORGES TEKNISK- VITENSKAPELIGE UNIVERSITET INSTITUTT FOR MATERIALTEKNOLOGI Faglig kontakt under eksamen: Kjell Wiik; Tel.: 73594082/Mob. tel.: 922 65
Eksamen TMT4112, 18. desember-2009 Side 1 av 6 NTNU NORGES TEKNISK- VITENSKAPELIGE UNIVERSITET INSTITUTT FOR MATERIALTEKNOLOGI Faglig kontakt under eksamen: Kjell Wiik; Tel.: 73594082/Mob. tel.: 922 65
LØSNINGSFORSLAG EKSAMEN TEP 4115/4120 TERMODYNAMIKK 1 (KONT) Fredag 19. august 2005 Tid: kl. 09:00-13:00
 Side v 8 NORGES TEKNISK-NATURVITENSKAPELIGE UNIVERSITET (NTNU) - TRONDHEIM INSTITUTT FOR ENERGI OG PROSESSTEKNIKK LØSNINGSFORSLAG EKSAMEN TEP 45/40 TERMODYNAMIKK (KONT) Fredg 9. ugust 005 Tid: kl. 09:00
Side v 8 NORGES TEKNISK-NATURVITENSKAPELIGE UNIVERSITET (NTNU) - TRONDHEIM INSTITUTT FOR ENERGI OG PROSESSTEKNIKK LØSNINGSFORSLAG EKSAMEN TEP 45/40 TERMODYNAMIKK (KONT) Fredg 9. ugust 005 Tid: kl. 09:00
FLERVALGSOPPGAVER REDOKS-/ELEKTORKJEMI
 FLERVALGSOPPGAVER REDOKS-/ELEKTORKJEMI Hjelpemidler: Periodesystem (kalkulator der det er angitt) Hvert spørsmål har ett riktig svaralternativ. Når ikke noe annet er oppgitt kan du anta STP (standard trykk
FLERVALGSOPPGAVER REDOKS-/ELEKTORKJEMI Hjelpemidler: Periodesystem (kalkulator der det er angitt) Hvert spørsmål har ett riktig svaralternativ. Når ikke noe annet er oppgitt kan du anta STP (standard trykk
Fasit til finalerunde Kjemiolympiaden 2002 Blindern 19. april 2002
 asit til finalerunde Kjemiolympiaden 2002 lindern 19. april 2002 ppgave 1 (10%) a) Elektroner beveger seg fra blystaven mot hydrogenelektroden. lyionene beveger seg via saltbroen til hydrogenelektronden.
asit til finalerunde Kjemiolympiaden 2002 lindern 19. april 2002 ppgave 1 (10%) a) Elektroner beveger seg fra blystaven mot hydrogenelektroden. lyionene beveger seg via saltbroen til hydrogenelektronden.
Eksamen. Emnekode: KJEMI1/FAD110. Emnenavn: Kjemi 1. Dato: 27.02.2015. Tid (fra-til): 0900-1300. Tillatte hjelpemidler: Kalkulator, KjemiData.
 Bokmål Eksamen Emnekode: KJEMI1/FAD110 Emnenavn: Kjemi 1 Dato: 27.02.2015 Tid (fra-til): 0900-1300 Tillatte hjelpemidler: Kalkulator, KjemiData Faglærer(e) : Anne Brekken Sensurfrist : 20.03.2015 Antall
Bokmål Eksamen Emnekode: KJEMI1/FAD110 Emnenavn: Kjemi 1 Dato: 27.02.2015 Tid (fra-til): 0900-1300 Tillatte hjelpemidler: Kalkulator, KjemiData Faglærer(e) : Anne Brekken Sensurfrist : 20.03.2015 Antall
9 Potenser. Logaritmer
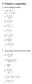 9 Potenser. Logritmer Foret utregingene nedenfor: 5 5 c 6 7 d e 5 f g h i Regn ut og gjør svrene så enkle som mulige: c y y d e f g h i j y y + y + y + + y Prisen på en motorsg vr kr 56 i 99. Vi regner
9 Potenser. Logritmer Foret utregingene nedenfor: 5 5 c 6 7 d e 5 f g h i Regn ut og gjør svrene så enkle som mulige: c y y d e f g h i j y y + y + y + + y Prisen på en motorsg vr kr 56 i 99. Vi regner
9 SYRER OG BASER. Syre: HCl H (aq) + Cl (aq) Her er Cl syreresten til HCl. Arrhenius' definisjon begrenser oss til vannløsninger.
 9 SYRER OG BASER 9.1 DEFINISJONER Historie. Begrepet syrer har eksistert siden tidlig i kjemiens historie. I denne gruppen plasserte man stoffer med bestemte egenskaper. En av disse egenskapene var sur
9 SYRER OG BASER 9.1 DEFINISJONER Historie. Begrepet syrer har eksistert siden tidlig i kjemiens historie. I denne gruppen plasserte man stoffer med bestemte egenskaper. En av disse egenskapene var sur
Prøveeksamen i Fysikk/kjemi Løsningsforslag Prøve 4
 Program for lektro og Datateknikk/ AFT Prøveeksamen i Fysikk/kjemi Løsningsforslag Prøve 4 Oppgave 1 a) Det skal settes navn på 10 ioner : i) SO4 2 : sulfation ii) S 2 : sulfidion iii) Cl : kloridion iv)
Program for lektro og Datateknikk/ AFT Prøveeksamen i Fysikk/kjemi Løsningsforslag Prøve 4 Oppgave 1 a) Det skal settes navn på 10 ioner : i) SO4 2 : sulfation ii) S 2 : sulfidion iii) Cl : kloridion iv)
Universitetet i Oslo Det matematisk-naturvitenskapelige fakultet løsningsforslag
 Universitetet i Oslo Det matematisk-naturvitenskapelige fakultet løsningsforslag Eksamen i KJM00 Generell kjemi Eksamensdag: onsdag 9. desember 205 Oppgavesettet består av 7 oppgaver med følgende vekt
Universitetet i Oslo Det matematisk-naturvitenskapelige fakultet løsningsforslag Eksamen i KJM00 Generell kjemi Eksamensdag: onsdag 9. desember 205 Oppgavesettet består av 7 oppgaver med følgende vekt
Universitetet i Oslo Det matematisk -naturvitenskapelige fakultet
 Universitetet i Oslo Det matematisk -naturvitenskapelige fakultet Løsningsforslag Eksamen i KJM1101 Generell kjemi Fredag 8. desember 2017 kl. 14.30-18.30 (4 timer) Alle 17 oppgaver skal besvares. Hver
Universitetet i Oslo Det matematisk -naturvitenskapelige fakultet Løsningsforslag Eksamen i KJM1101 Generell kjemi Fredag 8. desember 2017 kl. 14.30-18.30 (4 timer) Alle 17 oppgaver skal besvares. Hver
Den 35. internasjonale Kjemiolympiade i Aten, juli uttaksprøve. Fasit.
 Oppgave 1 A) d B) c C) b D) d E) a F) a G) c H) d I) c J) b Den 35. internasjonale Kjemiolympiade i Aten, juli 2003. 1. uttaksprøve. Fasit. Oppgave 2 A) a B) b C) a D) b Oppgave 3 Masseprosenten av hydrogen
Oppgave 1 A) d B) c C) b D) d E) a F) a G) c H) d I) c J) b Den 35. internasjonale Kjemiolympiade i Aten, juli 2003. 1. uttaksprøve. Fasit. Oppgave 2 A) a B) b C) a D) b Oppgave 3 Masseprosenten av hydrogen
Løsningsforslag kapittel 3
 Løsningsoslg kpittel 3 3.1 ) Uttykket o (den konigusjonelle) entopien S e gitt ved S k ln W, de W uttykke ntll skillbe mikotilstnde. Siden kystllen inneholde n vknse odelt ove N N! N! tomplsse e W og S
Løsningsoslg kpittel 3 3.1 ) Uttykket o (den konigusjonelle) entopien S e gitt ved S k ln W, de W uttykke ntll skillbe mikotilstnde. Siden kystllen inneholde n vknse odelt ove N N! N! tomplsse e W og S
EKSAMENSOPPGAVE. Kalkulator «Huskelapp» -A4 ark med skrift på begge sider Enkel norsk-engelsk/engelsk-norsk ordbok
 Fakultet for naturvitenskap og teknologi EKSAMENSOPPGAVE Eksamen i: KJE-1001 Introduksjon til kjemi og kjemisk biologi Dato: 22.02.2017 Klokkeslett: 09:00-15:00 Sted: Åsgårdveien 9 Tillatte hjelpemidler:
Fakultet for naturvitenskap og teknologi EKSAMENSOPPGAVE Eksamen i: KJE-1001 Introduksjon til kjemi og kjemisk biologi Dato: 22.02.2017 Klokkeslett: 09:00-15:00 Sted: Åsgårdveien 9 Tillatte hjelpemidler:
Figur s Figurer kapittel 9: Elektrokjemi. ytre krets. ioner. oksidasjon. reduksjon. indre krets
 Figur s. 204 ytre krets oksidasjon ioner + reduksjon indre krets Forenklet illustrasjon av en elektrokjemisk celle. Reduksjon og oksidasjon skjer på hvert sitt sted ved at elektroner går gjennom en leder
Figur s. 204 ytre krets oksidasjon ioner + reduksjon indre krets Forenklet illustrasjon av en elektrokjemisk celle. Reduksjon og oksidasjon skjer på hvert sitt sted ved at elektroner går gjennom en leder
Kjemien stemmer KJEMI 1
 Figur s. 34 Egenskaper hos syrer / sure løsninger Smaker surt Endrer farge på indikatorer og noen plantefarger Egenskaper hos baser / basiske løsninger Smaker bittert Endrer farge på indikatorer og noen
Figur s. 34 Egenskaper hos syrer / sure løsninger Smaker surt Endrer farge på indikatorer og noen plantefarger Egenskaper hos baser / basiske løsninger Smaker bittert Endrer farge på indikatorer og noen
MENA1001 Deleksamen 2017 Forside
 MENA1001 Deleksamen 2017 Forside MENA1001 Tidspunkt: Onsdag 11. oktober 2017, kl. 9.00-10.00 Alle 20 oppgaver skal besvares. Hver oppgave teller likt. Det er 1 poeng for korrekt svar, 0 poeng for feil
MENA1001 Deleksamen 2017 Forside MENA1001 Tidspunkt: Onsdag 11. oktober 2017, kl. 9.00-10.00 Alle 20 oppgaver skal besvares. Hver oppgave teller likt. Det er 1 poeng for korrekt svar, 0 poeng for feil
R.ANNAMALAI
 PTA - I-V M.Sc (Che).,M.Sc (Psy).,M.Phil.,B.Ed. PGT(CHEMISTRY), GOVT. GIRLS HR. SEC. SCHOOL GINGEE, email: ssssmalai@gmail.com. PTA - - I E n =-313.6/n 2, E n =-34.84 n XeF 4 AgCl AgNO 3 AgF AgBr MnO 2
PTA - I-V M.Sc (Che).,M.Sc (Psy).,M.Phil.,B.Ed. PGT(CHEMISTRY), GOVT. GIRLS HR. SEC. SCHOOL GINGEE, email: ssssmalai@gmail.com. PTA - - I E n =-313.6/n 2, E n =-34.84 n XeF 4 AgCl AgNO 3 AgF AgBr MnO 2
Kjemiske tegn Finn alle grunnstoffer med kjemisk tegn som begynner på a) A b) S 1.2
 OPPGAVER (1 atomer, molekyler, ioner) 1.1 Kjemiske tegn Finn alle grunnstoffer med kjemisk tegn som begynner på a) A b) S 1.2 Atomkjernen Hva er antall protoner, nøytroner, nukleoner i 35 235 3 80 a) S
OPPGAVER (1 atomer, molekyler, ioner) 1.1 Kjemiske tegn Finn alle grunnstoffer med kjemisk tegn som begynner på a) A b) S 1.2 Atomkjernen Hva er antall protoner, nøytroner, nukleoner i 35 235 3 80 a) S
EKSAMEN I TMT4105 KJEMI
 Fag TMT4105 KJEMI Side 1 av 14 NORGES TEKNISK- NATURVITENSKAPELIGE UNIVERSITET INSTITUTT FOR MATERIALTEKNOLOGI Studienr Studieprogram :.. Faglig kontakt under eksamen : Navn : Håvard Karoliussen Tlf. :
Fag TMT4105 KJEMI Side 1 av 14 NORGES TEKNISK- NATURVITENSKAPELIGE UNIVERSITET INSTITUTT FOR MATERIALTEKNOLOGI Studienr Studieprogram :.. Faglig kontakt under eksamen : Navn : Håvard Karoliussen Tlf. :
EKSAMEN TMT4110 og TMT4112 KJEMI
 Side 1 av 8 NTNU NORGES TEKNISK- VITENSKAPELIGE UNIVERSITET INSTITUTT FOR MATERIALTEKNOLOGI Faglig kontakt under eksamen: Institutt for materialteknologi, Gløshaugen Kjell Wiik; Tel.: 73594082/Mob. tel.:
Side 1 av 8 NTNU NORGES TEKNISK- VITENSKAPELIGE UNIVERSITET INSTITUTT FOR MATERIALTEKNOLOGI Faglig kontakt under eksamen: Institutt for materialteknologi, Gløshaugen Kjell Wiik; Tel.: 73594082/Mob. tel.:
TALM1008 Fysikk og Kjemi Løsning kjemidel kont august 2013
 Program for Elektro og Datateknikk/ AFT TALM1008 Fysikk og Kjemi Løsning kjemidel kont august 2013 Oppgave 1 a) Det skal skrives navn på tre forbindelser : KNO 2 : kaliumnitritt. Ionet NO 2 kalles for
Program for Elektro og Datateknikk/ AFT TALM1008 Fysikk og Kjemi Løsning kjemidel kont august 2013 Oppgave 1 a) Det skal skrives navn på tre forbindelser : KNO 2 : kaliumnitritt. Ionet NO 2 kalles for
Kapittel 4 Ulike kjemiske reaksjoner og støkiometri i løsninger
 Kapittel 4 Ulike kjemiske reaksjoner og støkiometri i løsninger 1. Vann som løsningsmiddel 2. Elektrolytter Sterke elektrolytter Svake elektrolytter Ikke-eletrolytter 3. Sammensetning av løsning Molaritet
Kapittel 4 Ulike kjemiske reaksjoner og støkiometri i løsninger 1. Vann som løsningsmiddel 2. Elektrolytter Sterke elektrolytter Svake elektrolytter Ikke-eletrolytter 3. Sammensetning av løsning Molaritet
Fasit Kjemien stemmer Forkurs
 Fasit Kjemien stemmer Forkurs Kapittel 1 Kjemiens egenart 1.1 a) 3, b) 5 og c) 2 1.2 a) et elektronpar b) tiltrekningskrefter mellom positive og negative ioner c) et elektronpar 1.3 a) Antall protoner
Fasit Kjemien stemmer Forkurs Kapittel 1 Kjemiens egenart 1.1 a) 3, b) 5 og c) 2 1.2 a) et elektronpar b) tiltrekningskrefter mellom positive og negative ioner c) et elektronpar 1.3 a) Antall protoner
UNIVERSITETET I OSLO
 UNIVERSITETET I OSLO Det matematisk-naturvitenskapelige fakultetet Eksamen i: KJM 1100 Generell kjemi Eksamensdag: 18. desember 2012 Tid for eksamen: 14.30 18.30 Oppgavesettet er på 5 sider Vedlegg: Periodesystemet
UNIVERSITETET I OSLO Det matematisk-naturvitenskapelige fakultetet Eksamen i: KJM 1100 Generell kjemi Eksamensdag: 18. desember 2012 Tid for eksamen: 14.30 18.30 Oppgavesettet er på 5 sider Vedlegg: Periodesystemet
FASIT til 2. UTTAKSPRØVE
 Kjemi OL FASIT til 2. UTTAKSPRØVE til den 41. Internasjonale Kjemiolympiaden 2009 i Cambridge, England Oppgave 1 (36 poeng, 2 poeng per deloppgave) 1) C 2) B 3) A 4) A 5) C 6) A 7) C 8) C 9) C 10) C 11)
Kjemi OL FASIT til 2. UTTAKSPRØVE til den 41. Internasjonale Kjemiolympiaden 2009 i Cambridge, England Oppgave 1 (36 poeng, 2 poeng per deloppgave) 1) C 2) B 3) A 4) A 5) C 6) A 7) C 8) C 9) C 10) C 11)
Eksamensoppgave i TMT4110 Kjemi
 Side 1 av 1 Institutt for materialteknologi Eksamensoppgave i TMT110 Kjemi LØSNINGSFORSLAG Faglig kontakt under eksamen: Førsteamanuensis Hilde Lea Lein Tlf.: 735 50880 Eksamensdato: 8. mai 013 Eksamenstid
Side 1 av 1 Institutt for materialteknologi Eksamensoppgave i TMT110 Kjemi LØSNINGSFORSLAG Faglig kontakt under eksamen: Førsteamanuensis Hilde Lea Lein Tlf.: 735 50880 Eksamensdato: 8. mai 013 Eksamenstid
LØSNINGSFORSLAG TIL ØVING NR. 11, VÅR 2014
 NTNU Norges teknisk-naturvitenskapelige universitet Fakultet naturvitenskap og teknologi Institutt for materialteknologi TMT4110 KJEMI LØSNINGSFORSLAG TIL ØVING NR. 11, VÅR 2014 OPPGAVE 1 a) Kovalent binding:
NTNU Norges teknisk-naturvitenskapelige universitet Fakultet naturvitenskap og teknologi Institutt for materialteknologi TMT4110 KJEMI LØSNINGSFORSLAG TIL ØVING NR. 11, VÅR 2014 OPPGAVE 1 a) Kovalent binding:
LØSNINGSFORSLAG TIL EKSAMEN MAI 2006
 NTNU Norges teknisknaturvitenskapelige universitet Fakultet for naturvitenskap og teknologi Institutt for materialteknologi Seksjon uorganisk kjemi TMT KJEMI LØSNINGSFORSLAG TIL EKSAMEN MAI 006 OPPGAVE
NTNU Norges teknisknaturvitenskapelige universitet Fakultet for naturvitenskap og teknologi Institutt for materialteknologi Seksjon uorganisk kjemi TMT KJEMI LØSNINGSFORSLAG TIL EKSAMEN MAI 006 OPPGAVE
Norges teknisk-naturvitenskapelige universitet, Trondheim Institutt for kjemi. Bokmål Student nr.:
 Norges teknisk-naturvitenskapelige universitet, Trondheim Institutt for kjemi KJ1000 Generell kjemi Bokmål Student nr.: Studieprogram: Eksamen lørdag 2. juni 2007, 0900-1300 Tillatte hjelpemidler: kalkulator
Norges teknisk-naturvitenskapelige universitet, Trondheim Institutt for kjemi KJ1000 Generell kjemi Bokmål Student nr.: Studieprogram: Eksamen lørdag 2. juni 2007, 0900-1300 Tillatte hjelpemidler: kalkulator
Den 34. internasjonale Kjemiolympiade i Groningen, juli uttaksprøve. Fasit.
 Den 34. internasjonale Kjemiolympiade i Groningen, juli 00. Oppgave 1 A) 3 B) C) 4 Oppgave 1. uttaksprøve. Fasit. D) 3 E) 4 F) 3 G) 3 H) 3 I) A) Reaksjonen er summen av de to reaksjonene lengre opp. Likevektskonstanten
Den 34. internasjonale Kjemiolympiade i Groningen, juli 00. Oppgave 1 A) 3 B) C) 4 Oppgave 1. uttaksprøve. Fasit. D) 3 E) 4 F) 3 G) 3 H) 3 I) A) Reaksjonen er summen av de to reaksjonene lengre opp. Likevektskonstanten
LØSNINGSFORSLAG TIL ØVING NR. 5, HØST 2009
 NTNU Nrges teknisknturvitenskpelige universitet kultet fr nturvitenskp g teknlgi Institutt fr mterilteknlgi TMT11 JEMI LØSNINGSORSLAG TIL ØVING NR. 5, HØST 009 OPPGAVE 1 ) Hg(OH) (s) = Hg + + OH sp,hg
NTNU Nrges teknisknturvitenskpelige universitet kultet fr nturvitenskp g teknlgi Institutt fr mterilteknlgi TMT11 JEMI LØSNINGSORSLAG TIL ØVING NR. 5, HØST 009 OPPGAVE 1 ) Hg(OH) (s) = Hg + + OH sp,hg
Universitetet i Oslo Det matematisk -naturvitenskapelige fakultet
 Universitetet i Oslo Det matematisk -naturvitenskapelige fakultet Løsningsforslag Eksamen i KJM1100 Generell kjemi Fredag 8. desember 2017 kl. 14.30-18.30 (4 timer) Alle 17 oppgaver skal besvares. Hver
Universitetet i Oslo Det matematisk -naturvitenskapelige fakultet Løsningsforslag Eksamen i KJM1100 Generell kjemi Fredag 8. desember 2017 kl. 14.30-18.30 (4 timer) Alle 17 oppgaver skal besvares. Hver
TFY4104 Fysikk. Institutt for fysikk, NTNU. Lsningsforslag til ving 8. a =
 TFY414 Fysikk. Institutt for fysikk, NTNU. Lsningsforslg til ving 8. Oppgve 1. ) C F = E = m Newtons. lov. Her er = e, s elektronets kselersjon blir = e m E lts mot venstre. b) C Totlt elektrisk felt i
TFY414 Fysikk. Institutt for fysikk, NTNU. Lsningsforslg til ving 8. Oppgve 1. ) C F = E = m Newtons. lov. Her er = e, s elektronets kselersjon blir = e m E lts mot venstre. b) C Totlt elektrisk felt i
LØSNINGSFORSLAG TIL ØVING NR. 6, HØST 2009
 NTNU Norges teknisknaturvitenskapelige universitet Fakultet for naturvitenskap og teknologi Institutt for materialteknologi TMT11 JEMI LØSNINGSFORSLAG TIL ØVING NR. 6, HØST 009 OPPGAVE 1 a) Sterk syre,
NTNU Norges teknisknaturvitenskapelige universitet Fakultet for naturvitenskap og teknologi Institutt for materialteknologi TMT11 JEMI LØSNINGSFORSLAG TIL ØVING NR. 6, HØST 009 OPPGAVE 1 a) Sterk syre,
3. Massevirkningsloven eller likevektsuttrykk for en likevekt
 apittel 8 jemisk likevekt 1. Reversible reaksjoner. Hva er likevekt? 3. Massevirkningsloven eller likevektsuttrykk for en likevekt 4. Likevektskonstanten (i) Hva sier verdien oss? (ii) Sammenhengen mellom
apittel 8 jemisk likevekt 1. Reversible reaksjoner. Hva er likevekt? 3. Massevirkningsloven eller likevektsuttrykk for en likevekt 4. Likevektskonstanten (i) Hva sier verdien oss? (ii) Sammenhengen mellom
Innhold. Forord... 11
 Innhold Forord... 11 Kapittel 1 Atomet og periodesystemet... 13 1.1 Kjemi og atomet... 13 Atomet består av protoner, nøytroner og elektroner... 14 Grunnstoffer... 14 Atomnummer og massenummer... 15 Isotoper...
Innhold Forord... 11 Kapittel 1 Atomet og periodesystemet... 13 1.1 Kjemi og atomet... 13 Atomet består av protoner, nøytroner og elektroner... 14 Grunnstoffer... 14 Atomnummer og massenummer... 15 Isotoper...
Norges teknisk-naturvitenskapelige universitet, Trondheim Institutt for kjemi. Bokmål Student nr.:
 Norges teknisk-naturvitenskapelige universitet, Trondheim Institutt for kjemi KJ1000 Generell kjemi Bokmål Student nr.: Studieprogram: Eksamen fredag 3. desember 2004, 0900-1300 Tillatte hjelpemidler:
Norges teknisk-naturvitenskapelige universitet, Trondheim Institutt for kjemi KJ1000 Generell kjemi Bokmål Student nr.: Studieprogram: Eksamen fredag 3. desember 2004, 0900-1300 Tillatte hjelpemidler:
Fasit til norsk finale for uttak til den. 41. internasjonale kjemiolympiaden i Cambridge, England, juli 2009
 Kjemi L Fasit til norsk finale for uttak til den 41. internasjonale kjemiolympiaden i Cambridge, England, 18.-27. juli 2009 1 ppgave 1 (14 poeng) 1) B 2) C 3) C 4) D 5) C 6) C 7) D ppgave 2 (12 poeng)
Kjemi L Fasit til norsk finale for uttak til den 41. internasjonale kjemiolympiaden i Cambridge, England, 18.-27. juli 2009 1 ppgave 1 (14 poeng) 1) B 2) C 3) C 4) D 5) C 6) C 7) D ppgave 2 (12 poeng)
Oppgave 1 (35 poeng) 1. uttak til den 38. Kjemiolympiaden, Fasit og poengberegning. 1) D 2) B 3) A 4) A 5) D 6) C 7) D 8) C
 1. uttak til den 38. Kjemiolympiaden, 006. Fasit og poengberegning. ppgave 1 (35 poeng) 1) D ) B 3) A ) A 5) D 6) C 7) D 8) C 9) D 10) A 11) C 1) B 13) C 1) B 15) B 16) D 17) B 1 ppgave (15 poeng) A. a)
1. uttak til den 38. Kjemiolympiaden, 006. Fasit og poengberegning. ppgave 1 (35 poeng) 1) D ) B 3) A ) A 5) D 6) C 7) D 8) C 9) D 10) A 11) C 1) B 13) C 1) B 15) B 16) D 17) B 1 ppgave (15 poeng) A. a)
Universitetet i Oslo Det matematisk-naturvitenskapelige fakultet
 Universitetet i Oslo Det matematisk-naturvitenskapelige fakultet Eksamen i KJM1100 Generell kjemi - løsningsforslag 16. desember 2016 kl. 14.30-18.30 Oppgavesettet består av 18 oppgaver med vekting angitt
Universitetet i Oslo Det matematisk-naturvitenskapelige fakultet Eksamen i KJM1100 Generell kjemi - løsningsforslag 16. desember 2016 kl. 14.30-18.30 Oppgavesettet består av 18 oppgaver med vekting angitt
EKSAMENSOPPGAVE I KJE-1001
 Side 1 av 6 sider EKSAMENSOPPGAVE I KJE-1001 Eksamen i : KJE-1001 Eksamensdato : Mandag 25.februar 2013 Tid : 09:00-15:00 Sted : Aud. Max. Tillatte hjelpemidler : Kalkulator "Huskelapp" = ett A4-ark med
Side 1 av 6 sider EKSAMENSOPPGAVE I KJE-1001 Eksamen i : KJE-1001 Eksamensdato : Mandag 25.februar 2013 Tid : 09:00-15:00 Sted : Aud. Max. Tillatte hjelpemidler : Kalkulator "Huskelapp" = ett A4-ark med
Kap. 3 Krumningsflatemetoden
 SIDE. KRUMNINGSFLTEMETODEN I kpittel. og. hr vi sett t en bjelkes krefter og deformsjon kn beskrives ved fire integrler som henger smmen : Skjærkrft : V d Vinkelendring : φ M d Moment : M V d Forskyvning
SIDE. KRUMNINGSFLTEMETODEN I kpittel. og. hr vi sett t en bjelkes krefter og deformsjon kn beskrives ved fire integrler som henger smmen : Skjærkrft : V d Vinkelendring : φ M d Moment : M V d Forskyvning
KANDIDATEN MÅ SELV KONTROLLERE AT OPPGAVESETTET ER FULLSTENDIG
 Høgskolen i Østfold Avdeling for ingeniør- og realfag EKSAMENSOPPGAVE Fag: IRK104 Grunnleggende kjemi Sensurfrist : tirsdag 23. september 28 Lærer : Birte J. Sjursnes Grupper : K3A Dato : 02.09.28 Tid
Høgskolen i Østfold Avdeling for ingeniør- og realfag EKSAMENSOPPGAVE Fag: IRK104 Grunnleggende kjemi Sensurfrist : tirsdag 23. september 28 Lærer : Birte J. Sjursnes Grupper : K3A Dato : 02.09.28 Tid
KJ1042 Grunnleggende termodynamikk med laboratorium. Eksamen vår 2012 Løsninger
 Side 1 av 10 KJ1042 Grunnleggende termodynamikk med laboratorium. Eksamen vår 2012 Løsninger Oppgave 1 a) Et forsøk kan gjennomføres som vist i figur 1. Røret er isolert, dvs. at det ikke tilføres varme
Side 1 av 10 KJ1042 Grunnleggende termodynamikk med laboratorium. Eksamen vår 2012 Løsninger Oppgave 1 a) Et forsøk kan gjennomføres som vist i figur 1. Røret er isolert, dvs. at det ikke tilføres varme
Naturfag 2, Na210R510
 Individuell skriftlig eksamen i Naturfag 2, Na210R510 10 studiepoeng ORDINÆR EKSAMEN 13. desember 2011 Sensur faller innen 05.01.2012 BOKMÅL. Resultatet blir tilgjengelig på studentweb første virkedag
Individuell skriftlig eksamen i Naturfag 2, Na210R510 10 studiepoeng ORDINÆR EKSAMEN 13. desember 2011 Sensur faller innen 05.01.2012 BOKMÅL. Resultatet blir tilgjengelig på studentweb første virkedag
1. UTTAKSPRØVE. til den. 41. Internasjonale Kjemiolympiaden 2009 i Cambridge, England
 Kjemi OL 1. UTTAKSPRØVE til den 41. Internasjonale Kjemiolympiaden 2009 i Cambridge, England Dag: En dag i ukene 42-44. Varighet: 90 minutter. Hjelpemidler: Lommeregner og Tabeller og formler i kjemi.
Kjemi OL 1. UTTAKSPRØVE til den 41. Internasjonale Kjemiolympiaden 2009 i Cambridge, England Dag: En dag i ukene 42-44. Varighet: 90 minutter. Hjelpemidler: Lommeregner og Tabeller og formler i kjemi.
1. UTTAKSPRØVE. til den 44. Internasjonale Kjemiolympiaden 2012. i Washington DC, USA. Oppgaveheftet skal leveres inn sammen med svararket
 Kjemi OL 1 UTTAKSPRØVE til den 44 Internasjonale Kjemiolympiaden 2012 i Washington DC, USA Dag: En dag i ukene 40-42 Varighet: 90 minutter Hjelpemidler: Lommeregner og Tabeller og formler i kjemi Maksimal
Kjemi OL 1 UTTAKSPRØVE til den 44 Internasjonale Kjemiolympiaden 2012 i Washington DC, USA Dag: En dag i ukene 40-42 Varighet: 90 minutter Hjelpemidler: Lommeregner og Tabeller og formler i kjemi Maksimal
Vann er en amfolytt, det kan både avgi og ta opp H +. I vann har vi derfor en. Denne egenprotolysen har et.
 Syrer o baser Det sentrale i en syre-base reaksjon er utvekslinen av H -atomer., o en syre-basereaksjon kan kalles en protolysereaksjon. Her er det vikti å huske på at H -atomer ikke alltid er det samme
Syrer o baser Det sentrale i en syre-base reaksjon er utvekslinen av H -atomer., o en syre-basereaksjon kan kalles en protolysereaksjon. Her er det vikti å huske på at H -atomer ikke alltid er det samme
LØSNINGSFORSLAG TIL EKSAMEN MAI 2007
 NTNU Noges teknisk-ntuvitenskpelige univesitet Fkultet fo ntuvitenskp og teknologi Institutt fo mteilteknologi TMT40 KJEMI LØSNINGSFORSLAG TIL EKSAMEN MAI 007 OPPGAVE ) - ph definees som den negtive logitmen
NTNU Noges teknisk-ntuvitenskpelige univesitet Fkultet fo ntuvitenskp og teknologi Institutt fo mteilteknologi TMT40 KJEMI LØSNINGSFORSLAG TIL EKSAMEN MAI 007 OPPGAVE ) - ph definees som den negtive logitmen
Studium/klasse: Masterutdanning i profesjonsretta naturfag. 8 (inkludert denne og vedlegg)
 Eksamensoppgave høsten 2010 Ordinær eksamen Bokmål Fag: Grunnleggende kjemi Eksamensdato: 7.desember 2010 Studium/klasse: Masterutdanning i profesjonsretta naturfag Emnekode: NAT400 Eksamensform: Skriftlig
Eksamensoppgave høsten 2010 Ordinær eksamen Bokmål Fag: Grunnleggende kjemi Eksamensdato: 7.desember 2010 Studium/klasse: Masterutdanning i profesjonsretta naturfag Emnekode: NAT400 Eksamensform: Skriftlig
EKSAMEN TMT4112 KJEMI
 Eksamen TMT4112, 18. desember-2012 Side 1 av 8 NTNU NORGES TEKNISK- VITENSKAPELIGE UNIVERSITET INSTITUTT FOR MATERIALTEKNOLOGI Faglig kontakt under eksamen: Kjell Wiik; Tel.: 73594082/Mob. tel.: 922 65
Eksamen TMT4112, 18. desember-2012 Side 1 av 8 NTNU NORGES TEKNISK- VITENSKAPELIGE UNIVERSITET INSTITUTT FOR MATERIALTEKNOLOGI Faglig kontakt under eksamen: Kjell Wiik; Tel.: 73594082/Mob. tel.: 922 65
Vår 2004 Ordinær eksamen
 år Ordinær eksmen. En bil kjører med en hstighet på 9 km/h lngs en rett strekning. Sjåføren tråkker plutselig på bremsene, men gjør dette med økende krft slik t (den negtive) kselersjonen (retrdsjonen)
år Ordinær eksmen. En bil kjører med en hstighet på 9 km/h lngs en rett strekning. Sjåføren tråkker plutselig på bremsene, men gjør dette med økende krft slik t (den negtive) kselersjonen (retrdsjonen)
Øving 9. Dersom ikke annet er oppgitt, antas det at systemet er i elektrostatisk likevekt.
 Institutt for fysikk, NTNU TFY4155/FY1003: Elektromgnetisme år 2009 Øving 9 eiledning: Mndg 09. og fredg 13. (evt 06.) mrs Innleveringsfrist: Fredg 13. mrs kl. 1200 (Svrtbell på siste side.) Opplysninger:
Institutt for fysikk, NTNU TFY4155/FY1003: Elektromgnetisme år 2009 Øving 9 eiledning: Mndg 09. og fredg 13. (evt 06.) mrs Innleveringsfrist: Fredg 13. mrs kl. 1200 (Svrtbell på siste side.) Opplysninger:
TALM1008 Fysikk og Kjemi Løsning kjemidel eksamen 19/5-14
 Program for Elektro og Datateknikk/ AFT TALM1008 Fysikk og jemi Løsning kjemidel eksamen 19/5-14 Oppgave 1 a) Det skal skrives navn på fem forbindelser : LiCl : Litiumklorid H 3PO 4 : Fosforsyre FeI 3
Program for Elektro og Datateknikk/ AFT TALM1008 Fysikk og jemi Løsning kjemidel eksamen 19/5-14 Oppgave 1 a) Det skal skrives navn på fem forbindelser : LiCl : Litiumklorid H 3PO 4 : Fosforsyre FeI 3
Kjemi 1. Figur s Figurer kapittel 8: Syrer og baser. gir andre farger enn syrer gir. ph < 7 ph > 7. Reagerer med uedelt metall og gir H 2 -gass
 Figur s. 42 Egenskaper hos syrer / sure løsninger Smaker surt Endrer farge på indikatorer og noen plantefarger Egenskaper hos baser / basiske løsninger Smaker bittert Endrer farge på indikatorer og noen
Figur s. 42 Egenskaper hos syrer / sure løsninger Smaker surt Endrer farge på indikatorer og noen plantefarger Egenskaper hos baser / basiske løsninger Smaker bittert Endrer farge på indikatorer og noen
LØSNINGSFORSLAG TIL ØVING NR. 5, Vår 2014
 NTNU Nrges teknisknturvitenskpelige universitet kultet nturvitenskp g teknlgi Institutt fr mterilteknlgi TMT1 JEMI LØSNINGSORSLAG TIL ØVING NR. 5, Vår 01 OPPGAVE 1 ) Vi kmbinerer den vnlige løselighetslikevekten
NTNU Nrges teknisknturvitenskpelige universitet kultet nturvitenskp g teknlgi Institutt fr mterilteknlgi TMT1 JEMI LØSNINGSORSLAG TIL ØVING NR. 5, Vår 01 OPPGAVE 1 ) Vi kmbinerer den vnlige løselighetslikevekten
EKSAMEN TMT4112 KJEMI
 Eksamen TMT4112, 18. desember-2012 Side 1 av 8 NTNU NORGES TEKNISK- VITENSKAPELIGE UNIVERSITET INSTITUTT FOR MATERIALTEKNOLOGI Faglig kontakt under eksamen: Kjell Wiik; Tel.: 73594082/Mob. tel.: 922 65
Eksamen TMT4112, 18. desember-2012 Side 1 av 8 NTNU NORGES TEKNISK- VITENSKAPELIGE UNIVERSITET INSTITUTT FOR MATERIALTEKNOLOGI Faglig kontakt under eksamen: Kjell Wiik; Tel.: 73594082/Mob. tel.: 922 65
Temahefte nr. 1. Hvordan du regner med hele tall
 1 ARBEIDSHEFTE I MATEMATIKK SNART MATTE EKSAMEN Hvordn du effektivt kn forberede deg til eksmen Temhefte nr. 1 Hvordn du regner med hele tll Av Mtthis Lorentzen mttegrisenforlg.com Opplysning: De nturlige
1 ARBEIDSHEFTE I MATEMATIKK SNART MATTE EKSAMEN Hvordn du effektivt kn forberede deg til eksmen Temhefte nr. 1 Hvordn du regner med hele tll Av Mtthis Lorentzen mttegrisenforlg.com Opplysning: De nturlige
Finalerunde Kjemiolympiaden 2002 Blindern 19. april 2002 Kl
 Finalerunde Kjemiolympiaden 2002 lindern 19. april 2002 Kl. 09.00-12.00 ppgavesettet består av 7 sider inkludert formel- og tabellark. ppgave 1 (10%) I hele denne oppgaven ser vi bort fra overspenning
Finalerunde Kjemiolympiaden 2002 lindern 19. april 2002 Kl. 09.00-12.00 ppgavesettet består av 7 sider inkludert formel- og tabellark. ppgave 1 (10%) I hele denne oppgaven ser vi bort fra overspenning
Løsningsforslag TFE4120 Elektromagnetisme 24. mai = 2πrlɛE(r) = Q innenfor S =
 Norges teknisk nturvitenskpelige universitet Institutt for elektronikk og telekommuniksjon Side 1 v 5 Løsningsforslg TFE4120 Elektromgnetisme 24. mi 2011 Oppgve 1 ) Av symmetrigrunner må det elektriske
Norges teknisk nturvitenskpelige universitet Institutt for elektronikk og telekommuniksjon Side 1 v 5 Løsningsforslg TFE4120 Elektromgnetisme 24. mi 2011 Oppgve 1 ) Av symmetrigrunner må det elektriske
KOSMOS. 5: Elektroner på vandring Figur side Modell av et heliumatom. Elektron. Nøytron. p + Proton. Protoner
 5: Elektroner på vandring Figur side 132 Elektron e p Nøytron n e Proton Modell av et heliumatom. Protoner Nøytroner Elektroner Nukleoner Elementærladning Elementærpartikler er små partikler i sentrum
5: Elektroner på vandring Figur side 132 Elektron e p Nøytron n e Proton Modell av et heliumatom. Protoner Nøytroner Elektroner Nukleoner Elementærladning Elementærpartikler er små partikler i sentrum
reduseres oksidasjon
 Redoksreaksjoner En redoksreaksjon er en reaksjon der ett eller flere elektroner overføres fra en forbindelse til en annen. En reduksjon er en prosess hvor en forbindelse mottar ett eller flere elektroner.
Redoksreaksjoner En redoksreaksjon er en reaksjon der ett eller flere elektroner overføres fra en forbindelse til en annen. En reduksjon er en prosess hvor en forbindelse mottar ett eller flere elektroner.
2. Hva er formelen for den ioniske forbindelsen som dannes av kalsiumioner og nitrationer?
 Side 1 av 6 Del 1 (50 p). Flervalgsoppgaver. Hvert riktig svar med riktig forklaring gir 2.5 poeng. Riktig svar uten forklaring eller med feil forklaring gir 1.5 poeng. Feil svar (med eller uten forklaring)
Side 1 av 6 Del 1 (50 p). Flervalgsoppgaver. Hvert riktig svar med riktig forklaring gir 2.5 poeng. Riktig svar uten forklaring eller med feil forklaring gir 1.5 poeng. Feil svar (med eller uten forklaring)
Løsningsforslag til øving 4
 1 Oppgve 1 FY1005/TFY4165 Termisk fysikk Institutt for fysikk, NTNU åren 2015 Løsningsforslg til øving 4 For entomig gss hr vi c pm = 5R/2 og c m = 3R/2, slik t γ = C p /C = 5/3 Lngs dibten er det (pr
1 Oppgve 1 FY1005/TFY4165 Termisk fysikk Institutt for fysikk, NTNU åren 2015 Løsningsforslg til øving 4 For entomig gss hr vi c pm = 5R/2 og c m = 3R/2, slik t γ = C p /C = 5/3 Lngs dibten er det (pr
Sammendrag, forelesning onsdag 17/ Likevektsbetingelser og massevirkningsloven
 Sammendrag, forelesning onsdag 17/10 01 Kjemisk likevekt og minimumspunkt for G Reaksjonsligningen for en kjemisk reaksjon kan generelt skrives: ν 1 X 1 + ν X +... ν 3 X 3 + ν 4 X 4 +... 1) Utgangsstoffer
Sammendrag, forelesning onsdag 17/10 01 Kjemisk likevekt og minimumspunkt for G Reaksjonsligningen for en kjemisk reaksjon kan generelt skrives: ν 1 X 1 + ν X +... ν 3 X 3 + ν 4 X 4 +... 1) Utgangsstoffer
Auditorieoppgave nr. 1 Svar 45 minutter
 Auditorieoppgave nr. 1 Svar 45 minutter 1 Hvilken ladning har et proton? +1 2 Hvor mange protoner inneholder element nr. 11 Natrium? 11 3 En isotop inneholder 17 protoner og 18 nøytroner. Hva er massetallet?
Auditorieoppgave nr. 1 Svar 45 minutter 1 Hvilken ladning har et proton? +1 2 Hvor mange protoner inneholder element nr. 11 Natrium? 11 3 En isotop inneholder 17 protoner og 18 nøytroner. Hva er massetallet?
FLERVALGSOPPGAVER ATOMER og PERIODESYSTEMET
 FLERVALGSOPPGAVER ATOMER og PERIODESYSTEMET Hjelpemidler: Periodesystem Atomer 1 Hvilket metall er mest reaktivt? A) sølv B) bly C) jern D) cesium Atomer 2 Hvilket grunnstoff høyest 1. ioniseringsenergi?
FLERVALGSOPPGAVER ATOMER og PERIODESYSTEMET Hjelpemidler: Periodesystem Atomer 1 Hvilket metall er mest reaktivt? A) sølv B) bly C) jern D) cesium Atomer 2 Hvilket grunnstoff høyest 1. ioniseringsenergi?
Løsningsforslag, Midtsemesterprøve fredag 13. mars 2009 kl Oppgavene med kort løsningsforslag (Versjon A)
 Institutt for fysikk, NTNU FY100 Elektrisitet og mgnetisme TFY4155 Elektromgnetisme Vår 2009 Løsningsforslg, Midtsemesterprøve fredg 1. mrs 2009 kl 1415 1615. Fsit side 10. Oppgvene med kort løsningsforslg
Institutt for fysikk, NTNU FY100 Elektrisitet og mgnetisme TFY4155 Elektromgnetisme Vår 2009 Løsningsforslg, Midtsemesterprøve fredg 1. mrs 2009 kl 1415 1615. Fsit side 10. Oppgvene med kort løsningsforslg
Løsningsforslag Kollokvium 1
 Løsningsforslg Kollokvium 1 30. jnur 015 Her finner dere et løsningsforslg for oppgvene som ble diskutert på Kollokvium 1. Oppgve 1 Regning med enheter ) Energienheten 1 ev (elektronvolt) er definert som
Løsningsforslg Kollokvium 1 30. jnur 015 Her finner dere et løsningsforslg for oppgvene som ble diskutert på Kollokvium 1. Oppgve 1 Regning med enheter ) Energienheten 1 ev (elektronvolt) er definert som
Løsningsforslag, Midtsemesterprøve torsdag 6. mars 2008 kl Oppgavene med kort løsningsskisse
 Institutt for fysikk, NTNU FY1003 Elektrisitet og mgnetisme TFY4155 Elektromgnetisme Vår 2008 Løsningsforslg, Midtsemesterprøve torsdg 6. mrs 2008 kl 1000 1200. Fsit side 12. Oppgvene med kort løsningsskisse
Institutt for fysikk, NTNU FY1003 Elektrisitet og mgnetisme TFY4155 Elektromgnetisme Vår 2008 Løsningsforslg, Midtsemesterprøve torsdg 6. mrs 2008 kl 1000 1200. Fsit side 12. Oppgvene med kort løsningsskisse
FLERVALGSOPPGAVER SYRER OG BASER
 FLERVALGSOPPGAVER SYRER OG BASER Hjelpemidler: Periodesystem og kalkulator Hvert spørsmål har et riktig svaralternativ. Når ikke noe annet er oppgitt kan du anta STP (standard trykk og temperatur). Syrer
FLERVALGSOPPGAVER SYRER OG BASER Hjelpemidler: Periodesystem og kalkulator Hvert spørsmål har et riktig svaralternativ. Når ikke noe annet er oppgitt kan du anta STP (standard trykk og temperatur). Syrer
KJEMIOLYMPIADEN 2000 2. UTTAKINGSPRØVE.
 KJEMIOLYMPIADEN 2000 2. UTTAKINGSPRØVE. Dato: 17. februar 2000 Varighet: 180 minutter (3 timer) Tillatte hjelpemidler: Kalkulator og Tabeller i kjemi 1998 fra RVO/Gyldendal OBS! Du klarer antakelig ikke
KJEMIOLYMPIADEN 2000 2. UTTAKINGSPRØVE. Dato: 17. februar 2000 Varighet: 180 minutter (3 timer) Tillatte hjelpemidler: Kalkulator og Tabeller i kjemi 1998 fra RVO/Gyldendal OBS! Du klarer antakelig ikke
TFY4104 Fysikk. Institutt for fysikk, NTNU. Høsten Løsningsforslag til øving 8. a = e m E
 TFY414 Fysikk. Institutt for fysikk, NTNU. Høsten 16. Løsningsforslg til øving 8. Oppgve 1. ) C F = E = m Newtons. lov. Her er = e, så elektronets kselersjon blir = e m E ltså mot venstre. b) C Totlt elektrisk
TFY414 Fysikk. Institutt for fysikk, NTNU. Høsten 16. Løsningsforslg til øving 8. Oppgve 1. ) C F = E = m Newtons. lov. Her er = e, så elektronets kselersjon blir = e m E ltså mot venstre. b) C Totlt elektrisk
Øving 13, løsningsskisse.
 TFY455/FY3 Elektr & mgnetisme Øving 3, løsningsskisse nduksjon Forskyvningsstrøm Vekselstrømskretser nst for fysikk 5 Oppgve nduktns for koksilkbel ) Med strømmen jmt fordelt over tverrsnittet på lederne
TFY455/FY3 Elektr & mgnetisme Øving 3, løsningsskisse nduksjon Forskyvningsstrøm Vekselstrømskretser nst for fysikk 5 Oppgve nduktns for koksilkbel ) Med strømmen jmt fordelt over tverrsnittet på lederne
