Refusjonsrapport Aromasin (eksemestan), adjuvant behandling av brystkreft
|
|
|
- Daniel Jacobsen
- 8 år siden
- Visninger:
Transkript
1 Refusjonsrapport Aromasin (eksemestan), adjuvant behandling av brystkreft 1 Oppsummering Formål: Å vurdere Aromasin (eksemestan) for pliktmessig refusjon etter forskrift av 18. april 1997 nr. 330 om stønad til dekning av utgifter til viktige legemidler og spesielt medisinsk utstyr (blåreseptforskriften) 9 pkt. Indikasjon det er søkt refusjon for: Adjuvant behandling av postmenopausale kvinner med østrogenreseptor-positiv, invasiv brystkreft, etter tidligere 2-3 års adjuvant tamoksifen behandling. Bakgrunn: Brystkreft er en ondartet svulst som oppstår i brystet. Det finnes flere typer, men de fleste utgår fra brystkjertlene. Biologisk er brystkreft karakterisert ved svært varierende sykdomsforløp. I den ene enden av skalaen finnes rasktvoksende svulster med tidlig spredning, mens det i den andre enden av skalaen finnes langsomtvoksende svulster som forblir lokale i brystkjertelen. Brystkreft er den hyppigste kreftform hos kvinner i Norge, og utgjør om lag 23 % av alle krefttilfeller hos kvinner. Hvert år diagnostiseres mer enn 2700 nye tilfeller, og antallet nye tilfeller (insidens) er jevnt økende. Målsettingen med behandlingen er å etablere kontroll over brystkreftsykdommen og bedre muligheten for helbredelse. I dette ligger intensjonen om å forhindre plager av lokal svulst, forebygge tilbakefall av lokal svulst og forhindre videre spredning. Den viktigste behandling ved brystkreft er kirurgi og eventuelt strålebehandling. Kirurgi er fortsatt hovedmetoden for å oppnå kontroll over kreftsvulst i bryst og armhule. Selv om leveutsiktene ved brystkreft er bedret gjennom de siste tiår, vil en relativt stor andel av pasientene måtte påregne tilbakefall av sykdommen. På grunn av gunstige effekter av tilleggsbehandling (adjuvant) med kjemoterapi og hormonell (endokrin) behandling, får brystkreftpasientene i dag tilbud om slik behandling i en eller annen form. Flere nyere kliniske studier viser at adjuvant behandling med aromatasehemmere gir en noe bedre effekt på sykdomsfri overlevelse av brystkreft etter operasjon enn tamoksifen. Eksemestan er en aromatasehemmer som har anti-tumoreffekt ved at østrogennivåene i brystvevet nedsettes gjennom å hemme enzymet som danner østrogener. Østrogenreduksjon via hemming av aromatase er en effektiv og selektiv behandling mot hormonavhengig brystkreft hos postmenopausale kvinner. Hos postmenopausale brystkreftpasienter har en daglig dose på 25 mg eksemestan redusert østrogennivåene med ca 98 % Brev stiles til Statens legemiddelverk. Vennligst oppgi vår referanse. Statens legemiddelverk Tlf.: Kto Besøksadr.: Sven Oftedals vei 8, 0950 Oslo Fax: post@legemiddelverket.no Org.nr Varelev.: Sven Oftedals vei 6, 0950 Oslo
2 2/25 Resultat: Effekten av eksemestan ble undersøkt i IES (Intergroup Exemestan Study) studien som er en randomisert, multisenter, dobbeltblind studie. I studien inngikk 4724 postmenopausale kvinner med brystkreft med positiv eller ukjent østrogen-reseptorstatus som hadde vært sykdomsfrie etter å ha fått adjuvant tamoksifen terapi i 2 til 3 år, randomisert til å motta 3 til 2 år med eksemestan eller tamoksifen for å fullføre totalt 5 år med hormonbehandling. Etter 30,6 måneder median oppfølging viste resultatene at behandling med eksemestan ga bedre effekt (hazard ratio 0,68 95 % KI 0,56-82 p<0,001) enn tamoksifen på det primære endepunktet sykdomsfri overlevelse (DSF). Søker har benyttet en kostnad-effekt analyse for å vise at behandling med eksemestan er kostnadseffektivt sammenlignet med tamoksifen. Kostnadseffektivitetsanalysen er basert på en Markovmodell. Resultatene indikerer at behandling med eksemestan synes å gi en mer-effekt i form av at gjennomsnittspasienten får hhv. lengre sykdomsfri overlevelse og flere levemåneder/år. Selv om eksemestan koster 10 ganger mer enn tamoksifen, gir modellen resultater som vanligvis regnes som kostnadseffektive. Dette skyldes de helsemessige gevinstene som medfører at annen dyr kreftbehandling kan reduseres.
3 3/25 Vedtak: Etter en samlet vurdering mener Statens legemiddelverk at det er en sannsynligshetsovervekt for at behandling med eksemestan er kostnadseffektiv som adjuvant behandling av kvinner med østrogenreseptorpositiv brystkreft. Statens legemiddelverk vedtar at Aromasin (eksemestan) innvilges refusjon etter 9 punkt 9, bokstav a) for indikasjonen behandling av: Adjuvant behandling av postmenopausale kvinner med østrogenreseptor-positiv, invasiv brystkreft, etter tidligere 2-3 års adjuvant tamoksifen behandling. Med følgende refusjonsvilkår: - Refusjonen er indikasjonsspesifikk og refusjon omfatter kun behandling av: Adjuvant behandling av postmenopausale kvinner med østrogenreseptor-positiv, invasiv brystkreft, etter tidligere 2-3 års adjuvant tamoksifen behandling. Og forbehold: - Vedtaket er tidsbegrenset frem til og med Innen skal refusjonssøker sende inn en ny helseøkonomisk analyse av eksemestan. Statens legemiddelverk vil da foreta en revurdering av refusjonsstatus for Aromasin (eksemestan). Vedtaket er betinget i den forstand at det kan revurderes og endres dersom det tilkommer nye forhold som endrer grunnlaget eller premissene for refusjonsvedtaket.
4 4/25 Innholdsfortegnelse 1 OPPSUMMERING... 1 INNHOLDSFORTEGNELSE SØKNADSLOGG INTRODUKSJON/BAKGRUNN EKSISTERENDE BEHANDLINGSMULIGHETER Kirurgi og strålebehandling Adjuvant systemisk behandling BEHANDLING MED AROMASIN (EKSEMESTAN) EN LEGEMIDDELØKONOMISK ANALYSE AV EKSEMESTAN DISKUSJON KONKLUSJON REFERANSER... 24
5 5/25 2 Søknadslogg Refusjonssøker: Preparat: Virkestoff: Indikasjon det er søkt refusjon for: Pfizer A/S. Aromasin Eksemestan Adjuvant behandling av postmenopausale kvinner med østrogenreseptor-positiv, invasiv brystkreft, etter tidligere 2-3 års adjuvant tamoksifenbehandling. ATC-nr: L02B G06 Søknadsprosess: Søknad mottatt Statens legemiddelverk: Saksbehandling startet Vedtak fattet: Saksbehandlingstid: 174 dager Dokumentasjonsgrunnlaget for aromatasehemmere (generelt) som adjuvant behandling av kvinner med brystkreft, har vært diskutert i Blåreseptnemnda våren Introduksjon/Bakgrunn 3.1 Brystkreft Brystkreft er en ondartet svulst som oppstår i brystet. Det finnes flere typer, men de fleste utgår fra brystkjertlene. Biologisk er brystkreft karakterisert ved svært varierende sykdomsforløp. I den ene enden av skalaen finnes rasktvoksende svulster med tidlig spredning, mens det i den andre enden av skalaen finnes langsomtvoksende svulster som forblir lokale i brystkjertelen. Personer med forhøyet risiko for å få brystkreft (arvelig) tilbys en adekvat oppfølging for å kunne stille diagnosen brystkreft så tidlig som mulig. Tidlig diagnose er, tross store forskjeller i biologi, den viktigste faktor for å bedre prognosen for pasienter med brystkreft. Dette er vist i flere screeningundersøkelser. Utvikling av brystkreft deles ofte inn i fire stadier, og leveutsiktene avhenger av hvilket stadium kreften er i når den oppdages. For brystkreft i 1. og 2. stadium er utsiktene gode, fordi kreftsvulsten er begrenset til brystkjertelen (stadium 1) og nærliggende lymfekjertler (stadium 2). Andelen kvinner som får stillet diagnosen i tidlig stadium er økende. I 1995 hadde mer enn 60 % av kvinnene ved diagnosetidspunktet påvisbar kreft kun i selve brystet (stadium 1). Mammografiscreening er sannsynligvis forklaringen på dette. Den observerte økningen i antall nye tilfeller av brystkreft i de senere årene utgjøres hovedsakelig av kvinner med brystkreft i stadium 1.
6 6/25 % Figur 1: Stadiumfordeling- Brystkreft i Norge 1995 Stadium 1 Stadium 2 Stadium 3 Stadium 4 Stadium 1: Påvisbar liten svulst i brystet Stadium 2: Svulst begrenset til bryst og nærliggende lymfeknuter Stadium 3: Svulsten er mer omfangsrik. Stadium 4: Spredning til andre organer Kilde Blåboka Norsk Bryst Cancer Gruppe 5 Forekomst Brystkreft er den hyppigste kreftform hos kvinner i Norge og utgjør om lag 23 % av alle krefttilfeller hos kvinner 1. Beregninger viser at hver 11. kvinne vil utvikle brystkreft. Hvert år diagnostiseres mer enn 2700 nye tilfeller, og antallet nye tilfeller (insidens) er jevnt økende 2 (se figur 2). Rundt kvinner i Norge lever i dag med diagnosen brystkreft, og det er først og fremst kvinner over 50 år som rammes. Trolig utgjør denne gruppen ca 80 % av alle brystkrefttilfellene. Majoriteten av kvinnene har brystkreft begrenset til bryst og nærliggende områder, det vil si stadium 1 og stadium 2 (se figur 1). Dødeligheten av brystkreft utgjør ca 700 tilfeller per år 3.
7 7/ Forekomst av brystkreft blant kvinner i Norge Figur 2: Forekomst av brystkreft blant kvinner i Norge Rater per kvinneår Alder ved diagnose Kilde Kreftregisteret 2006 RS Jan06 Etiologi Det er ingen sikker kunnskap om årsakene til kreftsykdommen, men risiko synes å være knyttet til arv, hormonelle og sosioøkonomiske forhold, høyde og vekt. Av kvinner som rammes av denne kreftformen, regner en i dag med at fem til ti prosent av tilfellene skyldes arv. Hormonelle forhold som tidlig menstruasjon, sen førstegangsfødsel, barnløshet og sen overgangsalder øker også risikoen for brystkreft. 3.2 Eksisterende behandlingsmuligheter Kirurgi og strålebehandling Målsettingen med behandlingen er å etablere kontroll over brystkreftsykdommen og bedre muligheten for helbredelse. I dette ligger intensjonen om å forhindre plager av lokal svulst, forebygge tilbakefall av lokal svulst og forhindre videre spredning. Den viktigste behandling ved brystkreft er kirurgi og eventuelt strålebehandling. Kirurgi er fortsatt hovedmetoden for å oppnå kontroll over kreftsvulst i bryst og armhule. Strålebehandling kan gis både før og etter operasjon, eller som eneste form for lokal behandling. Postoperativ strålebehandling er mest brukt og kan redusere antall tilbakefall og øke overlevelsen ved brystkreft i stadium 2.
8 8/ Adjuvant systemisk behandling Selv om leveutsiktene ved brystkreft er bedret gjennom de siste tiår, vil en relativt stor andel av pasientene måtte påregne tilbakefall av sykdommen. Innen 10 år etter diagnostisering/behandling vil ca 25 % av pasienter i stadium 1 og % av pasientene i stadium 2 oppleve tilbakefall. På grunn av gunstige effekter av tilleggsbehandling (adjuvant) med kjemoterapi og hormonell (endokrin) behandling får brystkreftpasientene i dag tilbud om slik behandling i en eller annen form. Flere nyere kliniske studier viser at adjuvant behandling med aromatasehemmere gir en noe bedre effekt på sykdomsfri overlevelse av brystkreft etter operasjon enn tamoksifen Hormonbehandling Brystkjertelvevets vekst og funksjon er avhengig av et komplekst samspill mellom mange hormoner. Denne følsomheten for hormoner vil et svulstvev beholde i varierende grad. Derfor vil et sentralt terapeutisk angrepspunkt ved brystkreft være behandling som på forskjellige måter hindrer eksempelvis østrogenets stimulerende virkning på brystkreftceller. I behandling av hormonfølsom brystkreft hos postmenopausale kvinner er følgelig hormonbehandling blitt et naturlig valg. Antiøstrogen Tamoksifen har i mer enn 30 år vært gullstandarden i endokrin adjuvant behandling av postmenopausale kvinner med østrogenreseptorpositiv (ER+) brystkreft. Inntil nylig har 5 år med post-operativ tamoksifenbehandling hos kvinner med ER+ brystkreft vært standard behandling. Adjuvant behandling med tamoksifen har i studier vist at risikoen for tilbakefall, inkludert kontralateral brystkreft (kreft i det andre brystet), er redusert med 47 %, og risiko for død med 26 % 7. På tross av de gunstige effektene av adjuvant tamoksifenbehandling, opplever mange pasienter tilbakefall, alvorlige bivirkninger som dyp venetrombose og endometrie cancer 8. Et annet problem med tamoksifen kan være utvikling av resistens mot legemidlet. Flere nyere kliniske studier viser at adjuvant behandling med tredjegenerasjons aromatasehemmere gir en noe bedre effekt på sykdomsfri overlevelse av brystkreft etter operasjon enn tamoksifen Aromatasehemmere Aromatasehemmere har anti-tumoreffekt ved at østrogennivåene i brystvevet nedsettes gjennom å hemme enzymet som danner østrogener. Aromatasehemmere kan inndeles i to hovedgrupper: De såkalte ikke-steroide reversible hemmerne som anastrozol og letrozol, og de irreversible aromataseinaktivatorene som eksemestan. Aromatasehemmere virker kun på østrogensyntesen hos postmenopausale kvinner og hos menn, og har liten effekt på østrogenspeilet til premenopausale kvinner. Dette skyldes trolig at den hemmende effekten blir kompentsert av andre fysiologiske mekanismer. Følgelig skal aromatasehemmere kun brukes av postmenopausale kvinner og eventuelt av menn.
9 9/25 Progesteroner De mest brukte progesteronene er megestrol acetat og medroksyprogesteron. På grunn av høy forekomst av bivirkninger ved bruk av disse legemidlene blir progesteroner lite benyttet og da kun ved terapisvikt som tredje/fjerde-linjebehandling. Aktuelle kandidater for adjuvant behandling med aromatasehemmere Adjuvant behandling av brystkreft med aromatasehemmere er indisert for bruk hos postmenopasusale kvinner som har en hormonfølsom krefttype. Dette utgjør ca 64 % av alle pasienter med brystkreft. Av disse vil om lag 75 % ha brystkreft i stadium 1 eller stadium 2, og det forventes at de fleste vil få tilbud om endokrin behandling etter operasjon for å redusere risikoen for tilbakefall. Behandlingsregime, inkludert behandling med aromatasehemmere, vil variere på bakgrunn av blant annet prognose. Gitt tall fra kreftregisteret vil det til enhver tid utgjøre ca 6000 pasienter. Refusjonssøker har anslått at om lag 700 pasienter årlig vil starte med eksemestanbehandling for den aktuelle indikasjonen. Gitt 6000 aktuelle kandidater for behandling med aromatasehemmere og like markedsandeler for de ulike aromatasehemmerne, anslår Legemiddelverket det derfor å være ca 2000 pasienter som vil få adjuvant behandling med eksemestan. 4 Behandling med Aromasin (eksemestan) 4.1 Innledning Brystkreft er den vanligste kreftformen hos kvinner, og hver 11. kvinne vil i løpet av livet utvikle sykdommen. En økende populasjon av eldre kvinner kan føre til en stigende forekomst av postmenopausal brystkreft. Indikasjon Aromasin (eksemestan) er indisert for - Adjuvant behandling av postmenopausale kvinner med østrogenreseptor-positiv, invasiv brystkreft, etter tidligere 2-3 års adjuvant tamoksifenbehandling. - Behandling av avansert brystkreft hos kvinner med naturlig eller kunstig indusert postmenopausal status med progresjon av sykdommen etter tidligere behandling med antiøstrogener. Effekt er ikke vist hos pasienter med negativ østrogen-reseptor status. Indikasjonen det søkes refusjon for er uthevet i kursiv, øvrig indikasjon er tidligere innvilget refusjon. I denne rapporten omtales kun adjuvant behandling med eksemestan. Virkningsmekanisme Eksemestan er en sterioid aromatase-inaktivator som binder seg irreversibelt til aromataseenzymet slik at muligheten for å lage østrogen ødelegges. Hos postmenopausale kvinner produseres østrogenene primært ved omdannelse av androgener til østrogener ved hjelp av aromatase-enzymet i perifere vev. Østrogenreduksjon via hemming av aromatase er en effektiv og selektiv behandling av hormonavhengig brystkreft hos postmenopausale kvinner.
10 10/25 Hos postmenopausale brystkreftpasienter har en daglig dose på 25 mg eksemestan redusert østrogennivåene med ca 98 % 9. Effekt har ikke blitt påvist hos pasienter med negativ østrogen-reseptorstatus. 4.2 Effektstudier, design og resultater Design I IES (Intergroup Exemestan Study) 6, som er en randomisert, multisenter, dobbeltblind studie, ble effekten av eksemestan undersøkt. I studien inngikk 4724 postmenopausale kvinner med brystkreft med positiv eller ukjent østrogen-reseptorstatus som hadde vært sykdomsfrie etter å ha fått adjuvant tamoksifen terapi i 2 til 3 år, randomisert til å motta 3 til 2 år med eksemestan eller tamoksifen for å fullføre totalt 5 år med hormonbehandling. Figur 3: Studiedesign IES-studien Tamoksifen 2,5 år Eksemestan 2,5 år Tamoksifen i 5 år Endepunkt Det primære endepunkt var sykdomsfri overlevelse (disease-free survival), definert som tid fra randomisering til tilbakefall/nydiagnostisering av brystkreft uavhengig av lokalisasjon eller død uavhengig av årsak. Sekundære endepunkter inkluderte blant annet totaldødelighet og forekomst av kontralateral brystkreft. Resultater Etter 30,6 måneder median oppfølging viste resultatene at behandling med eksemestan ga bedre effekt (hazard ratio 0,68,95 % KI 0,56-0,82 p<0,001) enn tamoksifen på det primære endepunktet sykdomsfri overlevelse (DSF). Oppfølgingstiden fører til en relativ gevinst i sykdomsfri overlevelse på 32 % (4,7 % absolutt forskjell), og var uavhengig av lymfeknutestatus eller tidligere kjemoterapi. Eksemestan reduserte også signifikant risikoen for kontralateral brystkreft (hazard ratio 0,32, p=0,0034). Analysen viste at generell overlevelse ikke var signifikant forskjellig i de to gruppene, med 116 døde i eksemestangruppen og 137 i tamoksifengruppen (hazard ratio 0,86, p=0,23). På grunn for kort observasjonstid er det per i dag ikke mulig å konkludere med at forskjellen i sykdomsfri overlevelse kan overføres til fordel i total overlevelse for eksemestan.
11 11/25 Tabell 1: Resultater fra IES studien intention to treat populasjonen Endepunkt Eksemestan Tamoksifen Hazard Ratio (95% konfidensin- Populasjon H endelser /N (%) H endelser /N (%) tervall) p-verdi* Sykdomsfri overlevelse a Alle pasienter 213 /2352 (9,1%) 306 /2372 (12,9%) 0,69 (0,58-0,82) 0,00003 ER+ pasienter 164 /2008 (8,2%) 248 /2011 (12,3%) 0,65 (0,53-0,79) 0,00001 Kontralateral brystkreft Alle pasienter 8 /2352 (0,3%) 25 /2372 (1,1%) 0,32 (0,15-0,72) 0,00340 ER+ pasienter 5 /2008 (0,3%) 23 /2011 (1,1%) 0,22 (0,08-0,57) 0,00069 Brystkreftfri overlevelse b Alle pasienter 171 /2352 (7,3%) 262 /2372 (11,0%) 0,65 (0,54-0,79) <0,00001 ER+ pasienter 128 /2008 (6,4%) 215 /2011 (10,7%) 0,58 (0,47-0,73) <0,00001 Overlevelse uten fjernmetastase c Alle pasienter 142 /2352 (6,0%) 204 /2372 (8,6%) 0,70 (0,56-0,86) 0,00083 ER+ pasienter 107 /2008 (5,3%) 163 /2011 (8,1%) 0,65 (0,51-0,83) 0,00048 Total overlevelse d Alle pasienter 116 /2352 (4,9%) 137 /2372 (5,8%) 0,86 (0,67-1,10) 0,22962 ER+ pasienter 90 /2008 (4,5%) 104 /2011 (5,2%) 0,87 (0,66-1,16) 0,33671 * Log-rank test; ER+ pasienter = østrogenreseptor positive pasienter. a Sykdomsfri overlevelse er definert som første forekomst av lokal- eller fjernmetastaser, kontralateral brystkreft, eller død uansett grunn. b Brystkreftfri overlevelse er definert som første forekomst av lokal- eller fjernmetastaser, kontralateral brystkreft eller brystkreftdød. c Overlevelse uten fjernmetastase er definert som første fjernmetastase eller brystkreftdød. d Total overlevelse er definert som død uavhengig av grunn. 4.3 Dosering Anbefalt dose er én tablett (25 mg) én gang daglig inntil progresjon. I henhold til indikasjonen skal behandling med eksemestan av pasienter med tidlig brystkreft, vedvare i totalt fem år med kombinert sekvensiell adjuvant hormonterapi (tamoksifen etterfulgt av eksemestan), eller frem til tilbakefall oppstår. Definert døgndose for eksemestan er fastsatt av WHO til å være 25 mg. Dette tilsvarer én tab- daglige dosen den enkelte pasient tar ikke avvike vesentlig fra DDD. Salget i DDD av ekse- lett daglig. Den definerte døgndose (DDD) må generelt betraktes som en teknisk verdi som ligger nær opp til et gjennomsnitt av de dosene som benyttes. Dette kan innebære at DDD ikke nødvendigvis er den mest forskrevne eller brukte dose. Når det gjelder bruk av eksemestan som adjuvant behandling av postmenopausale kvinner med brystkreft, vil trolig den mestan har økt vesentlig fra 2004 til Trolig skyldes dette at preparatet i 2005 fikk indkasjonsutvidelse som omfatter adjuvant behandling (tidligere bare avansert brystkreft), samt at spesialistmiljøet innen diagnostikk og behandling av brystkreft i Norge, NBCG (Norsk Bryst Cancer Gruppe) endret sine retningslinjer for adjuvant behandling 1.
12 12/ Bivirkninger Eksemestan var generelt godt tolerert i alle kliniske studier; bivirkningene var vanligvis milde til moderate 9. Det var 6,3 % av pasientene som ble behandlet med eksemestan som avbrøt behandlingen på grunn av bivirninger. Hos pasienter med tidlig brystkreft var de mest vanlige rapporterte bivirkningene hetetokter (22%), leddsmerter (17%) og tretthet (17%). De fleste bivirkningene kan knyttes til den normale farmakologiske konsekvensen av tap av østrogen, som eksempelvis hetetokter. Hjerte-karbivirkninger Da østrogen generelt påvirker en rekke fysiologiske prosesser, kan man ikke utelukke uønskede effekter når østrogensyntesen hemmes. I enkelte studier av aromatasehemmere 6 10 er det blant annet vist tegn til oversykelighet av hjerte-karsykdommer. Behandling med aromatasehemmere over tid kan medføre at lipidprofilen endres i uønsket retning. Geisler og Lønning har i en oversiktsartikkel 11 gjennomgått flere studier av behandling med både tamoksifen og ulike aromatasehemmere med hensyn på hjerte-karsykdom. Deres konklusjon er at man i dag ikke vet om det er noen forskjell i økt risiko mellom behandling med tamoksifen eller aromatasehemmere. Bentetthet Behandling med aromatasehemmere kan over tid gi akselerert osteoporose. Årsaken til dette er at lave østrogennivåer er assosiert med tap av bentetthet. Følgelig vil lang tid med østrogensuppresjon kunne føre til lavere benmasse. I motsetning til aromatasehemmernes mulige negative effekt på bentetthet, har behandling med tamoksifen en beskyttende effekt mot osteoporose. I de kliniske studiene ATAC 4, IES 6 og MA-17 5 der adjuvant behandling med aromatasehemmere er undersøkt, er det i samtlige studier registrert økt forekomst av brudd, men resultatene var kun signifikant i ATAC. Lønning påpeker i en oversiktsartikkel 12 at det er et problem at pasientene i kontrollarmene i ATAC og IES studiene fikk kontinuerlig behandling med tamoksifen, hvilket sannsynligvis har bidratt til redusert frakturforekomst. Trolig gir også de ulike aromatasehemmerne forskjellig grad av risiko for benbrudd og tap av bentetthet da de har forskjellig struktur. McCloskey har forsøkt å redegjøre for dette i en oversiktsartikkel 13, men mener det er for tidlig å trekke konklusjoner om hvorvidt dette er et problem som har klinisk betydning da fenomenet foreløpig er lite studert. I en liten studie av Lønning og medarbeidere 14 er effekten av eksemestan på bentetthet blant postmenopausale kvinner med tidlig brystkreft undersøkt. Resultatene tilsier at eksemestan i liten grad øker bentapet, men de anbefaler likevel at bentettheten bør følges under behandling med aromatasehemmer. På bakgrunn av blant annet denne studien anbefaler Norsk Bryst Cancer Gruppe at bentettheten skal måles før behandling med aromatasehemmer startes. Dette gjentas etter 1 år og deretter hvert annet år. Videre anbefaler de i sine retningslinjer at alle pasienter som behandles adjuvant med aromatasehemmere bør få et daglig tilskudd av vitamin D og kalsium 1.
13 13/ Interaksjoner Eksemestan bør brukes med forsiktighet sammen med legemidler som metaboliseres via CYP 3A4 og har smal terapeutisk indeks. Det finnes ikke klinisk erfaring fra samtidig bruk av eksemestan og andre legemidler til behandling av kreft. Eksemestan skal ikke gis sammen med legemidler som inneholder østrogen, da disse vil motvirke den farmakologiske effekten. 5 En legemiddeløkonomisk analyse av eksemestan 5.1 Refusjonssøknadens modell- og metodeapparat Søker har benyttet en kostnad-effekt analyse for å vise at behandling med eksemestan er kostnadseffektivt sammenlignet med tamoksifen. Kostnadseffektivitetsanalysen er basert på en Markovmodell. Markovmodellens pasientpopulasjon er kvinner med behandlet operabel brystkreft etterfulgt av 2-3 års adjuvant tamoksifenbehandling. Pasientpopulasjonen tilsvarer pasientene i IESstudien 6. Etter 2-3 års adjuvant tamoksifenbehandling blir pasientene enten byttet til eksemestan i de resterende 2-3 årene, eller fortsetter på tamoksifen. Begge pasientgruppene fullfører totalt 5 år med adjuvant behandling. Modellen kjøres i 6 måneders sykluser til alle pasientene er døde. Ved slutten av hver syklus befinner pasientene seg i en av 10 Markovtilstander. Hver Markovtilstand er assosiert med bestemte kostnader og helseeffekter. Når modellen kjøres blir disse registrert og summert fortløpende for alle pasientene. Endringer i pasientenes tilstand skjer ved eventuelle endringer i tilbakefall eller død. Pasienter som opplever et tilbakefall er ekskludert fra risiko for nye tilbakefall. Modellen begrenser seg til kun å ta hensyn til en type tilbakefall per pasient. Etter at type tilbakefall eller død er bestemt, har alle pasienter som fortsatt er i live én gitt sannsynlighet for å utvikle osteoporose. Pasienter som utvikler osteoporose vil ha sykdommen resten av livet. En overgang fra en tilstand med osteoporose til en tilstand uten osteoporose er ikke mulig i modellen. Ved slutten av hver syklus befinner pasientene seg i en av følgende Markovtilstander: No recurrence, No osteoporosis Local recurrence, No osteoporosis Distant recurrence, No osteoporosis Contralateral breast cancer, No osteoporosis No recurrence, osteoporosis Local recurrence, osteoporosis Distant recurrence, osteoporosis
14 14/25 Contralateral breast cancer, osteoporosis Death from breast cancer Death from other causes 5.2 Helseeffekter, helsegevinst ved vurderte behandlingsalternativ Tabell 2: Oversikt over datakilder Parameter Datakilde Land År Mortalitetsrate SSB Norge 2003 Risiko for tilbakefall IES Internasjonal 2004 Mortalitetsrate etter tilbakefall Kreftregisteret SEER-Medicare Norge USA Kostnader ved tilbakefall SEER-Medicare ISF USA Norge Legemiddelkostnader SLV Norge 2005 Vi ser av tabell 2 at data for å beregne mortalitetsrate er hentet fra Statistisk sentralbyrå 15. Videre er risikoen for tilbakefall hentet fra IES-studien 6. IES-studien er en internasjonal studie med stor norsk deltakelse. I og med at det ikke er tilgjengelig effektdata utover årene 1-4, er det i analysen lagt til grunn at risikoen for tilbakefall i perioden 5-10 år er lik risikoen for tilbakefall for tamoksifengruppen i årene 1-4 (som jo er høyere enn risikoen for tilbakefall for eksemestangruppen). For mortalitet etter tilbakefall brukes data fra Det norske Kreftregisteret og SEER-Medicare 16. Etter tilbakefall vil pasientene ha en forhøyet risiko for brystkreftrelatert død avhengig av type tilbakefall. I modellen skilles det mellom lokalt tilbakefall, kontralateralt tilbakefall og fjernspredning, der fjernspredning er mest livstruende og kontralateralt tilbakefall er minst livstruende. Modellen antar at pasienter kun har forhøyet risiko for død 10 år etter tilbakefall. I modellen varierer sannsynligheten for å dø av fjernspredning og lokalt tilbakefall med tiden, mens sannsynligheten for å dø av kontralateralt tilbakefall er konstant. Pasienter med fjernspredning i modellen antas å ha samme risiko for død som norske pasienter med brystkreft stadium 4. Når det gjelder mortalitetssannsynlighet for lokalt tilbakefall brukes amerikanske data, da det ikke finnes norske data for dette. Søker antar at de amerikanske dataene er representative for norske forhold. Når det gjelder mortalitetssannsynlighet for pasienter med kontralateralt tilbakefall antas det i modellen at pasientene har en prognose som tilsvarer overlevelsen til norske pasienter som diagnostiseres med brystkreft på et tidlig tidspunkt, dvs. stadium I og II.
15 15/25 I tabell 3 under oppsummeres hvilke helsetilstander som knyttes til de ulike Markovtilstandene. Tabell 3. Helse ved Markovtilstander Markov tilstand No recurrence, No osteoporosis Local recurrence, No osteoporosis Distant recurrence, No osteoporosis Contralateral breast cancer, No osteoporosis No recurrence, osteoporosis Local recurrence, osteoporosis Distant recurrence, osteoporosis Contralateral breast cancer, osteoporosis Death from breast cancer Death from other causes Helseeffekt I live, sykdomsfri I live, forhøyet risiko for brystkreft I live, forhøyet risiko for brystkreft I live, forhøyet risiko for brystkreft I live, forhøyet risiko for brystkreft I live, forhøyet risiko for brystkreft I live, forhøyet risiko for brystkreft I live, forhøyet risiko for brystkreft Død Død 5.3 Studiens kostnadsperspektiv Søker legger til grunn at analysen vurderer kostnadene fra et samfunnsmessig perspektiv, dvs. at alle relevante kostnader regnes med uavhengig av hvem som betaler. Modellen tar imidlertid kun hensyn til direkte kostnader som skyldes medisinsk behandling av brystkreft. I den grad det faktisk er indirekte kostnader, fanges disse ikke opp av modellen. 5.4 Kostnader Direkte og indirekte kostnader I refusjonssøknaden er det som nevnt kun tatt med direkte kostnader som skyldes medisinsk behandling av brystkreft. Søker tar ikke høyde for den potensielle gevinsten ved at flere kan arbeide dersom de velger behandling med eksemestan fremfor tamoksifenbehandling. Søker anfører at det ikke er gjennomført norske studier på individnivå for å estimere kostnader ved tilbakefall av brystkreft. Søker har derfor benyttet seg av data fra SEER-Medicare 16.
16 16/25 Tabell 4. Kostnader ved Markovtilstander Markov tilstand Alle i live No recurrence, No osteoporosis Local recurrence, No osteoporosis Distant recurrence, No osteoporosis Contralateral breast cancer, No osteoporosis No recurrence, osteoporosis Local recurrence, osteoporosis Distant recurrence, osteoporosis Contralateral breast cancer, osteoporosis Death from breast cancer Death from other causes Helseeffekt Legemiddelkostnad ved adjuvant behandling fra valg av terapi til fullført 5 års behandling Ingen ekstra kostnader Totalkostnad ved lokalt tilbakefall (registreres en gang per pasient) Totalkostnad ved fjernspredning (registreres en gang per pasient) Totalkostnad ved kontralateralt tilbakefall (registreres en gang per pasient) Årlig kostnad ved behandling av osteoporose Totalkostnad ved lokalt tilbakefall, årlig kostnad for osteoporosebehandling Totalkostnad ved fjernspredning (registreres en gang per pasient), årlig kostnad for osteoporosebehandling Totalkostnad ved kontralateralt tilbakefall(registreres en gang per pasient), årlig kostnad for osteoporosebehandling Død, ingen ekstra kostnader Død, ingen ekstra kostnader SEER-Medicare inneholder data fra 14 helseregistre som dekker ca. 26 prosent av den amerikanske befolkningen. Overlevelsesdata og all medisinsk ressursbruk med tilhørende kostnader i en periode over 10 år etter tilbakefall ble registrert. Kostnader ved tilbakefall ble estimert ved å analysere ressursbruk i forhold til tid etter tilbakefall. Totalkostnaden ble deretter beregnet ved å multiplisere ressursbruk med pasientenes overlevelse og gir et estimat for gjennomsnittskostnad i en pasientpopulasjon der pasientenes oppfølgingstid varierer pga. ulik livslengde. Ved omregning fra USD til NOK er det lagt til grunn en valutakurs på 6.40 NOK/USD. Søker anser kostnadene fra SEER-Medicare studien for å være representative også for norske forhold, samt et konservativt kostnadsestimat for behandling av tilbakefall.
17 17/25 Tabell 5. Kostnader over 10 år per type tilbakefall Type tilbakefall Totale behandlingskostnader i $ Totale behandlingskostnader i NOK Kontralateralt Lokalt Fjernspredning Legemiddelets kostnadseffektivitet Tabell 6. Resultat av modell: LYG Kostnad/LYG Kostnad/ekstrasykdomsfri Probablistisk måned Eksemestan 35,67 år/100 pasienter Kroner 2975 kroner Gjennomsnittsverdi av 1000 simuleringer: Kroner Resultatene indikerer at behandling med eksemestan synes å gi en mer-effekt i form av at gjennomsnittspasienten får hhv. lengre sykdomsfri overlevelse og flere levemåneder/år. Selv om eksemestan koster 10 ganger mer enn tamoksifen, gir modellen resultater som vanligvis regnes som kostnadseffektive. Dette skyldes de helsemessige gevinstene som medfører at annen dyr kreftbehandling kan reduseres. 5.5 Sensitivitetsanalyse (diskontering etc.) Kostnader og helseeffekter er diskontert med 3 prosent. I sensitivitetsanalysen kjøres modellen også med 0 og 5 prosent rente. Søker har i etterkant foretatt sensitivitetsanalyse med 6 prosents diskonteringsrate. Modellen gir i begge tilfeller resultater som vanligvis regnes som kostnadseffektive. Det er gjennomført sensitivitetsanalyser i begge analysene. I refusjonssøknaden endres hver enkelt variabel med +/- 20 prosent. Søker har i etterkant foretatt sensitivitetsanalyse der kostnadene endres til +/- 50 prosent av base case. I begge tilfeller gir modellen resultater som vanligvis regnes som kostnadseffektive. Det er i tillegg utført en probabalistisk sensitivitetsanalyse, der aktuelle variabler i modellen gis en sannsynlighetsfordeling Gitt disse sannsynlighetsfordelingene kjøres en Monte Carlo simulering med 1000 repetisjoner for kostnadseffektivitetsraten til aromasin. Dersom samfunnet er villig til å betale kroner per sparte leveår er det i følge simuleringen 90 prosent sannsynlig at aromasin er kostnadseffektiv behandling sammenliknet med tamoxifen. Som vist i tabell 3 holder også et snitt av disse verdiene seg innenfor verdier som vanligvis anses som kostnadseffektive.
18 18/25 6 Diskusjon 6.1 En totalvurdering Manglende langtidsdata Foreløpig eksisterer det lite data på overlevelse og øvrige langtidseffekter av aromatasehemmere som legemiddelgruppe ved adjuvant behandling av postmenopausale kvinner med tidlig brystkreft. Dette skyldes i hovedsak at oppfølgingstiden til nå er for kort, men produsenten av eksemestan har antydet at resultater fra oppfølgingsstudier vil foreligge innen tre til fem år. Blåreseptnemnda har vurdert deler av dokumentasjonsgrunnlaget for refusjonssøknaden og mener det på det nåværende tidspunkt ikke er rimelig å stille krav om langtidsdata på overlevelse. På bakgrunn av de data som foreligger mener de det er en plausibel sammenheng mellom fjernspredning og død. Følgelig er effekt på sykdomsfri overlevelse et adekvat endepunkt. Behandlingsregime Ledende brystkreftmiljøer oppfatter den største usikkerheten ved adjuvant behandling med aromatasehemmere er knyttet til valg av preparat og behandlingsregime. I de pivotale kliniske studiene av aromatasehemmere er det tre ulike tredjegenerasjons aromatasehemmere (anastrozol, letrozol og eksemestan). Samtlige av aromatasehemmerne har i studiene vært sammenlignet med tamoksifen, men da studiene har svært forskjellig design, kan resultatene ikke sammenlignes direkte (se figur 4). Figur 4. Studiedesign for effektstudier av aromatasehemmere. Kilde: Tidsskrift for Den Norske Lægeforening 2005;125(6):723-8.
19 19/25 De pivotale studiene dannet også grunnlaget for de ulike aromatasehemmernes godkjente medisinske indikasjoner. Dette innebærer at per i dag har ingen av aromatasehemmerne identisk indikasjon. Til det foreligger sammenlignende studier av - behandlingsregime o adjuvant behandling med aromatasehemmere igangsettes umiddelbart etter operasjon (initiell) uten forbehandling med tamoksifen o etter to år med tamoksifen (sekvensiell) o etter 5 år med tamoksifen (forlenget behandling) - valg av aromatasehemmer er det foreløpig usikkert hva som er optimal adjuvant behandling med aromatasehemmere ved tidlig hormonfølsom brystkreft. Norsk Bryst Cancer Gruppe har i sine retningslinjer 1 sidestilt de tre aromatasehemmerne som er på markedet. Sikkerhet Det er også knyttet usikkerhet rundt langtids effekter av adjuvant behandling med aromatasehemmere. Tilgjengelige data indikerer at aromatasehemmere generelt er godt tolerert og ikke assosiert med økt risiko for livmorhalskreft og venetrombose slik som behandling med tamoksifen er. Likevel er en bekymring ved bruk av aromatasehemmere over tid en mulig akselerert osteoporose og en eventuell negativ effekt på plasma-lipidprofil 12. Modellen Søker har som nevnt benyttet en Markovmodell for å vise at eksemestan er kostnadseffektiv adjuvant behandling for postmenopausale kvinner med østrogenreseptorpositiv invasiv brystkreft, etter tidligere 2-3 års adjuvant tamoksifenbehandling, sammenlignet med ytterligere 2-3 år adjuvant tamoksifenbehandling. Mangelende transparens er ofte et problem med denne typen modeller. Modellene er komplekse og det ligger til grunn omfattende beregninger. Dette gjør det utfordrende å etterprøve de faktiske utregningene. Det vil alltid være kilder til usikkerhet ved den type simuleringer søker har benyttet seg av. For det første er det usikkert om modellspesifikasjonen er riktig, dvs. om modellen beskriver virkeligheten hensiktsmessig. For det andre er det usikkert om parameterverdiene som benyttes i modellen har riktige tallverdier. Legemiddelverket mener at den helseøkonomiske analysen som er gjennomført for eksemestan er særlig utsatt for parameter-usikkerhet. Dette skyldes blant annet:
20 20/25 At modellen brukes til å anslå sparte leveår (LYG) uten at det eksisterer kliniske data for endepunktet. Usikkerhet ved estimatene for overgangssannsynligheter for de ulike tilstandene i Markovmodellen. Legemiddelverket mener det er sannsynlig at utfallet ved bruk av aromatasehemmere vil bli sparte leveår og ikke bare forlenget sykdomsfri overlevelse (DFS). Det er imidlertid ikke konkrete holdepunkter for en slik konklusjon ennå. Et mulig, dog lite sannsynlig, scenario, kan for eksempel være at den helsemessige gevinsten består i at pasienten opplever en forlenget sykdomsfri periode, samtidig som at LYG forblir uendret med aromatasehemmere. Siden effekt på DFS synes vist, mener Legemiddelverket det derfor kunne vært interessant/hensiktsmessig å vurdere QALY-effekt av preparatene. Forlenget sykdomsfri periode, selv om levetiden ikke forlenges, vil ha positiv effekt på livskvaliteten. På oppfordring fra Legemiddelverket gjennomførte søker cost-utility analyser for eksemestane. Resultatene fra denne analysen ga også verdier som vanligvis oppfattes som kostnadseffektive. Overgangssannsynligheter Estimatene for overgangssannsynligheter for de ulike tilstandene i Markovmodellen spiller en viktig rolle i beregningene av legemiddelets kostnadseffektivitet. Tilgangen og kvaliteten på dataene som brukes til å beregne sannsynlighetene har stor betydning for utfallet. Risikoen for tilbakefall er hentet fra IES-studien 6 som er en internasjonal studie med stor norsk deltakelse. Dette øker sannsynligheten for at resultatene av studien er representative for norske forhold. I og med at det ikke er tilgjengelig effektdata utover årene 1-4, er det i analysen lagt til grunn at risikoen for tilbakefall i perioden 5-10 år er lik risikoen for tilbakefall for tamoksifengruppen i årene 1-4 (som jo er høyere enn risikoen for tilbakefall for eksemestangruppen). Dermed ekstrapoleres det ingen tilleggseffekt av eksemestan utover det som faktisk ble observert i årene 1-4 i IES studien. Legemiddelverket slutter seg til søkers vurdering om at dette reduserer risikoen for å overdrive den positive effekten av eksemestan i modellen. Når det gjelder mortalitetssannsynlighet for lokalt tilbakefall brukes, som nevnt ovenfor, amerikanske data, da det ikke finnes norske data for dette. Søker antar at de amerikanske dataene er representative for norske forhold. Hvorvidt dette er en rimelig antagelse er usikkert. I mangel av noe annet er det likevel trolig den beste datakilden. Kostnader Som nevnt under punkt 5.4 er det: 1. Kun tatt med direkte kostnader som skyldes medisinsk behandling av brystkreft.
21 21/25 a. Søker tar således ikke høyde for den potensielle reduksjonen i produksjonstap ved at flere kan arbeide (som følge av færre døde og færre tilbakefall) dersom de velger behandling med eksemestan fremfor tamoksifenbehandling. 2. Ikke gjennomført norske studier på individnivå for å estimere kostnader ved tilbakefall av brystkreft. a. Søker har derfor benyttet seg av data fra SEER-Medicare for å estimere kostnader ved behandling av tilbakefall av brystkreft. I de legemiddeløkonomiske analysene som sendes inn med refusjonssøknader ønskes de samfunnsøkonomiske kostnadene ved et tiltak belyst. Ved at søker utelater den potensielle gevinsten ved at flere kan komme tilbake i arbeid og produksjon dersom de behandles med eksemestan fremfor tamoksifenbehandling fra den økonomiske analysen, blir analysen ufullstendig fra et samfunnsøkonomisk perspektiv. Det trekker imidlertid i utgangspunktet i søkers disfavør å utelate fra den økonomiske analysen potensielle reduserte samfunnsøkonomiske kostnader ved at flere kvinner kan komme tilbake i jobb som følge av behandling med eksemestan. Preparatet fremstår som mindre kostnadseffektivt enn hva som kan være tilfelle. De faktiske produksjonsgevinstene er imidlertid usikre og vanskelige å beregne. De avhenger blant annet av alderen på kvinnene som oppnår bedre helse eller som ikke dør av brystkreft, dvs. om disse er i yrkesaktiv alder. Det er videre uheldig at det ikke benyttes norske data for å beregne kostnadene forbundet med ulike typer tilbakefall. Dette øker usikkerheten ved relevansen for kostnadsanslagene som benyttes i modellen. Hovedproblemet er om kostnadsdataene som ligger til grunn for modellens kostnadsanslag er representative for Norge. Søker argumenterer for at det er tilfelle. Vi slutter oss imidlertid til søkers vurdering om at estimatene for direkte kostnader som er benyttet i modellen, på bakgrunn av hva som er vanlig norsk behandling av tilbakefall og gjeldende takster, fremstår som rimelige. I modellen genererer pasienter som får tilbakefall en bestemt gjennomsnittskostnad. Kostnadene i modellen oppstår kun en gang og tar inn over seg pasientenes overlevelse gitt tilstanden de er i. Til tross for at den benyttede totalkostnaden for behandling av tilbakefall over 10 år også tar høyde for pasientenes overlevelse, mener Legemiddelverket det hadde vært hensiktsmessig å fordele behandlingskostnadene over tid. Mange av de som påbegynner behandling for tilbakefall, dør før behandlingen er fullført. Å fordele kostnadene over tid øker sannsynligheten for at de samlede behandlingskostnadene ved tilbakefall ikke tas med dersom pasienten dør fullstendig behandling er fullført. Dersom pasientene som starter på behandling for tilbakefall dør før hele behandlingen ved tilbakefall er fullført, mens modellen tar med kostnadene knyttet til full behandling, overestimeres i så fall behandlingskostnadene ved tilbakefall.
22 22/25 Legemiddelverket mener risikoen for å overvurdere kostnadene ved tilbakefall er større ved den valgte metoden, siden alle som får tilbakefall i modellen generer den angitte kostnaden med en gang. Dermed kan eksemestan fremstå som mer kostnadseffektivt enn det som kan være tilfelle, siden færre antas å få tilbakefall med eksemestan enn med tamoksifen. Andre kostnads-effektivitetsstudier av aromatasehemmere Per i dag likestiller NBCGs retningslinjer for adjuvant endokrin behandling av brystkreft alle aromatasehemmerne med hensyn på effekt og følgelig behandlingsregime. Dette på tross av ulik godkjent medisinsk indikasjon for de ulike aromatasehemmerne. Begrunnelsen for dette er antagelsen om at den gunstige mereffekten ved aromatasehemmere er en klasseeffekt. Legemiddelverket har ikke funnet noen studier der de ulike aromatasehemmerne sammenlignes med hensyn på effekt og kostnadseffektivitet. Derimot har legemiddelverket funnet artikler der dette er diskutert for anastrozol og letrozol I disse artiklene fremstår aromatasehemmere som mindre kostnadseffektive enn det som fremgår av den innsendte analysen for eksemestan. Basert på antagelsen om aromatasehemmernes klasseeffekt, ble refusjonssøker bedt om å kommentere avvikene i kostnadseffektivitetsratioene beskrevet i artikkelen til Karnon 20. Refusjonssøker valgte i sin kommentar til legemiddelverket å fokusere på at artikkelen vurderte kostnadseffektivitet for anastrozol og letrozol, samt andre behandlingsregimer. De stilte seg dessuten kritisk til artikkelens metode for innsamling og behandling av data. Legemiddelverket er fremdeles av den oppfatning at de avvikende resultatene er interessante med hensyn på å vurdere den innsendte legemiddeløkonomiske modellens validitet. Til tross for søkers noe ufullstendige tilbakemelding, mener Legemiddelverket at avvikene hovedsaklig skyldes en kombinasjon av ulike overgangssannsynligheter som inngår i modellene, ulike kostnader og kvantifisering av disse. Legemiddelverket mener således at mange små forskjeller i modellene, som angitt i ovennevnte artikler, kan gi store utslag i kostnadseffektivitetsratioer.
23 23/25 7 Konklusjon Etter en samlet vurdering mener Statens legemiddelverk at det er en sannsynligshetsovervekt for at behandling med eksemestan er kostnadseffektiv som adjuvant behandling av kvinner med østrogenreseptorpositiv brystkreft. Statens legemiddelverk vedtar at Aromasin (eksemestan) innvilges refusjon etter 9 punkt 9, bokstav a) for indikasjonen behandling av: Adjuvant behandling av postmenopausale kvinner med østrogenreseptor-positiv, invasiv brystkreft, etter tidligere 2-3 års adjuvant tamoksifenbehandling. Med følgende refusjonsvilkår: - Refusjonen er indikasjonsspesifikk og refusjon omfatter kun behandling av: Adjuvant behandling av postmenopausale kvinner med østrogenreseptor-positiv, invasiv brystkreft, etter tidligere 2-3 års adjuvant tamoksifenbehandling. Og forbehold: - Vedtaket er tidsbegrenset frem til og med Innen skal refusjonssøker sende inn en ny helseøkonomisk analyse av eksemestan. Statens legemiddelverk vil da foreta en revurdering av refusjonsstatus for Aromasin (eksemestan). Vedtaket er betinget i den forstand at det kan revurderes og endres dersom det tilkommer nye forhold som endrer grunnlaget eller premissene for refusjonsvedtaket. STATENS LEGEMIDDELVERK Erik Hviding Anders Hansen Kristin Svanqvist seksjonssjef forsker Rådgiver
24 24/25 8 Referanser 1. Brystkreft diagnostikk og behandling. Blåboka Norsk Bryst Cancer Gruppe oppdatert versjon Kreftregisteret. Personlig meddelelse Steinar Thoresen mars Baum M, Budzar AU, Cuzick J, Forbes J, Houghton JH, Klijn JG, et al. Anastrozole alone or in combination with tamoxifen versus tamoxifen alone for adjuvant treatment of postmenopausal women with early breast cancer: first results of the ATAC randomised trial. Lancet 2002;359(9324): Goss PE, Ingle JN, Martino S, Robert NJ, Muss HB, Piccart MJ, et al. A Randomized Trial of Letrozole in Postmenopausal Women after Five Years of Tamoxifen Therapy for Early-Stage Breast Cancer. N Engl J Med 2003;349(19): Coombes RC, Hall E, Gibson LJ, Paridaens R, Jassem J, Delozier T, et al. A Randomized Trial of Exemestane after Two to Three Years of Tamoxifen Therapy in Postmenopausal Women with Primary Breast Cancer. N Engl J Med 2004;350(11): Early Breast Cancer Trialists' Collaborative G. Effects of chemotherapy and hormonal therapy for early breast cancer on recurrence and 15-year survival: an overview of the randomised trials. The Lancet;365(9472): Early Breast Cancer Trialists' Collaborative G. Tamoxifen for early breast cancer: an overview of the randomised trials. The Lancet 1998;351(9114): Preparatomtale for legemidler.summary of Product Characteristic (SPC) for Aromasin The Breast International Group 1-98 Collaborative G. A Comparison of Letrozole and Tamoxifen in Postmenopausal Women with Early Breast Cancer. N Engl J Med 2005;353(26): Geisler J, Lonning PE. Aromatase inhibitors as adjuvant treatment of breast cancer. Crit Rev Oncol Hematol 2006;57(1): Lønning PE. Aromatasehemmere i behandling av brystkreft. Tidsskr Nor Lægeforen 2005;125(6): McCloskey E. Effects of third-generation aromatase inhibitors on bone. European Journal of Cancer;In Press, Corrected Proof. 14. Lonning PE, Geisler J, Krag LE, Erikstein B, Bremnes Y, Hagen AI, et al. Effects of exemestane administered for 2 years versus placebo on bone mineral density, bone biomarkers, and plasma lipids in patients with surgically resected early breast cancer. J Clin Oncol 2005;23(22): Statistisk sentralbyrå. Dødelighetstabeller Refusjonssøker har hentet data fra The Surveillance Epidemiology and End Results (SEER Medicare data). Analysis of SEER- Medicare data modell parameters concerning breast cancer recurrence Henderson IC. Aromatase inhibitors in the management of early breast cancer: optimizing the clinical benefit. Semin Oncol 2004;31(6 Suppl 12): Cuzick J, Sasieni P, Howell A. Should aromatase inhibitors be used as initial adjuvant treatment or sequenced after tamoxifen? British Journal of Cancer 2006;94: Bruce EH. Benefit and projected cost-effectiveness of anastrozole versus tamoxifen as initial adjuvant therapy for patients with early-stage estrogen receptor-positive breast cancer. Cancer 2004;101(6): Karnon J. Aromatase inhibitors in breast cancer: a review of cost considerations and cost effectiveness. Pharmacoeconomics 2006;24(3):
25 25/ Karnon J, Delea T, Johnston SR, Smith R, Brandman J, Sung J, et al. Cost Effectiveness of Extended Adjuvant Letrozole in Postmenopausal Women after Adjuvant Tamoxifen Therapy : The UK Perspective. Pharmacoeconomics 2006;24(3): Lonning PE. Comparing cost/utility of giving an aromatase inhibitor as monotherapy for 5 years versus sequential administration following 2-3 or 5 years of tamoxifen as adjuvant treatment for postmenopausal breast cancer. Ann Oncol 2006;17(2):
Refusjonsrapport Arimidex (anastrozol), adjuvant behandling av brystkreft
 Refusjonsrapport Arimidex (anastrozol), adjuvant behandling av brystkreft 1 Oppsummering Formål: Å vurdere Arimidex (anastrozol) for pliktmessig refusjon etter forskrift av 18. april 1997 nr. 330 om stønad
Refusjonsrapport Arimidex (anastrozol), adjuvant behandling av brystkreft 1 Oppsummering Formål: Å vurdere Arimidex (anastrozol) for pliktmessig refusjon etter forskrift av 18. april 1997 nr. 330 om stønad
Refusjonsrapport Femar (letrozol), adjuvant behandling av brystkreft
 Refusjonsrapport Femar (letrozol), adjuvant behandling av brystkreft 1 Oppsummering Formål: Å vurdere Femar (letrozol) for pliktmessig refusjon etter forskrift av 18. april 1997 nr. 330 om stønad til dekning
Refusjonsrapport Femar (letrozol), adjuvant behandling av brystkreft 1 Oppsummering Formål: Å vurdere Femar (letrozol) for pliktmessig refusjon etter forskrift av 18. april 1997 nr. 330 om stønad til dekning
Refusjonsrapport Femar (letrozol), adjuvant behandling av brystkreft
 Refusjonsrapport Femar (letrozol), adjuvant behandling av brystkreft 1 Oppsummering Formål: Å vurdere Femar (letrozol) for pliktmessig refusjon etter forskrift av 18. april 1997 nr. 330 om stønad til dekning
Refusjonsrapport Femar (letrozol), adjuvant behandling av brystkreft 1 Oppsummering Formål: Å vurdere Femar (letrozol) for pliktmessig refusjon etter forskrift av 18. april 1997 nr. 330 om stønad til dekning
Deres dato Deres referanse Vår dato Vår referanse Seksjon/saksbehandler 2005-10-31 200506318 LØ/LR/ABH
 Deres dato Deres referanse Vår dato Vår referanse Seksjon/saksbehandler 2005-10-31 200506318 LØ/LR/ABH Refusjonsrapport 1. OPPSUMMERING Formål: Å vurdere darifenacin (Emselex) for pliktmessig refusjon
Deres dato Deres referanse Vår dato Vår referanse Seksjon/saksbehandler 2005-10-31 200506318 LØ/LR/ABH Refusjonsrapport 1. OPPSUMMERING Formål: Å vurdere darifenacin (Emselex) for pliktmessig refusjon
17. NBCGs anbefalinger til standard endokrin og behandling av metastatisk brystkreft
 17. NBCGs anbefalinger til standard endokrin og behandling av metastatisk brystkreft Endokrin behandling Målet med systemisk behandling av metastatisk/avansert brystkreftsykdom er å hindre sykdomsprogresjon
17. NBCGs anbefalinger til standard endokrin og behandling av metastatisk brystkreft Endokrin behandling Målet med systemisk behandling av metastatisk/avansert brystkreftsykdom er å hindre sykdomsprogresjon
Brystkreft: hyppigheten øker men dødeligheten går ned hvorfor? Lars Vatten, dr med Professor i epidemiologi. Det medisinske fakultet NTNU, Trondheim
 Brystkreft: hyppigheten øker men dødeligheten går ned hvorfor? Lars Vatten, dr med Professor i epidemiologi Det medisinske fakultet NTNU, Trondheim 1 Dødelighetskurven for brystkreft viste en svakt økende
Brystkreft: hyppigheten øker men dødeligheten går ned hvorfor? Lars Vatten, dr med Professor i epidemiologi Det medisinske fakultet NTNU, Trondheim 1 Dødelighetskurven for brystkreft viste en svakt økende
1 OPPSUMMERING. Brev stiles til Statens legemiddelverk. Vennligst oppgi vår referanse.
 Rapport og vedtak fra Statens legemiddelverk vedrørende søknad om opptak av fulvestrant (Faslodex) på listen over refusjonsberettigede legemidler etter 9 i forskrift om godtgjørelse av utgifter til viktige
Rapport og vedtak fra Statens legemiddelverk vedrørende søknad om opptak av fulvestrant (Faslodex) på listen over refusjonsberettigede legemidler etter 9 i forskrift om godtgjørelse av utgifter til viktige
11.05.2012. Mammografiscreening med fokus på Norge. Kreftscreening. Grunnlag for screening i en befolkningen. Mammografi screening
 Kreftscreening Mammografiscreening med fokus på Norge Mette Kalager Lege og postdoc Tidlig deteksjon Prevensjon Blanding av de to 3 Grunnlag for screening i en befolkningen Vanlig sykdom Høy dødelighet
Kreftscreening Mammografiscreening med fokus på Norge Mette Kalager Lege og postdoc Tidlig deteksjon Prevensjon Blanding av de to 3 Grunnlag for screening i en befolkningen Vanlig sykdom Høy dødelighet
Bruk av forløpsdata i legemiddeløkonomiske analyser. Gyldig fra 13-04-2015 Statens legemiddelverk
 Notat Bruk av forløpsdata i legemiddeløkonomiske analyser Gyldig fra 13-04-2015 Statens legemiddelverk Brev stiles til Statens legemiddelverk. Vennligst oppgi vår referanse. Statens legemiddelverk Telefon
Notat Bruk av forløpsdata i legemiddeløkonomiske analyser Gyldig fra 13-04-2015 Statens legemiddelverk Brev stiles til Statens legemiddelverk. Vennligst oppgi vår referanse. Statens legemiddelverk Telefon
Forslag om nasjonal metodevurdering
 Forslag om nasjonal metodevurdering Viktig informasjon se på dette først! Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Forslag om nasjonal metodevurdering Viktig informasjon se på dette først! Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Kort vurdering. Vurdering av innsendt dokumentasjon Statens legemiddelverk
 Kort vurdering ID-nr 2015_019: Bruk av bevacizumab (Avastin) ved avansert livmorhalskreft og ved tilbakefall av livmorhalskreft». Vurdering av innsendt dokumentasjon 29-08-2016 Statens legemiddelverk Brev
Kort vurdering ID-nr 2015_019: Bruk av bevacizumab (Avastin) ved avansert livmorhalskreft og ved tilbakefall av livmorhalskreft». Vurdering av innsendt dokumentasjon 29-08-2016 Statens legemiddelverk Brev
Forslag til nasjonal metodevurdering
 Forslag til nasjonal metodevurdering Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig informasjon for utfylling av skjemaet
Forslag til nasjonal metodevurdering Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig informasjon for utfylling av skjemaet
SUTENT (sunitinib) til behandling for dine pasienter med metastatisk nyrekreft
 SUTENT (sunitinib) til behandling for dine pasienter med metastatisk nyrekreft Hvordan virker SUTENT for pasienter som er eldre sammenlignet med yngre pasienter? Hvordan optimalisere doseringen med Sutent?
SUTENT (sunitinib) til behandling for dine pasienter med metastatisk nyrekreft Hvordan virker SUTENT for pasienter som er eldre sammenlignet med yngre pasienter? Hvordan optimalisere doseringen med Sutent?
Deres dato Deres referanse Vår dato Vår referanse Seksjon/saksbehandler LØ/LR/ABH/THH
 Deres dato Deres referanse Vår dato Vår referanse Seksjon/saksbehandler 2005-01-31 200410133 LØ/LR/ABH/THH Refusjonsrapport 1. OPPSUMMERING Formål: Å vurdere solifenacin (Vesicare) for pliktmessig refusjon
Deres dato Deres referanse Vår dato Vår referanse Seksjon/saksbehandler 2005-01-31 200410133 LØ/LR/ABH/THH Refusjonsrapport 1. OPPSUMMERING Formål: Å vurdere solifenacin (Vesicare) for pliktmessig refusjon
Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Mikkel Bo Johansen 17.09.2014 14/08565-6 Seksjon for legemiddelrefusjon/ Einar Andreassen
 Alcon Nordic A/S Edvard Thomsens Vej 14 2300 København S Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Mikkel Bo Johansen 17.09.2014 14/08565-6 Seksjon for legemiddelrefusjon/ Einar REFUSJONSVEDTAK
Alcon Nordic A/S Edvard Thomsens Vej 14 2300 København S Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Mikkel Bo Johansen 17.09.2014 14/08565-6 Seksjon for legemiddelrefusjon/ Einar REFUSJONSVEDTAK
Behandlingsmålet er å senke øyetrykket tilstrekkelig til å unngå synsfeltskader eller progresjon av slike skader.
 Refusjonsrapport Azarga til behandling av glaukom 1 OPPSUMMERING Formål: Å vurdere forhåndsgodkjent refusjon for Azarga (brinzolamid og timolol) etter forskrift av 28. juni 2007 nr. 814 om stønad til dekning
Refusjonsrapport Azarga til behandling av glaukom 1 OPPSUMMERING Formål: Å vurdere forhåndsgodkjent refusjon for Azarga (brinzolamid og timolol) etter forskrift av 28. juni 2007 nr. 814 om stønad til dekning
Fotograf: Wilse, A. B. / Oslo byarkiv
 Fotograf: Wilse, A. B. / Oslo byarkiv Fotograf: Wilse, A. B. / Oslo byarkiv Lørdagsseminar 8.november 214 Kampen mot kreft Velkommen ved prodekan Kristin Heggen og professor Marit Bragelien Veierød Kulturelt
Fotograf: Wilse, A. B. / Oslo byarkiv Fotograf: Wilse, A. B. / Oslo byarkiv Lørdagsseminar 8.november 214 Kampen mot kreft Velkommen ved prodekan Kristin Heggen og professor Marit Bragelien Veierød Kulturelt
Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 12.03.2014 13/14033-6 Seksjon for legemiddelrefusjon/ Christina Kvalheim
 NOVARTIS NORGE AS Postboks 4284 Nydalen 0401 Oslo Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 12.03.2014 13/14033-6 Seksjon for legemiddelrefusjon/ Christina REFUSJONSVEDTAK Vi viser til Deres søknad
NOVARTIS NORGE AS Postboks 4284 Nydalen 0401 Oslo Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 12.03.2014 13/14033-6 Seksjon for legemiddelrefusjon/ Christina REFUSJONSVEDTAK Vi viser til Deres søknad
Ashkan Kourdalipour, Jørgensen Kristian Samdal
 Zambon Zambon S.p.A., Italia Repr. Nigaard Pharma Storg. 8 B Postboks 373 2001 Lillestrøm Deres referanse Vår dato Vår referanse Seksjon/saksutredere LØ/LR/ Christina Kuljis/ Eivind 09/06/2016 15/16242
Zambon Zambon S.p.A., Italia Repr. Nigaard Pharma Storg. 8 B Postboks 373 2001 Lillestrøm Deres referanse Vår dato Vår referanse Seksjon/saksutredere LØ/LR/ Christina Kuljis/ Eivind 09/06/2016 15/16242
OPPDATERT NOTAT NIVOLUMAB TIL PASIENTER MED IKKE-SMÅCELLET LUNGEKREFT AV TYPEN PLATEEPITELKARSINOM SOM IKKE UTTRYKKER PD-L1
 Helsedirektoratet Postboks 7000 St. Olavsplass 0130 OSLO Sekretariatet for nye metoder Deres ref.: Dato: Vår ref.: Saksbehandler: 23.11.2017 17/15899-1 BSt CH OPPDATERT NOTAT NIVOLUMAB TIL PASIENTER MED
Helsedirektoratet Postboks 7000 St. Olavsplass 0130 OSLO Sekretariatet for nye metoder Deres ref.: Dato: Vår ref.: Saksbehandler: 23.11.2017 17/15899-1 BSt CH OPPDATERT NOTAT NIVOLUMAB TIL PASIENTER MED
Refusjonsrapport. Vurdering av søknad om forhåndsgodkjent refusjon 2. 11-11-2013 Statens legemiddelverk
 Refusjonsrapport aflibercept (Eylea) til behandling av aldersrelatert våt makula-degenerasjon (våt AMD). Vurdering av søknad om forhåndsgodkjent refusjon 2 11-11-2013 Statens legemiddelverk Brev stiles
Refusjonsrapport aflibercept (Eylea) til behandling av aldersrelatert våt makula-degenerasjon (våt AMD). Vurdering av søknad om forhåndsgodkjent refusjon 2 11-11-2013 Statens legemiddelverk Brev stiles
Plan. Innledning Prioriteringskriterier - hvorfor kostnadseffektivitet Hvordan måles og verdsettes kostnadseffektivitet, herunder
 Plan Innledning Prioriteringskriterier - hvorfor kostnadseffektivitet Hvordan måles og verdsettes kostnadseffektivitet, herunder ICER dvs merkostnad per mereffekt Effekt QALYs, kvalitetsjusterte leveår
Plan Innledning Prioriteringskriterier - hvorfor kostnadseffektivitet Hvordan måles og verdsettes kostnadseffektivitet, herunder ICER dvs merkostnad per mereffekt Effekt QALYs, kvalitetsjusterte leveår
Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: / Seksjon for legemiddelrefusjon/ Kirsti Hjelme
 MSD (NORGE) AS Postboks 458 Brakerøya 3002 Drammen Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 21.10.2013 13/15074-3 Seksjon for legemiddelrefusjon/ Kirsti Hjelme REFUSJONSVEDTAK Vi viser til Deres
MSD (NORGE) AS Postboks 458 Brakerøya 3002 Drammen Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 21.10.2013 13/15074-3 Seksjon for legemiddelrefusjon/ Kirsti Hjelme REFUSJONSVEDTAK Vi viser til Deres
Tablett, drasjert. Rund, bikonveks, offwhite drasjert tablett merket med 7663 på en side.
 1. LEGEMIDLETS NAVN Aromasin 25 mg tabletter, drasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder eksemestan 25 mg. Hver tablett inneholder 30,2 mg sukrose og 0,003 mg metylparahydroksybenzoat
1. LEGEMIDLETS NAVN Aromasin 25 mg tabletter, drasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder eksemestan 25 mg. Hver tablett inneholder 30,2 mg sukrose og 0,003 mg metylparahydroksybenzoat
Cancer in Norway 2015
 Cancer in Norway 2015 Kreftinsidens, mortalitet, overlevelse og prevalens i Norge Norsk sammendrag CiN 2015 Image: Shutterstock Norsk sammendrag Kreft i Norge 2015 Hvordan forstå krefttall I vår årlige
Cancer in Norway 2015 Kreftinsidens, mortalitet, overlevelse og prevalens i Norge Norsk sammendrag CiN 2015 Image: Shutterstock Norsk sammendrag Kreft i Norge 2015 Hvordan forstå krefttall I vår årlige
200700549-6 LØ/LR/KHS 2007-02-26 side 3/5
 Referat fra møte i Blåreseptnemnda 31.januar 2007 Tilstede fra Blåreseptnemnda: Kristian Hagestad (leder), Anne Elise Eggen, Hans Arne Melleby, Eline Aas, Trine Bjørner, Sigurd Hortemo, Bjarne Robberstad
Referat fra møte i Blåreseptnemnda 31.januar 2007 Tilstede fra Blåreseptnemnda: Kristian Hagestad (leder), Anne Elise Eggen, Hans Arne Melleby, Eline Aas, Trine Bjørner, Sigurd Hortemo, Bjarne Robberstad
Forslag om nasjonal metodevurdering
 Forslag om nasjonal metodevurdering Viktig informasjon se på dette først! Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Forslag om nasjonal metodevurdering Viktig informasjon se på dette først! Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Carl Samuelsen / Seksjon for legemiddelomsetning/ Leung Ming Yu
 BOEHRINGER INGELHEIM NORWAY KS Postboks 405 1373 Asker Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Carl Samuelsen 26.10.2015 15/10613-5 Seksjon for legemiddelomsetning/ Leung Ming REFUSJONSVEDTAK
BOEHRINGER INGELHEIM NORWAY KS Postboks 405 1373 Asker Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Carl Samuelsen 26.10.2015 15/10613-5 Seksjon for legemiddelomsetning/ Leung Ming REFUSJONSVEDTAK
Hvite til gulhvite, runde, bikonvekse, filmdrasjerte tabletter som er preget med E25 på den ene siden og er glatte på den andre siden.
 1. LEGEMIDLETS NAVN Exemestan Sandoz 25 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder eksemestan 25 mg. Hjelpestoff med kjent effekt: mannitol 90,40 mg.
1. LEGEMIDLETS NAVN Exemestan Sandoz 25 mg filmdrasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder eksemestan 25 mg. Hjelpestoff med kjent effekt: mannitol 90,40 mg.
Refusjonsrapport preparat til behandling gastrointestinal stromal tumor
 Refusjonsrapport preparat til behandling gastrointestinal stromal tumor 1 OPPSUMMERING Formål: Å vurdere Sutent (sunitinib) for pliktmessig refusjon etter forskrift av 18. april 1997 nr. 330 om stønad
Refusjonsrapport preparat til behandling gastrointestinal stromal tumor 1 OPPSUMMERING Formål: Å vurdere Sutent (sunitinib) for pliktmessig refusjon etter forskrift av 18. april 1997 nr. 330 om stønad
Økonomisk modell for colorectal cancer - foreløpige resultater og bruksområder
 Økonomisk modell for colorectal cancer - foreløpige resultater og bruksområder Ved Pål Joranger Høgskolen i Oslo og Akershus/ Universitetet for miljø- og biovitenskap Den nasjonale helseøkonomikonferansen
Økonomisk modell for colorectal cancer - foreløpige resultater og bruksområder Ved Pål Joranger Høgskolen i Oslo og Akershus/ Universitetet for miljø- og biovitenskap Den nasjonale helseøkonomikonferansen
Refusjonsrapport - 1 Oppsummering
 Refusjonsrapport - 1 Oppsummering Formål: Å vurdere preparat for pliktmessig refusjon etter forskrift av 18. april 1997 nr. 330 om stønad til dekning av utgifter til viktige legemidler og spesielt medisinsk
Refusjonsrapport - 1 Oppsummering Formål: Å vurdere preparat for pliktmessig refusjon etter forskrift av 18. april 1997 nr. 330 om stønad til dekning av utgifter til viktige legemidler og spesielt medisinsk
181: Behandling skal kun startes av spesialist i indremedisin, barnesykdommer eller ved sykehusavdeling med tilsvarende spesialitet
 Novo Nordisk Scandinavia AS Baker Østbys vei 5Postboks 24 1309 RUD Norge Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 29.01.2016 15/16181-3 Seksjon for legemiddelrefusjon/ Pilar martin Vivaldi/ Anne
Novo Nordisk Scandinavia AS Baker Østbys vei 5Postboks 24 1309 RUD Norge Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 29.01.2016 15/16181-3 Seksjon for legemiddelrefusjon/ Pilar martin Vivaldi/ Anne
Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Petter Foss 30.04.2014 13/13693-3 Seksjon for legemiddelrefusjon/ Kirsti Hjelme
 NOVARTIS NORGE AS Postboks 4284 Nydalen 0401 Oslo Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Petter Foss 30.04.2014 13/13693-3 Seksjon for legemiddelrefusjon/ Kirsti Hjelme REFUSJONSVEDTAK Vi viser
NOVARTIS NORGE AS Postboks 4284 Nydalen 0401 Oslo Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Petter Foss 30.04.2014 13/13693-3 Seksjon for legemiddelrefusjon/ Kirsti Hjelme REFUSJONSVEDTAK Vi viser
Kurs i legemiddeløkonomi 20. mai 2015
 Kurs i legemiddeløkonomi 20. mai 2015 Erik Sagdahl erik.sagdahl@legemiddelverket.no Morten Aaserud morten.aaserud@legemiddelverket.no Legemidler. Finansiering/betaling Blåresept Sykehus Forhåndsgodkjent
Kurs i legemiddeløkonomi 20. mai 2015 Erik Sagdahl erik.sagdahl@legemiddelverket.no Morten Aaserud morten.aaserud@legemiddelverket.no Legemidler. Finansiering/betaling Blåresept Sykehus Forhåndsgodkjent
Beregning av absolutt prognosetap i hurtig metodevurderinger av legemidler bruke beregningsprinsippet for behandling eller forebygging?
 Beregning av absolutt prognosetap i hurtig metodevurderinger av legemidler bruke beregningsprinsippet for behandling eller forebygging? Notat fra en tverretatlig arbeidsgruppe 1 31.01.2019 1 Bestående
Beregning av absolutt prognosetap i hurtig metodevurderinger av legemidler bruke beregningsprinsippet for behandling eller forebygging? Notat fra en tverretatlig arbeidsgruppe 1 31.01.2019 1 Bestående
Bakgrunnsstoff om lungekreft og Iressa til pressen på forespørsel
 Utl fakta Bakgrunnsstoff om lungekreft og Iressa til pressen på forespørsel Lungekreft er en av våre vanligste kreftformer, og er den kreftsykdommen som dreper flest mennesker i Norge. I løpet av dette
Utl fakta Bakgrunnsstoff om lungekreft og Iressa til pressen på forespørsel Lungekreft er en av våre vanligste kreftformer, og er den kreftsykdommen som dreper flest mennesker i Norge. I løpet av dette
Om persontilpasset medisin
 Om persontilpasset medisin Giske Ursin Kreftregisteret Eldre legers forenings høstmøte, Soria Moria Hotell, 4. nov 2018 Hva er persontilpasset medisin? «... forebygging, diagnostikk, behandling og oppfølging
Om persontilpasset medisin Giske Ursin Kreftregisteret Eldre legers forenings høstmøte, Soria Moria Hotell, 4. nov 2018 Hva er persontilpasset medisin? «... forebygging, diagnostikk, behandling og oppfølging
Epidemiologi - en oppfriskning. Epidemiologi. Viktige begreper 12.04.2015. Deskriptiv beskrivende. Analytisk årsaksforklarende. Ikke skarpt skille
 Epidemiologi - en oppfriskning Epidemiologi Deskriptiv beskrivende Hyppighet og fordeling av sykdom Analytisk årsaksforklarende Fra assosiasjon til kausal sammenheng Ikke skarpt skille Viktige begreper
Epidemiologi - en oppfriskning Epidemiologi Deskriptiv beskrivende Hyppighet og fordeling av sykdom Analytisk årsaksforklarende Fra assosiasjon til kausal sammenheng Ikke skarpt skille Viktige begreper
Forslag til nasjonal metodevurdering
 Forslagsskjema, Versjon 2 17. mars 2014 Forslag til nasjonal metodevurdering Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Forslagsskjema, Versjon 2 17. mars 2014 Forslag til nasjonal metodevurdering Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Fellesregistre - Kreftregisteret. Jan F Nygård Kreftregisteret
 Fellesregistre - Kreftregisteret Jan F Nygård Kreftregisteret Kreftregisteret > Opprettet i 1951 > Samle inn opplysninger om all kreft i Norge (Kreftregisterforskiften); > Formål: Etablere viten og spre
Fellesregistre - Kreftregisteret Jan F Nygård Kreftregisteret Kreftregisteret > Opprettet i 1951 > Samle inn opplysninger om all kreft i Norge (Kreftregisterforskiften); > Formål: Etablere viten og spre
Onkologisk Forum, Espen Movik, forsker
 Onkologisk Forum, 19.11.09 Metylnaltrekson Kunnskapsesenterets ved obstipasjon hos palliative nye PPT-mal pasienter Espen Movik, forsker Om rapporten Kunnskapssenterets rapport publisert i oktober 09.
Onkologisk Forum, 19.11.09 Metylnaltrekson Kunnskapsesenterets ved obstipasjon hos palliative nye PPT-mal pasienter Espen Movik, forsker Om rapporten Kunnskapssenterets rapport publisert i oktober 09.
Brystkreft Diagnose Behandling Kontroller
 Brystkreft Diagnose Behandling Kontroller SØ-9110 Innhold 3 4 5-7 8-9 10-11 12-13 14 15 16 Forord Brystkreftsykdommen Behandlingsformer Mulige komplikasjoner etter operasjonen Oppfølging etter operasjonen
Brystkreft Diagnose Behandling Kontroller SØ-9110 Innhold 3 4 5-7 8-9 10-11 12-13 14 15 16 Forord Brystkreftsykdommen Behandlingsformer Mulige komplikasjoner etter operasjonen Oppfølging etter operasjonen
Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Petter Foss / Seksjon for legemiddelomsetning/ Leung Ming Yu
 NOVARTIS NORGE AS Postboks 4284 Nydalen 0401 Oslo Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Petter Foss 26.10.2015 15/1182-4 Seksjon for legemiddelomsetning/ Leung Ming REFUSJONSVEDTAK Vi viser
NOVARTIS NORGE AS Postboks 4284 Nydalen 0401 Oslo Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Petter Foss 26.10.2015 15/1182-4 Seksjon for legemiddelomsetning/ Leung Ming REFUSJONSVEDTAK Vi viser
Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Eva Callert / Seksjon for legemiddelrefusjon/ Helle Endresen
 Chiesi pharma AB Box 63 S-182 11 Danderyd Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Eva Callert 16.10.2014 14/10880-5 Seksjon for legemiddelrefusjon/ Helle Endresen REFUSJONSVEDTAK Vi viser til
Chiesi pharma AB Box 63 S-182 11 Danderyd Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: Eva Callert 16.10.2014 14/10880-5 Seksjon for legemiddelrefusjon/ Helle Endresen REFUSJONSVEDTAK Vi viser til
Lungekreftkostnader nå og i fremtiden
 Lungekreftkostnader nå og i fremtiden Hvor ligger de største kostnadene? Hvilken kostnadsutvikling kan vi vente? DM Arena Lungekreft, Oslo 8 februar 2018 Kreft: Høye behandlingskostnader og stort produksjonstap
Lungekreftkostnader nå og i fremtiden Hvor ligger de største kostnadene? Hvilken kostnadsutvikling kan vi vente? DM Arena Lungekreft, Oslo 8 februar 2018 Kreft: Høye behandlingskostnader og stort produksjonstap
Forslag til nasjonal metodevurdering
 Forslagsskjema, Versjon 2 17. mars 2014 Forslag til nasjonal metodevurdering Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Forslagsskjema, Versjon 2 17. mars 2014 Forslag til nasjonal metodevurdering Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Bevacizumab ved behandling av ovariecancer. Av Professor Gunnar Kristensen
 Bevacizumab ved behandling av ovariecancer Av Professor Gunnar Kristensen Den amerikanske studiegruppe GOG vurderte i studie GOG218 tillegget av bevacizumab til standard kjemoterapi (karboplatin pluss
Bevacizumab ved behandling av ovariecancer Av Professor Gunnar Kristensen Den amerikanske studiegruppe GOG vurderte i studie GOG218 tillegget av bevacizumab til standard kjemoterapi (karboplatin pluss
Hva skal vi gjøre når vi ikke kan gjøre alt? Helseforetakenes onkologiseminar 31/1-18 Jon Magnussen
 Hva skal vi gjøre når vi ikke kan gjøre alt? Helseforetakenes onkologiseminar 31/1-18 Jon Magnussen jon.magnussen@ntnu.no Overordnet om prioritering Innhold Alternativkostnad Betalingsvillighet og pris
Hva skal vi gjøre når vi ikke kan gjøre alt? Helseforetakenes onkologiseminar 31/1-18 Jon Magnussen jon.magnussen@ntnu.no Overordnet om prioritering Innhold Alternativkostnad Betalingsvillighet og pris
Oppdatering av hurtig metodevurdering
 Oppdatering av hurtig metodevurdering Bestilling ID2017_012 Nivolumab (Opdivo) til andrelinjebehandling av avansert nyrecellekarsinom Vurdering av oppdatert dokumentasjon av overlevelsesdata og helseøkonomiske
Oppdatering av hurtig metodevurdering Bestilling ID2017_012 Nivolumab (Opdivo) til andrelinjebehandling av avansert nyrecellekarsinom Vurdering av oppdatert dokumentasjon av overlevelsesdata og helseøkonomiske
Refusjon av legemidler i Norge
 Refusjon av legemidler i Norge Seniorrådgiver Morten Aaserud Statens legemiddelverk Møte i Norsk Biotekforum 22.september 2011 Plan del 1 Folketrygdens refusjon av legemidler målsetting og system Vurdering
Refusjon av legemidler i Norge Seniorrådgiver Morten Aaserud Statens legemiddelverk Møte i Norsk Biotekforum 22.september 2011 Plan del 1 Folketrygdens refusjon av legemidler målsetting og system Vurdering
Forslag om nasjonal metodevurdering
 Forslag om nasjonal metodevurdering Viktig informasjon se på dette først! Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Forslag om nasjonal metodevurdering Viktig informasjon se på dette først! Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Tablett, drasjert. Rund, bikonveks, offwhite drasjert tablett merket med 7663 på en side.
 1. LEGEMIDLETS NAVN Aromasin 25 mg drasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder eksemestan 25 mg. Hver tablett inneholder 30,2 mg sukrose og 0,003 mg metylparahydroksybenzoat
1. LEGEMIDLETS NAVN Aromasin 25 mg drasjerte tabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver tablett inneholder eksemestan 25 mg. Hver tablett inneholder 30,2 mg sukrose og 0,003 mg metylparahydroksybenzoat
Epidemiologi - en oppfriskning. En kort framstilling. Er det behov for kunnskaper om epidemiologi?
 Epidemiologi - en oppfriskning En kort framstilling Dere kan finne en kort gjennomgang av epidemiologifaget i et kapittel som jeg skrev i en bok. Jacobsen BK. Epidemiologi. I: Kvantitativ forskningsmetodologi
Epidemiologi - en oppfriskning En kort framstilling Dere kan finne en kort gjennomgang av epidemiologifaget i et kapittel som jeg skrev i en bok. Jacobsen BK. Epidemiologi. I: Kvantitativ forskningsmetodologi
Vedlegg til vignette 58/11-2 Innføring av nye kreftlegemidler
 Stein Kaasa på vegne av arbeidsgruppen for utarbeidelse av nasjonale retningslinjer for behandling av sarkom Sykdom Bløtvevssarkom 1 Antall pasienter Usikre tall, mellom 160 og 300 diagnostiseres årlig
Stein Kaasa på vegne av arbeidsgruppen for utarbeidelse av nasjonale retningslinjer for behandling av sarkom Sykdom Bløtvevssarkom 1 Antall pasienter Usikre tall, mellom 160 og 300 diagnostiseres årlig
Refusjonsrapport. Vurdering av søknad om forhåndsgodkjent refusjon 2. 12-12-2014 Statens legemiddelverk
 Refusjonsrapport Afinitor (Everolimus) til behandling av avansert hormonreseptorpositiv og HER2/neu-negativ brystkreft i kombinasjon med eksemestan. Vurdering av søknad om forhåndsgodkjent refusjon 2 12-12-2014
Refusjonsrapport Afinitor (Everolimus) til behandling av avansert hormonreseptorpositiv og HER2/neu-negativ brystkreft i kombinasjon med eksemestan. Vurdering av søknad om forhåndsgodkjent refusjon 2 12-12-2014
INVITASJON til forebyggende undersøkelse mot tarmkreft
 MOT TARMKREFT ELSER K FOREBYGGENDE UNDERSØ INVITASJON til forebyggende undersøkelse mot tarmkreft MOT TARMKREFT ELSER K FOREBYGGENDE UNDERSØ Kreftregisteret og Sørlandet Sykehus Kristiansand tilbyr deg
MOT TARMKREFT ELSER K FOREBYGGENDE UNDERSØ INVITASJON til forebyggende undersøkelse mot tarmkreft MOT TARMKREFT ELSER K FOREBYGGENDE UNDERSØ Kreftregisteret og Sørlandet Sykehus Kristiansand tilbyr deg
Erfaringer med blåreseptordningen Elisabeth Bryn Avdelingsdirektør Avdeling for legemiddeløkonomi
 Erfaringer med blåreseptordningen Elisabeth Bryn Avdelingsdirektør Avdeling for legemiddeløkonomi 10.06.2013 Plan 1. Innledning 2. Blåreseptordningen 3. Erfaringer og eksempler 4. Konklusjon Legemiddelpolitiske
Erfaringer med blåreseptordningen Elisabeth Bryn Avdelingsdirektør Avdeling for legemiddeløkonomi 10.06.2013 Plan 1. Innledning 2. Blåreseptordningen 3. Erfaringer og eksempler 4. Konklusjon Legemiddelpolitiske
Denosumab (Xgeva) til forebygging av skjelettrelaterte. voksne med benmetastaser fra solide tumorer. Oppdatering av tidligere helseøkonomisk analyse
 Denosumab () til forebygging av skjelettrelaterte hendelser hos voksne med benmetastaser fra solide tumorer. Oppdatering av tidligere helseøkonomisk analyse 01-10-2014 Statens legemiddelverk 1 Innhold
Denosumab () til forebygging av skjelettrelaterte hendelser hos voksne med benmetastaser fra solide tumorer. Oppdatering av tidligere helseøkonomisk analyse 01-10-2014 Statens legemiddelverk 1 Innhold
Screening kva er forskingsbasert?
 Screening kva er forskingsbasert? Geir Sverre Braut, SUS Sola, 7. september 2017 Grunnkurs D (Forsking i allmennpraksis) Med inspirasjon og ein del lånte plansjar frå professor Lars Vatten, NTNU Læringsutbytte
Screening kva er forskingsbasert? Geir Sverre Braut, SUS Sola, 7. september 2017 Grunnkurs D (Forsking i allmennpraksis) Med inspirasjon og ein del lånte plansjar frå professor Lars Vatten, NTNU Læringsutbytte
Rådsavgjørelse 13.08.07: Klage på markedsføring av Exforge (Amlodipin/Valsartan), Novartis (R1207)
 Rådsavgjørelse 13.08.07: Klage på markedsføring av Exforge (Amlodipin/Valsartan), Novartis (R1207) Saken ble innklaget av AstraZeneca AS Gebyr 50.000,-. Navn på firma som klager: AstraZeneca AS Navn på
Rådsavgjørelse 13.08.07: Klage på markedsføring av Exforge (Amlodipin/Valsartan), Novartis (R1207) Saken ble innklaget av AstraZeneca AS Gebyr 50.000,-. Navn på firma som klager: AstraZeneca AS Navn på
Deres ref. Dato Vår ref. Arkivkode Seksjon/Saksbehandler Petter Foss 15-02-2011 11/01145-3 511.1 Seksjon for legemiddelrefusjon/ Enrique Ji~ez
 Statens legemiddelverk Norwegian Medicines Agency Novartis Norge AS Postboks 237 Økern 0510 OSLO Norge DAGSPOST Deres ref. Dato Vår ref. Arkivkode Seksjon/Saksbehandler Petter Foss 15-02-2011 11/01145-3
Statens legemiddelverk Norwegian Medicines Agency Novartis Norge AS Postboks 237 Økern 0510 OSLO Norge DAGSPOST Deres ref. Dato Vår ref. Arkivkode Seksjon/Saksbehandler Petter Foss 15-02-2011 11/01145-3
Deres ref.: Dato: Vår ref.: Saksbehandler: / Christina Sivertsen
 MSD (NORGE) AS Postboks 458 Brakerøya 3002 Drammen Deres ref.: Dato: Vår ref.: Saksbehandler: 01.06.2018 18/04022-3 Christina Sivertsen REFUSJONSVEDTAK Statens legemiddelverk viser til deres dokumentasjon
MSD (NORGE) AS Postboks 458 Brakerøya 3002 Drammen Deres ref.: Dato: Vår ref.: Saksbehandler: 01.06.2018 18/04022-3 Christina Sivertsen REFUSJONSVEDTAK Statens legemiddelverk viser til deres dokumentasjon
Brystkreft. Informasjon fra Kreftforeningen
 Brystkreft Informasjon fra Kreftforeningen Hensikten med dette faktaarket er å gi en kortfattet, generell informasjon til pasienter, pårørende og andre som er berørte av brystkreft. De det gjelder vil
Brystkreft Informasjon fra Kreftforeningen Hensikten med dette faktaarket er å gi en kortfattet, generell informasjon til pasienter, pårørende og andre som er berørte av brystkreft. De det gjelder vil
Ulike typer screening
 Ulike typer screening Hvordan virker dette på overdiagnostikk? Moderne bildediagnostikk og medisinske tester, for mye av det gode? Mette Kalager Lege, PhD Min bakgrunn Kirurg Sykehuset Telemark, OUS Radiumhospitalet
Ulike typer screening Hvordan virker dette på overdiagnostikk? Moderne bildediagnostikk og medisinske tester, for mye av det gode? Mette Kalager Lege, PhD Min bakgrunn Kirurg Sykehuset Telemark, OUS Radiumhospitalet
Vedlegg II. Endringer til relevante avsnitt i preparatomtale og pakningsvedlegg
 Vedlegg II Endringer til relevante avsnitt i preparatomtale og pakningsvedlegg 1 For preparater som inneholder angiotensinkonverterende enyzymhemmerne (ACEhemmere) benazepril, kaptopril, cilazapril, delapril,
Vedlegg II Endringer til relevante avsnitt i preparatomtale og pakningsvedlegg 1 For preparater som inneholder angiotensinkonverterende enyzymhemmerne (ACEhemmere) benazepril, kaptopril, cilazapril, delapril,
Forslag om nasjonal metodevurdering
 Forslag om nasjonal metodevurdering Viktig informasjon se på dette først! Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Forslag om nasjonal metodevurdering Viktig informasjon se på dette først! Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: / Seksjon for legemiddelomsetning/ Leung Ming Yu
 Wickstrøm & Langkilde ApS Hjulmagervej 4A DK-7100 Velje Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 26.01.2016 15/14643-5 Seksjon for legemiddelomsetning/ Leung Ming REFUSJONSVEDTAK Vi viser til
Wickstrøm & Langkilde ApS Hjulmagervej 4A DK-7100 Velje Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 26.01.2016 15/14643-5 Seksjon for legemiddelomsetning/ Leung Ming REFUSJONSVEDTAK Vi viser til
Forslag om nasjonal metodevurdering
 Forslag om nasjonal metodevurdering Viktig informasjon se på dette først! Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Forslag om nasjonal metodevurdering Viktig informasjon se på dette først! Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Residiv og overlevelse etter brystbevarende behandling av brystkreft370 4
 Originalartikkel Residiv og overlevelse etter brystbevarende behandling av brystkreft370 4 Sammendrag Bakgrunn. Formålet med denne retrospektive studien var å undersøke lokal sykdomskontroll og overlevelse
Originalartikkel Residiv og overlevelse etter brystbevarende behandling av brystkreft370 4 Sammendrag Bakgrunn. Formålet med denne retrospektive studien var å undersøke lokal sykdomskontroll og overlevelse
Deres dato Deres referanse Vår dato Vår referanse Seksjon/saksbehandler Carl Samuelsen /10249 LØ/LR/Leung Ming Yu
 Boehringer Ingelheim Norway KS Postboks 405 1373 Asker Deres dato Deres referanse Vår dato Vår referanse Seksjon/saksbehandler 2015-07-16 Carl Samuelsen 2015-09-28 15/10249 LØ/LR/Leung Ming Yu REFUSJONSVEDTAK
Boehringer Ingelheim Norway KS Postboks 405 1373 Asker Deres dato Deres referanse Vår dato Vår referanse Seksjon/saksbehandler 2015-07-16 Carl Samuelsen 2015-09-28 15/10249 LØ/LR/Leung Ming Yu REFUSJONSVEDTAK
Innføring av nye kreftlegemidler Et likeverdig tilbud i Norge
 Innføring av nye kreftlegemidler Et likeverdig tilbud i Norge Stein Kaasa, prosjektdirektør Kjell M Tveit,avdelingsleder OUS Figur 1. Antall krefttilfeller i Norge, 2000-2009. Med kreftregisterets fremskrivning
Innføring av nye kreftlegemidler Et likeverdig tilbud i Norge Stein Kaasa, prosjektdirektør Kjell M Tveit,avdelingsleder OUS Figur 1. Antall krefttilfeller i Norge, 2000-2009. Med kreftregisterets fremskrivning
Utvalgsstørrelse, styrke
 Utvalgsstørrelse, styrke Lise Lund Håheim DDS, PhD Professor II, Forskerlinjen, UiO Seniorforsker, Nasjonalt kunnskapssenter for helsetjenesten, Oslo Seniorforsker, Institutt for oral biologi, UiO Introduksjonskurset,
Utvalgsstørrelse, styrke Lise Lund Håheim DDS, PhD Professor II, Forskerlinjen, UiO Seniorforsker, Nasjonalt kunnskapssenter for helsetjenesten, Oslo Seniorforsker, Institutt for oral biologi, UiO Introduksjonskurset,
Rotigotin depotplaster (Neupro) I behandlingen av Parkinsons sykdom
 Rotigotin depotplaster (Neupro) I behandlingen av Parkinsons sykdom Oppsummering Rotigotin depotplaster (Neupro)er en non-ergot dopaminagonist, og kan brukes for symptomatisk behandling av Parkinsons sykdom
Rotigotin depotplaster (Neupro) I behandlingen av Parkinsons sykdom Oppsummering Rotigotin depotplaster (Neupro)er en non-ergot dopaminagonist, og kan brukes for symptomatisk behandling av Parkinsons sykdom
Innhold. Insidens av brystkreft, livmorhalskreft og eggstokkreft. Insidens av bryst-, livmorhals- og eggstokkreft. Screening. Overlevelse.
 Innhold Insidens av brystkreft, livmorhalskreft og eggstokkreft Inger Kristin Larsen, PhD, Forsker, Kreftregisteret Insidens av bryst-, livmorhals- og eggstokkreft Screening Overlevelse Årsak Fertilitet
Innhold Insidens av brystkreft, livmorhalskreft og eggstokkreft Inger Kristin Larsen, PhD, Forsker, Kreftregisteret Insidens av bryst-, livmorhals- og eggstokkreft Screening Overlevelse Årsak Fertilitet
Analyser av kostnader og kostnadseffektivitet ved ulike screeningmetoder for tarmkreft
 Analyser av kostnader og kostnadseffektivitet ved ulike screeningmetoder for tarmkreft Eline Aas, Helseøkonomisk Analyse AS 1 Sammendrag Tarmkreft (kreft i tykktarm og endetarm) er blant de hyppigst forekommende
Analyser av kostnader og kostnadseffektivitet ved ulike screeningmetoder for tarmkreft Eline Aas, Helseøkonomisk Analyse AS 1 Sammendrag Tarmkreft (kreft i tykktarm og endetarm) er blant de hyppigst forekommende
Anbefalinger om bruk av HPV vaksine. Berit Feiring Avdeling for vaksine Nasjonalt folkehelseinstitutt
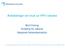 Anbefalinger om bruk av HPV vaksine Berit Feiring Avdeling for vaksine Nasjonalt folkehelseinstitutt FHI anbefaler at HPV-vaksinen innføres i vaksinasjonsprogrammet Anbefalingen fra FHI bygger på flere
Anbefalinger om bruk av HPV vaksine Berit Feiring Avdeling for vaksine Nasjonalt folkehelseinstitutt FHI anbefaler at HPV-vaksinen innføres i vaksinasjonsprogrammet Anbefalingen fra FHI bygger på flere
God helse gode liv Prioriteringer i helsetjenesten. Bjørn-Inge Larsen Helsedirektør
 God helse gode liv Prioriteringer i helsetjenesten Bjørn-Inge Larsen Helsedirektør Helseutgifter per person 1990-2007 ($PPP) 6000 5000 USD 4000 3000 2000 Denmark Finland Norway Sweden 1000 0 1990 1995
God helse gode liv Prioriteringer i helsetjenesten Bjørn-Inge Larsen Helsedirektør Helseutgifter per person 1990-2007 ($PPP) 6000 5000 USD 4000 3000 2000 Denmark Finland Norway Sweden 1000 0 1990 1995
Foreslått utvidet program for testing for genmutasjon og forebyggende fjerning av bryst og eggstokker: Kostnad-nytte-betraktninger
 Foreslått utvidet program for testing for genmutasjon og forebyggende fjerning av bryst og eggstokker: Kostnad-nytte-betraktninger Erik Nord Seniorforsker ved Nasjonalt folkehelseinstitutt Professor i
Foreslått utvidet program for testing for genmutasjon og forebyggende fjerning av bryst og eggstokker: Kostnad-nytte-betraktninger Erik Nord Seniorforsker ved Nasjonalt folkehelseinstitutt Professor i
Diagnostisering av endometriecancer i allmennmedisin
 Diagnostisering av endometriecancer i allmennmedisin PMU 2016 Trine Livik Haugen Lege Lillestrøm Legesenter Kasuistikk - Kvinne, 72 år - Gul utflod i fire måneder. Står på Eviana. GU: Atrofiske forhold.
Diagnostisering av endometriecancer i allmennmedisin PMU 2016 Trine Livik Haugen Lege Lillestrøm Legesenter Kasuistikk - Kvinne, 72 år - Gul utflod i fire måneder. Står på Eviana. GU: Atrofiske forhold.
HØRINGSNOTAT. Endringer i blåreseptforskriften stønad til legemidler for behandling av hepatitt C
 Helse- og omsorgsdepartementet HØRINGSNOTAT Endringer i blåreseptforskriften stønad til legemidler for behandling av hepatitt C April 2015 1. Høringsnotatets hovedinnhold Helse- og omsorgsdepartementet
Helse- og omsorgsdepartementet HØRINGSNOTAT Endringer i blåreseptforskriften stønad til legemidler for behandling av hepatitt C April 2015 1. Høringsnotatets hovedinnhold Helse- og omsorgsdepartementet
Bjørn H. Grønberg PRC & Kreftklinikken, St. Olavs Hospital. European Palliative Care Research Centre (PRC)
 1 Umiddelbar vedlikeholdsbehandling med pemetrexed versus observasjon etterfulgt av andrelinjes behandling med pemetrexed ved progresjon av avansert ikke-småcellet lungekreft en nasjonal fase III studie
1 Umiddelbar vedlikeholdsbehandling med pemetrexed versus observasjon etterfulgt av andrelinjes behandling med pemetrexed ved progresjon av avansert ikke-småcellet lungekreft en nasjonal fase III studie
Mest til skade? Jan Mæhlen og Per-Henrik Zahl. Mammografiscreeningen
 Mammografiscreeningen Mest til skade? I Sverige og Norge har mammografiscreeningen ført til at hyppigheten av brystkreft har økt sterkt i de screenede aldersgruppene, men screeningen har ikke redusert
Mammografiscreeningen Mest til skade? I Sverige og Norge har mammografiscreeningen ført til at hyppigheten av brystkreft har økt sterkt i de screenede aldersgruppene, men screeningen har ikke redusert
Endringer i refusjonslisten 15. november og 1. desember 2015
 Endringer i refusjonslisten 15. november og 1. desember 2015 1. Nye virkestoff A06AH03_1 Naloksegol Refusjonsberettiget bruk: Behandling av opioidindusert forstoppelse hos voksne pasienter når respons
Endringer i refusjonslisten 15. november og 1. desember 2015 1. Nye virkestoff A06AH03_1 Naloksegol Refusjonsberettiget bruk: Behandling av opioidindusert forstoppelse hos voksne pasienter når respons
HPV, celleforandringer og kreft. Av Sveinung Sørbye Overlege, klinisk patologi UNN
 HPV, celleforandringer og kreft Av Sveinung Sørbye Overlege, klinisk patologi UNN Hvorfor får nesten aldri nonner livmorhalskreft? Humant papillomavirus (HPV) Livmorhalskreft skyldes et virus som er seksuelt
HPV, celleforandringer og kreft Av Sveinung Sørbye Overlege, klinisk patologi UNN Hvorfor får nesten aldri nonner livmorhalskreft? Humant papillomavirus (HPV) Livmorhalskreft skyldes et virus som er seksuelt
REFUSJONSVEDTAK FOR JANUVIA I STYRKENE 25 OG 50 MG
 MSD (NORGE) AS Postboks 458 Brakerøya 3002 Drammen Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 08-08-2013 12/07838-18 Seksjon for legemiddelrefusjon/ REFUSJONSVEDTAK FOR JANUVIA I STYRKENE 25 OG
MSD (NORGE) AS Postboks 458 Brakerøya 3002 Drammen Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 08-08-2013 12/07838-18 Seksjon for legemiddelrefusjon/ REFUSJONSVEDTAK FOR JANUVIA I STYRKENE 25 OG
Forskrivning av liraglutid på blå resept etter 2
 Kontrollrapport 2017 Forskrivning av liraglutid på blå resept etter 2 Legers forskrivning Versjon: 1.3 Dato: 12. september 2017 Innhold Sammendrag... 3 1 Bakgrunn og formål... 4 1.1 Formålet med kontrollen...
Kontrollrapport 2017 Forskrivning av liraglutid på blå resept etter 2 Legers forskrivning Versjon: 1.3 Dato: 12. september 2017 Innhold Sammendrag... 3 1 Bakgrunn og formål... 4 1.1 Formålet med kontrollen...
Livstilsendringer og kreft; viktig å tenke på det? Ida Bukholm
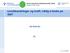 Livstilsendringer og kreft; viktig å tenke på det? Ida Bukholm JA Hvofor? Hoved mål; Best mulig behandling for pasientene EKSEMPEL KREFT I TYKKTARM OG BRYSTKREFT 2 Nødvendig med helsefremmende/forebyggende
Livstilsendringer og kreft; viktig å tenke på det? Ida Bukholm JA Hvofor? Hoved mål; Best mulig behandling for pasientene EKSEMPEL KREFT I TYKKTARM OG BRYSTKREFT 2 Nødvendig med helsefremmende/forebyggende
Bruk av Real World Data for evaluering av legemidler. Workshop Kreftregisteret 16 Desember 2016 Per H Fuglerud, Statistiker
 Bruk av Real World Data for evaluering av legemidler Workshop Kreftregisteret 16 Desember 2016 Per H Fuglerud, Statistiker Tema RWD og RWE og hva det brukes til på legemiddelområdet i dag Forskjeller mellom
Bruk av Real World Data for evaluering av legemidler Workshop Kreftregisteret 16 Desember 2016 Per H Fuglerud, Statistiker Tema RWD og RWE og hva det brukes til på legemiddelområdet i dag Forskjeller mellom
Forslag til nasjonal metodevurdering
 Forslagsskjema, Versjon 2 17. mars 2014 Forslag til nasjonal metodevurdering Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Forslagsskjema, Versjon 2 17. mars 2014 Forslag til nasjonal metodevurdering Innsendte forslag til nasjonale metodevurderinger vil bli publisert i sin helhet. Dersom forslagsstiller mener det er nødvendig
Refusjonsrapport insulin glulisine (Apidra) til behandling av diabetes
 Refusjonsrapport insulin glulisine (Apidra) til behandling av diabetes 1 Oppsummering Formål: Å vurdere insulin glulisine (Apidra) for pliktmessig refusjon etter forskrift av 18. april 1997 nr. 330 om
Refusjonsrapport insulin glulisine (Apidra) til behandling av diabetes 1 Oppsummering Formål: Å vurdere insulin glulisine (Apidra) for pliktmessig refusjon etter forskrift av 18. april 1997 nr. 330 om
Kunnskapsbasert HPV vaksinering Kan motstanden lenger forsvares? Ingvil Sæterdal, forsker
 Kunnskapsbasert HPV vaksinering Kan motstanden lenger forsvares? Ingvil Sæterdal, forsker Nytt tiltak Ikke nyttig Metodevurdering Entusiasme Overbevisning Press Nyttig Helsetjenestetilbud 31. august 2015
Kunnskapsbasert HPV vaksinering Kan motstanden lenger forsvares? Ingvil Sæterdal, forsker Nytt tiltak Ikke nyttig Metodevurdering Entusiasme Overbevisning Press Nyttig Helsetjenestetilbud 31. august 2015
Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 24.04.2014 14/00932-4 Seksjon for legemiddelrefusjon/ Helle Endresen/ Pilar Martin Vivaldi
 TAKEDA NYCOMED AS Postboks 205 1372 Asker Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 24.04.2014 14/00932-4 Seksjon for legemiddelrefusjon/ Helle Endresen/ Pilar Martin Vivaldi REFUSJONSVEDTAK Vi
TAKEDA NYCOMED AS Postboks 205 1372 Asker Deres ref.: Dato: Vår ref.: Seksjon/saksbehandler: 24.04.2014 14/00932-4 Seksjon for legemiddelrefusjon/ Helle Endresen/ Pilar Martin Vivaldi REFUSJONSVEDTAK Vi
PREPARATOMTALE. Mørk gul, standard konveks rund, filmdrasjert tablett preget med 93 på en side og B1 på den andre siden.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Letrozol Teva 2,5 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder 2,5 mg letrozol. Hjelpestoffer med kjent
PREPARATOMTALE 1. LEGEMIDLETS NAVN Letrozol Teva 2,5 mg tabletter, filmdrasjerte 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver filmdrasjerte tablett inneholder 2,5 mg letrozol. Hjelpestoffer med kjent
Rådsavgjørelse 20. april 2015: Klage på reklame for Zytiga <<Janssen-Cilag>> R1815
 Rådsavgjørelse 20. april 2015: Klage på reklame for Zytiga R1815 Saken ble innklaget av Rådets sekretariat. Gebyr kr 50.000,- Navn på firma som klager: Rådets sekretariat Navn på firma
Rådsavgjørelse 20. april 2015: Klage på reklame for Zytiga R1815 Saken ble innklaget av Rådets sekretariat. Gebyr kr 50.000,- Navn på firma som klager: Rådets sekretariat Navn på firma
Kolesterolsenkende behandling en oppdatering
 Kolesterolsenkende behandling en oppdatering Steinar Madsen medisinsk fagdirektør og avtalespesialist Helse Sør-Øst Legemiddelkostnader i Norge Milliarder NOK 30,0 25,0 Nye legemidler, nye behandlingsmuligheter
Kolesterolsenkende behandling en oppdatering Steinar Madsen medisinsk fagdirektør og avtalespesialist Helse Sør-Øst Legemiddelkostnader i Norge Milliarder NOK 30,0 25,0 Nye legemidler, nye behandlingsmuligheter
Overlevelsesdata; langtidsoverlevelse på ny kreftbehandling
 Overlevelsesdata; langtidsoverlevelse på ny kreftbehandling Giske Ursin Direktør Kreftoverlevere hvem er det? En som har fått en kreftdiagnose og fremdeles er i live = fra den dagen diagnosen stilles til
Overlevelsesdata; langtidsoverlevelse på ny kreftbehandling Giske Ursin Direktør Kreftoverlevere hvem er det? En som har fått en kreftdiagnose og fremdeles er i live = fra den dagen diagnosen stilles til
Detaljerte forklaringer av begreper og metoder.
 Appendiks til Ingar Holme, Serena Tonstad. Risikofaktorer og dødelighet oppfølging av Oslo-undersøkelsen fra 1972-73. Tidsskr Nor Legeforen 2011; 131: 456 60. Dette appendikset er et tillegg til artikkelen
Appendiks til Ingar Holme, Serena Tonstad. Risikofaktorer og dødelighet oppfølging av Oslo-undersøkelsen fra 1972-73. Tidsskr Nor Legeforen 2011; 131: 456 60. Dette appendikset er et tillegg til artikkelen
Cancer in Norway 2014
 Cancer in Norway 2014 Cancer incidence, mortality, survival and prevalence in Norway Norsk sammendrag CiN 2014 Image: Shutterstock Hvordan forstå krefttall Kreft er blant våre mest vanlige sykdommer, og
Cancer in Norway 2014 Cancer incidence, mortality, survival and prevalence in Norway Norsk sammendrag CiN 2014 Image: Shutterstock Hvordan forstå krefttall Kreft er blant våre mest vanlige sykdommer, og
RAPPORT. Legers forskrivning på blå resept. Kontroll 2-2015
 RAPPORT Legers forskrivning på blå resept Kontroll 2-2015 Legens reservasjon mot generisk bytte av legemidler 2014/2015 SAMMENDRAG... 3 1 INNLEDNING... 4 1.1 BAKGRUNN FOR KONTROLLEN... 4 1.2 VILKÅR FOR
RAPPORT Legers forskrivning på blå resept Kontroll 2-2015 Legens reservasjon mot generisk bytte av legemidler 2014/2015 SAMMENDRAG... 3 1 INNLEDNING... 4 1.1 BAKGRUNN FOR KONTROLLEN... 4 1.2 VILKÅR FOR
