Retningslinjer for håndtering av cytostatika utenfor sykehus
|
|
|
- Josef Engen
- 8 år siden
- Visninger:
Transkript
1 Retningslinjer for håndtering av cytostatika utenfor sykehus IK Statens helsetilsyns veiledningsserie 8/1995. Forord Behandling av kreftsykdommer med cytostatika kan foregå utenfor sykehus slik at pasienter kan få pleie og behandling i eget hjem, ev. ved legesenter/hos lege eller i sykehjem nær hjemstedet. Det er viktig at pasienter og pårørende kan være trygge på at behandlingen skjer på en like sikker måte som i sykehus. En forutsetning for dette er at sykepleier/lege mestrer håndtering av cytostatika. Ifølge forskrift om legemiddelforsyning m.v. i den kommunale helsetjeneste av 18. november 1987 (1) skal ikke tilvirkning av legemidler foregå i den kommunale helsetjeneste. Unntatt fra bestemmelsene er preparater som på grunn av kort holdbarhet skal tilberedes umiddelbart før bruk eller for meget kort tids forbruk (tørrampuller o.l.), samt tilsetning av sterilt legemiddel til infusjonsposer umiddelbart før bruk ( 7). Tilberedning av cytostatika til bruk i kommunehelsetjenesten skal derfor, såsant det er praktisk mulig, gjøres i apotek for å sikre kvaliteten av tilberedningen. Imidlertid har ferdig tilberedte cytostatikaoppløsninger ofte meget kort holdbarhet, og da kan det bli nødvendig at tilberedningen foretas ved den aktuelle deltjeneste. Dessuten har Direktoratet for arbeidstilsynet fastsatt forskrifter om håndtering av cytostatika av 18. desember Statens helsetilsyn har erfart at håndtering av cytostatika utenfor sykehus ofte foregår uten nødvendige hjelpemidler og uten at spesiell opplæring er gitt. I primærhelsetjenesten har retningslinjer for slik håndtering i sykehjem vært etterlyst. Håndtering av cytostatika omfatter både tilberedning av bruksferdig preparat og administrasjon av preparatet til pasient, og retningslinjene omfatter derfor begge deler. Statens helsetilsyn ba Norske Sykehusfarmasøyters Forening om bistand til dette arbeidet. Faggruppen for cytostatika i Norske Sykehusfarmasøyters Forening utarbeidet et forslag til retningslinjer. Med i faggruppen var sykehusfarmasøytene Gunn Fredriksen, Regionsykehuset i Trondheim Kirsten Myhr, Regionsykehuset i Trondheim Kari Smørdal, Sykehusapoteket i Molde Forslaget ble sendt på høring og er deretter videre bearbeidet av apoteker Helge Nordahl ved Radiumhospitalets apotek i samarbeid med Statens helsetilsyn. Statens helsetilsyn takker Norske Sykehusfarmasøyters Forening og Radiumhospitalets apotek for vel utført arbeid.
2 Statens helsetilsyn håper disse retningslinjene vil bidra til sikker håndtering av cytostatika utenfor sykehus. Anne Alvik helsedirektør Hva er cytostatika? Cytostatika er legemidler som brukes i behandling av kreftsykdommer. I noen tilfelle brukes de også ved reumatiske lidelser og ved hudsykdommer. De tilhører ATC-gruppe L01 (Felleskatalogens gule sider). Cytostatika skader eller dreper kreftceller ved å påvirke arvestoffet i cellene. Siden legemidlene virker på alle celler i vekst, rammer de også normale celler og kan gi alvorlige bivirkninger. Viktig! Alle som har ansvar for eller konkret står overfor oppgaven å skulle tilberede eller administrere cytostatika til pasienter, skal ha fått nødvendig opplæring (2) og bør - ha studert disse retningslinjene - følge Arbeidstilsynets forskrifter om håndtering av cytostatika (2) - ha tilgjengelig håndboken "Cytostatika. Medikamentell kreftbehandling", heretter kalt håndboken (3) - ha og bruke personlig verneutstyr (se Personlig verneutstyr) - ha tenkt over og tatt forholdsregler for eventuelle problemer underveis. Regelverk og risiko Forskrifter om håndtering av cytostatika Direktoratet for arbeidstilsynet har gitt egne forskrifter for håndtering av cytostatika (2). Forskriftene inneholder bl.a. - krav til utstyr og lokaler for istandgjøring av pasientdoser - krav til personlig verneutstyr - krav til avfallshåndtering - krav til opplæring for personale som håndterer cytostatika - forbud mot arbeid med cytostatika for gravide kvinner og arbeidstakere med relevant legeattest - krav til registrering av personale som regelmessig arbeider med cytostatika. Risiko for personalet Risikoen for personalet som håndterer cytostatika, er størst ved istandgjøring og administrasjon av preparater til injeksjon/infusjon. Søl på huden og innånding av aerosolet (se side 10) kan gi systemvirkninger og må unngås. Flere cytostatika er dessuten sterkt hudirriterende og kan skade ubeskyttet hud. Cytostatika kan være kreftfremkallende og kan gi fosterskader i de doser som brukes i behandling. Det er kjent at yrkesmessig håndtering av cytostatika, uten adekvate vernetiltak, kan medføre skader på arveanlegg. Risikoen for helseskader er derimot minimale hvis
3 personalet beskytter seg selv og omgivelsene mot kontakt med stoffene (jf. Forskrifter om håndtering av cytostatika). Forbud mot arbeid med cytostatika Gravide kvinner og arbeidstakere med legeattest om at de midlertidig eller permanent ikke skal arbeide med cytostatika, skal overføres til arbeid der de ikke håndterer eller er utsatt for cytostatika (Forskrifter om håndtering av cytostatika, 5). Opplæring og informasjon Alt personale som skal arbeide med cytostatika, skal få hensiktsmessig opplæring og nødvendig informasjon om ulike sider ved håndtering av disse stoffene. Med tilstrekkelig kunnskap og ferdighet kan cytostatika håndteres forsvarlig og trygt. Forskrifter om håndtering av cytostatika, 3, stiller krav til arbeidsgiveren om å gi nødvendig opplæring. Tilsynsfarmasøyt i kommunene eller farmasøyter på det lokale apotek kan gi eller formidle råd om cytostatikahåndtering. Hospitering på sykehusapotek og kontakt med kreftsykepleier på sykehus kan også være en del av opplæringen. Den som skal ha ansvaret for å administrere cytostatika, må ha erfaring med venepunksjon for å redusere faren for vevsskade ved infusjon/injeksjon. Det kreves også kunnskaper om virkning/bivirkninger for å kunne svare på spørsmål fra pasient og pårørende, og mestre situasjoner som kan oppstå i forbindelse med virkning/bivirkninger av legemidlene. Forordning av cytostatika i samarbeid med sykehus Samarbeid med sykehuset Når pasienter skal ha fortsatt cytostatikabehandling i regi av primærhelsetjenesten etter utskrivning fra sykehus, er det både ønskelig og nødvendig at primærhelsetjenesten har kontakt med utskrivende avdeling i forbindelse med behandlingen. Spørsmål som angår tilberedning og administrasjon av cytostatika kan i de fleste tilfelle også besvares av vedkommende sykehusapotek, farmasøytiske avdeling eller tilsynsfarmasøyt. Forordning av cytostatika til pasient Det skal foreligge skriftlig ordinasjon fra lege til den enkelte pasient, med angivelse av cytostatikum, dose, administrasjonsmåte og eventuell fortynningsvæske (f.eks. natriumklorid 9 mg/ml eller glukose 50 mg/ml) og mengde av denne. Se etter om det finnes anvisninger i epikrisen fra sykehuset. Ved tvil, se kapitlene om håndtering og administrasjon av cytostatika i håndboken (3), Felleskatalogen eller pakningsvedlegg, eller kontakt sykehuset. For de preparater der det kreves kontroll av blodverdier før neste dose, må blodprøve være tatt og svar foreligge før tilberedning og administrasjon av cytostatika foretas. Kan preparatet fås bruksferdig fra apotek? Som nevnt i forordet, bør tilberedning av bruksferdig cytostatika oppløsning utføres i apotek. Alle selvstendige apotek kan levere cytostatikakurer. Når parenteral cytostatikabehandling skal gjennomføres i primærhelsetjenesten, bør pasientens utskrivende avdeling, ev. via sykehusapoteket eller sykehusets farmasøytiske avdeling, ta kontakt med det lokale apotek, ev. det sykehusapotek som ligger nærmest pasientens bosted, i god tid. Enkelte apotek kan trenge tid for å forberede levering av bruksferdig preparat første gang. Forskrifter om håndtering av cytostatika (2) skal følges.
4 Levering fra apotek bør foretrekkes dersom det er praktisk mulig. Ferdig tilberedte cytostatikakurer har kort holdbarhet, vanligvis ett døgn eller kortere. Tidspunkt og leveringsmåte må derfor avtales nøye. Hvis levering av bruksferdig preparat ikke lar seg gjøre på denne måten, må arbeidet utføres ved den aktuelle deltjenesten av lege eller sykepleier umiddelbart før preparatet skal gis. Den legen som er ansvarlig for å organisere legetjenesten, er også medisinskfaglig ansvarlig for legemiddelforsyningen, herunder tilberedning av legemidler (se 1, 2). Disse retningslinjene fra Statens helsetilsyn bør følges. To personer bør kontrollere og signere for utregning og tilberedning. Tilberedning av cytostatika Lokaler og utstyr for tilberedning Eget rom eller avtrekksbenk er ikke påkrevet når cytostatika håndteres sjelden (Forskrifter om håndtering av cytostatika, 1). Tilberedningen bør imidlertid skje på et skjermet sted uten trekk (ikke foran åpent vindu!), helst med håndvask i nærheten. Arbeidsbenken bør dekkes med et underlag med absorberende overside og vanntett underside. Stikksikker beholder for kanyler og ampuller bør stå klar, likeledes plastposer og kartonger for annet sikkerhetsavfall. Utstyr til bruk ved tilberedning inkluderer vanligvis overføringskanyler ("transfer needle"), infusjonsvæsker (natriumklorid 9 mg/ml, glukose 50 mg/ml og sterilt vann) i poser av ulike størrelser, sprøyter i passende dimensjoner, opptrekkskanyler 19 G (ikke grovere), sterile kompressor og spritputer. Ved opptrekk fra glassampuller bør det brukes filter, gjerne bøyelige filterstrå. Sprøyter bør fortrinnsvis være av polypropylen og ha luer lock fatning. Infusjonssett bør være av Y-type eller fireveissett med filter. Settet bør fylles med infusjonsvæske fra posen, ev. fra et sideløpende natriumkloriddrypp, før cytostatika tilsettes. Apoteket har oversikt over og kan skaffe aktuelt utstyr. Personlig verneutstyr Ved tilberedning av cytostatika må plasthansker ikke brukes. Bruk tykke latexhansker, skjorte eller frakk med lange ermer og tilsittende mansjetter, eventuelt spesielle, vannavstøtende armbeskyttere. Ved arbeid utenfor sikkerhetsbenk bør det i tillegg brukes vernebriller og åndedrettsvern (maske godkjent for bruk mot faste og væskeformige partikler). Operasjonsmunnbind gir ikke tilstrekkelig beskyttelse! Hansker bør skiftes minst hver halvtime. Etter bruk vrenges hanskene av og legges rett i avfallspose. Armbeskyttere kastes. Frakk legges i vanlig vask. Personlig verneutstyr som har vært brukt ved tilberedning eller administrasjon av cytostatika, skal tas av rett etter bruk og ikke brukes andre steder. Tilberedning av cytostatika Avsnittet vil bare ta for seg tilberedning for korttidsinfusjon ("minibag") og klargjøring av sprøyte. Administrasjon av preparater eller doser som krever store væskevolum vil normalt ikke være aktuelt utenfor sykehus. Sett frem alt nødvendig utstyr før tilberedningen starter.
5 Overføring av cytostatikaoppløsning til minibag Cytostatikaoppløsningen kan lettest overføres til posen ved hjelp av sprøyte. Posene er elastiske og tillater en viss overfylling. Elastisiteten varierer med posetypen, slik at det kan være greit å ha en øvre grense for overfylling på ca 10%. Hvis ekstravolumet blir for stort, må det først tas noe væske ut av posen. Mengden som skal overføres til posen beregnes slik: Dose (mg) = Mengde (ml) Konsentrasjon i hetteglass (mg/ml) Eksempel: Det skal tas ut en dose på 750 mg 5-fluorouracil av en oppløsning med styrke 50 mg/ml. Spørsmål: Hvor mange ml skal tas ut for å få 750 mg fluorouracil? Regn ut mengden slik: 750 mg 50 mg/ml = 15 ml Svar: 15 ml oppløsning inneholder 750 mg 5fluorouracil. Overføring av cytostatikatørrstoff til minibag Når hele innholdet i et hetteglass skal overføres til minibag, gjøres dette lettest ved hjelp av overføringskanyle. Selv om overføringskanylen er lett å bruke, kan det bli søl også med denne. Uerfarne brukere anbefales derfor å øve på overføringsteknikken først (pose og hetteglass med saltvann eller lignende). Studèr veiledningen som følger med overføringskanylen. Dersom bare deler av tørrstoffmengden i et hetteglass skal overføres, anbefales følgende fremgangsmåte: Ta riktig mengde oppløsningsvæske ut fra posen med sprøyte og løs opp innholdet i hetteglasset til anbefalt konsentrasjon (se pakningsvedlegget). Mengden som så skal overføres til posen beregnes slik: Dose (mg) = Mengde (ml) Konsentrasjon i hetteglass (mg/ml) Eksempel: Det skal tas ut en dose på 40 mg cytarabin fra et hetteglass med 100 mg tørrstoff. Fremgangsmåte: Løs alt tørrstoffet i 5 ml natriumkloridoppløsning fra minibagen til en styrke på 20 mg/ml. Spørsmå: Hvor mange ml skal tas ut for å få 40 mg cytarabin? Regn ut mengden slik: 450 mg 20 mg/ml = 2 ml Svar: 2 ml oppløsning inneholder 40 mg cytarabin.
6 Aerosoldannelse Når væske presses gjennom en trang åpning, f.eks. mellom gummipropp og utsiden av en kanyle, vil den dele seg i ørsmå dråper aerosoler som kan holde seg svevende i luften i lang tid. Slike lekkasjer skjer ofte, men oppdages langt fra alltid. Problemet kan reduseres ved hensiktsmessig arbeidsmåte: unngå å lage for stort trykk eller trykkforskjell når væske overføres. La luft og væske bytte plass i porsjoner unngå å perforere hetteglasspropper mange ganger ved ny perforering, bytt stikksted fang opp mulige aerosoler med sterile kompresser når kanylen stikkes inn i eller tas ut av hetteglass og pose ved å holde sprøytespissen i kompressen. Forholdsregler ved søl av cytostatika Søl på huden Skyll straks med mye vann, ev. såpevann. Sprut i øynene Skyll straks med mye vann eller natriumklorid 9 mg/ml. Kontakt øyelege. Søl på gulv, benker etc Tørk straks opp med engangskluter. Vask deretter med såpevann. Engangsklutene behandles som risikoavfall. Bruk tykke hansker, ev. to engangshansker utenpå hverandre. Plasthansker bør ikke brukes. Administrasion av cytostatika Administrasjon av cytostatika til pasient Den som skal administrere cytostatika, må ha erfaring med venepunksjon. Normalt er det legens ansvar å administrere intravenøs cytostatikabehandling. Hvis sykepleiere skal administrere cytostatika utenom sykehus, skal de få tilbud om opplæring. Sykepleier som ikke har hatt nødvendig opplæring, skal ikke administrere cytostatika. Den som gir injeksjon eller infusjon av cytostatika, bør benytte hansker. Intravenøs administrasjon ved infusjon er den mest brukte og den tryggeste måten å gi cytostatika på. Intravenøs administrasjon kan også gis ved injeksjon. Dette vil i praksis si korttidsinfusjon med minibag eller bolusinjeksjon med sprøyte. Korttidsinfusjon med minibag Dette er den mest brukte måten for å administrere cytostatika. Administrasjonen foregår i et "lukket" system, og det har vist seg at legemidlene tolereres godt av pasientene når de gis på denne måten. Følgende prosedyre kan benyttes: 1. Velg en storkalibret vene, fortrinnsvis på underarmen. Legg inn venekanyle. 2. Legg en kompress rundt injeksjonsstedet for å unngå søl på pasientens hud. 3. Heng opp natriumklorid 9 mg/ml ( ml) med Ysett. La denne gå inn med en hastighet på ca 500 ml/30 min og kontroller samtidig at væsken ikke går ekstravasalt. 4. Koble cytostatika i minibag til Ysettets andre gren. Natriumkloridinfusjonen kan stoppes midlertidig eller gå parallelt med legemidlet. 5. Når cytostatikainfusjonen er ferdig, skylles det etter med resten av natriumkloridløsningen. 6. Hvis flere cytostatika skal gis i samme kur, vil bruk av 4-grenet infusjonssett gi minst risiko
7 for søl. Det skylles med natriumklorid 9 mg/ml mellom hvert cytostatikum. Alternativt benyttes Ysett og bytte av poser etter at sidegrenen er skyllet med natriumkloridløsning. Bolusinjeksjon med sprøyte Denne måten å gi cytostatika på er ikke så vanlig lenger, men hvis metoden benyttes, bør det henges opp et nøytralt drypp (natriumklorid 9 mg/ml) slik det er beskrevet ovenfor. Cytostatika injiseres da i gummimuffen på infusjonssettet mens infusjonen går fritt (vanlig, enkelt infusjonssett). Etter at et cytostatikum er injisert, skylles det etter med resten av infusjonsvæsken. Intramuskulær injeksjon Intramuskulær injeksjon kan benyttes for visse cytostatika som ikke er vevsirriterende. Undersøk risikoen før injeksjon settes. Se håndboken (3) og Felleskatalogen. Subkutan injeksjon Subkutan injeksjon kan brukes for cytarabin. Ekstravasasjon av cytostatika Noen cytostatika er så vevsirriterende at infusjon/injeksjon utenfor venen (ekstravasasjon) kan medføre alvorlige skader. Det er derfor viktig å observere pasienten nøye og forvisse seg om at injeksjonen/infusjonen går intravenøst som den skal. Tegn på ekstravasasjon - sviende smerte rundt innstikkstedet - lokal hevelse - lokal rødflammethet i huden - stagnasjon av dråpetakt For nærmere råd og anvisninger se håndboken (3) s og tabell s Instillasjon av cytostatika i blæren Noen cytostatika kan brukes til lokalbehandling ved blærecancer. Instillasjon av et cytostatikum i blæren og tapping etter avsluttet behandling, bør foregå i et mest mulig lukket system for å unngå søl. Legemidlet tilberedes i en delvis tømt infusjonspose på 250 eller 500 ml, med plass til urin ved tømming av blæren. Posen kobles til pasientens kateter ved hjelp av en spesiell pose kateterkobling, og legemidlet presses inn i blæren. Kateteret klemmes av, men posen beholdes tilkoblet. Etter foreskrevet behandlingstid åpnes kateterklemmen og løsningen tømmes fra blæren til posen. Posen destrueres som risikoavfall. Cytostatika til oralt bruk Cytostatikapreparater til oralt bruk svelges hele med minst ett glass vann. Direkte hudkontakt bør unngås. Tabletter bør ikke knuses eller deles, kapsler ikke åpnes. Se håndboken (3), tabell s Avfall
8 Håndtering av avfall som har vært i kontakt med cytostatika Som cytostatikaavfall regnes legemiddelrester og alt utstyr som har vært brukt ved tilberedning og administrasjon av cytostatika. Ved håndtering av avfallet må det brukes latex engangshansker. Avfallet fordeles mellom kanylebøtter el.lign. og solide plastposer, f.eks. store Iynlåsposer som klemmes igjen. Luften klemmes ikke ut av posen før den lukkes. Alt avfall av denne typen bør helst samles i kartonger som merkes tydelig med "Cytostatika avfall" og sendes til forbrenning ved høy temperatur (>800 ). Avfallet bør fjernes snarest mulig fra arbeidsstedet. Dersom forbrenning ikke lar seg gjøre, bør større rester av cytostatika, f.eks. delvis brukte legemiddelglass og kurer som ikke er gitt, samles for seg, emballeres og merkes som angitt ovenfor og sendes til nærmeste sykehus eller apotek for destruksjon. Mindre rester, som f.eks. infusjonssett, tomme poser, hansker, tomme legemiddelglass og kanylebøtter, pakkes i plast og kasseres som risikoavfall. Håndtering av utskillelsesprodukter fra pasient Urin, oppkast og avføring fra pasienter som får cytostatika, kan innholde legemidler i aktiv form eller som nedbrytningsprodukter. Mengden cytostatika som skilles ut, avhenger av hvilket stoff som er gitt og dosens størrelse. Dosene som gis utenfor sykehus er moderate, og det går gjerne lang tid mellom hver cytostatikakur. Urin, avføring og oppkast representerer derfor normalt ingen risiko, men personalet bør bruke hansker og maske ved mulig kontakt med utskillelsesprodukter fra pasient som har fått cytostatika. Bekken og urinflasker må tømmes med en gang. Unngå at urinflasker og bekken blir stående utildekket. Litteratur som bør være tilgjengelig (1)Forskrift om legemiddelforsyning m.v. i den kommunale helsetjeneste fastsatt av Helsedirektoratet, 18. november Endret ved Sosialdepartementets vedtak av 21. januar (2) Forskrifter om håndtering av cytostatika. Direktoratet for arbeidstilsynet, 18. desember 1980, med endringer, senest 22. mars (3) Cytostatika. Medikamentell kreftbehandling. Institutt for farmakoterapi og Den Norske Kreftforening. 5. utgave Fås ved henvendelse til Norsk Medisinaldepot. (4) Felleskatalog over farmasøytiske spesialpreparater, nyeste utgave.felleskatalogen A/S, Oslo. (5) Norsk legemiddelhåndbok for helsepersonell, nyeste utgave.norsk legemiddelhåndbok I/S, Oslo. (6) Kirsten Myhr. Cytostatika. Håndtering og administrasjon. 2. utgave l991. Fås ved henvendelse til Pharmacia AS.
TRYGG INJEKSJON OG INFUSJONSPRAKSIS
 TRYGG INJEKSJON OG INFUSJONSPRAKSIS Farmasøyt Merethe Nilsen og farmasøyt Marianne Matre November 2017 Legemiddelhåndteringsforskriften 8 Tilberedning av legemidler skal skje på en forsvarlig måte og i
TRYGG INJEKSJON OG INFUSJONSPRAKSIS Farmasøyt Merethe Nilsen og farmasøyt Marianne Matre November 2017 Legemiddelhåndteringsforskriften 8 Tilberedning av legemidler skal skje på en forsvarlig måte og i
REKONSTITUERING, DOSERING OG ADMINISTRASJON
 KORREKT REKONSTITUERING FOR S.C. OG I.V. ADMINISTRASJON VELCADE (bortezomib) 3,5 mg pulver til oppløsning for injeksjon er tilgjengelig som intravenøs eller subkutan administrasjon. Kun til subkutan eller
KORREKT REKONSTITUERING FOR S.C. OG I.V. ADMINISTRASJON VELCADE (bortezomib) 3,5 mg pulver til oppløsning for injeksjon er tilgjengelig som intravenøs eller subkutan administrasjon. Kun til subkutan eller
Stell og observasjon av innstikksted samt skifte av treveiskran skal dokumenteres. Tilkobling til kateter Bruk av aseptisk teknikk og sterile hansker
 KORTTIDS SVK VOKSEN KAPITTEL FRA PROSEDYRE 14575: Sentrale venekatetre håndtering og stell Nivå 1 prosedyre for St Olavs Hospital. Gjelder fra 01.04.2014 utgår 01.04.2019. Korttids SVK voksne To ulike
KORTTIDS SVK VOKSEN KAPITTEL FRA PROSEDYRE 14575: Sentrale venekatetre håndtering og stell Nivå 1 prosedyre for St Olavs Hospital. Gjelder fra 01.04.2014 utgår 01.04.2019. Korttids SVK voksne To ulike
Tilberedning og injeksjon
 Se s. 2 for anbefalt dosering Tilberedning og injeksjon qilaris 150 mg pulver for oppløsning til injeksjon Veiledning for helsepersonell om behandling av urinsyregiktanfall som ikke responderer på standardbehandling
Se s. 2 for anbefalt dosering Tilberedning og injeksjon qilaris 150 mg pulver for oppløsning til injeksjon Veiledning for helsepersonell om behandling av urinsyregiktanfall som ikke responderer på standardbehandling
Tilberedning og injeksjon
 Se s. 2 og 10 for anbefalt dosering Tilberedning og injeksjon qilaris 150 mg pulver til injeksjonsvæske, oppløsning Veiledning for pasienter og helsepersonell om klargjøring og administrering av ILARIS
Se s. 2 og 10 for anbefalt dosering Tilberedning og injeksjon qilaris 150 mg pulver til injeksjonsvæske, oppløsning Veiledning for pasienter og helsepersonell om klargjøring og administrering av ILARIS
RoActemra for Systemisk Juvenil Idiopatisk Artritt (sjia) VEILEDER FOR DOSERING OG ADMINISTRASJON - TRINN FOR TRINN
 Til sykepleier - Veileder for dosering og administrasjon RoActemra for Systemisk Juvenil Idiopatisk Artritt (sjia) VEILEDER FOR DOSERING OG ADMINISTRASJON - TRINN FOR TRINN En veiledning som skal hjelpe
Til sykepleier - Veileder for dosering og administrasjon RoActemra for Systemisk Juvenil Idiopatisk Artritt (sjia) VEILEDER FOR DOSERING OG ADMINISTRASJON - TRINN FOR TRINN En veiledning som skal hjelpe
Tilberedning og injeksjon
 Se s. 2, 10 og 11 for dosering voksne og barn Tilberedning og injeksjon qilaris 150 mg pulver for oppløsning til injeksjon Veiledning for pasienter og helsepersonell om klargjøring og administrering av
Se s. 2, 10 og 11 for dosering voksne og barn Tilberedning og injeksjon qilaris 150 mg pulver for oppløsning til injeksjon Veiledning for pasienter og helsepersonell om klargjøring og administrering av
Natriumklorid Fresenius Kabi 9 mg/ml, oppløsningsvæske til parenteral bruk
 1. LEGEMIDLETS NAVN 1 Natriumklorid Fresenius Kabi 9 mg/ml, oppløsningsvæske til parenteral bruk 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 ml Natriumklorid 9 mg/ml inneholder: Natriumklorid Vann til
1. LEGEMIDLETS NAVN 1 Natriumklorid Fresenius Kabi 9 mg/ml, oppløsningsvæske til parenteral bruk 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 ml Natriumklorid 9 mg/ml inneholder: Natriumklorid Vann til
Vær sikker på at dyret har gjenvunnet normale svelgereflekser før det tilbys fôr og drikke.
 1. VETERINÆRPREPARATETS NAVN Sedastop vet. 5 mg/ml injeksjonsvæske, 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 ml inneholder: Virkestoff: Atipamezol 4,27 mg (tilsv. 5,0 mg atipamezolhydroklorid) Hjelpestoff:
1. VETERINÆRPREPARATETS NAVN Sedastop vet. 5 mg/ml injeksjonsvæske, 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 ml inneholder: Virkestoff: Atipamezol 4,27 mg (tilsv. 5,0 mg atipamezolhydroklorid) Hjelpestoff:
Tilkobling til kateter Bruk av aseptisk teknikk og sterile hansker
 KORTTIDSKATETER BARN KAPITTEL FRA PROSEDYRE 14575: Sentrale venekatetre håndtering og stell Nivå 1 prosedyre for St Olavs Hospital. Gjelder fra 01.04.2014 utgår 01.04.2019. Korttids SVK barn To ulike metoder
KORTTIDSKATETER BARN KAPITTEL FRA PROSEDYRE 14575: Sentrale venekatetre håndtering og stell Nivå 1 prosedyre for St Olavs Hospital. Gjelder fra 01.04.2014 utgår 01.04.2019. Korttids SVK barn To ulike metoder
Tilvirkning i apotek av adenosin til parenteral bruk
 Temarapport fra tilsynsavdelingen Rapport 2006-2 Saksnummer 200509071 Utarbeidet av legemiddelinspektør Jørgen Huse Tilvirkning i apotek av adenosin til parenteral bruk 1. Bakgrunn - formål Apotek har
Temarapport fra tilsynsavdelingen Rapport 2006-2 Saksnummer 200509071 Utarbeidet av legemiddelinspektør Jørgen Huse Tilvirkning i apotek av adenosin til parenteral bruk 1. Bakgrunn - formål Apotek har
NLSH 2006. Bodil Stien Haugene, NLSH 2006
 BASISKURS I LEGEMIDDELHÅNDTERING NLSH 2006 Hvordan finne prosedyren i Doc Map Pulsen Håndbøker Legemiddelhåndbok NLSH SYKEHUSAPOTEKETS FORPLIKTELSER Legemiddelleveranse. Smertekasetter. Cytostatikakurer.
BASISKURS I LEGEMIDDELHÅNDTERING NLSH 2006 Hvordan finne prosedyren i Doc Map Pulsen Håndbøker Legemiddelhåndbok NLSH SYKEHUSAPOTEKETS FORPLIKTELSER Legemiddelleveranse. Smertekasetter. Cytostatikakurer.
1. VETERINÆRPREPARATETS NAVN
 1. VETERINÆRPREPARATETS NAVN Metomotyl 2,5 mg/ml injeksjonsvæske til katt og hund Metomotyl 5 mg/ml injeksjonsvæske til katt og hund 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 2,5 mg/ml injeksjonsvæske
1. VETERINÆRPREPARATETS NAVN Metomotyl 2,5 mg/ml injeksjonsvæske til katt og hund Metomotyl 5 mg/ml injeksjonsvæske til katt og hund 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 2,5 mg/ml injeksjonsvæske
Veiledning for administrering av hetteglass og sprøyter (for pasienter, leger, sykepleiere, farmasøyter.)
 VEILEDNING FOR Å STARTE MED APIDRA 10 ml HETTEGLASS Apidra 100 E/ml injeksjonsvæske, oppløsning er en klar, fargeløs, vandig oppløsning uten synlige partikler. Hvert hetteglass inneholder 10 ml oppløsning
VEILEDNING FOR Å STARTE MED APIDRA 10 ml HETTEGLASS Apidra 100 E/ml injeksjonsvæske, oppløsning er en klar, fargeløs, vandig oppløsning uten synlige partikler. Hvert hetteglass inneholder 10 ml oppløsning
Kapittel 3 Medikamentregning
 Medikamentregning Side 1 av 7 Utregninger ved dosering, tillaging og administrering av legemidler til barn innebærer øket risiko for regnefeil og fortynningsfeil fordi legemidlene doseres pr. kg kroppsvekt
Medikamentregning Side 1 av 7 Utregninger ved dosering, tillaging og administrering av legemidler til barn innebærer øket risiko for regnefeil og fortynningsfeil fordi legemidlene doseres pr. kg kroppsvekt
Tilberedning og injeksjon
 Se s. 2 og 10 for anbefalt dosering Tilberedning og injeksjon qilaris 150 mg pulver til injeksjonsvæske, oppløsning Veiledning for pasienter og helsepersonell om klargjøring og administrering av ILARIS
Se s. 2 og 10 for anbefalt dosering Tilberedning og injeksjon qilaris 150 mg pulver til injeksjonsvæske, oppløsning Veiledning for pasienter og helsepersonell om klargjøring og administrering av ILARIS
1. VETERINÆRPREPARATETS NAVN. Rheumocam 5 mg/ml injeksjonsvæske, oppløsning til storfe og gris. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING
 1. VETERINÆRPREPARATETS NAVN Rheumocam 5 mg/ml injeksjonsvæske, oppløsning til storfe og gris. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En ml inneholder: Virkestoff: Meloksikam 5 mg Hjelpestoff: Etanol
1. VETERINÆRPREPARATETS NAVN Rheumocam 5 mg/ml injeksjonsvæske, oppløsning til storfe og gris. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En ml inneholder: Virkestoff: Meloksikam 5 mg Hjelpestoff: Etanol
[Version 8, 10/2012] VEDLEGG I PREPARATOMTALE
![[Version 8, 10/2012] VEDLEGG I PREPARATOMTALE [Version 8, 10/2012] VEDLEGG I PREPARATOMTALE](/thumbs/32/15375229.jpg) [Version 8, 10/2012] VEDLEGG I PREPARATOMTALE 1 1. VETERINÆRPREPARATETS NAVN Uniferon 200 mg/ml injeksjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoff: Hver ml inneholder 200
[Version 8, 10/2012] VEDLEGG I PREPARATOMTALE 1 1. VETERINÆRPREPARATETS NAVN Uniferon 200 mg/ml injeksjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoff: Hver ml inneholder 200
Tilberedning av Cinryze (C1-hemmer [human])
![Tilberedning av Cinryze (C1-hemmer [human]) Tilberedning av Cinryze (C1-hemmer [human])](/thumbs/64/50960156.jpg) Tilberedning og egenadministrasjon av din Cinryze- (C1-hemmer [human]) medisin 500 enheter pulver og væske til oppløsning til injeksjon Pasientinstruksjoner Denne instruksjonen er kun til bruk for pasienter
Tilberedning og egenadministrasjon av din Cinryze- (C1-hemmer [human]) medisin 500 enheter pulver og væske til oppløsning til injeksjon Pasientinstruksjoner Denne instruksjonen er kun til bruk for pasienter
Oppløsnings- og fortynningsvæske til pulvere, konsentrater og oppløsninger til injeksjon.
 1 1. LEGEMIDLETS NAVN Sterile Water Fresenius Kabi, oppløsningsvæske til parenteral bruk 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 100 ml oppløsningsvæske inneholder: 100 g vann til injeksjonsvæsker 3.
1 1. LEGEMIDLETS NAVN Sterile Water Fresenius Kabi, oppløsningsvæske til parenteral bruk 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 100 ml oppløsningsvæske inneholder: 100 g vann til injeksjonsvæsker 3.
Dag ml 0.9% NaCl Gjennomskylling iv i 500 ml 0.9% NaCl 30 min iv Sjekket kur: Side 2 av5
 Dokumentansvarlig: Nina Helbekkmo Dokumentnummer: PR18408 Godkjent av: Ulf Aasebø Gyldig for: Lungemedisinsk avdeling UNN Indikasjon: Småcellet lungecarsinom, begrenset sykdom. Kurativt mål. Behandlingsplan:
Dokumentansvarlig: Nina Helbekkmo Dokumentnummer: PR18408 Godkjent av: Ulf Aasebø Gyldig for: Lungemedisinsk avdeling UNN Indikasjon: Småcellet lungecarsinom, begrenset sykdom. Kurativt mål. Behandlingsplan:
Amgen Europe B.V. Nplate_EU_DosingCalculator_RMP_v3.0_NO_MAR2019. Nplate (romiplostim) Dosekalkulator
 Amgen Europe B.V. Nplate_EU_DosingCalculator_RMP_v3.0_NO_MAR2019 Nplate (romiplostim) Dosekalkulator Veiledning for håndtering Nplate kan kun rekonstitueres med sterilt vann til injeksjonsvæsker uten konserveringsmidler.
Amgen Europe B.V. Nplate_EU_DosingCalculator_RMP_v3.0_NO_MAR2019 Nplate (romiplostim) Dosekalkulator Veiledning for håndtering Nplate kan kun rekonstitueres med sterilt vann til injeksjonsvæsker uten konserveringsmidler.
Administrering av antibiotika i sykehjem
 Administrering av antibiotika i sykehjem Hilde Fjeld, farmasøyt 12. november 2018 Min kjøreplan Praktisk håndtering av antibiotika Holdbarhet Svelgeproblemer Miksturer, utblanding Parenteral behandling
Administrering av antibiotika i sykehjem Hilde Fjeld, farmasøyt 12. november 2018 Min kjøreplan Praktisk håndtering av antibiotika Holdbarhet Svelgeproblemer Miksturer, utblanding Parenteral behandling
Cisplatin Nyretoksisk! God hydrering nødvendig. Oppretthold adekvat diurese (se infusjonssskjema). Unngå nyretoksiske medikamenter i behandlingstiden
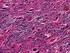 CISPLATIN - ETOPOSID Dokumentansvarlig: Nina Helbekkmo Dokumentnummer: PR3418 Godkjent av: Ulf Aasebø Gyldig for: Lungemedisinsk avdeling UNN Indikasjon: Småcellet lungecarsinom, begrenset sykdom. Kurativt
CISPLATIN - ETOPOSID Dokumentansvarlig: Nina Helbekkmo Dokumentnummer: PR3418 Godkjent av: Ulf Aasebø Gyldig for: Lungemedisinsk avdeling UNN Indikasjon: Småcellet lungecarsinom, begrenset sykdom. Kurativt
Porter fra B. Braun Celsite implanterbare porter. Pasienthåndbok for Celsite -porter
 Porter fra B. Braun Celsite implanterbare porter Pasienthåndbok for Celsite -porter Innhold Innhold Informasjon om min Celsite -port 3 Innledning 4 Ordliste 4 Celsite -port - Hvorfor trenger jeg en port?
Porter fra B. Braun Celsite implanterbare porter Pasienthåndbok for Celsite -porter Innhold Innhold Informasjon om min Celsite -port 3 Innledning 4 Ordliste 4 Celsite -port - Hvorfor trenger jeg en port?
1. LEGEMIDLETS NAVN. Addex - Kaliumklorid 1 mmol/ml, konsentrat til infusjonsvæske 2. KVALITATIV OG KVANTITATIV SAMMENSETNING
 1. LEGEMIDLETS NAVN Addex - Kaliumklorid 1 mmol/ml, konsentrat til infusjonsvæske 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Kaliumklorid 74,6 mg/ml, tilsvarende 1 mmol/ml Elektrolyttprofilen til 1 ml
1. LEGEMIDLETS NAVN Addex - Kaliumklorid 1 mmol/ml, konsentrat til infusjonsvæske 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Kaliumklorid 74,6 mg/ml, tilsvarende 1 mmol/ml Elektrolyttprofilen til 1 ml
22735 Menopur 600 IU + 1200 IU_Ferring 09.09.15 13.42 Side 2. Brukerveiledning. Menopur. 600 IU eller 1200 IU
 22735 Menopur 600 IU + 1200 IU_Ferring 09.09.15 13.42 Side 2 Brukerveiledning Menopur 600 IU eller 1200 IU 22735 Menopur 600 IU + 1200 IU_Ferring 09.09.15 13.42 Side 3 Sjekk at pakningen inneholder følgende
22735 Menopur 600 IU + 1200 IU_Ferring 09.09.15 13.42 Side 2 Brukerveiledning Menopur 600 IU eller 1200 IU 22735 Menopur 600 IU + 1200 IU_Ferring 09.09.15 13.42 Side 3 Sjekk at pakningen inneholder følgende
Trinn-for-trinn bruksanvisning til Enbrel 25 mg og 50 mg ferdigfylt penn MYCLIC
 Trinn-for-trinn bruksanvisning til Enbrel 25 mg og 50 mg ferdigfylt penn MYCLIC For ytterligere informasjon les Enbrel pakningsvedlegg før bruk Innholdsfortegnelse Viktig å huske før du begynner...3 Hvordan
Trinn-for-trinn bruksanvisning til Enbrel 25 mg og 50 mg ferdigfylt penn MYCLIC For ytterligere informasjon les Enbrel pakningsvedlegg før bruk Innholdsfortegnelse Viktig å huske før du begynner...3 Hvordan
Helsetilsynet i fylket. Lover og forskrifter knyttet til legemiddelhåndtering. Fylkesmannen. Historisk tilbakeblikk
 Helsetilsynet i fylket Lover og forskrifter knyttet til legemiddelhåndtering Knut Fredrik Thorne seniorrådgiver Helsetilsynet/Fylkesmannen i Østfold Helsetilsynet i fylket: Fører tilsyn med alt som har
Helsetilsynet i fylket Lover og forskrifter knyttet til legemiddelhåndtering Knut Fredrik Thorne seniorrådgiver Helsetilsynet/Fylkesmannen i Østfold Helsetilsynet i fylket: Fører tilsyn med alt som har
Pakningsvedlegg: Informasjon til brukeren. Diproderm øredråper 0,05 %, oppløsning. betametason
 PAKNINGSVEDLEGG Pakningsvedlegg: Informasjon til brukeren Diproderm øredråper 0,05 %, oppløsning betametason Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder
PAKNINGSVEDLEGG Pakningsvedlegg: Informasjon til brukeren Diproderm øredråper 0,05 %, oppløsning betametason Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder
Viktig sikkerhetsinformasjon for apotek
 (blinatumomab) Opplæringsbrosjyre for apotek (blinatumomab) Viktig sikkerhetsinformasjon for apotek Denne opplæringsbrosjyren inneholder viktig informasjon om rekonstituering og klargjøring av blinatumomab.
(blinatumomab) Opplæringsbrosjyre for apotek (blinatumomab) Viktig sikkerhetsinformasjon for apotek Denne opplæringsbrosjyren inneholder viktig informasjon om rekonstituering og klargjøring av blinatumomab.
Risikovurdering av legemiddeltilberedning i sykehusavdeling Pasientsikkerhetskonferansen 14. Februar 2018
 Risikovurdering av legemiddeltilberedning i sykehusavdeling Pasientsikkerhetskonferansen 14. Februar 2018 Kirsti Wang Forså Farmasøyt Sykehusapotek Nord Helgelandssykehuset Det går jo alltid bra eller?
Risikovurdering av legemiddeltilberedning i sykehusavdeling Pasientsikkerhetskonferansen 14. Februar 2018 Kirsti Wang Forså Farmasøyt Sykehusapotek Nord Helgelandssykehuset Det går jo alltid bra eller?
for Revmatoid Artritt (RA) og kjempecellearteritt (GCA) VEILEDER FOR DOSERING OG ADMINISTRASJON TRINN FOR TRINN
 Til sykepleier RoActemra iv og sc for Revmatoid Artritt (RA) og kjempecellearteritt (GCA) VEILEDER FOR DOSERING OG ADMINISTRASJON TRINN FOR TRINN En veiledning som skal hjelpe helsepersonell med dosering
Til sykepleier RoActemra iv og sc for Revmatoid Artritt (RA) og kjempecellearteritt (GCA) VEILEDER FOR DOSERING OG ADMINISTRASJON TRINN FOR TRINN En veiledning som skal hjelpe helsepersonell med dosering
STERIL KUN TIL ENGANGSBRUK IKKE-PYROGEN
 0086 TM Leveringssystem for legemidler til embolisering BRUKSANVISNING DC Bead Leveringssystem for legemidler til embolisering STERIL KUN TIL ENGANGSBRUK IKKE-PYROGEN Norsk BRUKSANVISNING DC Bead Leveringssystem
0086 TM Leveringssystem for legemidler til embolisering BRUKSANVISNING DC Bead Leveringssystem for legemidler til embolisering STERIL KUN TIL ENGANGSBRUK IKKE-PYROGEN Norsk BRUKSANVISNING DC Bead Leveringssystem
Kunsten å vaksinere. Synne Sandbu, overlege Avd. for vaksine Divisjon for smittevern Nasjonalt folkehelseinstitutt. Vaksinedagene 2006
 Kunsten å vaksinere Synne Sandbu, overlege Avd. for vaksine Divisjon for smittevern Nasjonalt folkehelseinstitutt 1 Vaksinedagene 2006 Helsesøstrene her i landet har ansvaret for gjennomføringen av barnevaksinasjonsprogrammet
Kunsten å vaksinere Synne Sandbu, overlege Avd. for vaksine Divisjon for smittevern Nasjonalt folkehelseinstitutt 1 Vaksinedagene 2006 Helsesøstrene her i landet har ansvaret for gjennomføringen av barnevaksinasjonsprogrammet
http://www.felleskatalogen.no/medisin/pasienter/pil-trulicity-lilly-595591
 Side 1 av 13 Pakningsvedlegg: Informasjon til brukeren Trulicity 0,75 mg injeksjonsvæske, oppløsning i ferdigfylt penn Trulicity 1,5 mg injeksjonsvæske, oppløsning i ferdigfylt penn dulaglutid Dette legemidlet
Side 1 av 13 Pakningsvedlegg: Informasjon til brukeren Trulicity 0,75 mg injeksjonsvæske, oppløsning i ferdigfylt penn Trulicity 1,5 mg injeksjonsvæske, oppløsning i ferdigfylt penn dulaglutid Dette legemidlet
NeuroBloc Botulinumtoksin type B injeksjonsvæske, oppløsning 5000 E/ml
 NeuroBloc Botulinumtoksin type B injeksjonsvæske, oppløsning 5000 E/ml NeuroBloc-veiledning for leger, utgave 1, august 2014 1 Viktig sikkerhetsinformasjon for leger Hensikten med denne håndboken er å
NeuroBloc Botulinumtoksin type B injeksjonsvæske, oppløsning 5000 E/ml NeuroBloc-veiledning for leger, utgave 1, august 2014 1 Viktig sikkerhetsinformasjon for leger Hensikten med denne håndboken er å
Legemiddelbruk. Bare en liten pille? Legemiddelbruk hos eldre. Legemiddelbruk. Effekter av legemidler hos eldre: Egen opplevelse av legemidlene:
 Bare en liten pille? En undersøkelse om eldres egne opplevelser av hverdagen med legemidler Molde, 10.5.2010 Lars André Olsen Legemiddelbruk Antall faste legemidler per døgn 4 legemidler per døgn 2 personer
Bare en liten pille? En undersøkelse om eldres egne opplevelser av hverdagen med legemidler Molde, 10.5.2010 Lars André Olsen Legemiddelbruk Antall faste legemidler per døgn 4 legemidler per døgn 2 personer
Tilberedning og injeksjon
 Se s. 2, 10 og 11 for dosering voksne og barn Tilberedning og injeksjon qilaris 150 mg pulver for oppløsning til injeksjon Veiledning for pasienter og helsepersonell om klargjøring og administrering av
Se s. 2, 10 og 11 for dosering voksne og barn Tilberedning og injeksjon qilaris 150 mg pulver for oppløsning til injeksjon Veiledning for pasienter og helsepersonell om klargjøring og administrering av
VEILEDER FOR DOSERING OG ADMINISTRASJON TRINN FOR TRINN
 Til sykepleier - Veileder for dosering og administrasjon RoActemra iv og sc for Revmatoid Artritt (RA) VEILEDER FOR DOSERING OG ADMINISTRASJON TRINN FOR TRINN En veiledning som skal hjelpe helsepersonell
Til sykepleier - Veileder for dosering og administrasjon RoActemra iv og sc for Revmatoid Artritt (RA) VEILEDER FOR DOSERING OG ADMINISTRASJON TRINN FOR TRINN En veiledning som skal hjelpe helsepersonell
Shire utgir dette materialet for risikohåndtering som en del av sin tilknytning til EMA for å implementere den godkjente risikohåndteringsplanen.
 Rekonstituering og administrering av Cinryze (C1-hemmer [human]) Shire utgir dette opplæringsmaterialet for å implementere den godkjente risikohåndteringsplanen som en del av sin forpliktelse overfor EMA.
Rekonstituering og administrering av Cinryze (C1-hemmer [human]) Shire utgir dette opplæringsmaterialet for å implementere den godkjente risikohåndteringsplanen som en del av sin forpliktelse overfor EMA.
4.1 Indikasjoner Sporelementtilskudd for å dekke basale til moderat økte behov ved parenteral ernæring.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Addaven, konsentrat til infusjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Addaven inneholder: 1 ml 1 ampulle (10 ml) Kromklorid (6H2O) 5,33 mikrog
PREPARATOMTALE 1. LEGEMIDLETS NAVN Addaven, konsentrat til infusjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Addaven inneholder: 1 ml 1 ampulle (10 ml) Kromklorid (6H2O) 5,33 mikrog
Instruksjonsveiledning i bruk av PRALUENT for pasient
 alirokumab Instruksjonsveiledning i bruk av PRALUENT for pasient Denne brosjyren er basert på pakningsvedlegget til Praluent. Les hele pakningsvedlegget og PRALUENT pennens bruksanvisning før du går i
alirokumab Instruksjonsveiledning i bruk av PRALUENT for pasient Denne brosjyren er basert på pakningsvedlegget til Praluent. Les hele pakningsvedlegget og PRALUENT pennens bruksanvisning før du går i
Inaktiverte hele bakterieceller av Haemophilus parasuis serotype 5, stamme 4800: 0,05 mg total nitrogen, induserer 9,1 ELISA enheter *.
 1. VETERINÆRPREPARATETS NAVN Porcilis Glässer Vet. injeksjonsvæske, suspensjon til gris 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 dose (2 ml) inneholder: Virkestoff(er): Inaktiverte hele bakterieceller
1. VETERINÆRPREPARATETS NAVN Porcilis Glässer Vet. injeksjonsvæske, suspensjon til gris 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 dose (2 ml) inneholder: Virkestoff(er): Inaktiverte hele bakterieceller
Legemiddelassistert rehabilitering ved narkotikamisbruk
 Skriv ut Lukk Legemiddelassistert rehabilitering ved narkotikamisbruk Rundskriv fra Statens helsetilsyn Til: Landets leger Landets apotek IK-15/2000 2000/1050 18.9.2000 Se også I-5/2003 Legemiddelassistert
Skriv ut Lukk Legemiddelassistert rehabilitering ved narkotikamisbruk Rundskriv fra Statens helsetilsyn Til: Landets leger Landets apotek IK-15/2000 2000/1050 18.9.2000 Se også I-5/2003 Legemiddelassistert
RoActemra iv for RA, pjia og sjia RoActemra sc for RA, GCA og pjia
 Til sykepleier RoActemra iv for RA, pjia og sjia RoActemra sc for RA, GCA og pjia VEILEDER FOR DOSERING OG ADMINISTRASJON TRINN FOR TRINN En veiledning som skal hjelpe helsepersonell med dosering og administrering
Til sykepleier RoActemra iv for RA, pjia og sjia RoActemra sc for RA, GCA og pjia VEILEDER FOR DOSERING OG ADMINISTRASJON TRINN FOR TRINN En veiledning som skal hjelpe helsepersonell med dosering og administrering
Din behandling med XALKORI (krizo nib) - vik g sikkerhetsinformasjon
 De e legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig. Helsepersonell oppfordres l å melde enhver mistenkt bivirkning. Se avsni 4 i pakningsvedlegget
De e legemidlet er underlagt særlig overvåking for å oppdage ny sikkerhetsinformasjon så raskt som mulig. Helsepersonell oppfordres l å melde enhver mistenkt bivirkning. Se avsni 4 i pakningsvedlegget
Rekonstituering og administrering av Cinryze (C1-hemmer [human]) Instruksjoner for helsepersonell
![Rekonstituering og administrering av Cinryze (C1-hemmer [human]) Instruksjoner for helsepersonell Rekonstituering og administrering av Cinryze (C1-hemmer [human]) Instruksjoner for helsepersonell](/thumbs/69/60787469.jpg) Rekonstituering og administrering av Cinryze (C1-hemmer [human]) Instruksjoner for helsepersonell Denne informasjonen leveres av Shire Pharmaceuticals. Dette legemidlet er underlagt særlig overvåking for
Rekonstituering og administrering av Cinryze (C1-hemmer [human]) Instruksjoner for helsepersonell Denne informasjonen leveres av Shire Pharmaceuticals. Dette legemidlet er underlagt særlig overvåking for
Nasjonale utblandingskort for IV medikamenter til barn
 Nasjonale utblandingskort for IV medikamenter til barn Hvordan skal kortene brukes? Årlig samling i kompetansenettverket for legemidler til barn Solstrand 15.november 2011 J01D C02 CEFUROKSIM Cefuroxim,
Nasjonale utblandingskort for IV medikamenter til barn Hvordan skal kortene brukes? Årlig samling i kompetansenettverket for legemidler til barn Solstrand 15.november 2011 J01D C02 CEFUROKSIM Cefuroxim,
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. Saizen click.easy 8mg, pulver og væske til injeksjonsvæske, oppløsning. Somatropin
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Saizen click.easy 8mg, pulver og væske til injeksjonsvæske, oppløsning. Somatropin Les nøye gjennom pakningsvedlegget før du begynner å bruke legemidlet. Ta vare
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Saizen click.easy 8mg, pulver og væske til injeksjonsvæske, oppløsning. Somatropin Les nøye gjennom pakningsvedlegget før du begynner å bruke legemidlet. Ta vare
Fakta om hiv og aids. Thai/norsk
 Fakta om hiv og aids Thai/norsk Aids er en alvorlig sykdom som siden begynnelsen av 1980-tallet har spredd seg over hele verden. Aids skyldes et virus, hiv, som overføres fra person til person i bestemte
Fakta om hiv og aids Thai/norsk Aids er en alvorlig sykdom som siden begynnelsen av 1980-tallet har spredd seg over hele verden. Aids skyldes et virus, hiv, som overføres fra person til person i bestemte
Kateter assosierte UVI Innlegging av KAD Indikasjon ved innlegging av KAD. Nettverkssamlingsmøte 22 januar 2014 Skei Hotell, Jølster
 Kateter assosierte UVI Innlegging av KAD Indikasjon ved innlegging av KAD Nettverkssamlingsmøte 22 januar 2014 Skei Hotell, Jølster Epidemiologi Helsetjenesteassosierte infeksjoner (HAI) er en hyppig komplikasjon
Kateter assosierte UVI Innlegging av KAD Indikasjon ved innlegging av KAD Nettverkssamlingsmøte 22 januar 2014 Skei Hotell, Jølster Epidemiologi Helsetjenesteassosierte infeksjoner (HAI) er en hyppig komplikasjon
VEDLEGG I PREPARATOMTALE
 VEDLEGG I PREPARATOMTALE 1 1. VETERINÆRPREPARATETS NAVN Hyobac App Multi Vet. injeksjonsvæske, emulsjon 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoffer Per dose (1,0 ml) Actinobacillus pleuropneumoniae,
VEDLEGG I PREPARATOMTALE 1 1. VETERINÆRPREPARATETS NAVN Hyobac App Multi Vet. injeksjonsvæske, emulsjon 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoffer Per dose (1,0 ml) Actinobacillus pleuropneumoniae,
Enbrel 25 mg og 50 mg injeksjonsvæske, oppløsning i ferdigfylt penn MYCLIC
 Enbrel 25 mg og 50 mg injeksjonsvæske, oppløsning i ferdigfylt penn MYCLIC Trinn-for-trinn bruksanvisning til hvordan du bruker Enbrel 25 mg og 50 mg ferdigfylt penn 1 MYCLIC 1. Enbrel (etanercept) preparatomtale
Enbrel 25 mg og 50 mg injeksjonsvæske, oppløsning i ferdigfylt penn MYCLIC Trinn-for-trinn bruksanvisning til hvordan du bruker Enbrel 25 mg og 50 mg ferdigfylt penn 1 MYCLIC 1. Enbrel (etanercept) preparatomtale
Særlige vurderinger ved tilberedning av antibiotikaløsninger
 Vedlegg 1 Særlige vurderinger ved tilberedning av antibiotikaløsninger Vedlegg til Veileder for risikovurdering av tilberedning av legemidler ved sykehusenes avdelinger Versjon 1.0, 19.04.16 Godkjent av
Vedlegg 1 Særlige vurderinger ved tilberedning av antibiotikaløsninger Vedlegg til Veileder for risikovurdering av tilberedning av legemidler ved sykehusenes avdelinger Versjon 1.0, 19.04.16 Godkjent av
Pediatrisk populasjon: Legemidlet bør ikke brukes til barn siden det ikke finnes tilgjengelige sikkerhetsdata.
 1. LEGEMIDLETS NAVN Kaliumklorid Orifarm 750 mg depottabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En depottablett inneholder 750 mg kaliumklorid. For fullstendig liste over hjelpestoffer, se pkt.
1. LEGEMIDLETS NAVN Kaliumklorid Orifarm 750 mg depottabletter 2. KVALITATIV OG KVANTITATIV SAMMENSETNING En depottablett inneholder 750 mg kaliumklorid. For fullstendig liste over hjelpestoffer, se pkt.
Hypoglykemiske tilstander, f.eks. insulinkoma. Behov for parenteral karbohydrattilførsel.
 PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Glukose B. Braun 50 mg/ml injeksjonsvæske, oppløsning Glukose B. Braun 500 mg/ml injeksjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 50 mg/ml. 1
PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Glukose B. Braun 50 mg/ml injeksjonsvæske, oppløsning Glukose B. Braun 500 mg/ml injeksjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 50 mg/ml. 1
Basale smittevernrutiner i helsetjenesten
 Smittevernkontoret Hilde Toresen T: 51508583 Anita Rognmo Grostøl T: 51508569 Hilde.toresen@stavanger.kommune.no Anita.rognmo.grostol@stavanger.kommune. no Torgveien 15 C 4016 Stavanger Basale smittevernrutiner
Smittevernkontoret Hilde Toresen T: 51508583 Anita Rognmo Grostøl T: 51508569 Hilde.toresen@stavanger.kommune.no Anita.rognmo.grostol@stavanger.kommune. no Torgveien 15 C 4016 Stavanger Basale smittevernrutiner
Pakningsvedlegg: Informasjon til pasienten. GRANUPAS 4 g enterogranulat para-aminosalisylsyre
 Pakningsvedlegg: Informasjon til pasienten GRANUPAS 4 g enterogranulat para-aminosalisylsyre Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Pakningsvedlegg: Informasjon til pasienten GRANUPAS 4 g enterogranulat para-aminosalisylsyre Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet. Det inneholder informasjon
Økt smerte er normalt med mindre det samtidig forekommer feber og svelgebesvær (fremfor alt drikkebesvær). Les mer under fanen Viktig.
 Smertebehandling Her får du informasjon om smertebehandling med legemiddel etter tonsilloperasjon. Du kan regne ut riktig dose av smertestillende legemiddel for barnet ditt. Vi gjør oppmerksom på at denne
Smertebehandling Her får du informasjon om smertebehandling med legemiddel etter tonsilloperasjon. Du kan regne ut riktig dose av smertestillende legemiddel for barnet ditt. Vi gjør oppmerksom på at denne
Patientinformation. Å leve med barneleddgikt - Juvenil idiopatisk artritt (JIA) En foreldreguide til barn som behandles med Metex /Metex penn
 SE Å leve med barneleddgikt - Juvenil idiopatisk artritt (JIA) Patientinformation En foreldreguide til barn som behandles med Metex /Metex penn metotreksat Kjære Foreldre, Ditt barn har blitt diagnostisert
SE Å leve med barneleddgikt - Juvenil idiopatisk artritt (JIA) Patientinformation En foreldreguide til barn som behandles med Metex /Metex penn metotreksat Kjære Foreldre, Ditt barn har blitt diagnostisert
NSF- Fagmøte 20.03.14 Ny legemiddelhåndteringsforskrift
 NSF- Fagmøte 20.03.14 Ny legemiddelhåndteringsforskrift Adm.dir Gunn Fredriksen 1 I hovedsak 2 endringer Dette har vi ventet på så lenge 1. Ordinering etter prosedyre (endring av 7) 2. Presisering av krav
NSF- Fagmøte 20.03.14 Ny legemiddelhåndteringsforskrift Adm.dir Gunn Fredriksen 1 I hovedsak 2 endringer Dette har vi ventet på så lenge 1. Ordinering etter prosedyre (endring av 7) 2. Presisering av krav
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. Epirubicin Actavis 10 mg og 50 mg pulver til injeksjons-/infusjonsvæske, oppløsning. epirubicinhydroklorid
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Epirubicin Actavis 10 mg og 50 mg pulver til injeksjons-/infusjonsvæske, oppløsning epirubicinhydroklorid Les nøye gjennom dette pakningsvedlegget før du begynner
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Epirubicin Actavis 10 mg og 50 mg pulver til injeksjons-/infusjonsvæske, oppløsning epirubicinhydroklorid Les nøye gjennom dette pakningsvedlegget før du begynner
VEDLEGG I PREPARATOMTALE
 VEDLEGG I PREPARATOMTALE 1/18 1. VETERINÆRPREPARATETS NAVN Neocolipor injeksjonsvæske, suspensjon 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoff(er): Per dose på 2 ml: E.coli adhesin F4 (F4ab, F4ac,
VEDLEGG I PREPARATOMTALE 1/18 1. VETERINÆRPREPARATETS NAVN Neocolipor injeksjonsvæske, suspensjon 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoff(er): Per dose på 2 ml: E.coli adhesin F4 (F4ab, F4ac,
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. DepoCyte 50 mg injeksjonsvæske, suspensjon Cytarabin
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN DepoCyte 50 mg injeksjonsvæske, suspensjon Cytarabin Les nøye gjennom dette pakningsvedlegget før du får begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget.
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN DepoCyte 50 mg injeksjonsvæske, suspensjon Cytarabin Les nøye gjennom dette pakningsvedlegget før du får begynner å bruke legemidlet. - Ta vare på dette pakningsvedlegget.
SIKKERHETSDATABLAD DESINFECT 44. Miljøskadelig. Giftig for vannlevende organismer: kan forårsake uønskede langtidsvirkninger i vannmiljøet.
 no 1. IDENTIFIKASJON AV STOFFET/STOFFBLANDINGEN OG AV SELSKAPET/FORETAKET: Produktnavn: Leverandør: ITW ApS Platinvej 21 6000 Kolding Telefon: +45 76 34 84 00 Telefaks: +45 75 50 43 70 Ansvarlig for sikkerhedsdatablad
no 1. IDENTIFIKASJON AV STOFFET/STOFFBLANDINGEN OG AV SELSKAPET/FORETAKET: Produktnavn: Leverandør: ITW ApS Platinvej 21 6000 Kolding Telefon: +45 76 34 84 00 Telefaks: +45 75 50 43 70 Ansvarlig for sikkerhedsdatablad
Pakningsvedlegg: Informasjon til brukeren. Esmeron 10 mg /ml injeksjonsvæske, oppløsning rokuroniumbromid
 PAKNINGSVEDLEGG 1 Pakningsvedlegg: Informasjon til brukeren Esmeron 10 mg /ml injeksjonsvæske, oppløsning rokuroniumbromid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
PAKNINGSVEDLEGG 1 Pakningsvedlegg: Informasjon til brukeren Esmeron 10 mg /ml injeksjonsvæske, oppløsning rokuroniumbromid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke dette legemidlet.
PREPARATOMTALE 1. VETERINÆRPREPARATETS NAVN. Nobivac DHP vet. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING. Virkestoff(er):
 PREPARATOMTALE 1. VETERINÆRPREPARATETS NAVN Nobivac DHP vet. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoff(er): En dose (1 ml) rekonstituert vaksine inneholder: Valpesykevirus, stamme Onderstepoort
PREPARATOMTALE 1. VETERINÆRPREPARATETS NAVN Nobivac DHP vet. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Virkestoff(er): En dose (1 ml) rekonstituert vaksine inneholder: Valpesykevirus, stamme Onderstepoort
Cerezyme hjemme. Håndbok for pasienter med Gaucher sykdom som får hjemmeinfusjon med Cerezyme
 Cerezyme hjemme Håndbok for pasienter med Gaucher sykdom som får hjemmeinfusjon med Cerezyme Versjon nr. 2: 24. januar 2011 (sist revidert desember 2014) Les all denne informasjonen nøye før du starter
Cerezyme hjemme Håndbok for pasienter med Gaucher sykdom som får hjemmeinfusjon med Cerezyme Versjon nr. 2: 24. januar 2011 (sist revidert desember 2014) Les all denne informasjonen nøye før du starter
PREPARATOMTALE. Gonazon
 PREPARATOMTALE Gonazon 1. VETERINÆRPREPARATETS NAVN Gonazon konsentrat til injeksjonsvæske for hunner i laksefamilien. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING HETTEGLASS INNEHOLDENDE KONSENTRAT : Virkestoff
PREPARATOMTALE Gonazon 1. VETERINÆRPREPARATETS NAVN Gonazon konsentrat til injeksjonsvæske for hunner i laksefamilien. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING HETTEGLASS INNEHOLDENDE KONSENTRAT : Virkestoff
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. Oxaliplatin Hospira 5 mg/ml, konsentrat til infusjonsvæske. Oksaliplatin
 Du må bare kjøre bil eller utføre risikofylt arbeid når det er trygt for deg. Legemidler kan påvirke din evne til å kjøre bil eller utføre risikofylt arbeid. Les informasjonen i pakningsvedlegget nøye.
Du må bare kjøre bil eller utføre risikofylt arbeid når det er trygt for deg. Legemidler kan påvirke din evne til å kjøre bil eller utføre risikofylt arbeid. Les informasjonen i pakningsvedlegget nøye.
PREPARATOMTALE. Sterilt vann Baxter Viaflo, oppløsningsvæske til parenteral bruk. Hver pose inneholder 100 % w/v vann til injeksjonsvæsker.
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Sterilt vann Baxter Viaflo, oppløsningsvæske til parenteral bruk 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver pose inneholder 100 % w/v vann til injeksjonsvæsker.
PREPARATOMTALE 1. LEGEMIDLETS NAVN Sterilt vann Baxter Viaflo, oppløsningsvæske til parenteral bruk 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver pose inneholder 100 % w/v vann til injeksjonsvæsker.
PICC-line Ambulerende sykepleieteam Fagdag før ferien 2014. Ambulerende sykepleieteam
 PICC-line Fagdag før ferien 2014 1 Hva er en PICC-line? PICC-line er forkortelse for Periferally Inserted Central Catheter En perifer inngang til det sentrale venøse system Brukes til kort og mellomlang
PICC-line Fagdag før ferien 2014 1 Hva er en PICC-line? PICC-line er forkortelse for Periferally Inserted Central Catheter En perifer inngang til det sentrale venøse system Brukes til kort og mellomlang
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN. Ipstyl Autogel 60 mg/90 mg/120 mg injeksjonsvæske, oppløsning i ferdigfylt sprøyte lanreotid
 PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Ipstyl Autogel 60 mg/90 mg/120 mg injeksjonsvæske, oppløsning i ferdigfylt sprøyte lanreotid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet.
PAKNINGSVEDLEGG: INFORMASJON TIL BRUKEREN Ipstyl Autogel 60 mg/90 mg/120 mg injeksjonsvæske, oppløsning i ferdigfylt sprøyte lanreotid Les nøye gjennom dette pakningsvedlegget før du begynner å bruke legemidlet.
PREPARATOMTALE. Aktiv ingrediens Mengde 1 ml rekonstituert Soluvit inneholder: Tiaminmononitrat 3,1 mg 0,31 mg (Tilsvarer Vitamin B1 2,5 mg)
 PREPARATOMTALE 1. LEGEMIDLETS NAVN Soluvit, pulver til infusjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 hetteglass Soluvit inneholder: Aktiv ingrediens Mengde 1 ml rekonstituert
PREPARATOMTALE 1. LEGEMIDLETS NAVN Soluvit, pulver til infusjonsvæske, oppløsning 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 hetteglass Soluvit inneholder: Aktiv ingrediens Mengde 1 ml rekonstituert
Legeforum.29.nov Kreftspl Edit Hodne Mork
 Legeforum.29.nov 2016. Kreftspl Edit Hodne Mork Indikasjon: Utilfredsstillende smerte/symptomlindring. Når pasienten ikke kan ta medikamenter peroralt. Kvalme og oppkast Utilfredsstillende absorpsjon via
Legeforum.29.nov 2016. Kreftspl Edit Hodne Mork Indikasjon: Utilfredsstillende smerte/symptomlindring. Når pasienten ikke kan ta medikamenter peroralt. Kvalme og oppkast Utilfredsstillende absorpsjon via
Brukerveiledning BCG-TICE. Deles kun ut av helsepersonell ved oppstart av BCG-TICE behandling
 BCG-TICE Deles kun ut av helsepersonell ved oppstart av BCG-TICE behandling Generelt Du har fått diagnostisert overflatisk blærekreft, og din urolog anbefaler behand ling med BCG. Her følger informasjon
BCG-TICE Deles kun ut av helsepersonell ved oppstart av BCG-TICE behandling Generelt Du har fått diagnostisert overflatisk blærekreft, og din urolog anbefaler behand ling med BCG. Her følger informasjon
OPPSTART OPPSTART OPPSTART. Med forlengelsesslange. Åpne Sangvia pakningen ved aseptisk prosedyre.
 OPPSTART Åpne Sangvia pakningen ved aseptisk prosedyre. 1. a) Fjern beskyttelseshettene fra utløpene i oppsamlingsenheten. b) Koble avfallsposen til utløpet for avfall (hvit kobling). c) Koble forlengelsesslangen
OPPSTART Åpne Sangvia pakningen ved aseptisk prosedyre. 1. a) Fjern beskyttelseshettene fra utløpene i oppsamlingsenheten. b) Koble avfallsposen til utløpet for avfall (hvit kobling). c) Koble forlengelsesslangen
Lukket legemiddelsløyfe
 Lukket legemiddelsløyfe Camilla Bjørnstad Ph.D-student, NSE Farmasøyt, Sykehusapotek Nord Agenda Mål med prosjektet Definisjoner Metode Datainnsamling Resultater Kalnes Resultater Vest Konklusjoner 1 Mål
Lukket legemiddelsløyfe Camilla Bjørnstad Ph.D-student, NSE Farmasøyt, Sykehusapotek Nord Agenda Mål med prosjektet Definisjoner Metode Datainnsamling Resultater Kalnes Resultater Vest Konklusjoner 1 Mål
PROSEDYRE FOR Tjenesteområde:
 PROSEDYRE FOR Tjenesteområde: Kategori: 3. Omsorgstjenester 3.2 Medikamenthåndtering Side 1 av 3 ANSVARSFORDELING OG NØDVENDIG BRUKERINFORMASJON Vedlegg: 2 Ansvarlig: Rådmannen Godkjent den: 17.12.2012
PROSEDYRE FOR Tjenesteområde: Kategori: 3. Omsorgstjenester 3.2 Medikamenthåndtering Side 1 av 3 ANSVARSFORDELING OG NØDVENDIG BRUKERINFORMASJON Vedlegg: 2 Ansvarlig: Rådmannen Godkjent den: 17.12.2012
Dette preparatet har markedsføringstillatelse for både human og veterinær bruk. Preparatomtale for veterinær bruk finnes nederst i dokumentet.
 Dette preparatet har markedsføringstillatelse for både human og veterinær bruk. Preparatomtale for veterinær bruk finnes nederst i dokumentet. 1. LEGEMIDLETS NAVN Pyrisept 2. KVALITATIV OG KVANTITATIV
Dette preparatet har markedsføringstillatelse for både human og veterinær bruk. Preparatomtale for veterinær bruk finnes nederst i dokumentet. 1. LEGEMIDLETS NAVN Pyrisept 2. KVALITATIV OG KVANTITATIV
PARENTERAL ERNÆRING. Hilde M. Sporsem Klinisk farmasøyt Sykehusapoteket Oslo, farmasøytiske tjenester Trinn 1 januar 2016
 PARENTERAL ERNÆRING Hilde M. Sporsem Klinisk farmasøyt Sykehusapoteket Oslo, farmasøytiske tjenester Trinn 1 januar 2016 Valg av parenteral ernæringsløsning Velge det produkt som sykehuset har LIS (legemiddelinnkjøp)
PARENTERAL ERNÆRING Hilde M. Sporsem Klinisk farmasøyt Sykehusapoteket Oslo, farmasøytiske tjenester Trinn 1 januar 2016 Valg av parenteral ernæringsløsning Velge det produkt som sykehuset har LIS (legemiddelinnkjøp)
- Hver 0,007 ml dose av vaksine inneholder følgende antall sporulerte oocyster derivert fra fem svekkede koksidielinjer med kort utviklingssyklus:
 1. VETERINÆRPREPARATETS NAVN HIPRACOX. Mikstur, suspensjon og oppløsning for spray for kyllinger. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Sammensetning per dose (0,007 ml) av HIPRACOX: 1. Virkestoffer:
1. VETERINÆRPREPARATETS NAVN HIPRACOX. Mikstur, suspensjon og oppløsning for spray for kyllinger. 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Sammensetning per dose (0,007 ml) av HIPRACOX: 1. Virkestoffer:
Råd til forskjellige kategorier personell om beskyttelse ved kontakt med vill- og tamfugl i ulike risikosituasjoner
 Råd til forskjellige kategorier personell om beskyttelse ved kontakt med vill- og tamfugl i ulike risikosituasjoner Generelt Etter spredning av fugleinfluensaviruset H5N1 til flere europeiske land er sannsynligheten
Råd til forskjellige kategorier personell om beskyttelse ved kontakt med vill- og tamfugl i ulike risikosituasjoner Generelt Etter spredning av fugleinfluensaviruset H5N1 til flere europeiske land er sannsynligheten
NY OG UTSATT EKSAMENSOPPGAVE/EKSAMENSOPPGÅVE
 HØGSKOLEN I BERGEN Avdeling for helse og sosialfag Institutt for Radiografi NY OG UTSATT EKSAMENSOPPGAVE/EKSAMENSOPPGÅVE Fag Utdanning : Farmakologi med medikamentregning : institutt for Radiografi Kull
HØGSKOLEN I BERGEN Avdeling for helse og sosialfag Institutt for Radiografi NY OG UTSATT EKSAMENSOPPGAVE/EKSAMENSOPPGÅVE Fag Utdanning : Farmakologi med medikamentregning : institutt for Radiografi Kull
Håndtering av legemidler i forbindelse med praksisstudier for Bachelor i sykepleie
 Høgskolen i Telemark Håndtering av legemidler i forbindelse med praksisstudier for Bachelor i sykepleie Avdeling for helse- og sosialfag ved Høgskolen i Telemark Utarbeidet av Siv Roel, Solvor Brungot
Høgskolen i Telemark Håndtering av legemidler i forbindelse med praksisstudier for Bachelor i sykepleie Avdeling for helse- og sosialfag ved Høgskolen i Telemark Utarbeidet av Siv Roel, Solvor Brungot
Legemiddelhåndtering. Greta Irene Hanset. 21. okt 2019
 Legemiddelhåndtering Greta Irene Hanset 21. okt 2019 Tema tilsyn Tilsyn med kommunale helse- og omsorgstjenester til personer med utviklingshemming Om kommunen legg til rette for at mennesker med utviklingshemming
Legemiddelhåndtering Greta Irene Hanset 21. okt 2019 Tema tilsyn Tilsyn med kommunale helse- og omsorgstjenester til personer med utviklingshemming Om kommunen legg til rette for at mennesker med utviklingshemming
Doseringen bestemmes av retningslinjene for legemidlet som skal løses opp eller fortynnes.
 PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Sterilt vann B. Braun oppløsningsvæske til parenteral bruk 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 100 ml inneholder: Vann til injeksjonsvæsker 100 ml 3. LEGEMIDDELFORM
PREPARATOMTALE 1 1. LEGEMIDLETS NAVN Sterilt vann B. Braun oppløsningsvæske til parenteral bruk 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 100 ml inneholder: Vann til injeksjonsvæsker 100 ml 3. LEGEMIDDELFORM
Basale smittevernrutiner i helsetjenesten (basale rutiner)
 Basale smittevernrutiner i helsetjenesten (basale rutiner) Presentasjon utarbeidet for undervisning i helseinstitusjoner Basale rutiner - introduksjon Gjelder ved arbeid med alle pasienter, uavhengig av
Basale smittevernrutiner i helsetjenesten (basale rutiner) Presentasjon utarbeidet for undervisning i helseinstitusjoner Basale rutiner - introduksjon Gjelder ved arbeid med alle pasienter, uavhengig av
Din veiledning til. Genotropin (somatropin, rbe) ferdigfylt injeksjonspenn
 Din veiledning til Genotropin (somatropin, rbe) ferdigfylt injeksjonspenn Penn Innhold Bruksanvisning 4 Bli kjent med GoQuick 5 Klargjøring av GoQuick 6 3 enkle trinn for daglig bruk 12 (MED nåleskjuler)
Din veiledning til Genotropin (somatropin, rbe) ferdigfylt injeksjonspenn Penn Innhold Bruksanvisning 4 Bli kjent med GoQuick 5 Klargjøring av GoQuick 6 3 enkle trinn for daglig bruk 12 (MED nåleskjuler)
Sikkerhetsdatablad. Ardex: 880, A37-mix, A46, F5, K75, S20. 1. Identifikasjon av stoffet/stoffblandingen og selskapet/foretaket. 2. Fareidentifikasjon
 Sikkerhetsdatablad 1. Identifikasjon av stoffet/stoffblandingen og selskapet/foretaket Revidert den: 20-03-2009/ JST Erstatter den: 30-09-2008 Bruk av produktet Ardex 880, A46, K75: Gulvsparkelmasse Ardex
Sikkerhetsdatablad 1. Identifikasjon av stoffet/stoffblandingen og selskapet/foretaket Revidert den: 20-03-2009/ JST Erstatter den: 30-09-2008 Bruk av produktet Ardex 880, A46, K75: Gulvsparkelmasse Ardex
VEDLEGG I PREPARATOMTALE
 VEDLEGG I PREPARATOMTALE 1 1. VETERINÆRPREPARATETS NAVN Porcilis APP vet. injeksjonsvæske, suspensjon 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver dose på 2 ml inneholder: Virkestoffer: 600 mg Actinobacillus
VEDLEGG I PREPARATOMTALE 1 1. VETERINÆRPREPARATETS NAVN Porcilis APP vet. injeksjonsvæske, suspensjon 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver dose på 2 ml inneholder: Virkestoffer: 600 mg Actinobacillus
1964- TOTAL PAIN. «Well doctor, the pain began in my back, but now it seems that all of me is wrong»
 SMERTELINDRING Anne Watne Størkson Kreftsykepleier/ fagsykepleier Palliativt team. Seksjon smertebehandling og palliasjon, HUS og Kompetansesenter i lindrande behandling helseregion Vest Okt.2013 DEFINISJON
SMERTELINDRING Anne Watne Størkson Kreftsykepleier/ fagsykepleier Palliativt team. Seksjon smertebehandling og palliasjon, HUS og Kompetansesenter i lindrande behandling helseregion Vest Okt.2013 DEFINISJON
EKSAMENSOPPGAVE/EKSAMENSOPPGÅVE
 AVDELING FOR HELSE- OG SOSIALFAG EKSAMENSOPPGAVE/EKSAMENSOPPGÅVE Utdanning Kull Emnekode og navn/namn Eksamensform : Bachelor i sykepleie : GRS11 / GRSD11 Ny/ utsatt prøve : Medikamentregning : Forprøve
AVDELING FOR HELSE- OG SOSIALFAG EKSAMENSOPPGAVE/EKSAMENSOPPGÅVE Utdanning Kull Emnekode og navn/namn Eksamensform : Bachelor i sykepleie : GRS11 / GRSD11 Ny/ utsatt prøve : Medikamentregning : Forprøve
Basale smittevernrutiner Smittevern NLSH 2009. Håndhygiene Hanskebruk Munnbind Beskyttelsesfrakk Risikoavfall Åse Mariann Bøckmann Hygienesykepleier
 Basale smittevernrutiner Smittevern NLSH 2009 Håndhygiene Hanskebruk Munnbind Beskyttelsesfrakk Risikoavfall Åse Mariann Bøckmann Hygienesykepleier Hvordan begrense smitte av influensa A (H1N1)? Influensa
Basale smittevernrutiner Smittevern NLSH 2009 Håndhygiene Hanskebruk Munnbind Beskyttelsesfrakk Risikoavfall Åse Mariann Bøckmann Hygienesykepleier Hvordan begrense smitte av influensa A (H1N1)? Influensa
Pakningsvedlegg: Informasjon til pasienten. Vyxeos 44 mg/100 mg pulver til konsentrat til infusjonsvæske, oppløsning daunorubicin og cytarabin
 Pakningsvedlegg: Informasjon til pasienten Vyxeos 44 mg/100 mg pulver til konsentrat til infusjonsvæske, oppløsning daunorubicin og cytarabin Les nøye gjennom dette pakningsvedlegget før du begynner å
Pakningsvedlegg: Informasjon til pasienten Vyxeos 44 mg/100 mg pulver til konsentrat til infusjonsvæske, oppløsning daunorubicin og cytarabin Les nøye gjennom dette pakningsvedlegget før du begynner å
PERIFER VENEKANYLE (PVK) INNLEGGELSE, STELL, DOKUMENTASJON, OBSERVASJON OG KOMPLIKASJONER HVORFOR PVK? VALG AV PVK
 PERIFER VENEKANYLE (PVK) INNLEGGELSE, STELL, DOKUMENTASJON, OBSERVASJON OG KOMPLIKASJONER Intensivsykepleier Ove Andre Minsås 6. september 2011 HVORFOR PVK? intravenøs væsketilførsel intravenøs smertebehandling
PERIFER VENEKANYLE (PVK) INNLEGGELSE, STELL, DOKUMENTASJON, OBSERVASJON OG KOMPLIKASJONER Intensivsykepleier Ove Andre Minsås 6. september 2011 HVORFOR PVK? intravenøs væsketilførsel intravenøs smertebehandling
Denne pasientveiledningen skal brukes som et tillegg til de spesifikke instruksjonene du har fått av legen.
 N ON-Q* -smertelindringssystem Pasientveiledning Pumpe A Select-A-Flow * Variabel hastighetskontroller Klemme Filter Festes Til Kateteret Slange B ONDEMAND * Bolusknapp Flyt-Kontroller C Fast Flythastighet
N ON-Q* -smertelindringssystem Pasientveiledning Pumpe A Select-A-Flow * Variabel hastighetskontroller Klemme Filter Festes Til Kateteret Slange B ONDEMAND * Bolusknapp Flyt-Kontroller C Fast Flythastighet
1. VETERINÆRPREPARATETS NAVN. AviPro THYMOVAC Lyofilisat til bruk i drikkevann 2. KVALITATIV OG KVANTITATIV SAMMENSETNING
 1. VETERINÆRPREPARATETS NAVN AviPro THYMOVAC Lyofilisat til bruk i drikkevann 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 dose inneholder: Virkestoff: levende kyllinganemivirus (CAV*), stamme Cux-1: 10
1. VETERINÆRPREPARATETS NAVN AviPro THYMOVAC Lyofilisat til bruk i drikkevann 2. KVALITATIV OG KVANTITATIV SAMMENSETNING 1 dose inneholder: Virkestoff: levende kyllinganemivirus (CAV*), stamme Cux-1: 10
Genestran Vet 75 mikrogram/ml injeksjonsvæske, oppløsning, for storfe, hest og svin
 1. VETERINÆRPREPARATETS NAVN Genestran Vet 75 mikrogram/ml injeksjonsvæske, oppløsning, for storfe, hest og svin 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver ml inneholder: Virkestoff: mikrogram R(+)-Kloprostenol
1. VETERINÆRPREPARATETS NAVN Genestran Vet 75 mikrogram/ml injeksjonsvæske, oppløsning, for storfe, hest og svin 2. KVALITATIV OG KVANTITATIV SAMMENSETNING Hver ml inneholder: Virkestoff: mikrogram R(+)-Kloprostenol
